不同来源金黄色葡萄球菌溶血素基因分布研究
2015-05-09汪永禄李凤娟王多春
汪永禄,李凤娟,陶 勇,王 利,王 艳,王多春
不同来源金黄色葡萄球菌溶血素基因分布研究
汪永禄1,李凤娟2,陶 勇1,王 利1,王 艳1,王多春3
目的 了解金黄色葡萄球菌溶血素的携带情况,为金黄色葡萄球菌的防治及溯源提供依据。方法 采用PCR扩增分别检测食品、临床患者和游泳池水等不同样本中hla、hlb、hlg和hld四种溶血素基因的分布情况,电泳检测扩增产物。结果 317株金黄色葡萄球菌中,hla、hlb、hlg、hld四种溶血素基因的检出情况分别为85.5%、76.3%、89.6%、89.0%;在2008-2012年之间,四种溶血素基因的检出率无统计学差异。317株金黄色葡萄球菌中共有11种溶血素基因分布模式, 检出率最高的模式为hlb/hlg,占71.9%, 其次为hla/hld(70.3%), 最少的是hla/hlb/hlg/hld(36.3%), 不含溶血素基因的占2.2%。多数模式在3种来源菌株中的分布模式均有所不同。2008-2012年,每年同时检出hla、hlb、hlg、hld的菌株阳性率分别为45.7%、29.4%、32.5%、33.3%和32.1%。结论 不同来源金黄色葡萄球菌中,溶血素基因携带及同时含有两种或者以上的情况普遍存在。
金黄色葡萄球菌;溶血素基因;分布
金黄色葡萄球菌作为引起细菌性食物中毒的一种重要病原菌,能够产生溶血毒素、杀白细胞素、肠毒素等多种毒力致病因子,且毒力强,具有在自然环境中广泛分布、抵抗力强等特征,食品受到该菌污染的机会很多。金黄色葡萄球菌不仅是引起细菌性食物中毒的重要病原菌,同时也是医院临床感染的常见病原体之一,可导致人类皮肤、黏膜、深部组织感染以及心内膜炎、肺炎、脓毒症、中毒休克综合症等多种疾病。溶血素是金黄色葡萄球菌的重要毒力因子,可通过作用于红血球、血小板及溶解中性球,使其中的溶菌酵素释出,破坏附近组织[1]。为了解不同来源标本金黄色葡萄球菌溶血素基因的分布情况,我们对马鞍山地区的来自于临床患者、食品和游泳池水样本中的金黄色葡萄球菌溶血素基因进行了检测。现报告如下。
1 材料与方法
1.1 材料
1.1.1 菌株来源 本实验菌株共317株,其中食品样本性菌株186株,分别为2008年29株、2009年30株、2010年40株、2011年57株、2012年30株;来自临床标本菌株83株,分别为2008年55株、2011年20株、2012年8株;来源于游泳池水样菌株48株,分别为2008年10株、2009年4株、2011年19株、2012年15株。所有分离的菌株均确定为革兰氏阳性菌、过氧化氢酶和血浆凝固酶阳性后,经细菌自动仪鉴定为金黄色葡萄球菌;同时对每株菌株耐热核酸酶基因进行PCR检测以进一步确定。质控菌株为金黄色葡萄球菌ATCC25923。
1.1.2 试剂与仪器 金黄色葡萄球菌染色体提取试剂盒(DNeasy blood and tissue kit)为QIAGEN公司产品;dNTP、2 000 bp、PCRMarker Taq酶及PCR产物纯化试剂盒购自大连宝生物生物有限公司;PCR仪(MycyderTMthermal cycler)为美国伯乐公司产品;革兰阳性菌鉴定卡(VITEK GPI)和VITEK-32细菌自动仪为法国梅里埃公司产品。其它培养基试剂为北京陆桥技术有限公司供应。
1.1.3 引物的设计与合成 根据在NCBI上查的的序列,利用DNAMAN和Primer 5.0软件,设计hla、hlb、hlg、hld的引物序列,PCR引物由上海生物工程有限公司合成,见表1; PCR引物合成及PCR产物纯化、测序由北京天一辉远生物有限公司完成。

表1 引物信息
1.2 方法
1.2.1 金黄色葡萄球菌的DNA的提取 取金黄色葡萄球菌培养物增菌液100 μL,12 000 r/min离心5 min,弃上清液,加入300 μL Tris洗涤,加入30 μL溶金葡菌素,混匀后37 ℃孵育10 min,然后加入0.1%SDS 30 μL,混匀后37 ℃孵育30 min,即制成PCR扩增模板。
1.2.2 PCR扩增 PCR扩增反应总体积为25 μL,其中预混反应液12 μL,模板DNA 2 μL,上游引物(10 μmoL/L)1 μL,下游引物(10 μmoL/L)1 μL,灭菌双蒸馏水9 μL。PCR反应条件:预变性94 ℃ 5 min;94 ℃40 s,49 ℃40 s(hla,hld),54 ℃40 s(hlb,hlg), 72 ℃1 min(30个循环);72 ℃10 min。
1.2.3 PCR产物进行琼脂糖凝胶电泳。琼脂糖浓度为1%,所用的DNA标准分子量(Marker)购自上海生工生物工程技术服务有限公司。
1.2.4 凝胶成像 电泳完成后的凝胶在凝胶成像系统中成像,观察PCR扩增条带结果。
2 结 果
2.1 溶血素基因检测结果 根据PCR检测结果,317株金黄色葡萄球菌中溶血素基因总检出率为97.5%,hla、hlb、hlg、hld4种溶血素基因的检出情况分别为85.5%、76.3%、89.6%、89.0%;3类不同来源标本的金黄色葡萄球菌中,hla、hlb、hlg、hld四种溶血素基因的检出情况,hla基因在临床样本中的检出率高于食品样本,差异具有统计学意义(P<0.05)。其余3种基因在3类不同来源标本中的检出率无统计学差异(P>0.05),见表2。
2.2 不同年份菌株溶血素基因检出情况 本研究对金黄色葡萄球菌4种溶血素基因携带情况进行比较发现,4种溶血素基因的检出率在分离年代上的差异无统计学意义(P>0.05)。见表3。
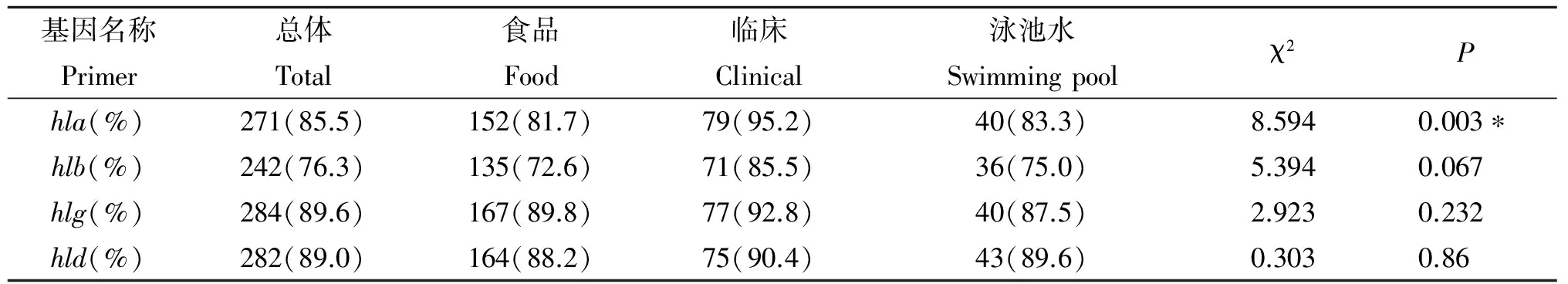
表2 不同来源样品中4种溶血素基因检出情况
注:*,差异具有统计学意义。*P<0.05.
Note:*P<0.05, the difference was statistically significant.
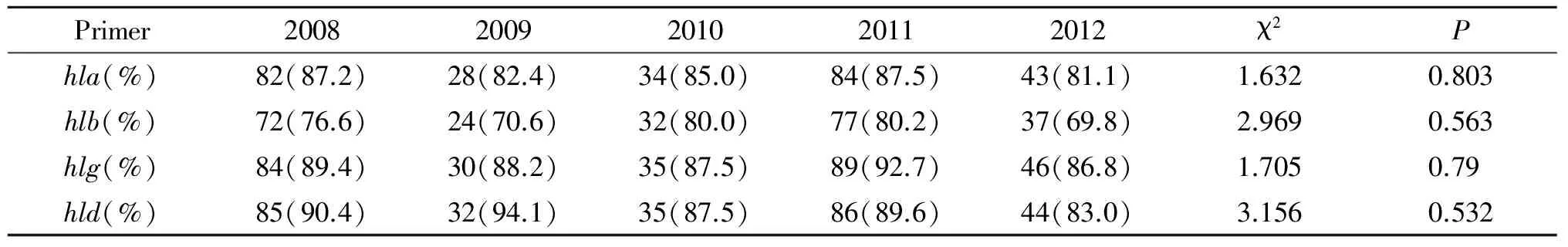
表3 不同年代间4种溶血素基因检出情况
2.3 4种溶血素基因在不同来源菌株中的分布模式 4种溶血素基因在317株金黄色葡萄球菌中共有11种分布模式,见表4。检出率最高的溶血素基因模式为hlb/hlg,占71.9%, 其次为hla/hld(70.3%), 最少的是hla/hlb/hlg/hld(36.3%), 不含溶血素基因的占2.2%。在溶血素基因模式中,hla/hlb/hlg/hld、hla/hlb/hlg和不含溶血素3种模式的分布,在不同来源样本之间无差别(P>0.05),其余类型在3种来源样本中的分布模式均有所不同,且经两两比较发现,hla/hlg/hld、hla/hlg/hld、hla/hlg/hld在游泳池水样本中的分离率高于食品,hla/hlb、hla/hlg在临床样本和游泳池水样本中的分离率都高于食品样本,hla/hld、hlb/hlg、hlb/hld在临床样本中的分离率高于食品样本,差异有统计学意义(P<0.05)。见表4。
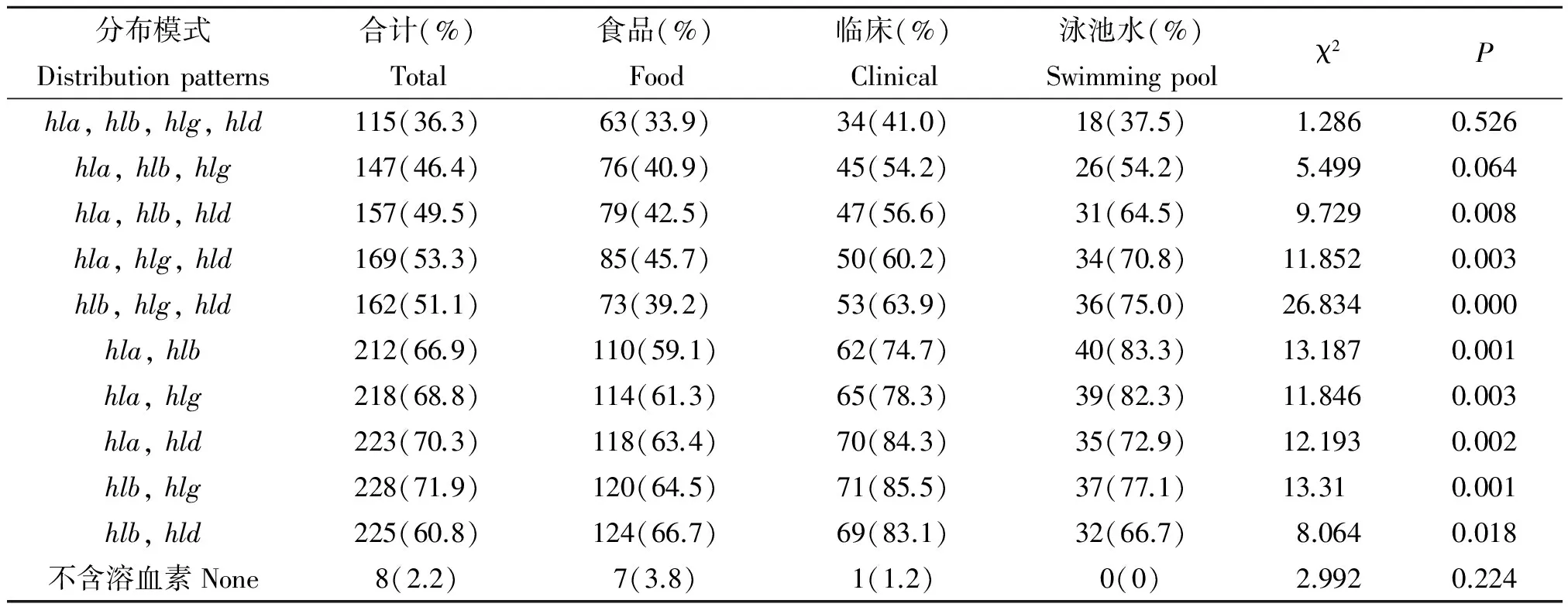
表4 不同来源菌株中四种溶血素基因的分布模式
2.4 四种溶血素基因在不同年份菌株中的分布模式 2008年至2012年5年中,每年同时检出hla、hlb、hlg、hld4种溶血素基因的菌株的分布情况分别为45.7%、29.4%、32.5%、33.3%和32.1%;每年同时检出hla、hlb、hlg3种溶血素基因的菌株的分布情况分别为46.8%、47.1%、45.0%、46.9%和45.3%;同时检出hla、hlb、hld的菌株的分布情况分别为48.9%、50.0%、52.5%、49.0%和49.1%;同时检出hla、hlg、hld的菌株的分布情况分别为51.1%、55.9%、55.0%、53.1%和54.7%;同时检出hlb、hlg、hld的菌株的分布情况分别为51.1%、50.0%、50.0%、51.0%和52.8%。4种溶血素基因在不同年份菌株中的分布差异无统计学意义(P>0.05)。见表5。
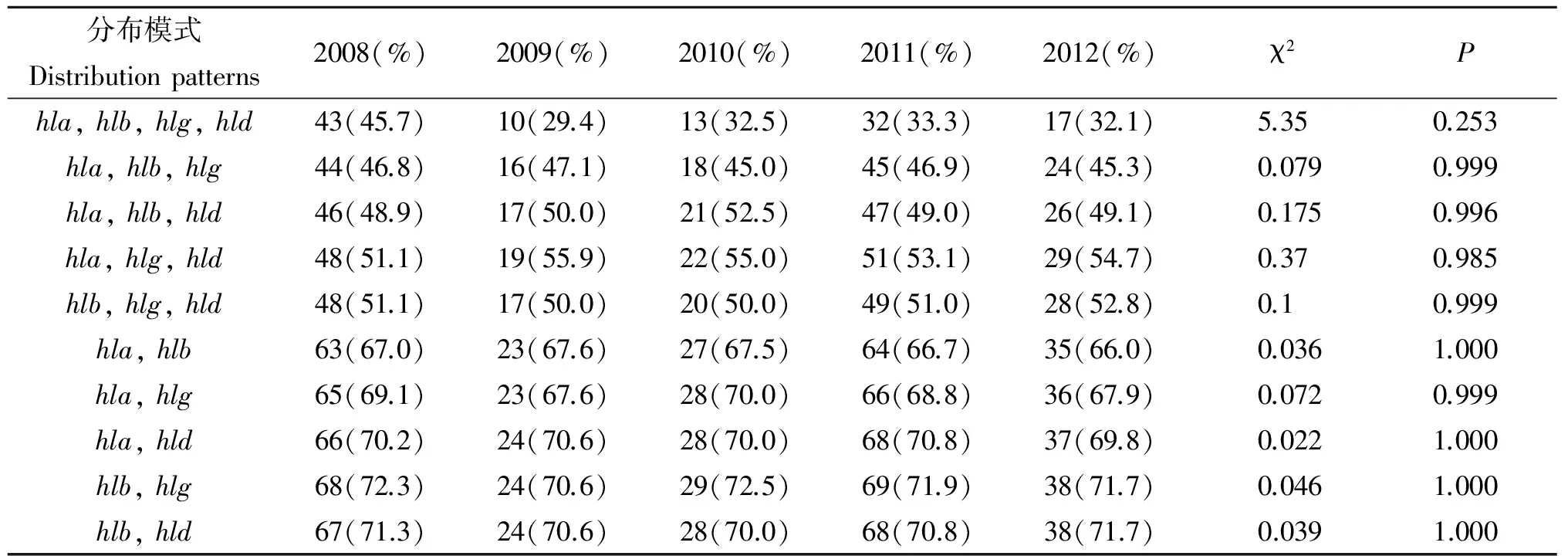
表5 不同年代间四种溶血素基因的分布模式
3 讨 论
金黄色葡萄球菌作为一种常见的致病菌,污染率高、耐药谱广、耐药性强,无论发达国家还是发展中国家,由其引起的食物中毒在细菌性食物中毒中占有较大的比例[2]。金黄色葡萄球菌主要是通过其产生的溶血素、凝固酶、杀白细胞素、肠毒素等多种致病因子,引起人和动物的多种疾病[3]。溶血素作为金黄色葡萄球菌的一种重要的致病因子,对人和哺乳动物有细胞毒作用,目前有关它的报道还比较少[4]。根据其抗原不同,金黄色葡萄球菌有α、β、γ、ε四种溶血素。目前,溶血素对组织造成损害的主要是α-溶血素和β-溶血素[5]。
本次对食品、临床患者和游泳池水金黄色葡萄球菌溶血素的检测结果表明, 97.5%的分离株含有一种或者以上溶血素基因,其中hla、hlb、hlg、hld的检出率分别为85.5%、76.3%、89.6%、89.0%。 魏志恒[4]等的研究中,金黄色葡萄球菌溶血素基因总检出率97.07%,其中α-溶血素基因总检出率95.21%,β-溶血素基因的总检出率为73.93%;卫沛楠[5]等人曾对石家庄地区食品中分离的131株金黄色葡萄球菌的hla、hlb两种溶血素基因的检测,阳性率分别为88.51%、60.81%。这些结果与本研究一致,提示许多地区金黄色葡萄球菌中溶血素基因携带率较高,对人体健康是一种潜在性危险,且hla的检出率高于hlb。Elizabete Rodrigues da Silva等[6]的研究结果显示,从患乳腺炎的山羊奶中筛选的金葡菌有76.7%分泌α-溶血素,74.4%分泌β-溶血素。与本研究的结果一致,且无论是人源还是动物源中,金黄色葡萄球菌α-溶血素和β-溶血素的携带率均较高,同时也提示,溶血素基因的分布携带率无地域性差异影响,菌株携带的溶血素基因型不会被其生存的环境所选择。另外,文献报道临床来源的菌株,在进化过程中获得一些基因组岛,如vSa4、噬菌体ФSal和ФSa3等[7],这些基因组岛的插入,可能会影响对溶血素基因的检测。从我们的实验结果看,临床来源菌株的hlb,PCR阳性率较高(85.5%),提示hlb基因的检测没有受到基因组岛插入的影响。
本研究还发现,除hla外,金黄色葡萄球菌的其它溶血素基因在临床、食品、游泳池水样本中的分布没有差异,说明金黄色葡萄球菌溶血素在食品样本中的携带率已与临床几乎相同。提示食品中金葡菌的污染可能主要由二次污染所致,食品加工及监测部门应该加强对食品卫生环境的管理[4]。同时,许多菌株普遍携带着两种及两种以上的溶血素基因,部分菌株甚至携带了4种,且携带率较高,说明溶血素普遍存在于金黄色葡萄球菌中,且不同溶血素之间可能存在着协同作用[8-9]。本研究中,无论是4种溶血素还是单独一种,携带率在年代分布上的差异都不具有统计学意义,但携带率都较高,提示金黄色葡萄球菌的毒力作用是由多基因共同作用的,所以应加强对金葡菌毒力基因的检测。
[1]Tu JJ, Zhang X, Xu YY, et al. Regulating effect of seaRS on the expression ofhlaand lukS-PV inStaphylococcusaureusclinical isolate[J]. Chin J Microbiol Immunol, 2013, 3(2): 91-96. (in Chinese) 屠金晶,张协,许园园,等. seaRS对金黄色葡萄球菌临床分离株的hla和luks-PV表达的影响[J]. 中华微生物学和免疫学杂志,2013,3(2):91-96.
[2]Deng ZJ, Li Y, Hong CJ, et al. Pollution analysis ofStaphylococcusaureusand detection of its toxin in food stuff[J]. Zhejiang J Prevent Med, 2011, 23(2): 92-96. (in Chinese) 邓泽静,李毅,洪程基,等. 食品中金黄色葡萄球菌污染状况及其毒素检测[J].浙江预防医学,2011,23(2):92-96.
[3]Lu CP. Veterinary microbiology[M]. 3rd ed. Beijing: China Agriculture Press, 2001: 200-204. (in Chinese) 陆承平. 兽医微生物学[M]. 3版.北京:中国农业出版社,2001:200-204.
[4]Wei ZH, Yu HW, Li N, et al. The distributing research of hemolysin genes inStaphylococcusaureus[J]. J Chin Food Sci Technol, 2009, 9(6): 152-156. (in Chinese) 魏志恒,于宏伟,李宁,等. 金黄色葡萄球菌溶血素基因分布的研究[J]. 中国食品学报, 2009,9(6):152-156.
[5]Wei PN, Lv GP, Xu BH. Genotypic and phenotypic analysis of hemolysis in foodborneStaphylococcusaureus[J]. J Hyg Res, 2012, 41(6): 934-937. (in Chinese) 卫沛楠,吕国平,徐保红. 食源性金黄色葡萄球菌溶血素基因的多重PCR检测和聚类分析[J]. 卫生研究,2012,41(6):934-937.
[6]Silva ER, Boecha JU, Martins JC, et al. Hemolysin production byStaphylococcusaureusspecies isolated from mastitic goat milk in Brazilian dairy herds[J]. Small Ruminant Res, 2005, 56: 271-275.
[7]Li HN, Zhao CJ, Chen HB, et al. Comparative genomic analysis of ST239-spa t037 MRSA and ST239-spa t030 MRSA[J]. Chin J Microbiol Immunol, 2012, 32(9): 770-773. (in Chinese) 李荷楠,赵春江,陈宏斌,等.ST239-spa t037 MRSA与ST239-spa t030 MRSA的比较基因组分析[J]. 中华微生物学和免疫学杂志,2012, 32(9): 770-773.
[8]Cifrian E, Guidry AJ, Bramley AJ, et al. Effect of staphylococcal betatoxin on the cytotoxicity, proliferation and adherence ofStaphylococcusaureusto bovine mammary epithelial cells[J]. Vet Microbiol, 1996, 48(3-4): 187-198.
[9]Cifrian E, Guidry AJ, O’Brien CN, et al. Effect of antibodies to staphylococcal alpha and beta toxins andStaphylococcusaureuson the cytotoxicity for and adherence of the organism to bovine mammary epithelial cells[J]. Am J Vet Res, 1996, 57(9): 1308-1311.
Wang Duo-chun, Email: wangduochun@icdc.cn
Distribution ofStaphylococcusaureushemolysin genes among different sources
WANG Yong-lu1,LI Feng-juan2,TAO Yong1,WANG Li1,WANG Yan1,WANG Duo-chun3
(1.Ma’anshanCenterforDiseaseControlandPrevention,Ma’anshan243000,China; 2.CenterforDiseaseControlandPreventionofHenanProvince,Zhengzhou450016,China; 3.NationalInstituteforCommunicableDiseaseControlandPrevention,ChinaCenterforDiseaseControlandPrevention,Beijing102206,China)
We investigated the distribution ofStaphylococcusaureushemolysin, providing the basis for prevention and control and traceability ofStaphylococcusaureus. PCR was using to detect hemolysin genes ofhla,hlb,hlgandhldin the samples of food, clinical and swimming pool. The PCR products were detected by electrophoresis. Among 317 strains, the detection rate of four hemolysin genes were 85.5%, 76.3%, 89.6% and 89%; no statistical differences distribution of the four hemolysin genes by year between 2008 and 2012. There were eleven kinds of haemolysin gene patterns among 317 strains, the highest pattern washlb/hlg, accounting for 71.9%, followed byhla/hld(70.3%), the least washla/hlb/hlg/hld(36.3%), the strains of no hemolysin gene accounted for 2.2%. The distribution of most patterns was different among different sources. From year of 2008 to 2012, the positive rate ofhla,hlb,hlgandhldcarried strains detected in each year were 45.7%, 29.4%, 32.5%, 33.3% and 32.1%. The four hemolysin genes were widespread among different sources of ofS.aureus.
Staphylococcusaureus; hemolysin gene; distribution
10.3969/j.issn.1002-2694.2015.09.010
王多春,Email:wangduochun@icdc.cn
1.安徽马鞍山市疾病预防控制中心,马鞍山 243000; 2.河南省疾病预防控制中心,郑州 453600; 3. 中国疾病预防控制中心传染病预防控制所,北京 102206
R378.1
A
1002-2694(2015)09-0831-04
2015-01-20;
2015-06-02
