新型基于1,8-萘酰亚胺的汞离子荧光探针的合成与性质研究
2015-05-09杨成玉蒋菊华周宝成韩益丰
宋 涛,杨成玉,蒋菊华,周宝成,韩益丰,b
(浙江理工大学 a.理学院,b.先进纺织材料与制备技术教育部重点实验室,杭州 310018)
新型基于1,8-萘酰亚胺的汞离子荧光探针的合成与性质研究
宋 涛a,杨成玉a,蒋菊华a,周宝成a,韩益丰a,b
(浙江理工大学 a.理学院,b.先进纺织材料与制备技术教育部重点实验室,杭州 310018)
设计合成了一种用于检测Hg2+的1,8-萘酰亚胺类荧光探针(NM1),采用现代波谱技术对探针的结构进行了表征,并考察了其光谱性能。研究结果表明,NM1对Hg2+有优秀的选择性和灵敏度,它们之间的结合比为1∶1,常见共存金属离子对其测定无干扰。此外,NM1还能够可视化检测Hg2+,这对检测水质和生物体内的Hg2+具有潜在的应用价值。
荧光探针; Hg2+离子; 1,8-萘酰亚胺; 可视化检测
0 引 言
Hg2+离子,广泛存在于自然界,是目前最引人关注的重金属污染物之一。Hg2+离子易与生物体内巯基化合物紧密结合,改变相关蛋白质的表达性质,使其在生物体内的正常代谢紊乱,从而严重影响有机体的功能[1]。Hg2+离子尤其是甲基汞等易被生物体吸收,可通过食物链传递,难以通过代谢排出体外,最终在生物体内高度地富集,严重危害人类的安全。因此,研制成本低、响应快、易实现、能应用于自然环境和生物体系的新型Hg2+检测手段成为人们日益关注的研究课题[2-4]。传统的用于检测Hg2+离子的方法主要有分光光度法、原子吸收和发射光谱法、质谱法和伏安法等,它们均需复杂的操作或是昂贵的仪器,不适用于实时、原位的分析检测。与之相比,近年来发展的荧光分析法因其高效灵敏、快速便捷而且能实时、定位检测等优点而受到生物化学和化学生物学研究者的广泛关注[5-7]。1,8-萘酰亚胺类化合物是一类重要的荧光染料,由于具有良好的光化学和热稳定性及结构易修饰等突出的光物理和化学性能,而被研究用作荧光标记物和特定金属离子的光化学传感器[8-10]。本论文利用1,8-萘酰亚胺为荧光母团,取代的8-羟基喹啉为识别基团而设计合成了可用于水相中Hg2+离子检测的荧光小分子探针。
1 实验部分
1.1 实验材料与仪器
试剂:4-溴-1,8-萘二甲酸酐(玛雅化学试剂有限公司)、正丁胺、哌嗪、氯乙酰氯、8-羟基喹啉、4-二甲氨基吡啶(DMAP)、乙二醇单甲醚、碘化钠等均为市售化学纯(国药集团化学试剂有限公司),甲醇、石油醚、乙酸乙酯、二氯甲烷等溶剂均为工业溶剂重蒸后使用。仪器:AVANCE-AV 400型核磁共振波谱仪(德国Bruker公司),LS45型荧光分光光度计(美国Perkin Elmer公司),DF-101D集热式磁力加热搅拌器(河南省予华仪器有限公司)。
1.2 探针分子NM1的合成
相应关键中间体和目标分子的合成路线见图1。
1.2.1 化合物3的合成
在500 mL的三口烧瓶中加入5.0 g 4-溴-1,8-萘二甲酸酐和200 mL乙醇,在氮气保护的条件下加热回流溶解,待原料溶解后,向反应液中注入2.5 mL正丁胺,升温至80℃,搅拌回流反应8 h,TLC检测反应完毕,冷却析晶,抽滤,冷乙醇洗涤3次,得到黄色针状固体5.1 g,产率85%,产物无需纯化可直接用于下一步反应。
1.2.2 化合物2的合成
在25 mL的两口烧瓶中依次加入1.1 g化合物3和1.4 g哌嗪,氮气保护,注入10 mL乙二醇单甲醚回流溶解,升温至120℃,搅拌回流反应8 h,TLC监测反应完毕。将反应液倒入100 mL水中,冷却析晶,抽滤后用乙醇重结晶得到黄色固体产物0.9 g,产率86%。1H NMR(400 MHz,CDCl3)δ8.51(d,J=7.2 Hz,1H),8.45 (d,J=8.1 Hz,1H),8.35(d,J=8.4 Hz,1H),7.62(t,J=7.8 Hz,1H),7.14(d,J=8.0 Hz,1H),4.17~4.01(m,2H),3.26~2.99(m,8H),1.64(t,J=7.5 Hz,2H),1.37(m,2H),0.90(t,J=7.3 Hz,3H).
1.2.3 化合物1的合成
在50 mL的两口烧瓶中加入0.9 g化合物2,0.7 g 4-二甲氨基吡啶(DMAP),20 mL无水CH2Cl2,氮气保护,冰水浴下滴加0.7 mL氯乙酰氯,搅拌1 min,加热回流反应6 h。TLC检测反应完毕,加入20 mL水淬灭反应,然后用10 mL CH2Cl2萃取3次,用无水硫酸钠干燥,旋干二氯甲烷,得到粗产物。再经快速硅胶柱分离得到0.6 g化合物1,产率56%。M.p.=159~161℃;1H NMR (400 MHz,CDCl3) δ8.52(d,J=7.1 Hz,1H),8.45 (d,J=7.9 Hz,1H),8.34(d,J=8.4 Hz,1H),7.66(t,J=7.8 Hz,1H),7.15(d,J=8.0 Hz,1H),4.09(t,J=7.3 Hz,2H),3.87(s,2H),3.73(s,2H),3.17(d,J=17.5 Hz,4H),2.13(s,2H),1.71~1.56(m,2H),1.37(dd,J=14.7,7.4 Hz,2H),0.90(t,J=7.2 Hz,3H).13C NMR(100 MHz,CDCl3)δ164.35,163.24,162.79,153.74,131.24,130.19,128.62,125.19,122.43,116.86,114.50,51.79,45.50,41.27,39.81,39.11,29.2,19.36,12.84.
1.2.4 探针分子NM1的合成
在25 mL的三口烧瓶中加入176 mg 8-羟基喹啉,用5 mL乙腈溶解,得到无色澄清溶液,再加入1 mL(5 M)氢氧化钠溶液,搅拌后得到黄色浑浊溶液,再加入0.5 g化合物1以及0.2 g碘化钠,80℃回流反应5 h,TLC检测,反应完毕,冷却有固体析出,减压过滤,用乙腈洗涤2次,得到粗产物。再经快速硅胶柱分离得到260 mg探针NM1,产率41%。M.p.=156-157℃;1H NMR (400 MHz,CDCl3)δ8.46 (dd,J=21.6,7.6 Hz,3H),8.31(d,J=8.3 Hz,1H),8.13(s,1H),7.60(dd,J=13.5,6.8 Hz,2H),7.24~7.05(m,3H),4.55(d,J=4.9 Hz,2H),4.08(t,J=7.3 Hz,2H),3.26(s,4H),2.83(s,4H),1.68~1.53(m,2H),1.36(dd,J=14.6,7.3 Hz,2H),0.89(t,J=7.2 Hz,3H).13C NMR (100 MHz,CDCl3)δ169.94,164.33,163.90,156.58,155.52,149.12,136.73,132.32,131.01,129.99,129.73,126.07,125.70,123.23,122.35,122.01,116.96,114.92,61.51,53.50,53.00,43.96,40.00,30.16,20.31,13.78.

图1 目标探针分子NM1的合成路线
2 结果与讨论
2.1 探针分子NM1对Hg2+响应的紫外光谱测定
由图2可以看出,逐渐向10 μM的探针溶液(0.01 M HEPES buffer,pH=7.17)中加入Hg2+离子,探针在405 nm处的吸收峰逐渐下降,并在470、340、285 nm处呈现三个等吸点,表明NM1与Hg2+之间形成了新的络合物。
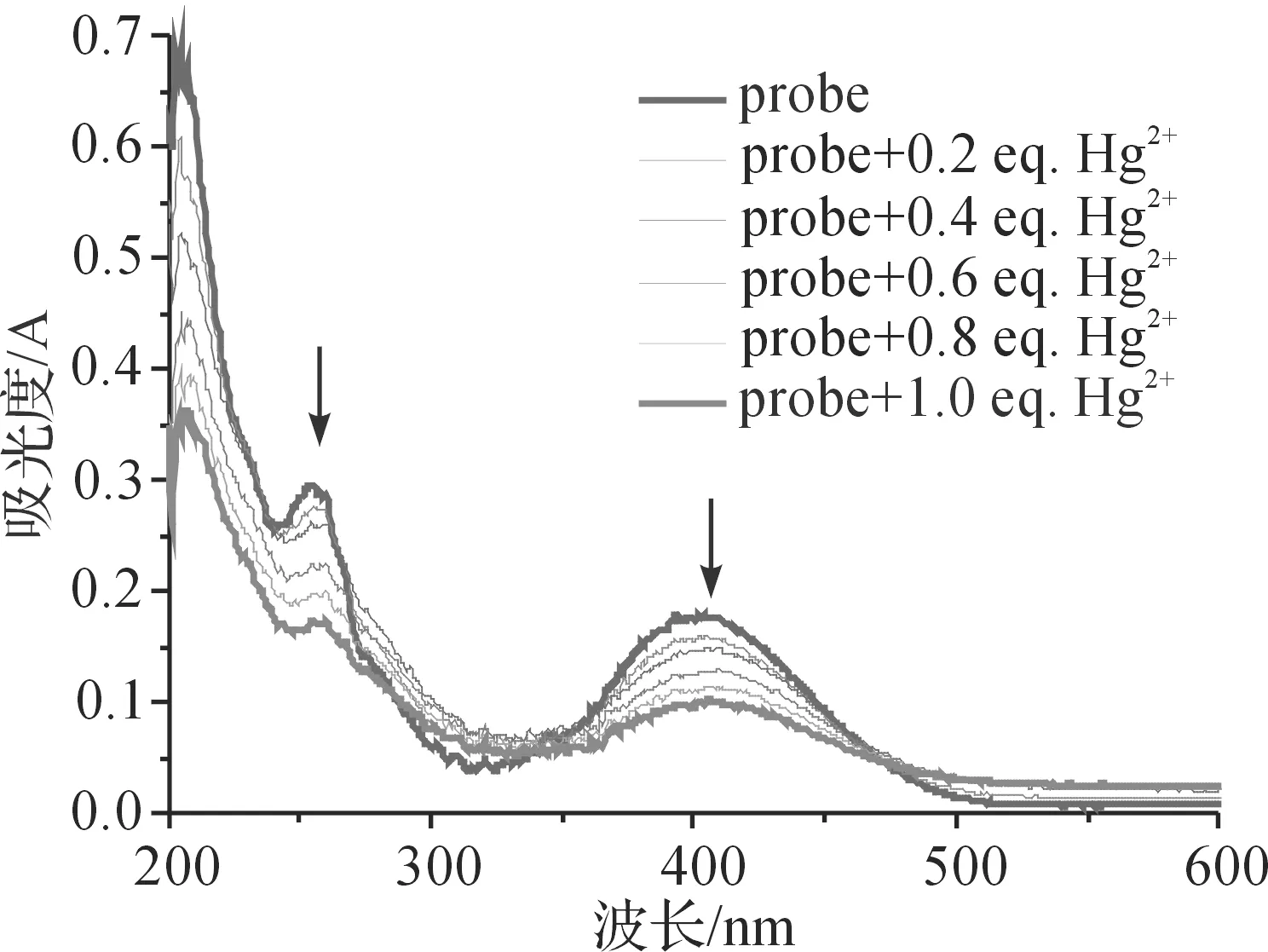
图2 NM1与Hg2+作用前后的紫外光谱变化
2.2 探针分子NM1对Hg2+的识别
2.2.1 探针分子NM1对Hg2+的选择性与竞争性测试
在10 μM的探针溶液(0.01 M HEPES buffer,pH=7.17)中,分别加入相同浓度(5 μM)的各种常见的金属离子溶液(Ag+,Al3+,Ca2+,Cd2+,Co2+,Cr3+,Cs+,Fe2+,Fe3+,K+,Li+,Mg2+,Mn2+,Na+,Ni2+,Pb2+,Sn2+,Zn2+,Hg2+)。选择性实验结果显示,除Hg2+离子以外,其余各种常见金属离子对探针分子NM1的荧光几乎无影响,表明探针分子NM1对Hg2+离子的优秀选择性(图3)。而进一步的竞争性实验显示,上述常见共存金属离子对Hg2+离子的测定无干扰。在10 μM的探针溶液(0.01 M HEPES buffer,pH=7.17)中,加入5 μM的Hg2+离子,再加入等当量的常见共存金属离子后,探针分子NM1的荧光并没有发生明显的改变(图4),表明探针分子NM1与Hg2+离子之间是特异性结合的。而当观察探针分子NM1在加入Hg2+离子前后的荧光变化时可以发现,加入Hg2+离子后溶液的荧光由极其微弱的黄绿色变成亮绿色,表明探针分子NM1可用于对Hg2+的可视化检测(图3)。

图3 NM1 (10 μM)对不同的金属离子(5 μM)的荧光响应

图4 在各种金属离子(5 μM)的存在下Hg2+对NM1 (10 μM)荧光的影响注:I0为空白探针的荧光强度,I为加入相应离子时探针的荧光强度。
2.2.2 探针分子NM1对Hg2+离子的荧光浓度滴定实验
在10 μM的探针溶液(0.01 M HEPES buffer,pH=7.17)中,逐渐加入Hg2+离子,随着Hg2+离子浓度逐渐的增加,探针分子NM1的荧光强度也逐渐增强,当Hg2+离子浓度为10 μM时(1eq)趋于一个固定值(图5)。荧光滴定实验结果显示,在低浓度下(0~10 μM)探针分子NM1的荧光强度与Hg2+的浓度呈良好的线性关系(Y=19.07+796.52X,R=0.987)(图6)。由此,根据检测线的计算方法可测得探针分子NM1对Hg2+离子的检测限为9.04 nM[10],该检测限远低于美国FDA规定的饮用水中Hg2+离子含量的标准值。因此,探针分子NM1可用于饮用水中痕量Hg2+的含量检测。
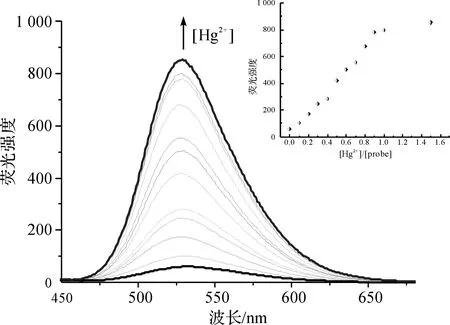
图5 NM1 (10 μM)随着Hg2+浓度增加(0~10 μM)荧光强度的变化

图6 Hg2+离子浓度(0~10 μM)与NM1荧光强度之间的关系
2.2.3 探针分子NM1对Hg2+离子的结合模式
为了进一步研究探针分子NM1与Hg2+离子之间的识别机理和结合模式,本文利用Job’s Plot法进行测定。从图7可以清楚地看出,Hg2+离子浓度为总浓度的0.5时荧光值的改变最为明显,这表明探针分子NM1与Hg2+离子之间以1∶1的方式进行结合。

图7 在10 mM HEPES缓冲溶液中(pH=7.17)NM1与Hg2+的Job’s plot图注:NM1与Hg2+的浓度和为10 μM,x为汞离子的摩尔分数,I0为空白探针的荧光强度,I为不同汞离子摩尔分数下探针的荧光强度。
3 结 论
a) 本论文设计合成了一种基于1,8-萘酰亚胺的OFF-ON型荧光小分子探针NM1,并通过光谱学手段确定了探针分子的结构。
b) 探针分子NM1对Hg2+离子具有优秀的选择性和响应灵敏度,而常见共存金属离子对其测定无干扰。
c) 由荧光滴定实验和job’s plot实验确定了探针分子NM1与Hg2+离子之间的结合比为1∶1。
d) 探针分子NM1对Hg2+离子的检测限可达9.04 nM,该值远低于美国FDA规定的饮用水中Hg2+离子含量的标准值,表明NM1可用于饮用水中痕量Hg2+的含量检测。
[1] Tchounwou P B,Ayensu W K,Ninashvili N,et al.Environmental exposure to mercury and its toxicopathologic implications for public health[J].Environmental Toxicology,2003,18(3): 149-175.
[2] Areti S,Yarramala D S,Samanta K,et al.Glyco-conjugate as selective switch-on molecule for Hg2+in the presence of albumin proteins,blood serum milieu and on silica gel solid support[J].RSC Advances,2014,4(35): 16290-16297.
[3] Zhang J,Yu S H.Highly photoluminescent silicon nanocrystals for rapid,label-free and recyclable detection of mercuric ions[J].Nanoscale,2014,6(8): 4096-4101.
[4] Huang J,Xu Y,Qian X.Rhodamine-based fluorescent off-on sensor for Fe3+-in aqueous solution and in living cells: 8-aminoquinoline receptor and 2: 1 binding[J].Dalton Transaction,2014,43(16): 5983-5989.
[5] Tian M,Liu L,Li Y,et al.An unusual OFF-ON fluorescence sensor for detecting mercury ions in aqueous media and living cells[J].Chemical Communication,2014,50: 2055-2057.
[6] Guo Z,Park S,Yoon J,et al.Recent progress in the development of near-infrared fluorescent probes for bioimaging applications[J].Chemical Society Review,2014,43: 16-29.
[7] Mauro M,Aliprandi A,Septiadi D,et al.When self-assembly meets biology: luminescent platinum complexes for imaging applications[J].Chemical Society Review,2014,43: 4144-4166.
[8] Cui L,Peng Z,Ji C,et al.Hydrazine detection in the gas state and aqueous solution based on the Gabriel mechanism and its imaging in living cells[J].Chemical Communication,2014,50: 1485-1487.
[9] Guo T,Cui L,Shen J,et al.A dual-emission and large Stokes shift fluorescence probe for real-time discrimination of ROS/RNS and imaging in live cells[J].Chemical Communication,2013,49: 1862-1864.
[10] Xu L,Xu Y,Zhu W,et al.A highly selective and sensitive fluorescence “turn-on” probe for Ag+in aqueous solution and live cells[J].Dalton Transaction,2012,41: 7212-7217.
(责任编辑:许惠儿)
Research on Synthesis and Propitiates of New Hg2+Ion Fluorescent Probe Based on 1,8-Naphthalimide
SONGTaoa,YANGCheng-yua,JIANGJu-huaa,ZHOUBao-chenga,HANYi-fenga,b
(a.School of Science; b.Key Laboratory of Advanced Textile Materials and Manufacturing Technology, Ministry of Education,Zhejiang Sci-Tech University,Hangzhou 310018,China)
A 1,8-naphthalimide-based fluorescent probe (NM1) for Hg2+ion detection was designed and synthesized.It was characterized by modern spectroscopy methods.Besides,its spectral property was investigated.The results show that NM1 exhibits excellent sensitivity and selectivity to Hg2+.The combination proportion is 1∶1.Common coexistent metal ions have no interference in detection.Furthermore,NM1 can achieve visual detection of Hg2+.Those results showed that NM1 has potential application value for the detection of Hg2+in water and in living systems.
fluorescent probe; Hg2+ion; 1,8-naphthalimide; visual detection
1673-3851 (2015) 02-0178-05
2014-05-29
国家自然科学基金项目(20902082);浙江省自然科学基金项目(Y201225426)
宋 涛(1987-),男,山东潍坊人,硕士研究生,主要从事有机化学方面的研究。
韩益丰,E-mail:hanyf@zstu.edu.cn
O656
A
