红枣中总黄酮类化合物的提取及其抗氧化性能的研究
2015-05-08陈宗保王国稳
陈宗保,王国稳
(1.上饶师范学院 江西省高等学校应用有机化学重点实验室,江西 上饶 334001;2.婺源县清华中学,江西 婺源 333200)
由于红枣中含有营养丰富,它具有多种营养保健功能,而且具有肉厚、色红、饱满、核小、味甜等特点。因此,在我国各地均有种植红枣。同样,红枣中还含有红枣多糖化合物、黄酮类化合物、三萜类化合物、腺苷、生物碱和甾醇等生物活性成分,这些化合物具有很强生理活性,能合理地调节生理功能[1]。据报道,食物中提取的黄酮类化合物能够达到预防冠状动脉及脑血管疾病的效果,有效地改善心脑血管中血液循环,降低中老年人血糖,提高人体抗氧化性及抗癌性等作用[2-3]。当前,各类食品中总黄酮化合物的提取方法一般包括振荡提取法、有机溶剂浸润提取法、超声波辅助提取法[4]。将提取的黄酮化合物经有效处理,研究其体外抗氧化性及清除自由基能力报道较多[5-8]。
本文采用有机溶剂乙醇为提取剂,结合超声波辅助技术对红枣中总黄酮化合物进行提取,优化了各种提取条件。然后,将提取的总黄酮化合物进行体外清除羟基自由基与超氧阴离子自由基能力的研究,并与L-抗坏血酸抗氧化性能进行比较,从而可知,红枣的抗氧化性能力,为判断红枣的品质提供科学依据。
1 材料与方法
1.1 材料与仪器
红枣(市售);芦丁,L-抗坏血酸(Vc),国药集团化学试剂有限公司(上海);邻二氮菲、邻苯三酚、过氧化氢、硫酸亚铁、磷酸氢二钠、Tris(三羟甲基氨基甲烷)、磷酸二氢钠、氢氧化钠及无水乙醇、AlCl3、KAc:均为市售国产分析纯试剂;二次蒸馏水。超声波提取仪HK-100B:杭州汇尔仪器公司;UV紫外-可见分光光度计:北京普析通用仪器公司;TG328A电光分析天平:上海第二天平仪器厂。
1.2 实验方法
1.2.1 样品处理:红枣洗净去核,切片,粉碎后,备用。称取枣粉20.0g两份,分别加入100mL 60%的乙醇,在超声功率为90W、温度为50℃下提取50min;抽滤2次,取滤液,再加入0.5g活性炭,抽滤,取滤液,最后减压蒸馏、浓缩。树脂纯化:把红枣黄酮浓缩液用D101树脂纯化。收集纯化提取液,再减压浓缩、真空干燥乙醇定容到50mL。
1.2.2 提取总黄酮含量的测定
1.2.2.1 最大吸收波长确定
准确称取芦丁标准样品2.5mg于25mL容量瓶中,加入30%乙醇稀释至刻度,得芦丁标准溶液(0.10mg/mL)。准确移取1.0mL于10mL容量瓶,分别加入0.1mol/L AlCl3溶液2mL,1.0mol/L KAc溶液3mL,振荡摇均,静置6min后,并加入30%乙醇至刻度,摇均后在420~540nm范围内进行光谱扫描,测得其最大吸收波长为510nm。
1.2.2.2 标准曲线制备
分别移取标准芦丁溶液0.1、0.2、0.3、0.4、0.6、0.8、1.0mL 置于 10mL 的容量瓶中,分别加入 0.1mol/L AlCl3溶液2mL,1.0mol/L KAc溶液3mL,振荡摇均,静置6min后,以30%乙醇稀释至刻度,摇均。在510nm波长处测定吸光度,得回归方程为 Y=0.1020x+0.0468,R=0.993。
1.2.2.3 样品测定
称取20.0g红枣粉于250mL烧杯中,按实验方法1.2.1处理后,并对总黄酮含量进行测定,结果为12.43mg/g(n=5),相对标准偏差为4.2%。
1.2.3 受试物溶液的配置
分别以无水乙醇溶配制六个不同浓度的提取物。六个10mL棕色容量瓶中分别加入0.2、0.4、0.6、0.8、1.0、1.2mL提取的总黄酮类化合物,再用二次蒸馏水定容致10mL,混合均匀,备用。然后,准确称取样品Vc25mg用无水乙醇溶解定容至25mL,适当稀释至所需浓度。
1.2.4 抗氧化性实验
1.2.4.1 清除羟基自由基能力
在清除羟基自由基能力的实验中,我们采用Fenton反应。其流程如下:在10mL棕色瓶中,分别加入用无水乙醇配制的 1.0mL 5mmol·L-1邻二氮菲溶液,0.5mL 磷酸缓冲溶液(pH7.4),0.2mL 0.1% 的 H2O2溶液和1.0mL 5mmol·L-1的FeSO4,然后,加入2.0mL配制好的不同浓度的提取物,37℃下加热30min后,测定在510nm处的吸光度Ai,同时测定无提取物的吸光度A。得到实验结果按下列式子计算提取物的羟基自由基清除能力(Scavenging activity,SA(%))。

1.2.4.2 清除超氧阴离子自由基能力
在清除超氧阴离子自由基能力的实验中,我们利用邻苯三酚自氧化反应。首先,在不同比色管中分别加入5.0mL Tris-HCl缓冲溶液中(pH8.2)和2.0mL 不同浓度提取物。然后,加入用0.01mmol·L-1HCl配制的0.5mL邻苯三酚(5.0mmol·L-1)溶液,充分混合。选定320nm为测定波长,每间隔30s,连续测定20次,通过吸光度随时间变化,计算的速率k1。同样,计算无提取物的速率k0,结果按下式计算提取物清除超氧阴离子自由基的能力。

2 结果与讨论
2.1 提取条件的优化
2.1.1 提取溶剂的选择:
准确称取各20.0g红枣粉末,采用超声波辅助提取方法,并优化超声波提取方法的各种影响因素(提取时间、温度、溶剂)。在超声波辅助提取法下,选用无水乙醇、60%乙醇,热水三种溶剂对红枣粉末进行有效提取。经过实验表明,采用60%乙醇提取的总黄酮量效果最高,其测定总黄酮化合物的含量为12.43mg/g,而无水乙醇与热水溶剂提取的总黄酮类化合物仅分别为9.78mg/g和5.26mg/g。因此,实验选择60%乙醇为超声波辅助提取方法的提取溶剂。
2.1.2 提取温度的选择
实验以60%乙醇为提取剂的条件,考察了在40℃、50℃、60℃、70℃、80℃五种不同温度的提取效率,结果如图1所示:当温度达到60℃时,提取效率达到最大,温度再升高基本保持不变。
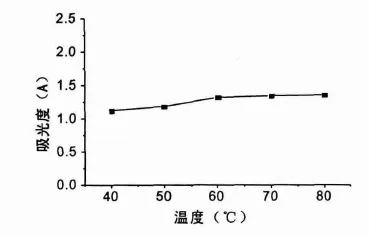
图1 温度对总黄酮化合物的影响
2.1.3 提取时间的选择
在以60%乙醇为提取剂与提取温度为60℃的实验条件,考察了提取时间的影响,结果发现,当提取时间达到50min,总黄酮化合物的含量基本没有变化,实验选择了提取时间为50min。
2.2 清除自由基的能力
2.2.1 清除羟基自由基能力
按照实验1.2.4.1方法进行清除羟基自由基的能力试验,从图2中可以看出,随着提取物浓度的增大,总黄酮提取物溶液对清除羟基自由基的能力在不断加强,与相同浓度Vc清除羟基自由基能力相比较,其清除能力略低。然而,红枣总黄酮提取物具有一定的抗清除羟基自由基能力。

图2 总黄酮提取物与Vc的清除羟基自由基能力
2.2.2 对超氧阴离子自由基清除能力
按照实验1.2.4.2方法比较了红枣提取的总黄酮类化合物与Vc对超氧阴离子自由基清除能力。实验结果表明(图3),随着红枣总黄酮提取物的浓度的不断增加,总黄酮提取物溶液对超氧阴离子自由基清除能力也在不断提高。清除超氧阴离子自由基清除能力与相同浓度的Vc比较,其清除能力有一定的下降。

图3 总黄酮提取物与Vc的清除超氧阴离子自由基能力
3 结论
利用超声波辅助提取法提取红枣中总黄酮类化合物,并优化提取条件,在最佳的提取条件下得到的总黄酮类化合物进行体外清除羟基自由基与超氧阴离子自由基能力,并与Vc的抗氧化性能比较。结果发现红枣总黄酮提取物具有一定的抗氧化能力,具有良好开发价值。
[1]张春兰,张锐利,熊素英,张建花,张娜,侯旭杰.超声波辅助提取红枣核中总黄酮的研究[J].安徽农业科学,2010,(12):6503-6505.
[2]霍文兰,刘步明,曹艳萍.陕北红枣总黄酮提取及其抗氧化性研究[J].食品科技,2006,(10):45-47.
[3]张平平,李黎,张东东,刘金福.金丝新4号枣果中黄酮类物质提取及纯化工艺的研究[J].食品与机械,2009,(6):75-79.
[4]陈宗保,郑大贵,叶青.微波辅助提取葛粉总黄酮及体外抗氧化性研究[J].食品科技,2009,(8):131-134.
[5]李铭芳,席峰,李清龙.红枣中生物黄酮的提取及分析方法研究[J].江西农业大学学报,2009,(6):1156-1159.
[6]樊海燕,赛音.广枣中黄酮类化合物提取工艺研究[J].内蒙古大学学报,2005,(1):81-83.
[7]张德权,台建祥,付勤.生物类黄酮的研究及应用概况[J].食品与发酵工业,1999,(25):52-57.
[8]Ferreira J F,Luthria D L,Sasaki T L.Flavonoids from artemisia annua L.as antioxidants and their potential synergism with artemisinin against malaria and cancer[J].Molecules,2010,(15):3135 -3170.
