分子印迹聚合物对林可霉素的静态吸附
2015-04-10张佑红钟季良李卫朋谌颉陈艳荣广健
张佑红,钟季良,李卫朋,谌颉,陈艳,荣广健
武汉工程大学化工与制药学院,湖北 武汉 430074
分子印迹聚合物对林可霉素的静态吸附
张佑红,钟季良,李卫朋,谌颉,陈艳,荣广健
武汉工程大学化工与制药学院,湖北 武汉 430074
采用二步溶胀法制备了林可霉素分子印迹聚合物,并通过静态吸附实验,考察了其吸附等温线,吸附动力学特性和吸附扩散过程.对所得实验数据进行分析,同时,对分子印迹聚合物的吸附性能进行了评价.结果表明:分子印迹聚合物的吸附等温线可以用朗缪尔方程进行较好的拟合,相关系数可达0.995 6;分子印迹聚合物的吸附动力学过程可以用准二级模型进行很好的描述,其相关系数可达0.999 2.内扩散模型拟合结果为分段的直线,说明吸附过程受多种作用力的影响.林可霉素分子印迹聚合物吸附容量较高,可达83.08 mg/g;结合过程很快,在非极性环境中80 min可达吸附平衡.制备的分子印迹聚合物是一种性能优良的新型吸附剂,可以成功地应用于吸附分离液体中的林可霉素.
分子印迹聚合物;林可霉素;静态吸附;动力学
0 引言
林可霉素是一类高效广谱的抗生素,它对革兰氏阳性菌和支原体有较强的抗菌和抑制作用,并具有抗菌谱广、抗菌力强、毒性低、给药方便等优点,因此在医药方面有着重要的应用[1].我国林可霉素提取方法为溶剂萃取法,此法原理简单,应用较为普遍,但存在着工艺流程复杂、消耗多、成本高等问题[2],因而设计一种高效简便的林可霉素分离方法具有重要意义.分子印迹聚合物[3]是一种具有特异空间结构和结合位点的新型高分子聚合物,对目标分子的选择性和识别性很高,适用于从混合体系中分离某种特定的成分,在化工、医药、环境和生物等领域得到了广泛的应用[4-9].
本实验在课题组以往的研究基础之上[10],以林可霉素为模板分子,聚苯乙烯微球为种球,选用二步溶胀聚合法[11],制备出了一种对林可霉素具有特异识别性的分子印迹聚合物,并研究了该聚合物对林可霉素的静态吸附行为.此研究对于以分子印迹聚合物作为吸附剂的研制与工业应用具有一定的理论和现实意义.
1 实验部分
1.1 试剂与仪器
盐酸林可霉素(工业级,南阳普康药业有限公司);二甲基丙烯酸乙二醇酯(分析纯,上海嘉辰化工有限公司);聚乙烯吡咯烷酮、三氟甲基丙烯酸(分析纯,上海阿拉丁试剂有限公司);十二烷基硫酸钠(分析纯,天津市博迪化工有限公司);聚乙烯醇(进口分装);苯乙烯、α-甲基丙烯酸、丙烯酰胺、偶氮二异丁腈、邻苯二甲酸二丁酯等其他试剂均为分析纯(国药集团化学试剂有限公司).
1260高效液相色谱仪(安捷伦科技有限公司),SXT-06索式提取器(上海洪纪仪器设备有限公司);HZQ-X100恒温振荡培养箱(金坛市杰瑞尔电器有限公司).
1.2 印迹聚合物的合成
1.2.1 聚苯乙烯微球制备量取50 mL乙醇和苯乙烯于100 mL锥形瓶中,加入1 g聚乙烯吡咯烷酮和0.2 g偶氮二异丁腈,在冰浴环境中于200 W超声10 min,然后将所得乳液转入四口瓶中,在氮气保护下,于70℃,200 r/min的搅拌速度下反应24 h.反应结束后,冷却至室温,离心除去上清液,将获得的聚苯乙烯微球反复洗涤干燥后备用.
1.2.2 林可霉素分子印迹聚合物的制备称取1 g聚苯乙烯微球和0.2 g十二烷基硫酸钠加入到30 mL超纯水中,于400 W超声15 min,将形成的悬浊液加入四口瓶中,在室温下以150 r/min的速度搅拌;称取0.1 g偶氮二异丁腈,0.5 mL邻苯二甲酸二丁酯,1 mL甲苯加入到30 mL超纯水中,于150 W超声5 min形成乳浊液,加入上述四口瓶中,在室温下搅拌溶胀24 h.0.461 g林可霉素,0.52 g甲基丙烯酸,4.96 g二甲基丙烯酸乙二醇酯,0.4 g聚乙烯醇,0.1 g十二烷基硫酸钠,5 mL正辛醇,10 mL氯仿加入到40 mL超纯水中,于400 w超声15 min形成乳浊液,加入上述四口瓶中继续搅拌溶胀24 h.称取0.2 g聚乙烯醇溶于20 mL超纯水,于400 W超声10 min,加入上述四口瓶中,升温至70℃,在氮气保护下反应24 h.混合物离心分离得到粒状聚合物,将其置于索式提取器内,以比例为9∶1的甲醇-乙酸混合液为溶剂清洗24 h以除去模板分子,然后再以纯甲醇继续洗涤5 h除去多余的乙酸,最后用超纯水离心洗涤除去甲醇,真空干燥备用.非印迹聚合物作为对照,制备时除了不加入林可霉素以外,其他方法与上述相同.
1.3 林可霉素吸附实验
称取50 mg的分子印迹聚合物于50 mL锥形瓶中,加入一定浓度的林可霉素溶液10 mL,用保鲜膜封口,在室温下以150 r/min恒温振荡.从聚合物接触溶液瞬间开始计时,在特定时间以注射器抽取该混合物以孔径0.45 μm微膜过滤,在214 nm处通过高效液相色谱仪测定滤液吸收峰,根据标准曲线测定其中林可霉素浓度.采用式(1)计算印迹聚合物吸附量:
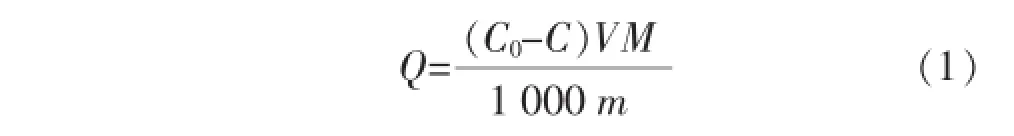
式中,Q为印迹聚合物的总吸附量(mg/g);C0为原林可霉素溶液的浓度(mmol/L);C为所测滤液中林可霉素的浓度(mmol/L);V为原林可霉素溶液的体积,mL;m为加入印迹聚合物的质量,g;M为林可霉素摩尔质量,g/mol.
1.4 分子印迹聚合物吸附机理分析
选用了Langmuir与Freundlich等温吸附模型[12]对印迹聚合物吸附行为进行了分析,其方程式分别如下所示.
Langmuir方程式为:
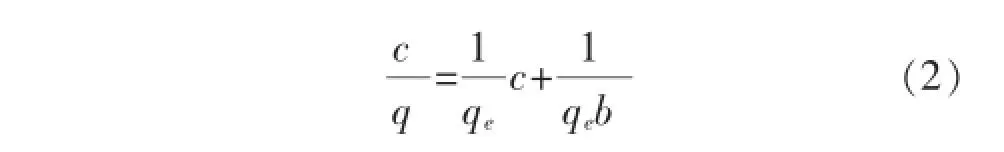
Freundlich方程式为:
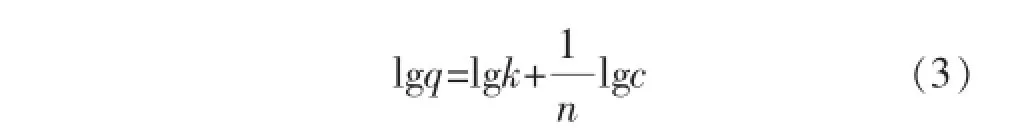
采用了准一级[13]、准二级[14]与内扩散吸附动力学[15]模型,对林可霉素分子印迹聚合物吸附动力学的实验数据进行了关联,其方程式分别如下所示.
准一级动力学方程式为:
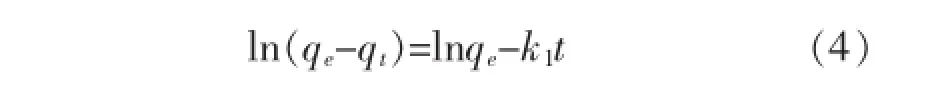
准二级动力学方程式为:
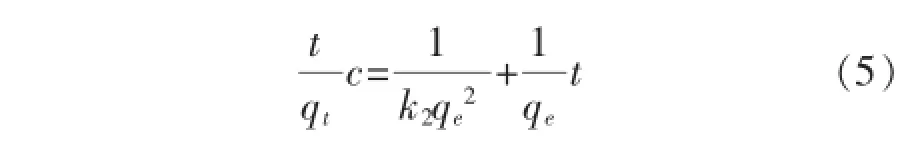
内扩散方程式为:
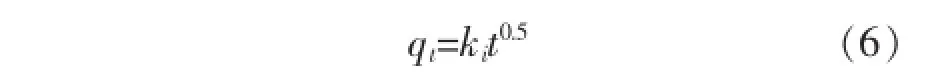
主要参数如表1所示.
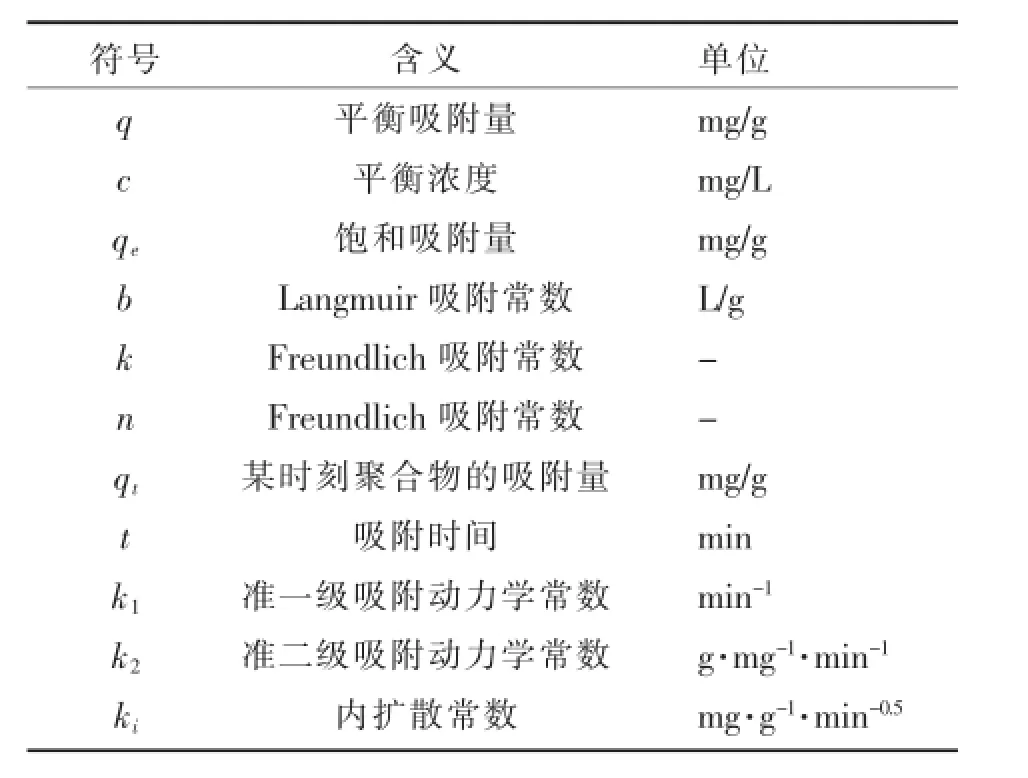
表1 吸附主要参数Table 1 Main parameters of adsorption
2 结果与讨论
2.1 吸附等温线与模型关联
在以氯仿为溶剂,温度为25℃的条件下,以平衡吸附量q对平衡浓度c作等温吸附图,结果如图1所示.由图可知,印迹聚合物与非印迹聚合物对林可霉素的吸附量都随着林可霉素的平衡浓度增加而增加,但前者要明显高于后者,说明在聚合物的合成过程中,印迹聚合物中形成了特异性结合位点,对林可霉素具有较高的吸附能力;而非分子印迹聚合物则不具备这种位点,对林可霉素的吸附是非特异性的,因而其吸附量低于分子印迹聚合物.
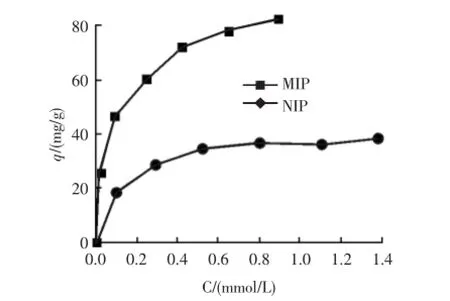
图1 分子印迹聚合物和非印迹聚合物的吸附等温线Fig.1 Adsorption isotherm of MIP and NIP
根据式(2)和式(3),以c/q为纵坐标,对平衡浓度c做线性拟合图;以lgq为纵坐标,对lgc做线性拟合图,结果如图2所示.拟合数据见表2.
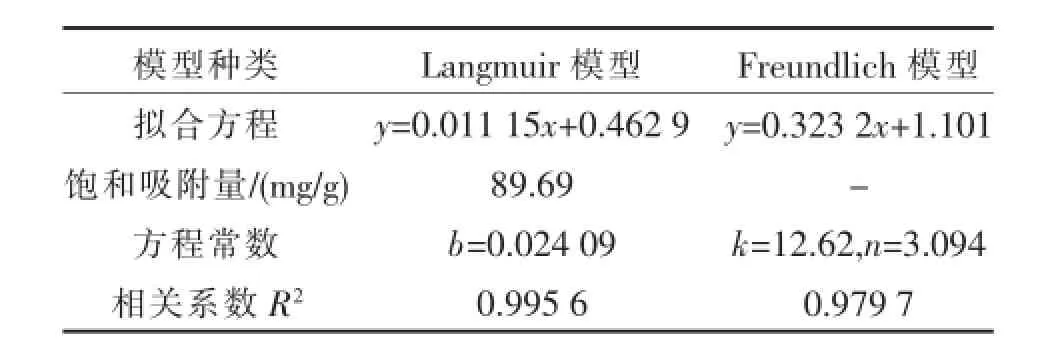
表2 Langmuir模型与Freundlich模型的拟合结果Table 2 Fitting results by Langmuir and Freundlich adsorption isotherm models
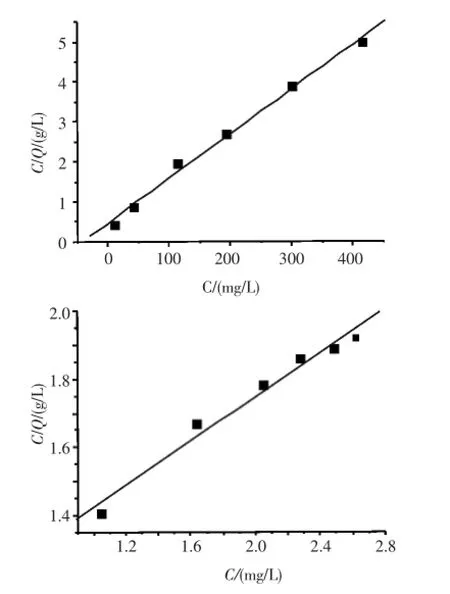
图2 Langmuir与Freundlich方程关联的吸附等温线拟合图Fig.2 Linear fit of adsorption isotherm by Langmuir and Freundlich equation
由拟合结果得知,Langmuir模型计算得出的饱和吸附量为89.69 mg/g,与实验所测最大吸附值83.08 mg/g较为接近,说明关联效果较好,这是因为分子印迹聚合物中的结合位点具有专一吸附的能力,每个位点仅和一个林可霉素分子结合,比较符合Langmuir模型的单分子层吸附理论;所得总吸附平衡常数值略低,这是由于印迹聚合物中的结合位点并非绝对等价,其中存在的少数非特异性结合位点,降低了其对林可霉素分子亲和力的原因所致.Freundlich模型计算所得1/n值为0.323 2,说明印迹聚合物对林可霉素的结合力较强,吸附性能很好,单位质量浓度吸附量为12.62 mg/g.两者相关系数相比,Langmuir模型要优于Freundlich模型,表明Langmuir模型对实验结果的关联程度更高,可以更为准确地描述林可霉素在印迹聚合物上的吸附过程.
2.2 动力学曲线分析与模型关联
在林可霉素浓度为2 mmol/L,温度为25℃的条件下,以吸附量qt对时间t作图,结果如图3所示.由图可知,当氯仿为溶剂时,分子印迹聚合物的吸附量在前20 min内迅速升高,表明印迹聚合物对林可霉素的结合是一个快速进行的过程,吸附能力很强;当选用正丁醇、乙酸乙酯等含有羟基、羰基等官能团的极性溶剂时,动力学曲线则变得较为平缓,这说明林可霉素分子在印迹聚合物上的吸附过程受到了一定的影响,因而非极性环境更加有利于林可霉素的吸附.
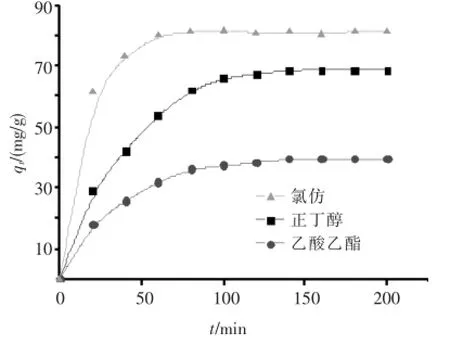
图3 分子印迹聚合物的吸附动力学曲线Fig.3 Adsorption kinetic curves of MIP
选用溶剂为氯仿时的实验数据,根据式(4)和式(5),分别以ln(qe-q)与t/q为纵坐标,吸附时间t为横坐标作线性拟合图,结果如图4所示.由图可知,准一级吸附模型对实验数据的拟合结果一般,并且随着浓度的增加,实验数据偏离直线的情况越来越明显,故准一级吸附动力学方程并不能对印迹聚合物的吸附过程做出较好的描述.而准二级吸附模型的拟合图像表现出良好的线性关系,其相关系数R2为0.999 2,由斜率计算得到的饱和吸附量为83.13 mg/g,这与实验值比较接近,说明准二级动力学模型可对印迹聚合物的吸附过程做出较为准确的描述.根据式(6)作q~t0.5图,结果如图5所示.图中的曲线分成了三个部分,开始0~20 min内扩散速率常数ki=13.72 mg·g-1·min-0.5,图线斜率较高,说明内扩散过程进行得较快,液膜扩散、表面吸附等外扩散过程发挥着主要作用;第二阶段20~80 min内扩散速率常数ki=5.68 mg·g-1·min-0.5,此时吸附过程主要集中在颗粒内扩散.第三阶段80~200 min曲线趋于水平,表明吸附已达平衡.
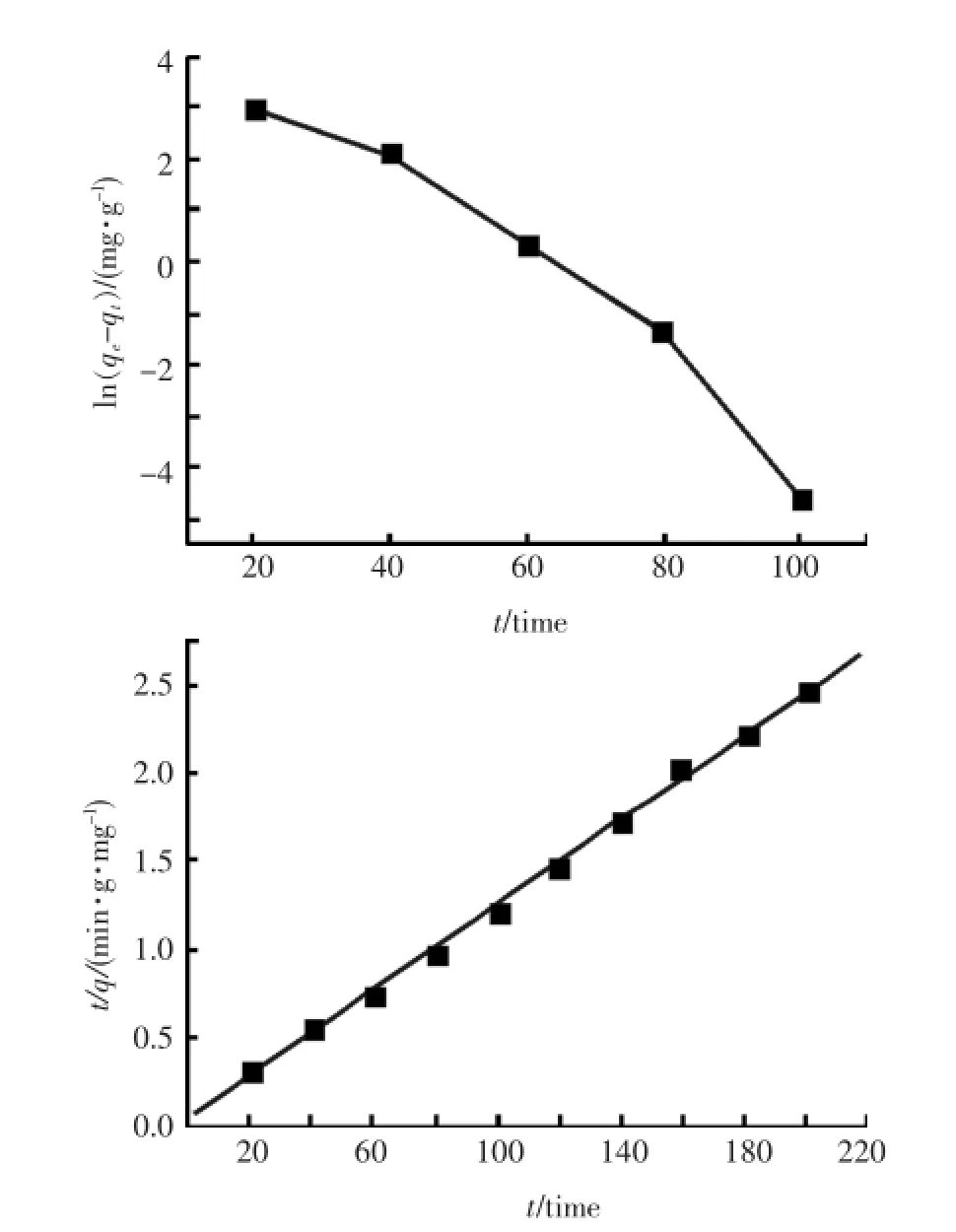
图4 准一级与准二级动力学模型的拟合图Fig.4 Linear fit of the pseudo first order kinetic model and pseudo second order kinetic model
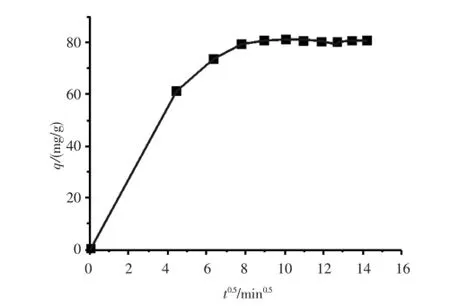
图5 内扩散模型的拟合图Fig.5 Fitting result of the internal diffusion model
3 结语
在室温下分子印迹聚合物可以有效地吸附林可霉素,吸附容量可达83.08 mg/g,其等温吸附曲线可用Langmuir模型进行很好的描述.聚合物的吸附过程进行得很快,但受溶剂极性影响较明显,在低极性溶剂中效果较优,80 min即达吸附平衡.吸附动力学行为可用准二级动力学方程进行很好的描述,吸附过程受液膜扩散、表面吸附和颗粒内扩散等多种作用力的共同影响.研究结果表明,林可霉素分子印迹聚合物是一种性能优良的吸附剂,对于工业生产中林可霉素的分离提纯有着重要的意义.今后的研究应对吸附机理作进一步的深入探讨,建立更为精确的数学模型,为其实际应用奠定理论基础.
致谢
感谢武汉工程大学化工与制药学院发表的《林可霉素A分子印迹聚合物微球的制备及性能》作者的前期工作,同时对河南南阳普康药业有限公司的支持深表感谢!
[1]郑学丽.林可霉素提炼工艺进展[J].河北化工,2003(5):12-13.
ZHENG Xue-li.Progress in Lincomycin hydrochloride purification process[J].Hebei Chemical Industry,2003(5):12-13(in Chinese).
[2]周倜,亓平言,苗勇,等.林可霉素提取过程生产现状和研究进展[J].国外医药抗生素分册,1999,20(2):61-63.
ZHOU T,QI P Y,MIAO Y,et al.A review on Lincomycin extraction process[J].World Notes on Antibiotics,1999,20(2):61-63(in Chinese).
[3]BAGGIANI C,GIOVANNOLI C,ANFOSSI L,et al.A connection between the binding properties of imprinted and nonimprinted polymers:a change of perspective in molecular imprinting[J].Journal of the American Chemical Society,2012,134(3):1513-1518.
[4]HELLING S,SHINDE S,BROSSERON F,et al.Ultratrace enrichment of tyrosine phosphorylated peptides on an imprinted polymer[J].Analytical Chemistry,2011,83(5):1862-1865.
[5]ZHAO Y,SHEN Y M,BAI L,et al.Synthesis and CO2 adsorption properties of molecularly imprinted adsorbents[J].Environmental Science and Technology,2012,46(3):1789-1795.
[6]HERRERO E P,VALLE E M,PEPPAS N A.Protein imprinting by means of alginate-based polymer microcapsules[J].Industrial and Engineering Chemistry Research,2010,49(20):9811-9814.
[7]PEETERS M,TROOST F J,MINGELS R H,et al.Impedimetric detection of histamine in bowel fluids using synthetic receptors with ph-optimized binding characteristics[J].Analytical Chemistry,2013,85(3):1475-1483.
[8]MINAMI K,IHARA M,KURODA S,et al.Open-sandwich molecular imprinting:making a recognition matrix with antigen-imprinted antibody fragments[J].Bioconjugate Chemistry,2012,23(7):1463-1469.
[9]KRYSCIO D R,SHI Y,REN P Y,et al.Molecular docking simulations for macromolecularly imprinted polymers[J].Industrial and Engineering Chemistry Research,2011,50(24):13877-13884.
[10]蒋兴娜,李卫朋,张佑红,等.林可霉素A分子印迹聚合物微球的制备及性能[J].武汉工程大学学报,2012,34(5):16-19.
JIANG X N,LI W P,ZHANG Y H,et al.Preparation and properties of lincomycin A molecularly imprinted polymer microspheres[J].Journal of Wuhan Institute of Technology,2012,34(5):16-19.(in Chinese).
[11]MASANORI N,MASAKI O,TASHIAKI N,et al.U-niformly sized molecularly imprinted polymer for atropine and its application to the determination of atropine and scopolamine in pharmaceutical preparations containing Scopolia extract[J].Journal of Pharmaceutical and Biomedical Analysis,2005,37(2):231-237.
[12]DERVANOSKI A,SOUZA S G,LUZ C D,et al.Multicomponent adsorption and desorption of btx compounds using coconut shell activated carbon:experiments,mathematical modeling,and numerical simulation[J].Industrial and Engineering Chemistry Research,2013,52(23):7895-7911.
[13]CHANG R L,HUI S K,IN H J,et al.Pseudo firstorder adsorption kinetics of n719 dye on tio2 surface[J].Applied Material Interfaces,2011,3(6):1953-1957.
[14]CALERO M,BLAZQUEZ G,MARTIN M A.Kinetic modeling of the biosorption of lead(ii)from aqueous solutions by solid waste resulting from the olive oil production[J].Journal of Chemical and Engineering Data,2011,56(7):3053-3060.
[15]KHALED A,NEMR A E,EL-SIKAILY A,et al.Remove of direct n blue-106 from artificial textile dye effluent using activated carbon from orange peel:adsorption isotherm and kinetic studies[J].Journal of Hazardous Materials,2009,165(1/2/3):100-110.
Static adsorption of molecularly imprinted polymer to Lincomycin
ZHANG You-hong,ZHONG Ji-liang,LI Wei-peng,CHEN Jie,CHEN Yan,RONG Guang-jian
School of Chemical Engineering and Pharmacy,Wuhan Institute of Technology,Wuhan 430074,China
Lincomycin molecular imprinted polymer was prepared by two-step swelling polymerization.The adsorption isothermal,adsorption kinetics and the diffusion process of molecularly imprinted polymer were investigated,and the adsorption properties of imprinted polymer were discussed by analyzing experiment data.The results show that the adsorption isothermal and the kinetics of imprinted ploymer are well fitted by Langmuir model and pseudo-second-order equation,whose regression coefficients are 0.995 6 and 0.999 2,respectively.The fitting result of internal diffusion model shows a segmented straight line,which indicates that the adsorption process is affected by a variety of forces.Lincomycin molecularly imprinted polymer has good adsorption capacity of 83.08 mg/g and rapid adsorption equilibrium within 80 min in non-polarity environment.The prepared molecularly imprinted polymer can be successfully applied to the separation of lincomycin in solution,as a new adsorption material with excellent performance.
molecularly imprinted polymer;lincomycin;static adsorption;kinetics
TQ317.3
A
10.3969/j.issn.1674-2869.2015.06.003
1674-2869(2015)06-0010-05
本文编辑:张瑞
2015-4-7
张佑红(1964-),男,湖南浏阳人,教授,博士,博士研究生导师.研究方向:细胞生物学、分子生物学.
