陶瓷膜反应器用于氯化亚铜催化剂的制备
2015-04-01饶辉张峰仲兆祥邢卫红金万勤
饶辉,张峰,仲兆祥,邢卫红,金万勤
(南京工业大学膜科学技术研究所,国家特种分离膜工程技术研究中心,江苏 南京 210009)
引言
二甲基二氯硅烷(M2)是合成有机硅材料的重要原料,工业上主要采用直接法生产M2[1-2],如何提高催化剂的活性从而获得更高的M2选择性和硅粉转化率一直是有机硅单体合成的研究重点[3-5]。
氯化亚铜是直接法生产 M2常用的催化剂之一,大量的研究表明氯化亚铜的表面形貌和粒径分布对催化剂活性有着重要的影响,且催化剂的粒径小、分布均一以及形貌规整的催化剂活性较高[6],如 Chen等[7]通过溶剂热法制得三角树枝状氯化亚铜颗粒,使用该氯化亚铜催化剂制备 M2,其催化性能优于商业氯化亚铜,表现为M2的选择性提高9.1%,硅粉的转化率提高8.9%。目前,粒径小、分布均一和形貌规整的氯化亚铜颗粒的制备方法主要是溶剂热法,但该方法存在一些问题,例如制备过程高温高压、能耗大、耗时长以及需要大量有机溶剂[8-9]。直接沉淀法是目前工业上制备氯化亚铜的常用方法,该方法具有过程简单、原料易得和易放大等优点[10-11]。但直接沉淀法制备氯化亚铜的过程中氯化亚铜晶体的生长易受到局部过饱和度的影响,难以形成粒径和形貌均一的颗粒[12]。
将膜技术与沉淀反应耦合,用于均匀颗粒的制备已有大量的研究工作,如李敏等[13]利用管式微反应器,制备了平均粒径约为2.5 μm的碳酸钙球形颗粒;Jia等[14]用管壳式中空纤维膜分散法制备出了粒径约为70 nm的硫酸钡颗粒。陶瓷膜具有优异的化学稳定性和较窄的孔径分布,在压差作用下,利用陶瓷膜孔将反应液均匀加入反应器中,从而抑制反应体系的局部过饱和现象,实现反应液快速高效的分散混合,提高反应效率。陶瓷膜反应器在加氢、氧化、沉淀等过程中已展示出良好的应用前景[15-16]。Jiang等[17]将陶瓷膜分散双氧水,用于苯二酚的制备过程,提高了反应的选择性和转化率;许志龙[18]将陶瓷膜与沉淀反应相结合,制备出平均粒径为3 μm的花瓣状纳米氧化锌团聚体,其光催化性能较商品化的二氧化钛P25提高了19%。目前尚没有将膜技术用于氯化亚铜颗粒的制备,另外氯化亚铜形貌与粒径对 M2的选择性和转化率的影响研究报道也不多。
因此,本文采用陶瓷膜反应器制备氯化亚铜催化剂,考察陶瓷膜孔径、稳定剂、进料速率和进料浓度等对 CuCl粒径和形貌的影响,从而制备出不同形貌和粒径的催化剂,通过二甲基二氯硅烷合成反应表征 CuCl颗粒的催化性能,以期获得高催化活性的氯化亚铜催化剂。
1 实验部分
1.1 试剂及仪器
五水硫酸铜(CuSO4·5H2O),分析纯,上海新宝精细化工厂;氯化钠(NaCl),分析纯,西陇化工股份有限公司;亚硫酸钠(Na2SO3),分析纯,国药集团化学试剂有限公司;聚乙烯吡咯烷酮,分析纯,国药集团化学试剂有限公司;硅粉,平均粒径 200 μm,江苏茂源进出口有限公司;氯甲烷,99.99%,上海亚帅特种气体有限公司;陶瓷膜,江苏久吾高科技股份有限公司;高压输液泵,UC-3281型,北京优联光电技术有限公司;恒温加热磁力搅拌器,KEMS-GS190·90,南京科尔仪器设备有限公司。
1.2 实验过程与表征方法
1.2.1 氯化亚铜的制备过程 陶瓷膜反应器为课题组自建装置,详细装置介绍见文献[18],连续相为CuSO4、NaCl和稳定剂的混合溶液,分散相为Na2SO3和稳定剂的混合溶液,稳定剂在连续相和分散相中的浓度相同,并且3种反应物的物质的量比例关系为:m(CuSO4)∶m(NaCl)∶m(Na2SO3)= 1∶1.1∶0.65。Na2SO3通过计量泵以一定的进料速率通入到陶瓷膜管中,通过陶瓷膜孔分散到连续相中,利用恒温加热磁力搅拌器控制反应温度,使反应温度为 85℃,无搅拌。反应时间为90 min,包括进料反应时间和进料结束后的反应陈化时间。产物通过抽滤、去离子水洗涤和无水乙醇洗涤后,放入80℃的真空干燥箱中干燥2 h,得到氯化亚铜颗粒。
1.2.2 氯化亚铜的微观结构表征 实验制备的氯化亚铜颗粒形貌通过日本日立公司的S4800型冷场发射扫描电镜(SEM)进行分析;氯化亚铜颗粒的结构使用日本理学XRD 6000型X射线衍射仪进行分析(XRD),Cu Kα射线(λ=0.15418 nm),扫描速度20(°)·min-1。氯化亚铜颗粒的粒径分布采用激光衍射粒度分析仪(Mastersizer3000, Malvern,Worcestershire, UK)测定。
1.2.3 氯化亚铜的催化性能表征 氯化亚铜颗粒的催化性能通过固定床反应器表征,实验装置流程如图1所示,主要由气源、质量流量控制器、固定床反应器、产物冷凝收集装置和尾气洗涤装置等构成。其中固定床反应器的加热部分由程序升温控制系统和铸铝套管构成,中间部分是长度为 550 mm、内径为13 mm玻璃反应管,距玻璃管底部65 mm处的玻璃内部镶有砂芯,砂芯起支撑触体(硅粉、催化剂和助催化剂)的作用。

图1 催化反应实验的装置流程图Fig.1 Schematic of catalysis experimental system
实验过程中触体由10 g硅粉、0.6 g氯化亚铜催化剂和0.1 g氧化锌组成。催化反应温度控制在330℃,气体流量为15 mg·min-1,反应时间为9 h。采用气相色谱(Shimadzu GC2014,日本)分析产物组成。M2选择性和硅粉转化率参照文献[19]的方式计算。
2 结果与讨论
2.1 分散相加入方式的影响
在Cu2+浓度为0.05 mol·L-1、分散相进料速率20 ml·min-1的条件下,考察了直接滴加、平均孔径为 4 μm 和平均孔径为 0.05 μm 陶瓷膜分散Na2SO3溶液对氯化亚铜颗粒形貌的影响,电镜照片、粒径分布和XRD分别如图2~图4所示。

图2 分散相加入方式对CuCl颗粒形貌的影响Fig.2 Influence of feeding method on morphology of cuprous chloride

图3 分散相加入方式对CuCl颗粒粒径分布的影响Fig.3 Particle size distribution under different feeding methods
从图2可以看出,3种加入方式制备的氯化亚铜均呈三角形,这是由于沉淀反应为扩散生长过程,生长过程中易聚结,形成三角形平面结构的大颗粒[20]。通过陶瓷膜分散Na2SO3溶液制备氯化亚铜,颗粒外形有明显的变化,团聚体的外形变小,小颗粒数量增多,这是因为通过膜孔分散Na2SO3溶液,液滴尺寸大大减小,传质过程得到强化,反应体系的过饱和度趋于均一,有利于一次性成核。由图3可见,3种颗粒的粒径分布均较宽,呈多峰分布。直接滴加制备的氯化亚铜平均粒径为 28.3 μm,而通过平均孔径为0.05 μm陶瓷膜加入Na2SO3溶液制备的氯化亚铜在3 μm处有个明显的分布峰,颗粒的平均粒径(D50)仅为8.6 μm。这是由于沉淀反应制备颗粒时,反应过程产生的晶体小颗粒会发生碰撞并聚结生长形成较大的颗粒,使得颗粒的粒径分布范围较宽,黄翠等[21]通过模型计算也得出相似的结果。
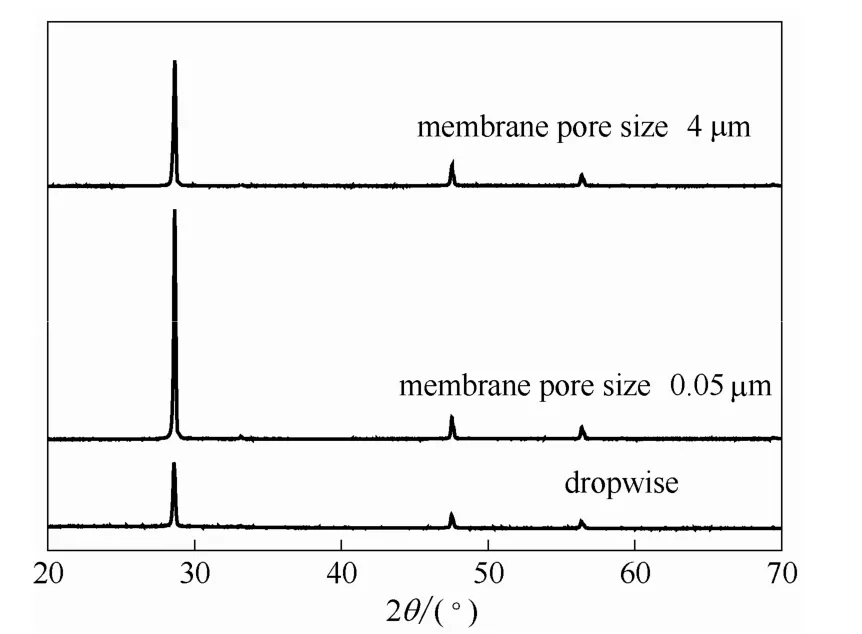
图4 不同分散相加入方式制得CuCl的XRDFig.4 XRD patterns of CuCl under different feeding methods
从图 4看出,3种加入方式制备的氯化亚铜XRD谱图衍射峰与标准谱图(JCPDS卡片号为6-344)的特征峰完全一致,表明得到的氯化亚铜具有立方晶型硫化锌结构,3个明显特征峰分别是28.5°、47.4°和56.3°,对应的晶面分别是111、220和311。孔径0.05 μm陶瓷膜分散Na2SO3溶液,制得的氯化亚铜的峰强度最大,颗粒的结晶度高。这是因为沉淀反应过程中会发生颗粒的聚结生长现象,大颗粒多为聚结体,降低了晶化程度,呈现出颗粒粒径增大,XRD峰强减小的现象。因此采用孔径为0.05 μm陶瓷膜分散Na2SO3溶液进行沉淀反应条件的优化。
2.2 稳定剂的种类对氯化亚铜颗粒的影响
通过加入非离子型稳定剂能在颗粒之间形成屏障,阻止颗粒的聚结是防止颗粒聚结生长常用的一种方法[22]。为进一步提高氯化亚铜颗粒形貌的规整度,在 Cu2+浓度为 0.05 mol·L-1、Na2SO3进料速率 20 ml·min-1和稳定剂的浓度为 1 μg·ml-1条件下,考察不同稳定剂对氯化亚铜颗粒形貌的影响。稳定剂分别为聚乙二醇(4000)、聚乙烯吡咯烷酮(PVP)和聚山梨酯(吐温80),结果如图5、图6所示。

图5 不同稳定剂制备的氯化亚铜颗粒的SEM图Fig.5 Influence of stabilizers on morphologies of CuCl
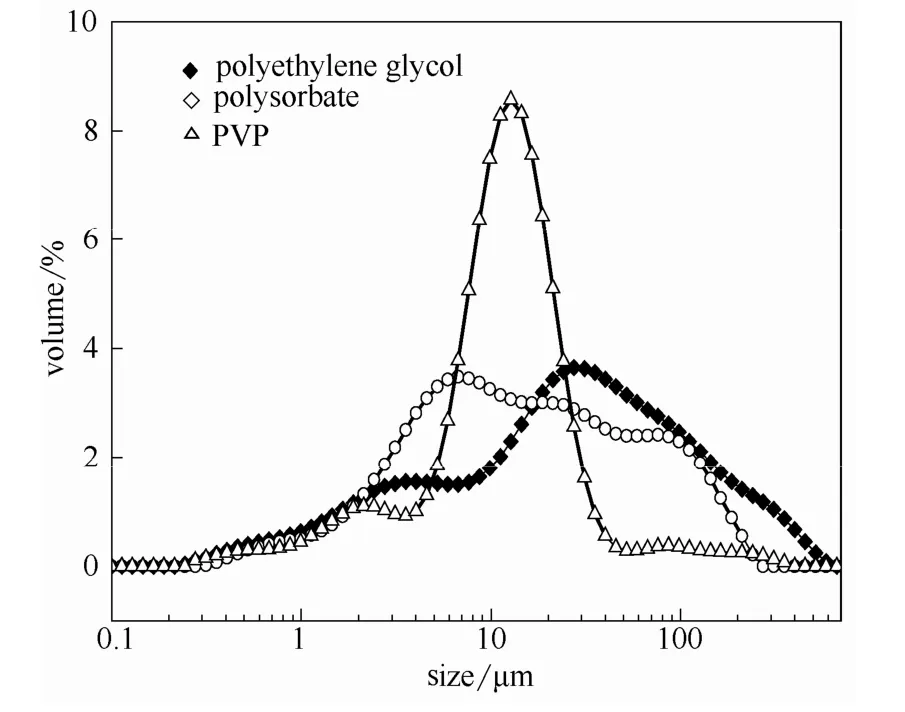
图6 不同稳定剂制得的氯化亚铜颗粒的粒径分布图Fig.6 Particle size distribution of CuCl under different stabilizers
从图5和图6可以看出,稳定剂对CuCl颗粒形貌和粒径分布影响显著,加入聚乙二醇(4000)、聚山梨酯得到的 CuCl颗粒主要呈三角形,粒径分布宽,平均粒径较大;加入PVP后得到的颗粒主要呈球形,大小比较均匀,该球形颗粒由许多纳米颗粒团聚而成,呈现单分散分布,平均粒径(D50)14.6 μm。这是因为 PVP分子具有较高的表面能,能够产生成核位置,使得CuCl的成核能力提高;另外,PVP分子中羰基(—CO)具有较高的极性能够和CuCl颗粒结合,促进CuCl小颗粒团聚形成大的球形颗粒[23]。
2.3 进料速率的影响
在 PVP浓度为 1 μg·ml-1,Cu2+浓度为 0.05 mol·L-1的条件下,考察了进料速率对氯化亚铜颗粒的影响,如图7、图8所示。

图7 进料速率对颗粒粒径的影响Fig.7 Particle size distribution of CuCl under different dispersed phase flow rates

图8 进料速率对氯化亚铜颗粒形貌的影响Fig8 Influence of dispersed phase flow rates onmorphologies of CuCl
从图7和图8可以看出,随着进料速率的增大,CuCl颗粒的平均粒径减小且颗粒均一性提高,当进料速率达到40 ml·min-1时,制备的氯化亚铜颗粒的平均粒径(D50)为8 μm。这主要是因为进料速率是由膜的操作压力控制的,进料速率增大,膜的操作压力也增大,促使分散相 Na2SO3溶液快速离开膜表面进入到反应体系中,反应体系的过饱和度趋于均一,颗粒的一次性成核数就越多,有效地把颗粒的成核阶段和生长阶段分开,从而使得颗粒的均一性提高[24]。
2.4 铜离子浓度对氯化亚铜颗粒的影响
在 PVP浓度为 1 μg·ml-1,进料速率 40 ml·min-1的条件下,考察铜离子浓度对CuCl颗粒的影响,如图9、图10所示。
由图9和图10可以看出,随着铜离子浓度增大,氯化亚铜颗粒平均粒径先减小后增大。这是由于反应物浓度升高,有利于体系形成较高的过饱和度,导致爆炸性成核,晶核的生成速率大于生长速率,有利于形成小颗粒沉淀。但随着反应物浓度的进一步提高,晶核的浓度与溶液之间存在一种平衡。晶核浓度增加,晶核之间有形成团聚体以降低表面能的趋势,使形成颗粒的粒径增大[25]。

图9 铜离子浓度对CuCl颗粒形貌的影响Fig.9 Influence of concentrations of Cu2+on morphologies of CuCl

图10 不同铜离子浓度得到的CuCl颗粒的粒径分布图Fig.10 Particle size distribution of CuCl under different concentrations of Cu2+
2.5 氯化亚铜催化性能的比较
实验选取4种自制CuCl颗粒以及购买的商业CuCl催化剂,通过直接法制备甲基氯硅烷的合成反应,考察5种催化剂的催化性能。结果见表1。自制的 4种氯化亚铜催化剂对 M2的选择性在94.0%~95.7%之间,远高于商业催化剂的74.9%,这是因为商业催化剂的粒径分布宽,呈多峰分布(图11),外形无规则(图12);自制催化剂粒径和形状对M2的选择性影响不大,但对硅粉转化率的影响较大,这是因为催化剂的粒径越小,越有利于形成硅铜合金,从而提高硅粉的转化率[26]。球形颗粒较三角形颗粒有更高的M2收率,这主要是由于球形颗粒的形貌规整,分散性高,能与硅粉形成更多的活性中心;而三角形颗粒的形貌不规整,分散性低,铜催化剂易聚集形成单质铜,导致催化剂失活。
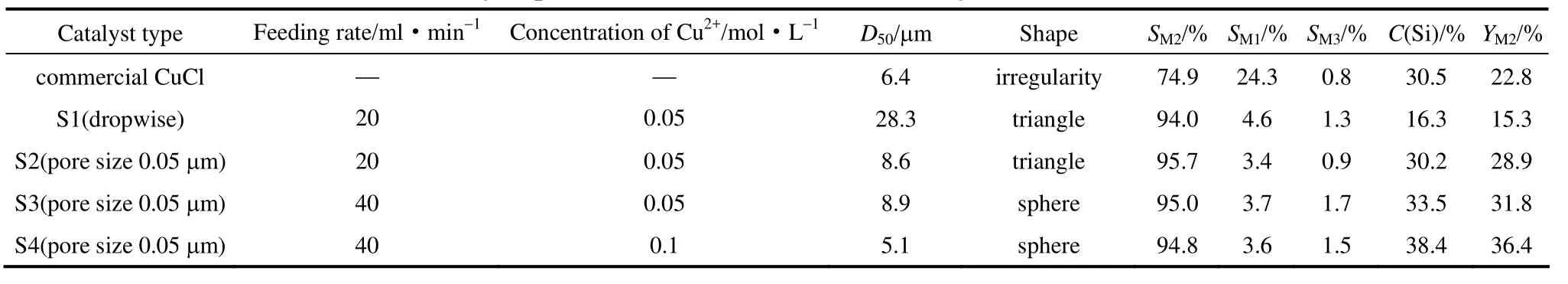
表1 几种催化剂的催化性能比较Table 1 Catalytic performance of various CuCl catalysts for Rochow reaction
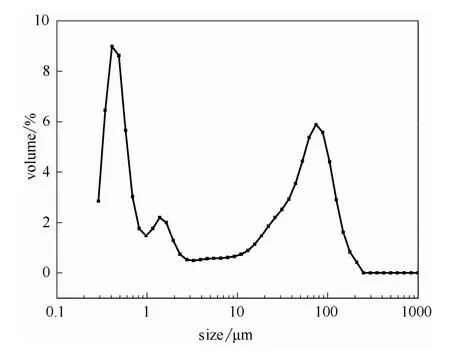
图11 商业CuCl催化剂的粒径分布Fig.11 Particle size distribution of commercial CuCl

图12 商业CuCl催化剂的SEM图Fig.12 SEM images of commercial CuCl
3 结 论
沉淀反应器与陶瓷膜耦合构成一体式膜反应器,制备出单分散形貌可控的氯化亚铜颗粒,陶瓷膜孔径与进料速率均会影响氯化亚铜颗粒尺寸,但不影响颗粒形状;稳定剂是控制催化剂形状的主要因素,PVP作为稳定剂可以制备出球形催化剂。随着膜通量的增大,CuCl颗粒的平均粒径减小且均一性提高;随着铜离子浓度增大,氯化亚铜颗粒平均粒径先减小后增大。在有机硅单体合成中,氯化亚铜粒径减小有利于提高催化活性,球形催化剂有利于提高硅粉转化率。将平均粒径为5.1 μm的单分散球形CuCl颗粒用于直接法制备有机硅单体的反应,M2的选择性和硅粉的转化率分别达到94%和38%,优于商业化氯化亚铜催化剂的性能。
符号说明
C(Si)——硅粉的转化率,%
D50——平均粒径或中位径,μm
SM1,SM2,SM3——分别表示M1、M2、M3的选择性,%
YM2——M2的产率,%
[1] Zhang Zhaogui(张招贵), Liu Feng(刘峰), Yu Zheng(余政). The Organic Silicon Compounds (有机硅化合物化学)[M]. Beijing:Chemical Industry Press, 2010.
[2] Zhu Xiaomin(朱晓敏), Zhang Jikai(章基凯). The Fundamentals of Organosilicon Material(有机硅材料基础)[M]. Beijing:Chemical Industry Press, 2013.
[3] Ward W J, Rizer A, Carroll K M,et al. Catalysis of the rochow direct process[J].Journal of Catalysis, 1986, 100(1):240-249.
[4] Brookes K H, Siddiqui M R H, Rong H M,et al. Effect of Al and Ca addition on the copper catalyzed formation of silanes from Si and CH3Cl[J].Applied Catalysis A:General, 2001, 206(2):257-265.
[5] Luo W X, Wang G R, Wang J F. Effect of CuCl particle size on the reduction reaction by silicon in preparation[J].Industrial &Engineering Chemistry Research, 2006, 45(1):129-133.
[6] Han Lu(韩琭), Luo Wuxi(罗务习), Liang Weihua(梁卫华),et al.Method and effect of catalyst dispersion in direct synthesis of DDS[J].Journal of Chemical Industry and Engineering(China)(化工学报),2003, 54(3):398-402.
[7] Chen X, Jia L H, Wang Y L. Solvothermal synthesis of copper(Ⅰ)chloride microcrystals with different morphologies as copper-based catalysts for dimethyldichlorosilane synthesis [J].Journal of Colloid and Interface Science, 2013, 404:16-23.
[8] Li Q, Shao M W, Yu G H. A solvent-reduction approach to tetrapod-like copper(Ⅰ) chloride crystallites [J].Journal of Materials Chemistry, 2003, 13(2):424-427.
[9] Xie T, Gong M, Niu Z Q. Shape-controlled CuCl crystallite catalysts for aniline coupling [J].Nano Research, 2010, 3(3):174-179.
[10] Liang Liwei(梁礼渭), Zeng Qingquan(曾清全), Xiong Weijiang(熊卫江). Preparation technology and prospect of cuprous chloride [J].Materials Research and Application(材料研究与应用), 2011, 5(4):296-299.
[11] Luo Wuxi(罗务习). Study on direct synthesis process of dimethyldichlorosilane monomer[D]. Beijing:Tsinghua University,2006.
[12] Jia Z Q, Liu Z Z. Membrane-dispersion reactor in homogeneous liquid process [J].Journal of Chemical Technology and Biotechnology,2013, 88(2):163-168.
[13] Li Min(李敏), Chen Jianfeng(陈建峰), Shao Lei(邵磊). Preparation of ultrafine calcium carbonate ultrafine particles using a novel tube-in-tube microreactor[J].Journal of Beijing University ofChemicalTechnology(北京化工大学学报), 2008, 35(3):14-18.
[14] Jia Z Q, Liu Z Z, He F. Synthesis of nanosized BaSO4and CaCO3particles with a membrane reactor:effects of additives on particles [J].Journal of Colloid and Interface Science,2003, 266(2):322-327.
[15] Chen R Z, Sun H L, Xing W H A. Submerged ceramic membrane reactor for thep-nitrophenol hydrogenation over nano-sized nickel catalysts [J].Journal of Nanoscience and Nanotechnology, 2009, 9(2):1470-1473.
[16] Luo H X, Wei Y Y, Jiang H Q. Performance of a ceramic membrane reactor with high oxygen flux Ta-containing perovskite for the partial oxidation of methane to syngas [J].Journal of Membrane Science,2010, 350(1/2):154-160.
[17] Jiang H, Meng L, Chen R Z,et al. A novel dual-membrane reactor for continuous heterogeneous oxidation catalysis [J].Industrial &Engineering Chemistry Research, 2011, 50(18), 10458-10464.
[18] Xu Zhilong(许志龙). Synthesis of nanostructured ZnO through a membrane dispersion reactor and the photocatalytic performance [D].Nanjing:Nanjing Tech University, 2014.
[19] Wu Junwei(武军伟), Xing Weihong(邢卫红), Zhang Feng(张峰),et al. Synthesis of dimethyldichlorosilane by the fluidized bed membrane reactor [J].CIESC Journal(化工学报), 2014, 65(7):2776-2784.
[20] Zhang Zhao(张昭), Peng Shaofang(彭少方), Liu Dongchang(刘栋昌).Inorganic Chemical Technology(无机精细化工工艺学) [M]. 2nd ed.Beijing:Chemical Industry Press, 2005.
[21] Huang Cui(黄翠), Wang Yujun(王玉军), Luo Guangsheng(骆广生).Preparation of nano-ZnO in membrane dispersion micro-reactor and modeling [J].CIESCJournal(化工学报), 2013, 64(11):4246-4254.
[22] Orel Z C, Matijevic E, Goia D V. Precipitation and recrystallization of uniform CuCl particles formed by aggregation of nanosize precursors[J].Colloid and Polymer Science, 2003, 281(8):754-759.
[23] Zhao B, Li S C, Zhang Q F,et al. Controlled synthesis of Cu2S microrings and their photocatalytic and field emission properties [J].Chemical Engineering Journal, 2013, 230:236-243.
[24] Hu Yingshun(胡英顺), Yin Qiuxiang(尹秋响), Hou Baohong(侯宝红),et al. Development of aggregation and agglomeration of particles in crystallization and precipitation [J].Chemical Industry and Engineering(化学工业与工程), 2005, 22(5):371-375.
[25] Dai Jianghong(戴江洪). Preparation and characterization of cuprous chloride micro-crystallization [D]. Ganzhou:Jiangxi University of Science and Technology, 2006.
[26] Harada K, Yamada Y. Process for producing trialkoxysilanes[P]:US,5362897 .1994-11-08.
