氟康唑共晶的热力学研究
2015-03-15任晓英杨彩琴
任晓英,赵 射,杨 玲,王 静,杨彩琴,王 伟*
(1.河北省保定市第二医院急诊科,河北 保定071051;2.河北医科大学药学院无机物化教研室,河北 石家庄050017)
药物共晶是根据晶体工程学原理将药物活性成分(active pharmaceutical ingredient,API)与其他生物相容性的分子,以氢键等非共价键形式按照一定化学计量比结合在同一晶格中的晶体[1]。经过合理设计的药物共晶可以显著改善药物的物理化学性质、溶解度、溶解速率和稳定性[2-5]。共晶中API与丁二酸为共晶形成物(co-crystal former,CCF)之间以氢键结合,不会破坏分子内部的共价键[6]。对于那些不可解离的药物,共晶是一种重要的改变固体形态的手段,对药物的处方前研究和剂型设计有深远影响[7]。药物工作者在进行共晶的研究中着眼点往往放在共晶对药物特性是否有了改善,从而忽略了共晶的热力学问题,即共晶分子是否具有热力学稳定性,而这个问题也是造成目前市场上还没有一个共晶药物上市的原因之一。所以对共晶的研究还要从化学研究的着眼点出发,深入的理论研究是必不可少的。氟康唑系三唑类抗真菌药[8],难溶于水。本实验以氟康唑为API,以丁二酸为CCF,制备氟康唑共晶,研究溶液中共晶的形成热力学及溶解热力学。
1 材料与方法
1.1 仪器与试药 KQ-100DE型数控超声波清洗器(昆山市超声仪器有限公司);AVATAR330IR红外光谱分析仪(美国尼高力);TU-1901双光束紫外可见分光光度计(北京普析通用仪器责任有限公司),Dlmax-2500粉末X射线衍射仪(日本Rigaku公司);XPR-700V热台偏光显微镜(上海团结仪器制造有限公司)。氟康唑(石家庄市第四制药厂);丁二酸(沈阳市试剂三厂,分析纯);甲醇(天津市永大化学试剂有限公司,分析纯);实验用水为蒸馏水。
1.2 方法
1.2.1 氟康唑含量方法 ①标准曲线:精密称取氟康唑原料药43.5mg,置于100mL容量瓶中,用少量蒸馏水溶解后稀释至刻度摇匀,得氟康唑储备液;精密量取氟康唑储备液1、2、4、6、8、10mL于10 mL容量瓶中,加蒸馏水稀释至刻度,在260nm波长处测定吸光度,得出回归方程A=0.002 1c+0.011(r=0.999 5),氟康唑浓度在43.5~435.0 μg/mL范围内线性关系良好。②回收率的测定:分别在高(204.73μg/mL)、中(170.61μg/mL)、低(136.49μg/mL)不同浓度的氟康唑溶液中计算氟康唑平均回收率为99.42%,RSD为0.45%(n=9);实验结果表明氟康唑的浓度测定不受丁二酸的干扰,故紫外分光光度法可定量测氟康唑的含量。③精密度试验:精密量取高、中、低不同浓度的氟康唑溶液,分别于同日内(5次)、不同日(5d)测定氟康唑含量;氟康唑高、中、低浓度日内RSD为0.07%,日间RSD为0.6%(n=15),日内、日间RSD均较小,日内、日间精密度符合方法学要求。
1.2.2 氟康唑共晶的制备 分析天平精密称取氟康唑与丁二酸共210mg(摩尔比1∶1)加入玛瑙研钵内,加适量甲醇辅助研磨10min,真空干燥备用。
1.2.3 X射线粉末衍射(X-ray powder diffraction,XRD)Cu Kα1辐射,石墨单色器,40kV,150mA,2θ扫描范围10~40°,扫描速度8°/min,步长0.02°。
1.2.4 氟康唑与丁二酸在溶液中的结合热力学
溶液中氟康唑与丁二酸的结合常数采用相溶解度法[9]。于 50mL 锥 形 瓶 中 加 入 0、2、4、6、8、10 mmol/mL的丁二酸溶液30mL,并加入过量的氟康唑,30℃超声2h达平衡,精密量取续滤液0.25mL于10mL容量瓶并稀释至刻度,于测定波长处测定吸收值,计算氟康唑浓度,以[API]0对[CCF]0作图,由回归方程的斜率和截距求出氟康唑与丁二酸溶液中的结合常数,即K=斜率/截距(1-斜率),△G=-RTlnK求出△G。
1.2.5 氟康唑共晶的溶解热力学 摩尔比1∶1氟康唑-丁二酸共晶体系溶解时,会存在以下2种情况:①溶解后的共晶饱和溶液既无络合反应也不发生进一步解离时,A的溶解度与溶液中C的浓度无关,则共晶的溶解度,测出共晶的溶解度,则可求出Ksp。再应用公式 计算△G=-RTlnSASC/Ksp计算△G。② 共晶溶解后的溶液中药物API(A)和CCF(C)之间有络合效应时,溶液中存在平衡:

其中,ACsolid和ACsoln表示共晶和共晶溶液,Asoln和Csoln分别表示API和CCF溶液。根据化学平衡定律,平衡常数表示为:
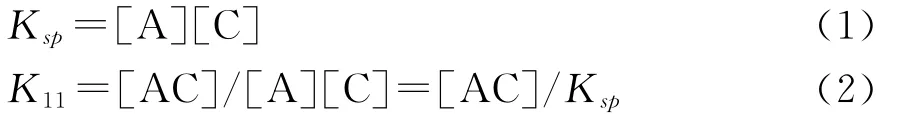
式中,Ksp为溶度积,K11为络合常数,[A]、[C]分别为API和CCF的浓度,[AC]为共晶浓度。令[A]T、[C]T分别为A和C的总浓度(溶液中的浓度和共晶中的浓度),则:

故有:

若K11Ksp<<[C]T,则有

以[A]T对1/[C]T作图,由回归方程的斜率求出Ksp,再由截距求出K11。
2 结 果
2.1 XRD分析 氟康唑、丁二酸在5~10°之间有特征的晶体衍射峰。氟康唑在9.9°、16.5°、20.0°,丁二酸在16.0°、19.9°、26.1°和37.9°处均有强晶体衍射峰出现,但形成氟康唑-丁二酸共晶后,氟康唑在9.9°及13.5°的衍射峰消失,在16.5°和20.0°处的衍射峰明显减弱,丁二酸在37.9°处强的衍射峰消失,共晶样品在7.9°和9.1°处出现了新的衍射峰,说明氟康唑与丁二酸形成了新的物相——共晶(图1)。

图1 原料药及共晶的XRD图谱a.氟康唑;b.丁二酸;c.研磨10min共晶Figure 1 XRD patterns of API,CCF and co-crystal
2.2 溶液中结合热力学 氟康唑的溶解度随丁二酸浓度的增加而增加,且呈线性关系,由此说明相溶解度曲线为AL型(图2)。又由于回归方程的斜率小于1,所以,API与CCF结合为1∶1[10]。由回归方程的斜率和截距求得K=5.4L/mol,△G=-4.2 kJ/mol<0,即该结合反应为自发反应。
2.3 共晶溶解热力学 分别测定不同温度下共晶在不同浓度的丁二酸溶液中的溶解度数据,以[A]T对 [C]T作图(图3A)和以[A]T对1/[C]T作图(图3B),由图3A可见氟康唑的溶解度随着丁二酸浓度的增大而减小,也就是说共晶的溶解度行为与难溶盐类似,会产生同离子效应。图3B呈现的[A]T对1/[C]T作图为直线关系,说明氟康唑共晶溶解后会发生进一步络合,由直线回归方程计算Ksp、求出络合常数K11(见表1)。

图2 共晶形成的相溶解度曲线Figure 2 Phase solubility curve of co-crystal formation
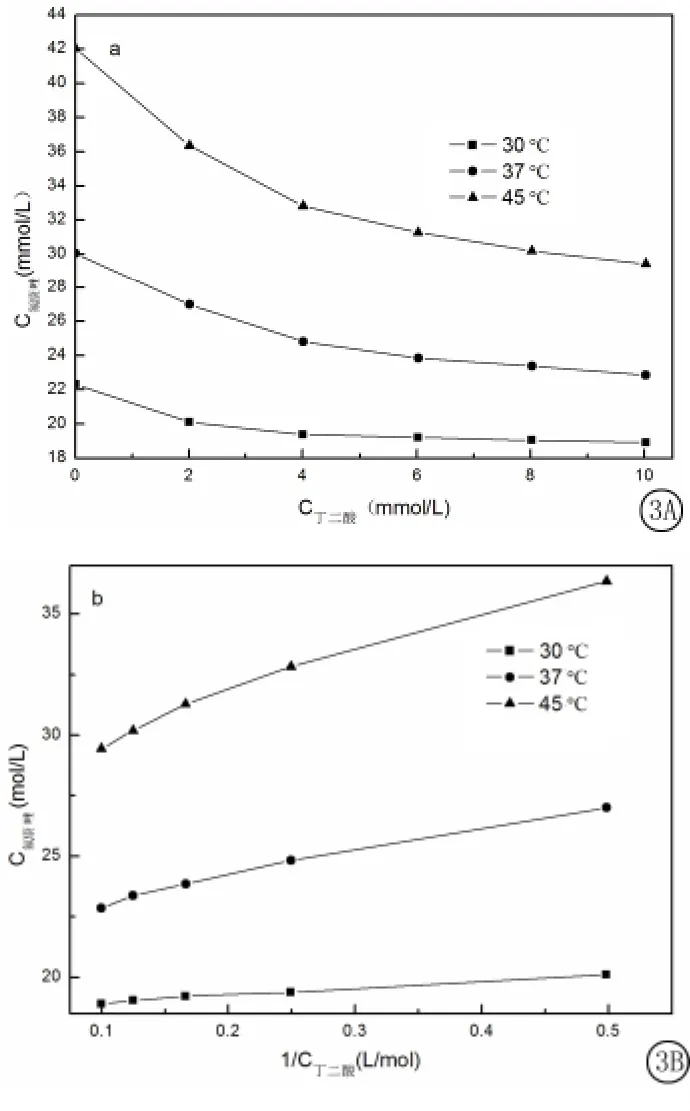
图3 共晶溶解的相溶解度曲线A.[A]T-[C]T;B.[A]T-1/[C]TFigure 3 Phase solubility curve of co-crystal dissolution

表1 共晶不同温度下的溶解热力学数值Table 1 The thermodynamic parameters of dissolution of co-crystal at different temperature
随温度提高,Ksp略有增大,说明共晶溶解是吸热反应,这与溶度积固有属性是一致的,而共晶溶解后在溶液中的络合能力随温度升高而减小。将30℃时丁二酸和氟康唑的水中溶解度(930mmol/L和18.27mmol/L)代入公式,求得△G=-12.78 kJ/mol<0。因此,可判断出形成共晶的反应是自发的且形成共晶的可能性大。
3 讨 论
药物与不同CCF形成的共晶会有不同的固体形态,通过选择不同的共晶形成物,可达到设计药物性质的目的。共晶结构预测对象不仅包括各组分形成共晶的可能性、分子间相互作用和堆积排列,还包括共晶的化学计量比、溶剂的影响等,但目前采用较多的晶体工程和计算分析等方法并不能绝对可靠地预测共晶的结构和性质,因此,共晶的筛选尚停留在反复尝试的阶段。
本实验采用相溶解度法研究溶液中API与CCF的结合热力学和共晶的溶解热力学,由结合常数可以评估共晶的结合稳定性及自发性趋势[11-12]。
摩尔比1∶1的共晶体系在溶液中存在的平衡及相应的△G如下所示:

△G=-RTlnα′A=-RTlnSA(由于 A是非电解质稀溶液,所以A的活度近似等于浓度,即等于A的溶解度) (7)
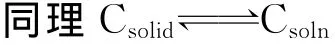

其中符号A代表API,C代表CCF,AC代表共晶,α′A代表A的活度,SA代表A的溶解度,αA代表共晶溶解的A的活度,αC共晶溶解的C的活度,△GA代表A溶解反应的吉布斯能变,△GC代表C溶解反应的吉布斯能变,△GAC代表共晶溶解反应的吉布斯能变,Ksp是共晶的溶度积常数。
将(1)+(2)-(3)得总反应为:
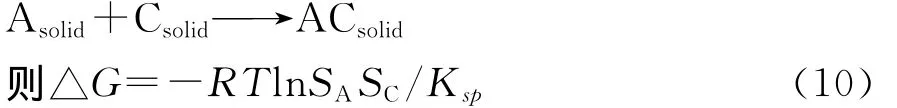
公式(10)揭示了共晶形成的本质,△G与温度以及API、CCF、共晶3种物质的溶解度有关。可通过计算△G的正负来判断一定条件下共晶形成的可能性:△G>0时,形成共晶的可能性小;△G<0时,则形成共晶的可能性大。
本研究对共晶的溶解后的存在形式进行了详细的分析,这些理论分析及实验设计为共晶的筛选及制备条件优选提供了支撑。
[1] Altonen J,Alles M,Mirza S,et al.Solid form screening--a review[J].Eur J Pharm Biopharm,2009,71(1):23-37.
[2] Schultheiss N,Newman A.Pharmaceutical cocrystals and their physicochemical properties[J].Cryst Growth Des,2009,9(6):2950-2967.
[3] Lian WG,Lin YL,Wang M,et al.Crystal engineering approach to produce complex of azelnidipine with maleic acid[J].Cryst Eng Comm,2013,15:3885-3891.
[4] Lin YL, Yang H,Yang CQ,et al.Preparation,characterization,and evaluation of dipfluzine-benzoic acid cocrystals with improved physicochemical properties[J].Pharm Res,2014,31(3):566-578.
[5] Bak A,Gore A,Yanez E,et al.The co-crystal approach to improve the exposure of a water-insoluble compound:MG 517 sorbic acid co-crystal characterization and pharmaco kinetics[J].Pharm Sci,2008,97(9):3942-3965.
[6] 王义成,冯成亮,杨素勤,等.药物共晶的最新研究进展[J].药学进展,2013,37(3):120-130.
[7] Swarbrick J.Encylopedia of pharmaceutical technology[M].New York:Informa Health Care USA Inc,2007:615-635.
[8] 李应,沈雁冰,朱贤丽.氟康唑治疗艾滋病并发隐球菌性脑膜炎的临床观察[J].临床荟萃,2012,27(5):431-433.
[9] Brewster ME,Loftsson T.Cyclodextrins as pharmaceutical solubilizers[J].Adv Drug Deliv Rev,2007,59(7):645-666.
[10] Higuchi T,Connors KA.Phase-solubility techniques[J].Adv Anal Chem Instrum,1965,4:117-210.
[11] 杨彩琴,王静,纪桂霞.羟丙基-β-环糊精对双苯氟嗪包合作用的热力学研究[J].化学研究与应用,2010,22(4):495-498.
[12] 吴海燕,杨彩琴,林玉龙,等.桂利嗪-聚乙烯吡咯烷酮固体分散体的研制[J].河北医科大学学报,2008,29(5):712-714.
