米托蒽醌治疗多发性硬化的疗效和安全性分析
2015-03-11许二赫刘江红张旭乡董会卿
刘 峥,魏 欣,陈 海,许二赫,刘江红,张旭乡,董会卿
多发性硬化(multiple sclerosis,MS)是一种慢性免疫介导的中枢神经系统炎性脱髓鞘性疾病,是导致中青年人群非外伤性致残的最常见疾病[1]。MS临床分为复发缓解型(relapsing-remitting MS,RRMS)、继发进展型(secondary progressive MS,SPMS)、进展复发型(progressive relapsing MS,PRMS)和原发进展型(primary progressive MS,PPMS)),RRMS 占MS 的85%,约有80%的RRMS后期转化为SPMS[2]。在我国缺乏治疗多发性硬化的国际一线药物β-干扰素(IFNβ)[3]和醋酸格来莫(GA)[4],致使国内的患者更容易转化为SPMS。在众多具有细胞毒性作用的免疫抑制剂中,只有米托蒽醌(mitoxantrone,MX)开展了针对SPMS 的随机、安慰剂对照、双盲的研究[5,6],美国FDA 在2000 年批准MX 用于治疗恶化的复发-缓解型(worsening relapsing-remitting MS,WRRMS)、SPMS 和PRMS,使MX 成为多发性硬化治疗的二线药物,在欧美广泛应用于基础治疗后仍进展的患者[7],甚至已经尝试应用于儿童患者[8],但在我国尚无应用,本研究拟探索国人应用MX 治疗WRRMS 和SPMS 的有效性和安全性。
1 资料和方法
1.1 病例资料 收集2009 年1 月~2014 年12 月于我院神经内科住院,接受MX 治疗的WRRMS 和SPMS 的患者9 例。入组标准:(1)年龄18~55 岁;(2)患者属于以下两种情况之一[9]:①RRMS 应用激素、丙种球蛋白、干扰素或其他免疫调节剂者,年复发率(annual relapsing rate,ARR)≥2,且出现残留症状,扩充的残疾状态量表评分[10](Expanded Disability Status Scale,EDSS)≥3,定义为恶化的RRMS;②SPMS 每年EDSS 进展≥1 分和(或)年复发≥2 次;(3)EDSS 评分为3.0~8.0;(4)既往没有使用过MX、没有进行CD34 自体造血干细胞移植,没有经过全身淋巴照射;(5)血常规中白细胞总数>4×109/L,中性粒细胞>2×109/L,血小板>100×109/L。排除标准:(1)白血病史者;(2)心脏病者其LVEF<50%或有心衰病史或心肌病者;(3)使用过MX 或蒽环类药物者;(4)妊娠或计划妊娠者;(5)严重肝病者[11]。
1.2 米托蒽醌的使用方法和剂量调整方法米托蒽醌的具体用法:12 mg/m2/次,此为入组后1 m的药量;每3 m应用一次,剂量同前,共2 y。用药之前0.5 h 可以给与止吐剂;用药期间,依患者的不良反应可调整剂量,主要监测指标为血常规、心脏功能和肝功能,血常规如果白细胞3~3.99×109/L,本次MX 用量调整为预计用量的90%,若白细胞为2~2.99×109/L,则本次MX 用量调整为预计用量的75%,若白细胞低于2×109/L,停止用药[6]。心脏监测心电图和心脏彩超,若左心室射血分数较上次降低10%,或绝对值小于50%,或出现充血性心力衰竭,则停止用药,由于潜在的心脏毒性,总剂量不能超过140 mg/m2。肝功能转氨酶如果高于正常10 倍以下,本次MX 减量为10 mg/m2,如果高于10倍则停止用药[12]。
1.3 用药前后进行临床和影像的评估和检测对患者首次用药时神经功能进行EDSS 评分[12],统计用药前、用药期间和用药后的年复发率(annualized relapse rate,ARR),用药期间每3 m 监测血常规、心脏彩超,每6 m 进行头颈的神经影像检查,另外记录药物的不良反应。
1.4 统计学处理 应用SPSS 10.0 软件进行分析。对统计数据首先应用Kolmogorov-Smirnov 检验(D 检验)和Shapiro-Wilk(W 检验)进行正态性检验,符合正态分布的,均数比较应用多因素的方差分析(q 检验);不符合正态分布的变量以及非连续变量,平均水平以中位数表示,不同组间比较采用非参数检验中的秩和检验。检验发现治疗期间年复发率为非正态分布,因此年复发率和非连续变量EDSS的平均水平以中位数表示,之间的比较应用秩和检验。以P<0.05 为差异有统计学意义。
2 结果
入组患者中男性2 例,女性7 例,SPMS 7 例,用药前平均病程为7.57±4.35 y;恶化的RRMS 2 例,用药前病程平均为2.75±0.35 y。9 例患者平均接受MX 治疗6 次(3~8),平均剂量72.00±25.29 mg/m2,平均随访时间为31.03±20.81 m,其中第4和第8 例患者因白细胞下降治疗过程中曾调整MX的剂量。9 位患者的神经功能、用药、复发和随访情况详见表1。
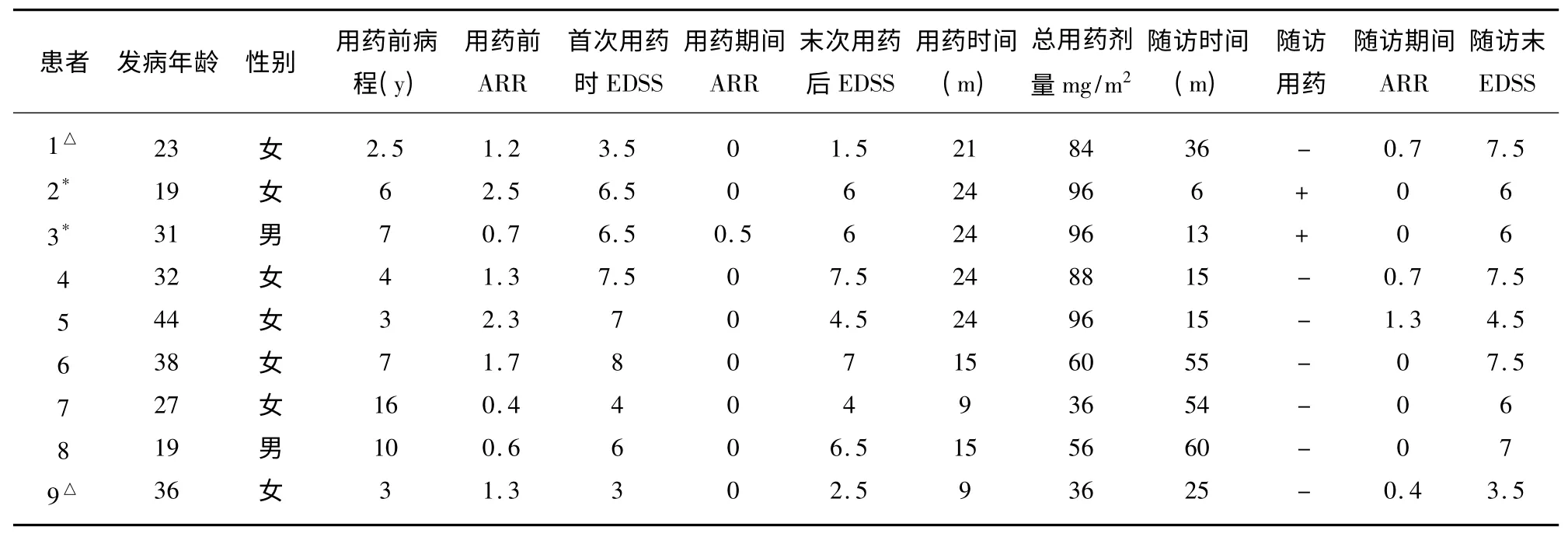
表1 9 例患者的神经功能、用药和随访情况
9 例患者的临床神经功能评分EDSS 在首次用药时中位数为6.5(3~8),用药期间EDSS 评分中位数为6(1.5~7.5),二者有显著性差异,P=0.048。用药前ARR 中位数为1.3(0.4~2.5),用药期间ARR 中位数为0(0~0.5),二者有显著性差异P=0.008,治疗期间8 例患者无发作(88.9%);用药后随访期间ARR 中位数为0.5(0~1.3),与用药期间ARR 相比无统计学差异,P=0.136,但随访结束时EDSS 评分为6(3.5~7.5),与用药期间EDSS 评分相比有统计学差异,P=0.042,提示病情恶化。
随访期间用药和复发情况:9 例患者中有2 例患者在停用MX 3 m 内开始服用吗替麦考酚酯0.25 bid,随访结束时该2 例患者没有复发,EDSS 评分维持在用药结束时的状态,随访期间未出现骨髓移植、肝功能损害等不良反应。其余7 例患者随访期间未用药,病例1 在随访的36 m 中复发两次,病例4 在随访的15 m 复发1 次,病例5 在随访的15 m 复发2次,病例9 在随访的25 m 复发1 次。
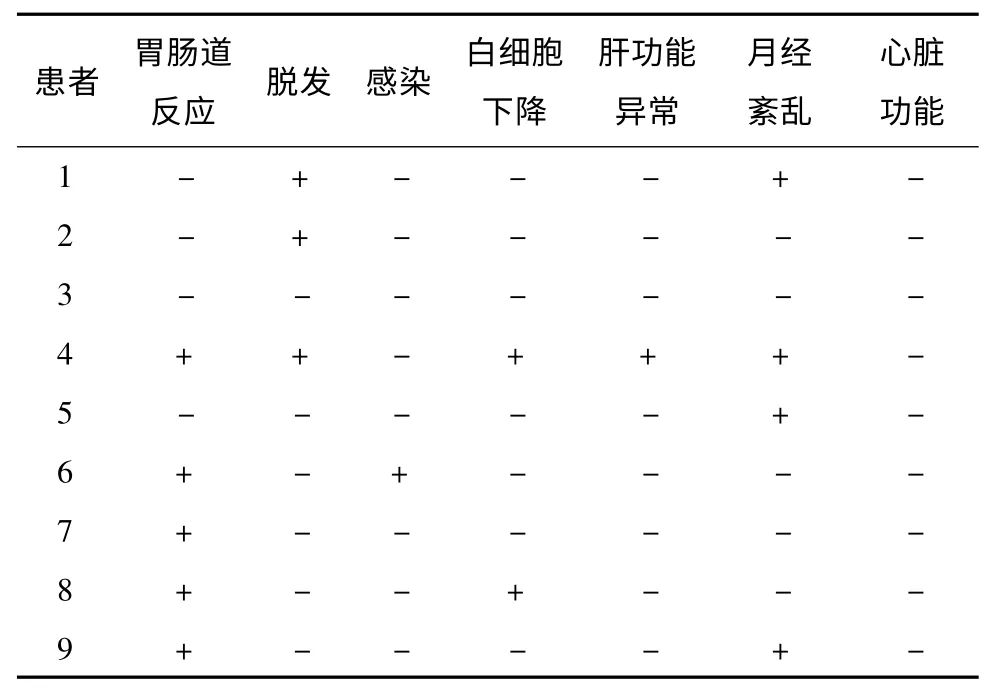
表2 9 例患者用药和随访期间出现的药物不良反应
用药和随访期间,9 例患者中出现胃肠道反应(恶心、呕吐)的有5 例(55.5%),出现脱发的有3 例(33.3%),支气管炎1 例(11.1%),外周血白细胞下降2 例(22.2%),肝功能异常1 例(11.1%),月经紊乱4 例(44.4%),未发现有心脏收缩功能减退和(或)心功能衰竭的患者,未发现出现治疗相关白血病的患者。
3 讨论
3.1 米托蒽醌的作用机制 MX 是一种蒽醌类具有抗肿瘤作用的免疫抑制剂[13]。作为嵌入剂,它能嵌入到DNA 碱基之间从而阻断DNA 合成与转录;作为酶抑制剂,MX 可抑制II 型拓扑异构酶的活性,阻止DNA 链的连接和修复。通过上述细胞毒性作用,MX 能抑制抗原递呈作用的巨噬细胞、辅助性T 细胞、小胶质细胞、效应B 细胞的功能,减少炎性因子和抗体的产生,从而对MS 患者发挥强大的免疫抑制作用[14]。
3.2 米托蒽醌用于多发性硬化的循证医学证据 MX 在20 世纪70 年代后期作为抗肿瘤药物面世,20 世纪80 年代国际上开展了MX 用于MS 动物模型的临床前试验,发现其对试验性变态反应性脑脊髓炎(experimental autoimmune encephalomyelitis,EAE)有效,具有剂量依赖性的免疫抑制作用,其免疫抑制作用在用药后的半月较环磷酰胺强10~20倍[15]。20 世纪末,欧洲进行了对照试验,发现MX较安慰剂组减少复发率66%[5,6],并有效减少MRI强化病灶,提高神经功能。2003 年美国FDA 依据欧洲的临床试验结果批准MX 用于恶化的RRMS 和SPMS。
3.3 本组患者应用米托蒽醌的有效性和依从性 在我国由于缺乏MS 治疗的一线药物β-干扰素(IFNβ)和醋酸格来莫(GA),致使相当一部分患者更易转化为恶化的RRMS 和SPMS,本组9 例患者中7 例SPMS 患者平 均病程7.57 y,而2 例恶化的RRMS 平均病程2.75 y,与国外患者比较并病程呈明显缩短,法国的一项802 例患者的研究中RRMS 用药前平均病程5.7 y,SPMS 平均病程13 y[16]。这9例患者用药期间的ARR 较用药前明显下降,多数患者在用药期间复发率为0,仅2 例患者复发1 次;神经功能缺损评分EDSS 在用药期间也显著下降,由于MX 并没有神经修复作用,这种神经功能改善是通过抑制脱髓鞘的免疫病理进程,调动自身的神经修复功能起作用的;但是我们发现第6,7,8 例患者病程较长,用药前后EDSS 评分变化不大,甚至有恶化者(例8),随访时虽然患者没有复发,但是EDSS 评分继续恶化,究其原因考虑为入组时患者处于SPMS的进展中后期,病理变化以神经变性为主,炎症反应相对缺乏,用药无效,因此提示我们应该在SPMS 的早期开始治疗效果更好。本组患者治疗的依从性:有4 例患者完成了2 y 8 次MX 的规范治疗,第6、7、8 例因为疗效不佳中途停药,第1 例和第9 例因担心远期副作用而未完成总疗程。
3.4 本组患者应用米托蒽醌的副作用情况本组患者副作用发生率超过10%的依次为(由多到少):胃肠道反应、内分泌紊乱、脱发、血液系统损害、肝功能异常,用药和随访期间未出现心脏功能损害和治疗相关白血病。MX 具有细胞毒性药物常见的副作用如胃肠道反应和骨髓抑制等,另外尤其要注意诱发白血病和心脏损害这两类严重副作用的发生情况,美国神经病学学会(AAN)在2010 年统计4000余例接受MX 治疗的多发性硬化患者发现[17],治疗相关的急性白血病的发生率为33/4076(0.81%),在影响心肌功能方面,12%的患者出现左心室射血分数下降至50%以下,0.4%出现充血性心力衰竭。2011 年法国统计其境内12 个中心802 例接受MX治疗的患者发现[16],1 例患者(0.1%)出现急性充血性心力衰竭,39 例(4.9%)出现无症状的左心室射血分数下降至50%以下,另外有2 例(0.25%)患者出现治疗相关白血病,2014 年一项德国的研究发现4.6%的患者有亚临床心脏损害[18]。2015 年多发性硬化杂志统计迄今应用MX 的12896 例患者发现治疗相关白血病的发病率为0.73%,大于80%的患者使用剂量超过60 mg/m2,提示剂量相关[19]。本组患者未出现心脏损害和白血病等严重并发症,一则我们的患者例数尚少观察时间尚短,二则我们应用MX的具体方法和国外有所不同,同样是每3 m 给予1次12 mg/m2的药物,国外是一次深静脉滴注本次的全量,且在5~15 min 注射完毕[20],而我们将这一次的量分成5 d 给与患者,每次静点时间不少于1 h,这样有可能减缓了蒽环类药物对心肌的损伤作用,曾有文献报道MX 缓慢静点可减少心脏副作用[17]。
3.5 米托蒽醌的后续治疗问题 由于潜在的心脏毒性,MX 应用的总剂量不超过140 mg/m2,多数患者<100 mg/m2,因此后续的免疫抑制治疗是我们用药后很快面临的问题,曾有学者研究发现MX的免疫抑制作用能持续到用药后的9 m[21],但是我们的患者1 和患者5 均在停药后的半年内发生了一次复发,显然MX 治疗之后还应后续其它免疫抑制或调节治疗,第2 例和第3 例患者都应用了吗替麦考酚酯治疗,随访期间病情平稳,未出现明显不良反应。目前国际上没有统一的后续治疗方案,后续的药物有干扰素[22],硫唑嘌呤和醋酸格雷莫等[23]。
4 小 结
米托蒽醌价格低廉、免疫抑制效果确切,在欧美已应用10 余年,在我国缺乏治疗MS 的一线和二线药物,MX 是值得推广应用的二线药物。用药过程中需要密切观察毒副作用,必要时适当做剂量调整,2 y应用结束后需有其它免疫调节剂进行后续治疗。另外,遴选患者时应注意:任何免疫抑制以及免疫调节治疗均在疾病的免疫活动阶段获益最多[24],而进入到以神经变性为主的阶段时,效果不佳。
[1]Kobelt G,Berg J,Atherly D,et al.Costs and quality of life in multiple sclerosis[J].Neurology,2006,66(11):1696-1702.
[2]Lublin FD,Reingold SC.Defining the clinical course of multiple sclerosis:results of an international survey.National Multiple Sclerosis Society(USA)Advisory Committee on Clinical Trials of New Agents in Multiple Sclerosis[J].Neurology,1996,46(4):907-911.
[3]The IFNB Multiple Sclerosis Study Group and The University of British Columbia MS/MRI Analysis Group.Interferon beta-1b in the treatment of multiple sclerosis:final outcome of the randomized controlled trial[J].Neurology,1995,45(7):1277-1285.
[4]Johnson KP,Brooks BR,Cohen JA,et al.Copolymer 1 reduces relapse rate and improves disability in relapsing-remitting multiple sclerosis:results of phase III multicenter,double-blind placebocontrolled trial.The Copolymer 1 MS study Group[J].Neurology,1995,45(7):1268-1276.
[5]Edan G,Miller D,Clanet M,et al.Therapeutic effect of mitoxantrone combined with methylprednisolone in multiple sclerosis:a randomised multicentre study of active disease using MRI and clinical criteria[J].J Neurol Neurosurg Psychiatry,1997,62(2):112-118.
[6]Hartung HP,Gonsette R,König N,et al.Mitoxantrone in Multiple Sclerosis Study Group(MIMS).Mitoxantrone in progressive multiple sclerosis:a placebo-controlled,double-blind,randomised,multicentre trial[J].Lancet,360(9350):2018-2025.
[7]Markowitz CE.Switching therapies in MS:what are the options[J].J Clin Psychiatry,2015,76(2):e6.
[8]Etemadifar M,Afzali P,Abtahi SH,et al.Safety and efficacy of mitoxantrone in pediatric patients with aggressive multiple sclerosis[J].Eur J Paediatr Neurol,2014,18(2):119-125.
[9]Gonsette RE.Mitoxantrone in progressive multiple sclerosis:when and how to treat[J].J Neurol Sci,2003,206(2):203-208.
[10]Kurtzke JF.Rating neurologic impairment in multiple sclerosis:an expanded disability status scale(EDSS)[J].Neurology,1983,33(11):1444-1452.
[11]Rizvi SA,Zwibel H,Fox EJ.Mitoxantrone for multiple sclerosis in clinical practice[J].Neurology,2004,63(12 Suppl 6):S25-S27.
[12]Neuhaus O,Kieseier BC,Hartung HP.Therapeutic role of mitoxantrone in multiple sclerosis[J].Pharmacology & Therapeutics,2006,109(1/2):198-209.
[13]Ehninger G,Schuler U,Proksch B,et al.Pharmacokinetics and metabolism of mitoxantrone.A review[J].Clin Pharmacokinet,1990,18(5):365-380.
[14]Fox EJ.Mechanism of action of mitoxantrone[J].Neurology,2004,63(12 Suppl 6):S15-18.
[15]Ridge SC,Sloboda AE,McReynolds RA,et al.Suppression of experimental allergic encephalomyelitis by mitoxantrone[J].Clin Immunol Immunopathol,1985,35(1):35-42.
[16]Le Page E,Leray E,Edan G.Long-term safety profile of mitoxantrone in a French cohort of 802 multiple sclerosis patients[J].Mult Scler,2011,17(7):867-875.
[17]Marriott JJ,Miyasaki JM,Gronseth G,et al.Evidence Report:The efficacy and safety of mitoxantrone(Novantrone)in the treatment of multiple sclerosis:Report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology[J].Neurology,2010,74(18):1463-1470.
[18]Fleischer V,Salmen A,Kollar S,et al.Cardiotoxicity of mitoxantrone treatment in a German cohort of 639 multiple sclerosis patients[J].J Clin Neurol,2014,10(4):289-295.
[19]Ellis R,Brown S,Boggild M.Therapy-related acute leukaemia with mitoxantrone:Four years on,what is the risk and can it be limited[J].Mult Scler,2015,21(5):642-645.
[20]Fox EJ.Management of worsening multiple sclerosis with mitoxantrone:a review[J].Clin Ther,2006,28(4):461-474.
[21]Neuhaus O,Wiendl H,Kieseier BC,et al.Multiple sclerosis:mitoxantrone promotes differential effects on immunocompetent cells in vitro[J].J Neuroimmunol,2005,168(1/2):128-137.
[22]Rieckmann P,Heidenreich F,Sailer M,et al.Treatment de-escalation after mitoxantrone therapy:results of a phase IV,multicentre,open-label,randomized study of subcutaneous interferon beta-1a in patients with relapsing multiple sclerosis[J].Ther Adv Neurol Disord,2012,5(1):3-12.
[23]Le PE,Leray E,Taurin G,et al.Mitoxantrone as induction treatment in aggressive relapsing remitting multiple sclerosis:treatment response factors in a 5 year follow-up observational study of 100 consecutive patients[J].J Neurol Neurosurg Psychiatry,2008,79(1):52-56.
[24]Esposito F,Radaelli M,Martinelli V,et al.Comparative study of mitoxantrone efficacy profile in patients with relapsing-remitting andsecondary progressive multiple sclerosis[J].Mult Scler,2010,16(12):1490-1499.
