渤海西南部近岸功能区表层沉积物重金属形态分析及环境评价*
2015-03-08王小静高晶晶刘季花
王小静 李 力 高晶晶 刘季花 张 颖
(国家海洋局第一海洋研究所 青岛 266061)
近岸海域是海陆相互作用较为活跃的地带, 对自然变化以及人类活动的响应也相对敏感。人类活动排放进入水体的重金属在离子交换、共沉淀、吸附、络合等物理化学作用下, 大多以相对不稳定的结合形态进入表层沉积物(Calmano et al, 1994)。表层沉积物中的重金属则通过再悬浮、氧化还原反应以及有机质的降解等物理化学过程重新进入水体, 对近岸海域生态系统造成二次污染(Sahuquillo et al, 2003)。沉积物既是水体重金属的“汇”, 又是其重要的“源”。重金属的总量分析可以反映沉积物受污染的状况, 但不能真实反映其潜在生态危害, 其迁移和生物有效性更大程度上是由其赋存形态决定的(李力等, 2012)。不同赋存形态的重金属地球化学行为及稳定性不同,对海域生态环境产生不同程度的危害(王海等, 2002)。
渤海目前有较多的功能区, 例如养殖区、排污区、港口等。各功能区依据其资源环境承载能力进行划分, 对促进人类活动、海洋经济与生态环境的协调发展有着重要意义。目前针对渤海功能区沉积物中重金属的研究大多只是利用总量进行生态效应评价(张雷等, 2011; 周斌等, 2013), 而对存在形态的研究相对较少。本文以渤海湾和莱州湾近岸功能区(港口、养殖区、排污区、湿地)表层沉积物中的重金属为研究对象, 运用BCR连续提取法对六种重金属(Cu、Pb、Zn、Cd、Ni、Cr)进行了形态分析, 结合次生相与原生相比值法对其污染水平进行评价; 同时测定了重金属的总含量, 应用 Hakanson潜在生态危害指数法对其潜在生态危害程度进行了评价。本文旨在结合这两种方法, 探明上述六种重金属在渤海湾和莱州湾近岸功能区表层沉积物中的存在形态、迁移转化程度,并预测其潜在生态危害。
1 材料与方法
1.1 研究区域与站位分布
渤海是一个半封闭的陆架边缘海, 同时也是中国唯一的内海, 主要由辽东湾、渤海湾、莱州湾和中部海域组成, 面积为7.7×104km2, 平均水深18m(李淑媛等, 1995)。渤海海水交换能力较差, 自净能力有限(Tao, 2006)。渤海河口及海岸带是重要的经济发展区。由于周边临港工业区的建设, 大量污染物通过河流、沿岸排污口以及大气沉降等途径进入渤海, 近岸海域陆源污染物约占入海污染物总量的87%(刘成等,2003)。
本次调查着重于渤海湾和莱州湾的几个功能区(天津港、大沽河排污区、弥河排污区、徐家铺养殖区、垦利养殖区、黄河口及湿地), 站位设置详见图1。海河沿岸工业发达, 天津港位于海河下游及其入海口处, 受人类活动影响较大。大沽河排污区位于渤海湾, 弥河排污区位于莱州湾, 大沽河的排污量远大于弥河。大沽河不仅是海河的入海口, 而且是天津市南排污河的入海口。南排污河接纳来自工农业以及城市生活污水, 为大沽河及其邻近海域的主要污染来源(刘俐等, 2006; 秦延文等, 2006)。徐家铺养殖区位于渤海湾齐河以南的海域, 主要养殖螃蟹以及贝类等水生动物, 以有机污染和咸污染为主(渤海碧海行动计划编写组, 2000); 垦利养殖区位于莱州湾, 主要养殖海参和虾。贝类养殖分布在浅海和潮间带区域, 螃蟹、海参和虾以池塘养殖为主, 池塘中的水通过人工挖掘的沟渠随着潮汐与海水进行混合和交换, 其中KL1站位位于垦利养殖区的养殖池塘中。黄河口及湿地的站点中, 河口及附近海域、黄河湿地以及小型的油气平台附近的站点分别以“HR”、“HW”和“GP”表示。
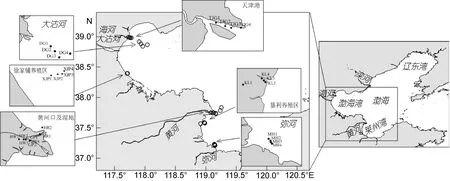
图1 渤海湾和莱州湾的采样站位Fig.1 Locations of sampling station in Bohai and Laizhou Bays
1.2 样品的采集与前处理
2012年8—9月用箱式采样器对研究海域的表层沉积物进行了采样。使用10%酸清洗过的塑料勺采集未受干扰的表层 0—2cm处的沉积物, 密封于塑料袋中冷藏。经冷冻干燥后, 用研钵研磨, 过200目尼龙筛, 密封保存。
1.3 分析项目
(1) 沉积物中重金属形态分析方法
采用改进的BCR顺序提取法(Rauret et al, 1999)对沉积物重金属的形态进行分析。BCR法将沉积物赋存形态分为4类: 弱酸溶态、可还原态、可氧化态和残渣态, 提取步骤如图2所示:
利用电感耦合等离子体质谱(ICP-MS)法测定各形态提取液中Cu、Cr、Zn、Pb、Ni、Cd等重金属元素, 各元素的回收率均在80%—120%之间。
(2) 重金属总量分析方法
准确称取 50.00mg干燥的样品置于聚四氟乙烯消解罐中, 加入高纯HNO3: HF(1: 1)溶液将样品充分溶解后, 放入190°C烘箱中加热分解48h。待其冷却后, 置于电热板上蒸干, 加入1mL HNO3蒸至湿盐状,之后加入 3mL体积分数为 50%的 HNO3和 0.5mL(1.0×10–6)Rh内标溶液, 置于 150°C烘箱中继续溶解8h以上, 定容待测。采用ICP-MS(Thermo XⅡ)测定Cu、Cr、Zn、Pb、Ni、Cd。
实验过程中为保证样品分析的精密度和准确度,测定了水系沉积物标样GBW07309。重复测定(n=11)后, 标样中几种金属回收率均在 95%—102%之间,相对标准偏差均小于5%。
(3) 粒度分析
采用激光粒度分析仪对沉积物粒度进行分析(Mastersizer 2000), 分析范围 0.02—2000µm, 并按以下 3 个粒级进行分类: 黏土(<4µm), 粉砂(4—63µm),砂(>63µm)。
上述各分析测试均在国家海洋局第一海洋研究所地质室海洋环境测试中心完成。
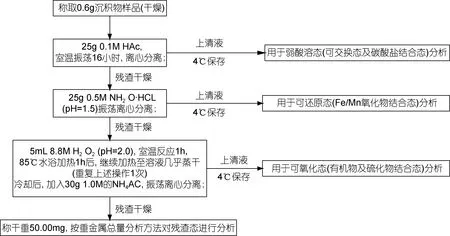
图2 形态提取实验流程图Fig. 2 Flowchart of the procedures for sequential experiment
1.4 研究方法
1.4.1 次生相与原生相分布比值法 陈静生等(1987)利用形态分析结果来评价重金属在表层沉积物中的活性, 并由此提出沉积物中重金属污染的评价方法, 即次生相与原生相分布比值法, 计算公式如下:
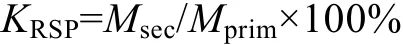
式中 Msec为沉积物次生相(即本研究的弱酸溶态、可氧化态与可还原态的含量总和)中的重金属含量,Mprim为沉积物原生相(即本研究的残渣态)中的重金属含量。KRSP用来表征污染程度, 其中KRSP<100%为无污染, 100%≤KRSP<200%为轻度污染, 200%≤KRSP<300%为中度污染, KRSP≤300%为重度污染。
1.4.2 Hakanson潜在生态风险评价 Hakanson(1980)提出的潜在生态危害指数法应用重金属总量的测试结果来进行评价, 可用来反映重金属对海洋生态系统和人类的潜在危害程度, 其计算公式如下:

表1 渤海沉积物金属背景值与Hakanson毒性响应系数Tab.1 Sediment background concentrations() in Bohai Sea and toxicity coefficients() of heavy metals
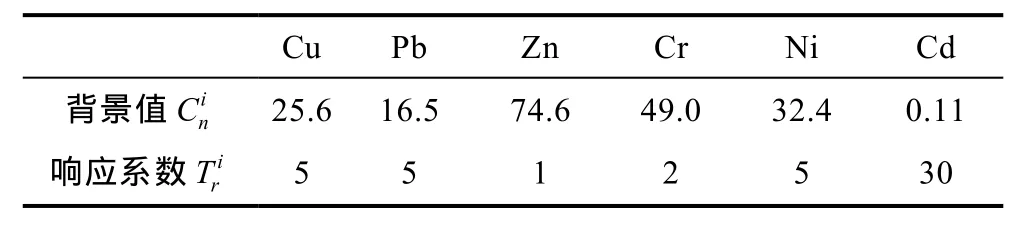
表1 渤海沉积物金属背景值与Hakanson毒性响应系数Tab.1 Sediment background concentrations() in Bohai Sea and toxicity coefficients() of heavy metals
Cu Pb Zn Cr Ni Cd背景值 i C 25.6 16.5 74.6 49.0 32.4 0.11 n响应系数 iT 5 5 1 2 5 30 r
2 结果与讨论
2.1 表层沉积物的粒度
参照谢帕德分类方法(Shepard, 1954), 对渤海功能区表层沉积物的类型进行划分(图3)。可以看出天津港、大沽河、徐家铺养殖区沉积物主要以黏土质粉砂为主,垦利养殖区主要以黏土质粉砂和砂质粉砂为主, 沉积物的颗粒较细; 黄河口湿地(HW、GP)主要以粉砂和砂质粉砂为主, 而河道中(HR)以粉砂质砂和砂为主, 弥河排污区主要以砂和粉砂质砂为主, 沉积物颗粒较粗。

表2 重金属潜在生态危害指标及等级划分标准Tab.2 Indices and grades of potential ecological risks of heavy metals
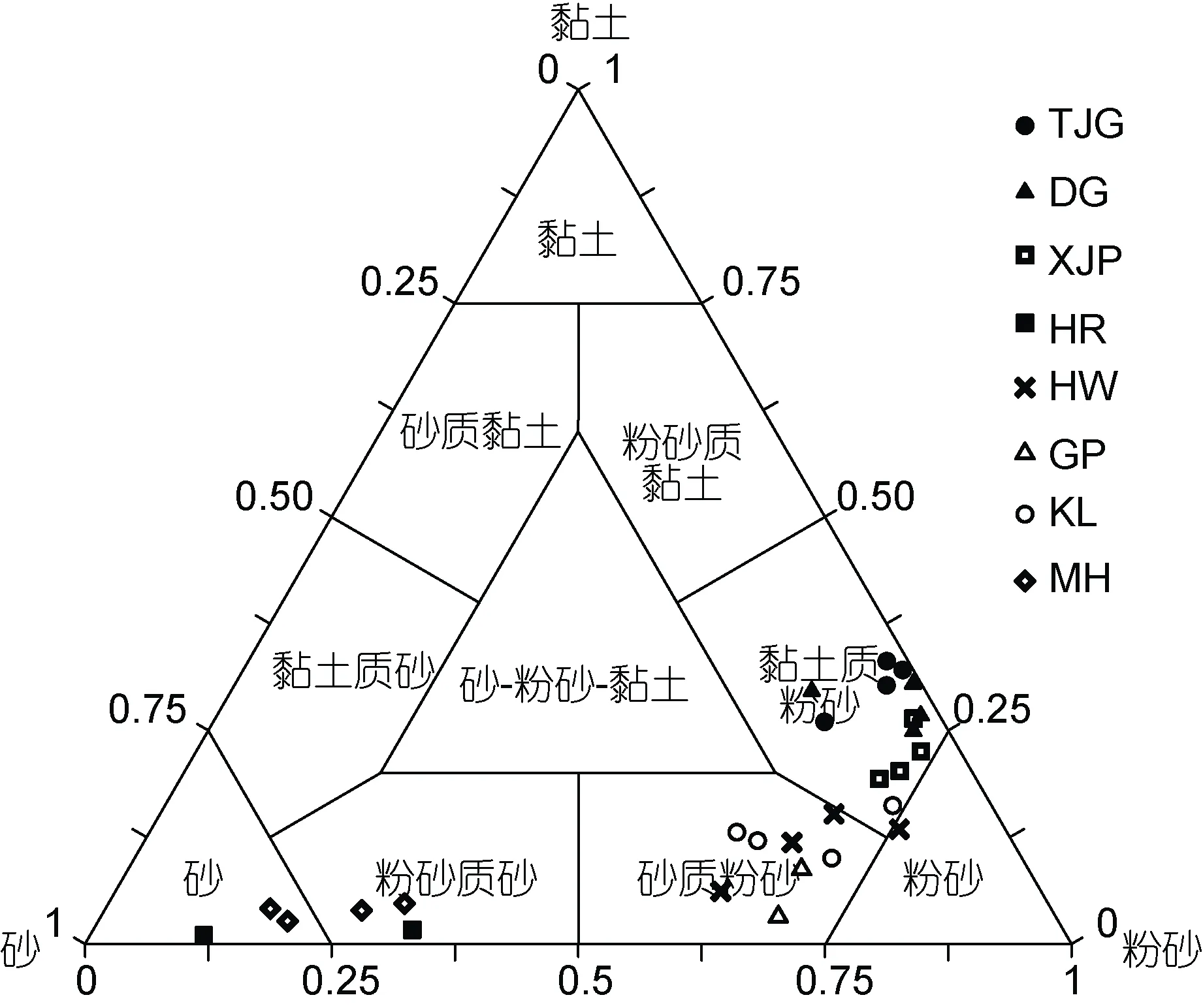
图3 谢帕德分类法得到的渤海功能区表层沉积物类型Fig. 3 Shepard classification of sediment types in the functionalzones in Bohai Sea
2.2 表层沉积物中重金属元素的赋存形态
渤海近岸功能区表层沉积物各重金属形态分布特征如图4所示。弱酸溶态、可氧化态、可还原态统称为可提取态, 可提取态所占比例越高, 越易造成金属二次污染, 其生物有效性或生物毒性也就越大。
由图4可知, Cd的可提取态在各个功能区占总含量的百分比最高(27%—66%)。可提取态Cd在黄河口及湿地、弥河排污区含量相对较低, 平均值分别为42%和 35%。在其它功能区, 可提取态 Cd的比例均为50%以上。Gao等(2012a, b)、秦延文等(2012)对渤海湾表层沉积物的研究结果也显示Cd的可提取态所占比例较其它金属高。Cd是典型的易受人为因素影响的元素, 其主要来源是工业废水, 如沿海冶炼厂的排污(Fan et al, 2002)。另外, 渤海湾近岸分布着许多矿床, 矿床开采的废水中通常也含有重金属 Cd(Qin et al, 2006)。在可提取态中, Cd主要以弱酸溶态存在(30%—48%), 该形态被认为是沉积物中最弱的结合形态, 易随着水中 pH值变化而重新溶解进入水体,进而被生物利用(Pardo et al, 1990)。弱酸溶态Cd在徐家铺养殖区与垦利养殖区所占百分比分别可达45%和 44%, 这表明 Cd在养殖区具有较强的迁移和转化性。孙启耀等(2011)在烟台典型生态区的研究中也指出, 养殖区沉积物中 Cd的弱酸溶态占有相对较高的比例(34%)。在渤海, 前人对沿岸底栖贝类体内重金属的调查研究显示, Cd的含量普遍超出海洋生物质量二类标准(2.0mg/kg), 个别站位甚至超过第三类标准(5.0mg/kg), 说明养殖区中的Cd易富集在生物体内进而造成生态危害(贺广凯, 1996; 范永胜等,2008)。
除Cd外, 可提取态含量较高的金属依次为Pb、Cu和Zn, 平均分别占总含量的36%、20%和15%。这三种金属的可提取态主要以可还原态的形式存在,尤其是Pb。可还原态Pb在徐家铺养殖区以及垦利养殖区的比例分别约为48%和40%, 此外在天津港以及大沽河的比例均为约35%, 这与之前Gao等(2012)、Gao等(2012)在渤海湾的研究结果相似。在可还原态中, 金属常与 Fe-Mn氧化物通过吸附作用或共沉淀作用赋存在一起。当海水-沉积物界面的氧化还原环境发生变化, 即更倾向于还原态时, 与铁锰氧化物结合的重金属会由于氧化物的还原而重新进入水体中,造成对水体的污染(Calmano et al, 1994; Ramos et al,1994)。
Ni在可提取态中主要以可氧化态的形式存在,平均占总含量的8%。与此结合的金属一般是作为中心离子与有机质配体结合或与S2-形成难溶的硫化物,具有较高的稳定性, 只有当水体氧化性较强时才可以释放。此外弱酸溶态Ni在黄河口及湿地、弥河排污区、垦利养殖区也占有一定的比例(约为总量的7%—9%), 具有一定的迁移性及潜在生态危害。
残渣态主要指赋存于原生或次生矿物中, 形态稳定, 一般情况下对沉积物中重金属的迁移和生物可利用性贡献较小。Cr的残渣态所占比例达96%—98%, 徐亚岩等(2012)在渤海柱状沉积物的研究中指出残渣态为Cr主要赋存形态, 说明Cr元素主要来自天然陆地来源。Cr在功能区表层沉积物中基本可认为是惰性的, 迁移性较弱, 对生物的的毒性也最弱。Zn、Cu、Ni在残渣态中的比例平均分别达到85%、80%、79%, 说明其在渤海功能区中潜在生态危害较小。

图4 研究区表层沉积物重金属各形态的分布特征Fig.4 The metal geochemical speciation in surface sediments of the study areas
2.3 次生相与原生相分布比值法评价
以次生相和原生相分布比值法对渤海功能区沉积物中重金属污染进行评价, 结果如图5所示。
各重金属元素在两相中的分布比值(KRSP)见图5a,可以看出, Cd的KRSP值最高, 范围为36%—193%, 平均值为101%; Pb在次生相中含量较高, KRSP值也相对较高, 平均值为60%; Ni、Cu、Zn的平均KRSP值依次为27%、26%、19%; Cr的优势结合相为原生相, KRSP值最小, 该指数在2%—4%之间, 平均值为3%。
对比不同功能区的结果可见, 弥河与黄河口及湿地Cd的KRSP<100%, 表明该区基本无污染; 在其余功能区 Cd在 100%—200%之间, 为轻度污染。Pb在徐家铺养殖区 KRSP>100%, 呈现轻度污染; 垦利养殖区Pb的KRSP值也相对较高, 为59%—105%。功能区Cu、Zn、Cr和Ni的KRSP值<100%, 人为污染很小,生态危害较弱。为更直观地表示不同站位重金属的总污染水平, 对几种金属的KRSP值进行了加和(图5b)。由图可知, 各功能区的生态危害程度依次为徐家铺养殖区>垦利养殖区>天津港>大沽河>黄河口及湿地>弥河。弥河排污区的生态危害较低, 可能为受沉积物粒度影响。弥河因沉积物颗粒较粗, 多为砂质, 较难富集污染物, 次生相金属含量较低。
2.4 表层沉积物重金属总含量
渤海近岸功能区表层沉积物重金属含量分布如图6所示。由图可知, 各功能区重金属含量为天津港>大沽河>徐家铺养殖区>垦利养殖区>黄河口及湿地>弥河。功能区 Cu浓度范围为 10—78mg/kg, 除天津港外, 均符合国家海洋沉积物一类质量标准(≤35mg/kg)。天津港Cu的平均含量为55mg/kg, 符合二类质量标准(≤100mg/kg)。渤海湾的三个功能区 Cu含量均超过其背景值。功能区 Pb的浓度范围为16—39mg/kg, 符合一类质量标准(≤60mg/kg), 但均超出背景值。Zn、Cr在天津港部分站位含量较高, 超出一类海洋沉积物标准值(分别为≤150mg/kg, ≤80mg/kg), 但在二类标准值范围内(分别为≤350mg/kg,≤150mg/kg), 分别为背景值的2.5倍和2.2倍; Cd在功能区含量变化幅度不大, 浓度范围为0.09—0.20mg/kg,低于一类海洋沉积物质量标准的最高值 0.50mg/kg,除弥河外, 均高于背景值。Ni的平均质量浓度为32mg/kg,与背景值接近。
天津港沿岸工业污水的排放以及船只的影响是其重金属含量高的主要原因。Meng等(2008)对渤海湾天津附近沉积物中重金属进行分析, 指出Pb、Zn、Cd是该区域主要的污染元素, 高值区分布在齐河和大沽河口附近。弥河、黄河口及湿地表层沉积物中重金属元素含量低且变化范围小, 基本属于较清洁水平。吴斌等(2013)在对黄河口表层沉积物的研究中也未检测到较高的重金属含量。吴晓燕等(2007)对黄河口沉积物进行了研究, 发现重金属含量为平水期>枯水期>丰水期, 这与沉积物粒度密切相关。沉积物中重金属主要结合在细颗粒物中, 并随之迁移(Lee et al,1998)。从沉积物粒级组分与重金属总量之间相关性分析(见表3)来看: 各重金属元素均在0.01水平上显著正相关, 说明它们之间可能具有相似的输入源; 重金属与黏土百分含量呈显著正相关, 而与砂的百分含量呈显著负相关, 这表明渤海功能区表层沉积物重金属易富集在细颗粒物。综上, 除现代工业活动影响外, 粒度也是影响功能区沉积物中重金属含量的主要因素。
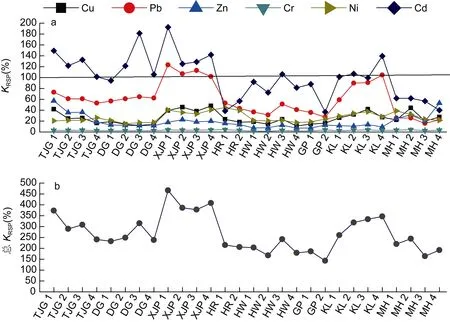
图5 (a)重金属在次生相与原生相中的分布比; (b)重金属KRSP的加和Fig.5 (a) The rations secondary phase and primary phase of heavy metals; (b) The sum of the heavy metal KRSP values

图6 渤海近岸功能区表层沉积物重金属元素含量(in mg/kg)Fig.6 Total metal concentrations in sediments of functionalzones in Bohai Sea(in mg/kg)
2.5 Hakanson潜在生态危害指数评价
应用Hakanson潜在生态危害指数法对渤海功能区沉积物中重金属的潜在生态风险进行评价。本研究依据两种背景值分别进行了评价, 分别为现有文献(吴景阳等, 1985; 李淑媛等, 1992)中提供的背景值和本研究中测得的残渣态含量, 计算结果分别见表 4、表5。
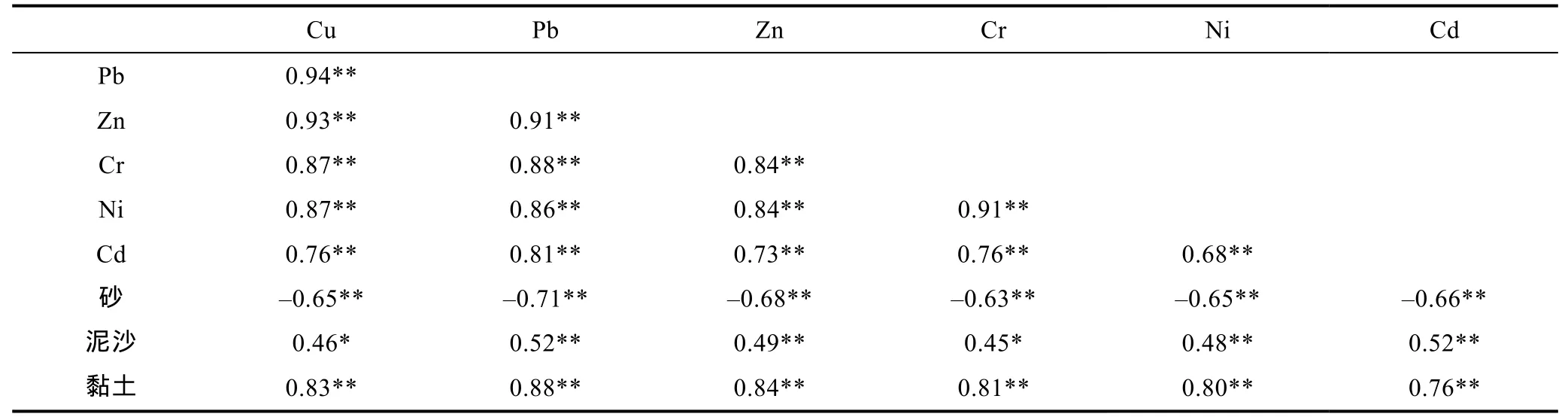
表3 渤海功能区沉积物粒度与金属总量的相关性分析Tab.3 Correlation matrix of sediment grain size and total metal concentrations in functionalzones of Bohai Sea
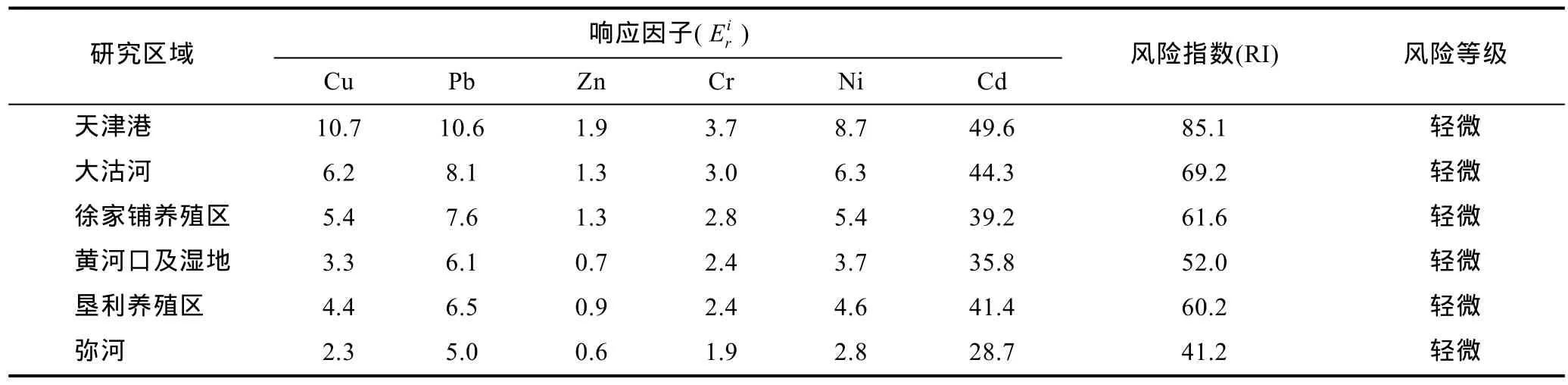
表4 表层沉积物重金属生物毒性响应因子、潜在生态风险指数及风险等级(背景值参照见表1)Tab.4 Toxicity response factor, and index and grade of ecological risk of heavy metal pollution in surface sediments (The background value references shown in Tab.1)
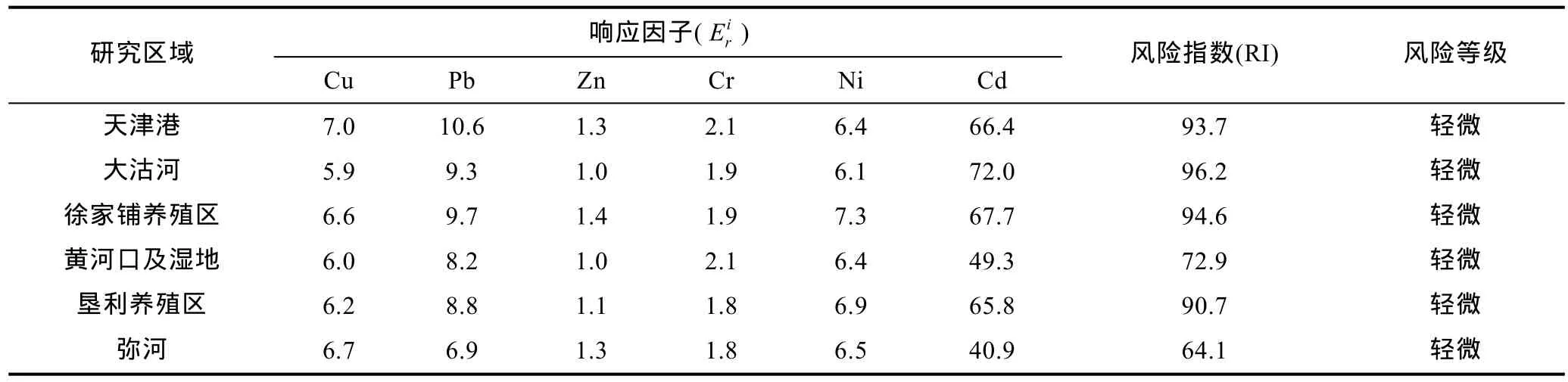
表5 表层沉积物重金属生物毒性响应因子、潜在生态风险指数及风险等级(背景值参照残渣态含量)Tab.5 Toxicity response factor, and index and grade ecological risk of heavy metal pollution in surface sediments(The residual content is considered as the background values)
各功能区重金属潜在生态危害指数 RI均小于150(表 4、表 5), 潜在生态危害程度为轻微; 由表 4可以看出各功能区的RI值由高到低为天津港、大沽河、徐家铺养殖区、垦利养殖区、黄河口及湿地、弥河; 而表5得出RI值依次为大沽河>徐家铺养殖区≥天津港>垦利养殖区>黄河口及湿地>弥河。天津港、大沽河和徐家铺养殖区均属于渤海湾, 而垦利养殖区及弥河排污区均属于莱州湾。张雷等(2011)对环渤海典型海域进行了研究, 发现渤海湾潜在生态危害大于莱州湾, 并认为这主要是来自渤海湾的陆源性输入以及海洋开发活动造成的。本研究认为, 除现代工业活动影响外, 粒度也是重要影响因素之一。重金属易吸附在细颗粒物上(表 3), 而渤海湾沉积物粒度与莱州湾相比较细(图 2), 使得渤海湾的功能区潜在生态危害大于莱州湾。
Cd在研究区表层沉积物中的含量远低于第Ⅰ类海洋沉积物质量标准(0.50mg/kg), 但其影响因子在整个生态风险指数中贡献较大, 达58%以上。秦延文等(2012)认为这主要是由于 Cd的生态毒性响应系数较高另外Cd的含量除弥河外均高于背景值,所以Cd在生态风险评价中的贡献率较大。
3 结论
Cd是本次调查中最主要的污染元素, 渤海功能区沉积物中Cd以弱酸溶态为主; Cu、Pb、Zn、Cr、Ni优势结合态为残渣态, 其中 Cr可认为是惰性的,对生物无毒性; 可提取态中Cu、Pb、Zn以可还原态为主, Ni以可氧化态为主, 迁移性及潜在的二次释放能力较强。次生相与原生相分布 KRSP指数分析可以得出: (1)Cd污染指数最高, Pb次之, 其余重金属基本无污染; (2)各功能区的污染水平依次为徐家铺养殖区>垦利养殖区>天津港>>大沽河>黄河口及湿地>弥河。
渤海功能区沉积物中Cu、Pb、Zn、Cr、Ni、Cd含量均在不同程度上超出背景值的范围。除现代工业活动影响外, 粒度也是影响功能区沉积物中重金属含量的主要因素。潜在生态危害指数法结果表明: (1)各金属潜在生态危害依次为 Cd>Pb>Ni≥Cu>Cr>Zn;Cd以中度污染为主, 其它元素为轻微污染; (2)渤海各功能区潜在生态危害程度为轻微, 整体上为渤海湾功能区潜在生态危害大于莱州湾。
通过对比发现, 潜在生态风险评价与基于地球化学形态的次生相和原生相分布比值法中Cd都是优势污染物, Pb次之, 具有较大的生态危害。这两种评价方法由于评价指标体系的不同, 对各功能区的评价结果又存在一定的差异。潜在生态危害指数法中天津港、大沽河的污染水平高于养殖区, 而次生相与原生相分布比值法认为养殖区的污染水平相对较高,因此在对功能区沉积物重金属的评价过程中, 两种方法都应加以考虑。
王 海, 王春霞, 王子健, 2002. 太湖表层沉积物中重金属的形态分析. 环境化学, 21(5): 430—435
刘 成, 王兆印, 何 耘等, 2003. 环渤海湾诸河口底质现状的调查研究. 环境科学学报, 23(1): 58—63
刘 俐, 熊代群, 高新华等, 2006. 海河及邻近海域表层沉积物重金属污染及其分布特征. 海洋环境科学, 25(2):40—44
孙启耀, 宋建国, 高彦博等, 2011. 烟台近岸典型生态区沉积物重金属形态分布及其污染状况. 海洋科学, 35(9):31—36
李 力, 马德毅, 2012. 应用生物配体模型评价海洋沉积物重金属毒性的研究进展. 海洋环境科学, 31(5): 758—764
李淑媛, 苗丰民, 刘国贤等, 1995. 渤海底质重金属环境背景值初步研究. 海洋学报, 17(2): 78—85
李淑媛, 郝 静, 1992. 渤海湾及其附近海域沉积物中Cu, Pb,Zn, Cd环境背景值的研究. 海洋与湖沼, 23(1): 39—48
吴晓燕, 刘汝海, 秦 洁等, 2007. 黄河口沉积物重金属含量变化特征研究. 海洋湖沼通报, (z1): 69—74
吴景阳, 李云飞, 1985. 渤海湾沉积物中若干重金属的环境地球化学Ⅰ.沉积物中重金属的分布模式及其背景值. 海洋与湖沼, 16(2): 92—101
吴 斌, 宋金明, 李学刚, 2013. 黄河口表层沉积物中重金属的环境地球化学特征. 环境科学, 34(4): 1324—1332
张 雷, 秦延文, 郑丙辉等, 2011. 环渤海典型海域潮间带沉积物中重金属分布特征及污染评价. 环境科学学报, 31(8):1676—1684
陈静生, 董 林, 邓宝山等, 1987. 铜在沉积物各相中分配的实验模拟与数值模拟研究—以潘阳湖为例. 环境科学学报, 7(2): 140—149
范永胜, 陈江麟, 刘文新等, 2008. 渤海沿岸底栖贝类体内微污染物残留. 海洋环境科学, 27(1): 25—29
周 斌, 刘 伟, 刘有刚等, 2013. 渤海湾南部典型生态区表层沉积物重金属潜在生态风险分析. 海洋环境科学, 32(4):533—537
贺广凯, 1996. 黄渤海沿岸经济贝类体中重金属残留量水平.中国环境科学, 16(2): 96—100
秦延文, 郑炳辉, 李小宝等, 2012. 渤海湾海岸带开发对近岸沉积物重金属的影响. 环境科学, 33(7): 2359—2367
秦延文, 孟 伟, 郑丙辉等, 2006. 渤海湾天津段潮间带沉积物柱状样重金属污染特征. 环境科学, 27(2): 268—273
徐亚岩, 宋金明, 李学刚等, 2012. 渤海湾表层沉积物各形态重金属的分布特征与生态风险评价. 环境科学, 33(3):732—740
渤海碧海行动计划编写组, 2000. 渤海碧海行动计划. 北京:国家环境保护总局, 36—39
Calmano W, Hong J, Föestner U, 1994. Binding and mobilization of heavy metals in contaminated sediments affected by pH and redox potential. Water science & Technology, 28(8—9):223— 235
Fan W H, Wang W X, Chen J S et al, 2002. Cu, Ni and Pb speciation in surface sediments from a contaminated bay of northern China. Marine Pollution Bulletin, 44(8): 820—826 Gao X L, Chen C T A, 2012a. Heavy metal pollution status in surface sediments of the coastalBohai Bay. Water Research,46(6): 1901—1911
Gao X L, Li P M, 2012b. Concentration and fractionation of trace metals in surface sediments of intertidal Bohai Bay, China.Marine Pollution Bulletin, 64(8): 1529—1536
Hakanson L, 1980. An ecological riskindex for aquatic pollution control.a sedimentological approach. Water Research, 14(8):975—1001
Lee C L, Fang M D, Hsieh M T, 1998. Characterization and distribution of metals in surficial sediments in Southwestern Taiwan. Marine Pollution Bulletin, 36(6): 464—471
Meng W, Qin Y W, Zheng B H et al, 2008. Heavy metal pollution in Tianjin Bohai Bay, China. Journal of Environmental Sciences, 20(7): 814—819
Pardo R, Barrado E, Lourdes P et al, 1990. Determination and speciation of heavy metals in sediments of the Pisuerga river.Water Research, 24(3): 373—379
Qin Y W, Meng W, Zheng B H et al, 2006. Heavy metal pollution in tidal zones of Bohai Bay using the dated sediment cores.Journal of Environmental Sciences, 18(3): 610—615
Ramos L, Hernandez L M, Gonzalez M J, 1994. Sequential fractionation ofcopper, lead, cadmium and zinc in soils from or near Doñana National Park. Journal of Environmental Quality, 23(1): 50–57
Rauret G, López-Sánchez J F, Sahuquillo A et al, 1999.Improvement of the BCR three step sequential extraction procedure prior to the certification of newsediment and soil reference materials. Journal of Environmental Monitoring, 1:57–61
Sahuquillo A, Rigol A, Rauret G, 2003. Overview of the use of leaching/extraction tests for risk assessment of trace metals in contaminated soils and sediments. TrAC Trends in Analytical Chemistry, 22(3): 152–159
Shepard F P, 1954. Nomenclature based on sand-silt-clay ratios.Journal of SedimentaryResearch, 24(3): 151–158
Tao J H, 2006. Numerical simulation of aquatic eco-environment of Bohai Bay. Journal of Hydrodynamics, Series B, 18(3):34—42
