玻璃体腔注射神经生长因子安全性研究及视网膜组织分布*
2015-03-08刘丹宁樊继山阴正勤
刘丹宁,樊继山,阴正勤
(1.重庆医科大学附属第二医院眼科 400010;2.重庆医科大学儿童医院药学部 400014;3.第三军医大学西南医院眼科,重庆400038)
从小鼠颌下腺提取的肌内注射剂型鼠神经生长因子(mNGF)是国家的Ⅰ类新药,临床上已将其应用于包括视神经损伤在内的神经损伤修复,并有望用于眼底疾病特别是视网膜色素变性(RP)的治疗研究[1-3],而药物能否在靶组织达到有效药物浓度是治疗的关键,由于其肌内注射的给药方式限制了达到眼部的药物浓度,必要的眼部浓度维持需要全身给予大剂量药物,增加了发生不良反应的风险[4-5]。因此,采用眼局部用药如玻璃体腔注射可能成为mNGF治疗RP的方法[6]。但全身应用的肌内注射型药物mNGF玻璃体腔注射后眼内的安全性如何,玻璃体腔注射mNGF后,药物能否迅速聚集于视网膜等问题,目前尚不清楚,极大地限制了mNGF治疗RP的应用前景。因此本研究观察了临床剂型mNGF(即小鼠颌下腺提取的肌内注射剂型mNGF)兔眼玻璃体腔注射的安全性,并在此基础上,观察了该浓度mNGF视网膜组织药物分布情况,为其后期临床研究奠定基础。
1 材料与方法
1.1 材料
1.1.1 实验动物 成年健康灰兔,雌雄不限,200~300kg,第三军医大学实验动物中心提供,动物饲养及实验操作在第三军医大学实验动物中心进行。
1.1.2 实验材料 mNGF(北京舒泰神药业有限公司,纯度为98%,国药准字S20060023 30μg/瓶),NGF 2.5S冻干粉(以色列Alomone labs,行125I标记用药),125I(第三军医大学核医学实验室提供),复方托吡卡胺滴眼液(日本参天制药株式会社),0.4%奥布卡因滴眼液(日本参天制药株式会社),其他均为国产分析纯试剂。
1.2 方法
1.2.1 动物分组及实验设计 (1)兔眼玻璃体腔注射mNGF安全性评估的动物分组:取成年健康灰兔6只,分2组,每组3只6眼,NGF组:玻璃体腔注射30μg/100μL mNGF,对照组:玻璃体腔注射0.9%生理盐水100μL。于玻璃体腔注药后1、7、30d分别行行为学观察,裂隙灯观察角膜清亮度、前房清亮程度、晶体透明度,眼B超检查玻璃体清亮程度,直接眼底镜观察眼底视网膜情况,并于30d时处死动物,取眼球行冰冻切片苏木精-伊红(HE)染色;(2)兔眼局部注射NGF后眼内药物分布的动物分组:取成年健康灰兔27只,玻璃体腔注射30μg/100μL125I-NGF。于注药后15、30min,1、3、6、8、12、24、48h处死动物,分别取眼内容物房水、玻璃体,眼球内壁组织虹膜睫状体、视网膜、脉络膜,眼球外壁组织角膜、巩膜进行125I-NGF的检测,每个时间点3只动物6眼。观察视网膜药物峰浓度及达峰时间。
1.2.2125I-NGF的标记、鉴定和检测125I-NGF的标记、鉴定:采用氯胺T法进行125I-NGF的标记(由第三军医大学核医学实验室协助)[7]。标记物鉴定结果:标记率为50,放化纯度:95%,比活度为2.294×1015Bq/kg,放射性活度为1.154×107Bq。药物配制比例为8∶100;125I-NGF的检测:液体取100 μL,固体称质量,置于称质量后的放射免疫管中,于γ-计数器上进行计数,以各组织各时间点125I-NGF的百分剂量率(%ID/g=样本γ-计数/标准液γ-计数/样本重量×100%)代表组织中NGF的含量。
1.2.3 玻璃体腔注射mNGF方法 玻璃体腔注射:称质量后,5%水合氯醛溶液8mL/kg腹腔注射麻醉,复方托吡卡胺滴眼液滴眼散瞳,0.4%奥布卡因滴眼液进行表面麻醉,于上方角巩膜缘处透明角膜区隧道穿刺抽出房水约50μL,于上方角巩膜缘后3mm隧道穿刺垂直巩膜进针,刺入玻璃体腔,经散大的瞳孔明确针尖在玻璃体腔后,缓慢注入药液100μL,棉签按压进针处,抽出针头,观察眼压及眼部血管充盈情况,给予氯霉素滴眼液点眼预防感染。
1.3 统计学处理 采用SPSS13.0软件进行统计分析,计量资料用±s表示,采用独立样本t检验,检验水准α=0.05,以P<0.05为差异有统计学意义。
2 结 果
2.1 兔眼玻璃体腔注射mNGF后眼部安全性评估
2.1.1 行为学观察 玻璃体腔注射后第1天两组动物均不喜睁眼,第2天好转,无抓挠眼部情况。注射前后观察兔觅食正常、活动灵活、体质量增加,未发现任何异常行为及症状。

图1 玻璃体腔注射125I-NGF后裂隙灯检查眼前节情况(×16)
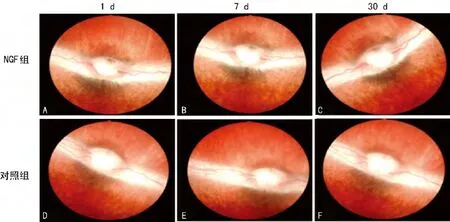
图2 玻璃体腔注射125I-NGF后眼底检查结果
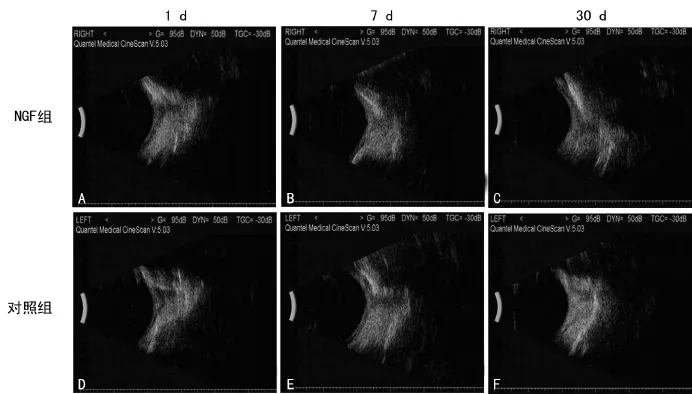
图3 两组动物玻璃体腔注射后眼部B超检查结果
2.1.2 眼前节检查 各组行玻璃体注射后1、7、30d,裂隙灯检查角膜均清亮透明,前房清亮,晶体透明,玻璃体透明,未见明显炎性反应,见图1。
2.1.3 眼底检查 视网膜未见出血,渗出,水肿,视网膜血管走行正常,视乳头无出血水肿,颜色正常,见图2。
2.1.4 眼部B超检查 两组动物行玻璃体注射后1、7、30d玻璃体腔未见明显炎性混浊,视网膜未见脱离等并发症,见图3。
2.1.5 HE染色组织病理学检查 术后30d治疗兔眼视网膜HE染色观察各层组织形态结构清晰,排列整齐,无炎性细胞浸润等异常表现,见图4。
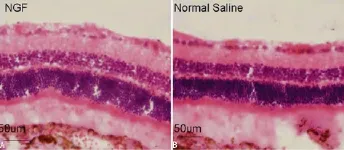
图4 两组动物玻璃体腔注射30d时视网膜HE染色结果

图5 玻璃体腔注射125I-NGF后兔眼视网膜组织药物含量变化趋势
2.2 玻璃体腔注射125I-NGF后视网膜组织药物含量变化趋势 眼局部注射125I-NGF后48h内,视网膜药物浓度趋势呈正态曲线分布。其达峰值时间为3h,峰值可达(118.32±18.74)%ID/g,见图5。
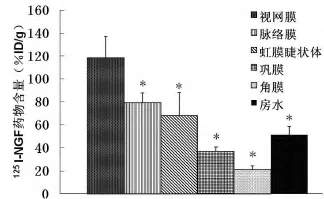
图6 玻璃体腔注射后兔眼各组织中125I-NGF含量峰值(%ID/g)
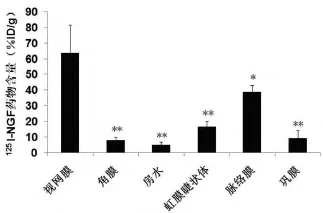
图7 玻璃体腔注射后30min兔眼各组织中125I-NGF含量(%ID/g)
2.3 玻璃体腔注射后眼内组织药物浓度峰值以视网膜为最高 玻璃体腔注射后眼部各组织药物峰值如图6所示,除玻璃体内因直接注射125I-NGF而导致很高药物浓度外,视网膜组织所获得药物含量为最高,能够保证眼视网膜获得治疗作用的药物浓度。兔眼各组织中125I-NGF达峰时间:房水、角膜、巩膜、虹膜睫状体、脉络膜、视网膜各为3、6、6、3、3、3h,可以看出视网膜达峰时间也较快,并在注射后30min内即可达到远高于其他眼内组织的浓度,见图7。
3 讨 论
目前临床上应用的mNGF主要通过肌内注射的方式给药,而改变给药途径,通过眼玻璃体腔注射,在不增加给药总量的基础上提高视网膜获取的药物浓度,可能成为治疗RP的有效方法,为了证实其可行性,本实验在动物体内观察了玻璃体腔注射的使用安全性及注射后药物能否在靶组织视网膜聚集,为下一步的有效性研究及临床试验提供参考数据。
本研究首先观察了mNGF经玻璃体腔注射后兔眼内各组织可能存在的损伤情况,确定其使用安全性,在临床使用的肌内注射剂型mNGF中,目前能够获得的最大使用浓度为30 μg/100μL。因此,本研究采用此浓度来进行临床前眼内组织安全性检测。药物对眼的损伤可分为直接接触和药物全身性吸收所引起的两大类[8],前者取决于药物的性质、剂量、使用时间等,是实验观察的重点,由于本药是国家批准的一类新药,故未再对后者进行观察。研究发现,注射后整个实验阶段的30d内,动物行为学上未见抓眼、流泪、分泌物增多等异常举动和反应,表明眼局部注射药物未对兔眼部造成明显的刺激。眼是由一系列透光及感光组织组成的视觉器官,如果药物造成眼部组织损伤,往往会呈现出透光度和感光度的改变,如角膜染色沉着、刺激性炎症,晶体浑浊,视网膜化学物质,以及色素沉着、水肿、出血、渗出,甚至视乳头水肿等形态学改变[8]。为了深入了解眼内各组织在注射药物后的反应,本研究通过裂隙灯、眼底镜、眼部B超等方法观察了角膜、前房、晶体、玻璃体及视网膜等眼内结构的整体情况,全面监测药物对眼内组织可能造成的任何损伤,结果显示,玻璃体腔注射mNGF后,角膜透明,前房清亮,晶体透明,玻璃体透明,视网膜颜色正常,未见视网膜脱离、出血、渗出及视乳头水肿等异常现象。这表明30μg/100μL肌内注射型mNGF经玻璃体腔注射使用后,未造成眼部组织的药物性损伤。此外,为了进一步确定药物对视网膜的组织层次是否存在影响,本研究通过冰冻切片HE染色对视网膜各层组织进行病理学观察,结果显示,视网膜各层组织结构清晰,排列整齐,无炎症细胞浸润等异常病理改变。上述结果表明,玻璃体腔注射浓度为30μg/100μL的mNGF是安全的。
眼局部给药的目的是希望药物能够在眼内靶组织中达到理想的药物浓度,玻璃体腔注射是否能成为有效治疗RP的方法,关键在于药物能否迅速到达视网膜组织并获得较高的药物浓度。因此本研究进一步检测了玻璃体腔注射125I-NGF后视网膜组织药物含量及分布趋势。结果发现玻璃体腔注射125INGF后,视网膜在注射后30min内即可获得远高于眼内其他各组织的药物浓度,并迅速在3h内达峰值,而且视网膜所获得的药物浓度峰值在眼内各组织中是最高的,这说明玻璃体腔注射NGF能够在视网膜组织快速聚集,相比肌内注射是一种更理想的眼部给药方法。这可能与其注射后的弥散路径及NGF药物性质有关。本研究发现玻璃体腔注射125I-NGF 30 min后,药物已经开始向房水及眼球内壁组织弥散,并且在各组织药物达峰值时的分布趋势由大到小为视网膜,脉络膜,虹膜睫状体,巩膜,角膜,房水,表明125I-NGF主要通过眼后节路径即视网膜-脉络膜-巩膜路径进行弥散,相比前节的房水、角膜等组织来说,位于眼后节的视网膜更容易获得较多的药物渗入[9-11]。此外,NGF为水溶性药物,存在于眼周血管与视网膜之间的血视网膜屏障,阻止水溶性药物弥散出眼外,将药物局限在视网膜组织中,延长了药物在眼内壁停留的时间[12-14]。其次,玻璃体腔注射125I-NGF后药物直达兔眼,而视网膜与玻璃体紧密相接,水溶性的125I-NGF可直接透过玻璃体向视网膜弥散,因而能在视网膜获得高水平125I-NGF含量[14-15]。
综上所述,玻璃体腔注射浓度为30μg/100μL的mNGF未对眼内组织造成损伤,且玻璃体强注射mNGF方法能够迅速在视网膜组织中达到较高的药物浓度,是mNGF治疗RP可行的眼局部治疗方法。
[1] Sivilia S,Giuliani A,Fernandez M,et al.Intravitreal NGF administration counteracts retina degeneration after permanent carotid artery occlusion in rat[J].BMC Neurosci,2009,10(1):52.
[2] He Y,Zhang Y,Liu X,et al.Recent advances of stem cell therapy for retinitis pigmentosa[J].Int J Mol Sci,2014,15(8):14456-14474.
[3] Sun X,Xu X,Wang F,et al.Effects of nerve growth factor for retinal cell survival in experimental retinal detachment[J].Curr Eye Res,2007,32(9):765-772.
[4] Kim YC,Chiang B,Wu X,et al.Ocular delivery of macromolecules[J].J Control Release,2014,190:172-181.
[5] Barar J,Javadzadeh AR,Omidi Y,et al.Ocular novel drug delivery:impacts of membranes and barriers[J].Expert Opin Drug Deliv,2008,5(5):567-581.
[6] Kearns VR,Williams RL.Drug delivery systems for the eye[J].Expert Rev Med Devices,2009,6(3):277-290.
[7] 唐刚华,唐小兰,姜国辉,等.125I-神经生长因子的制备及其药代动力学研究[J].核化学与放射化学,2002,24(1):56-60.
[8] 楼宜嘉.药物毒理学[M].3版.北京:人民卫生出版社,2011:114-117.
[9] Molokhia SA,Jeong EK,Higuchi WI,et al.Transscleral iontophoretic and intravitreal delivery of a macromolecule:study of ocular distribution in vivo and postmortem with MRI[J].Exp Eye Res,2009,88(3):418-425.
[10] Urtti A.Challenges and obstacles of ocular pharmacokinetics and drug delivery[J].Adv Drug Deliv Rev,2006,58(11):1131-1135.
[11] Ocular pharmacokinetics:topical,intravitreal,and systemic drug application[J].Ophthalmologe,2014,111(2):104-106.
[12] Kang-Mieler JJ,Osswald CR,Mieler WF.Advances in ocular drug delivery:emphasis on the posterior segment[J].Expert Opin Drug Deliv,2014,11(10):1647-1660.
[13] Krohne TU,Holz FG,Meyer CH.Pharmacokinetics of intravitreally administered VEGF inhibitors[J].Ophthalmologe,2014,111(2):113-120.
[14] Pitkanen L,Ranta VP,Moilanen H,et al.Permeability of retinal pigment epithelium:effects of permeant molecular weight and lipophilicity[J].Invest Ophthalmol Vis Sci,2005,46(2):641-646.
[15] Rawas-Qalaji M,Williams CA.Advances in ocular drug delivery[J].Curr Eye Res,2012,37(5):345-356.
