咪达那新凝胶的制备及其体外经皮透过性
2015-03-08蔡晨辰王荣雪于洪丹王俊伟何仲贵
蔡晨辰,王荣雪,于洪丹,王俊伟,何仲贵,徐 晖
(沈阳药科大学 药学院, 辽宁 沈阳 110016)
咪达那新凝胶的制备及其体外经皮透过性
蔡晨辰,王荣雪,于洪丹,王俊伟,何仲贵,徐 晖*
(沈阳药科大学 药学院, 辽宁 沈阳 110016)
目的制备咪达那新凝胶,考察药物的体外经皮透过性,探讨咪达那新经皮给药的可行性。方法制备了以羟丙纤维素为胶凝剂的咪达那新水-醇凝胶。采用水平扩散池,以大鼠腹部全皮为渗透膜,筛选经皮通透促进剂;采用Franz扩散池,分别用微孔滤膜和大鼠腹部全皮为渗透膜,研究咪达那新凝胶剂的药物释放和体外经皮通透性。结果Azone、油酸和肉豆蔻酸异丙酯等对咪达那新的经皮通透性有较好的促进效果。咪达那新凝胶中,乙醇、1,2-丙二醇和Transcutol P在一定浓度范围内对药物累积经皮通透量无显著影响,促渗剂azone能显著增加药物的累积经皮通透量。结论Azone作为渗透促进剂加入咪达纳新凝胶剂中,可显著增加药物的经皮透过性,咪达那新经皮给药制剂的研发具有可行性。
药剂学;凝胶剂;经皮给药;通透促进剂;咪达那新
膀胱过度活动症(over active bladder,OAB)是一种以尿急症状为特征的征候群,常伴有尿频和夜尿,或伴有急迫性尿失禁,严重降低患者的生存质量[1-2]。咪达那新(imidafenacin)作为一种新型二苯基丁酰胺类抗胆碱药,具有高度膀胱选择性,临床用于膀胱过度活动症的治疗。咪达那新薄膜包衣片和口腔崩解片已在日本上市,其缓释片、贴剂也有研究报道[3-4]。
OAB的多发群体主要为老年人或某些精神疾病患者,该群体大多存在服药吞咽困难的问题[5]。与传统制剂相比,经皮给药制剂具有避免首过效应、缓控释作用、降低药物对胃肠刺激、患者顺应性较好以及易于调节给药剂量等优点,在过去的30年间,上市的经皮给药制剂并不多,主要是由于皮肤的屏障作用,仅少数具有适宜理化性质的活性成分适用于经皮给药,如相对分子质量≦ 400~500,且油水分配系数logP应在2.0~3.0内等[6-8]。咪达那新相对分子质量为319.40(化学结构式见图1),熔点为192~196 ℃,油水分配系数(25 ℃)log P=2.15±3.54×10-2(Scifinders数据库),给药剂量低(每日口服剂量0.2 mg)[9],其理化性质和作用特点具有很好的经皮给药的可行性。
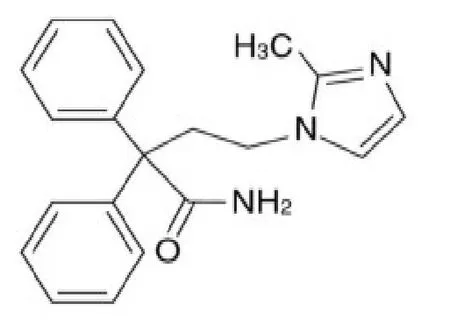
Fig. 1 The chemical structure of imidafenacin图1 咪达那新的化学结构式
本研究中,作者制备了咪达那新水-醇凝胶, 考察不同经皮通透促进剂和其他凝胶组成成分对药物经离体大鼠皮肤通透性的影响,以探讨咪达那新经皮给药的前景。
1 仪器与材料
L-2000高效液相色谱仪(日本Hitachi公司),YB-P6智能透皮仪实验仪(天津药典仪器厂)。
咪达那新(含量质量分数>99.0%,自制),高黏度羟丙纤维素(hydroxypropyl cellulose-high viscosit,HPC-H,日本NISSO 公司),无水乙醇(天津市大茂化学试剂有限公司),1,2-丙二醇(propylene glycol,PG,国药集团化学试剂有限公司),N-甲基吡咯烷酮(1-methyl-2-pyrrolidinone,NMP,国药集团化学试剂有限公司),肉豆蔻酸异丙酯(isopropyl myristate,IPM,国药集团化学试剂有限公司),油酸(oleic acid,OA,国药集团化学试剂有限公司),薄荷脑(江苏华神药业有限公司),氮酮(azone,国药集团化学试剂有限公司),二乙二醇单乙基醚(diethylene glycol monoethyl ether, Transcutol P,法国Gattefossé公司)。
SD大鼠,雄性,体质量为(230±20)g ,购自辽宁长生生物技术有限公司,许可证号为SCXK(辽)2010-0001。
2 方法与结果
2.1 咪达那新的测定方法
采用HPLC法测定咪达那新。色谱条件如下:色谱柱为DiamonsilⅡ® C18柱(200 mm×4.6 mm,5 µm),流动相为乙腈-20 mmol·L-1Na2HPO4缓冲液(磷酸调pH至7.45)(体积比为41∶59),流速为1.0 mL·min-1,柱温为40 ℃,检测波长为220 nm。该方法专属性良好,咪达那新质量浓度在1.0 ~100.0 mg·L-1内线性关系良好,经验证方法学符合要求。
2.2 经皮通透促进剂的筛选
采用水平扩散池,考察不同经皮通透促进剂对咪达那新经大鼠离体全皮透过的影响。将鼠皮固定在扩散池(有效扩散面积1.13 cm2)两池之间,供给池中加入质量分数为5%通透促进剂-乙醇溶液处理鼠皮角质层4 h,无水乙醇冲洗皮肤表面,加入3.5 mL咪达那新饱和溶液(溶剂为质量分数为40%的PG水溶液),接收池加入等量接受液[乙醇- Na2HPO4缓冲液(pH值5.8)体积比为10∶90的溶液],37 ℃恒温磁力搅拌,分别于2、5、8、11、19和24 h取样3.0 mL,同时补加等体积的等温接受液。样品经0.45 µm微孔滤膜过滤,取续滤液,HPLC法测定,计算累积透过量 [Qt(/g·m-2)]、稳态流量[Jss/(µg·h-1·m-2)]、通透系数[P/(cm·h-1)]和迟滞时间(tlag/h),结果见图2和表1。
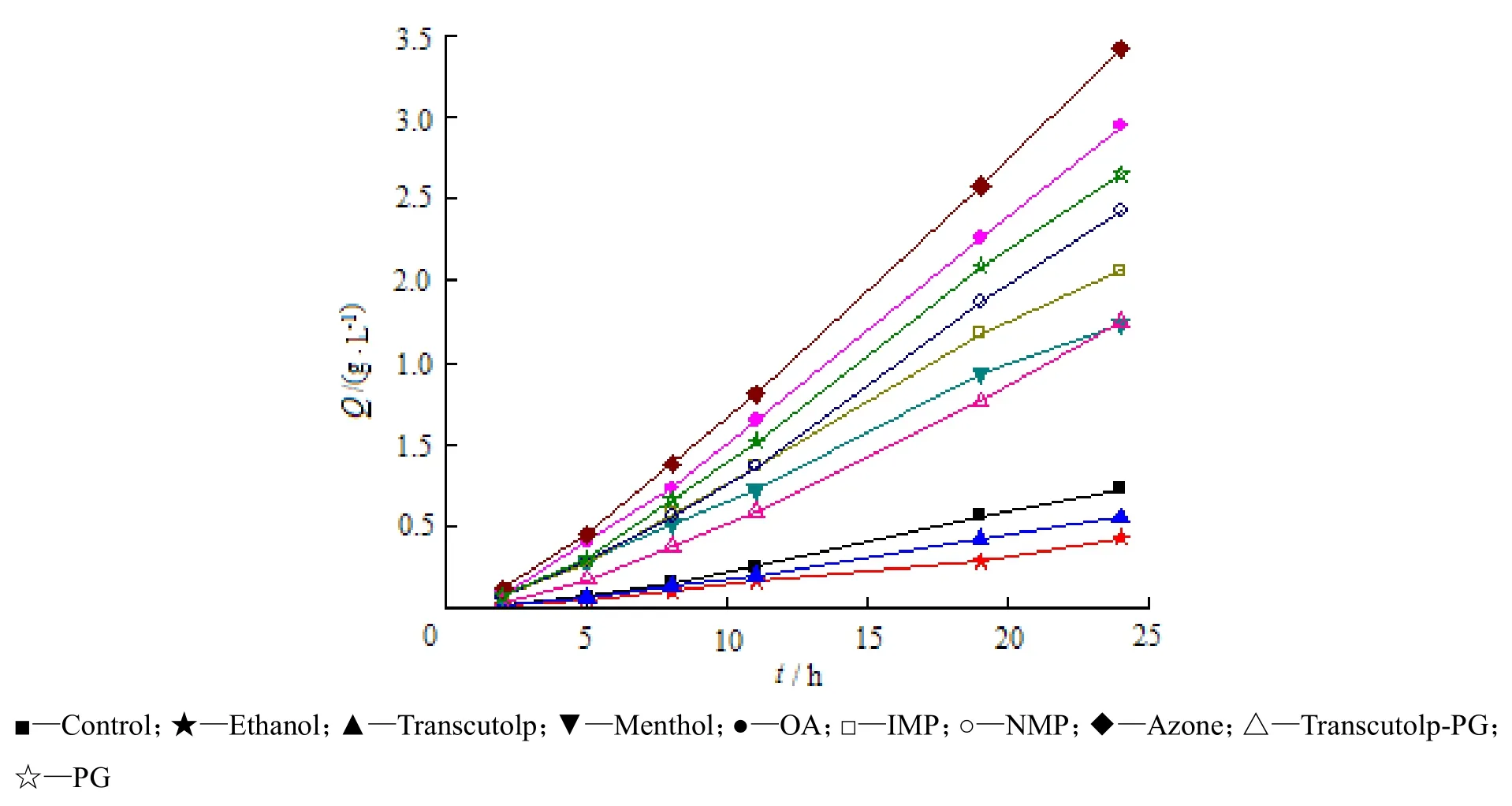
Fig. 2 Plots of the accumulative imidafenacin penetrated across rat skin versus time (n=4,±s)图2 咪达纳新经鼠皮的累积透过曲线(n=4,±s)
Table 1 The lag time(tlag), steady-state fluxes(Jss) and permeation coefficient(P) of imidafenacin penetration across rat skin(n=4,±s)表1 咪达纳新鼠皮透过性实验中的滞后时间(tlag)、稳态流量(Jss)、通透系数(P)结果(n=4,±s)
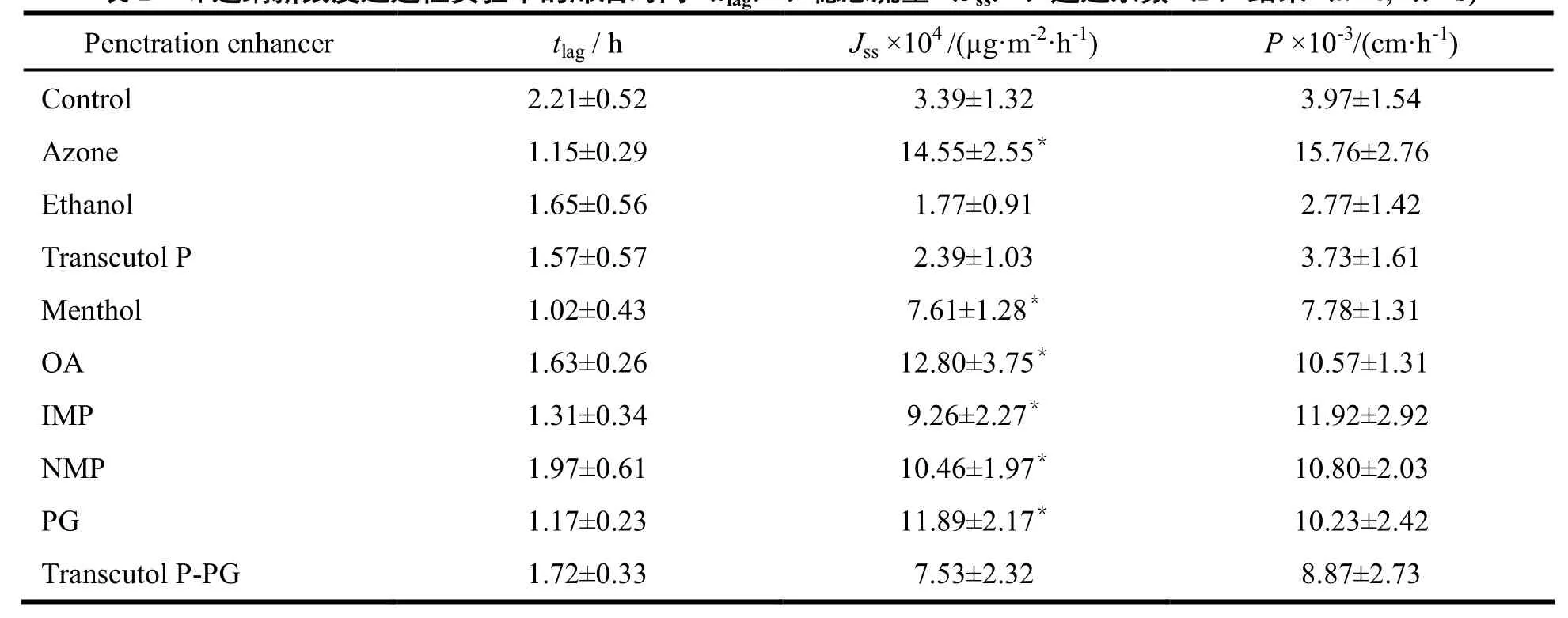
Table 1 The lag time(tlag), steady-state fluxes(Jss) and permeation coefficient(P) of imidafenacin penetration across rat skin(n=4,±s)表1 咪达纳新鼠皮透过性实验中的滞后时间(tlag)、稳态流量(Jss)、通透系数(P)结果(n=4,±s)
Note: *— P<0.05 when compared to control
Penetration enhancer tlag/ h Jss×104/(µg·m-2·h-1) P ×10-3/(cm·h-1) Control 2.21±0.52 3.39±1.32 3.97±1.54 Azone 1.15±0.29 14.55±2.55* 15.76±2.76 Ethanol 1.65±0.56 1.77±0.91 2.77±1.42 Transcutol P 1.57±0.57 2.39±1.03 3.73±1.61 Menthol 1.02±0.43 7.61±1.28* 7.78±1.31 OA 1.63±0.26 12.80±3.75* 10.57±1.31 IMP 1.31±0.34 9.26±2.27* 11.92±2.92 NMP 1.97±0.61 10.46±1.97* 10.80±2.03 PG 1.17±0.23 11.89±2.17* 10.23±2.42 Transcutol P-PG 1.72±0.33 7.53±2.32 8.87±2.73
结果表明,azone、OA和PG处理过的鼠皮,药物通透的时滞较短、促渗效果较明显,适合用作咪达那新凝胶剂的通透促进剂。
2.3 咪达那新凝胶剂的制备和体外经皮透过性
实验参考奥昔布宁凝胶剂(Gelnique™)的组成,以HPC为凝胶基质,乙醇、PG、Transcutol P和去离子水为溶剂,制备咪达那新水-醇凝胶[10-13],处方组成见表2。将HPC均匀分散在热水中,咪达那新溶解于上述有机溶剂中,缓慢搅拌下混合均匀,加去离子水至处方量,置冰水浴中冷却,匀速搅拌至形成细腻、黏稠度适宜的凝胶,冷藏保存。
采用Franz立式扩散池,考察凝胶处方中各成分对咪达那新经大鼠皮肤透过的影响。将鼠皮固定在两扩散池(有效扩散面积1.13 cm2)之间,并称取约1.0 g咪达那新凝胶,置于给药池一侧(实验过程中,凝胶为非封闭状态),接收池中加入5.5 mL接受液,将扩散池置于智能透皮试验仪中,设定温度37 ℃、转速100 r·min-1,分别于3、6、9、12和23 h取样3.0 mL,同时补加等体积的等温接受液,其他操作和数据处理同“2.2”条。
Table 2 The composition of the imidanafacin gels(n=4,±s)表2 咪达纳新凝胶剂的处方组成(n=4,±s)
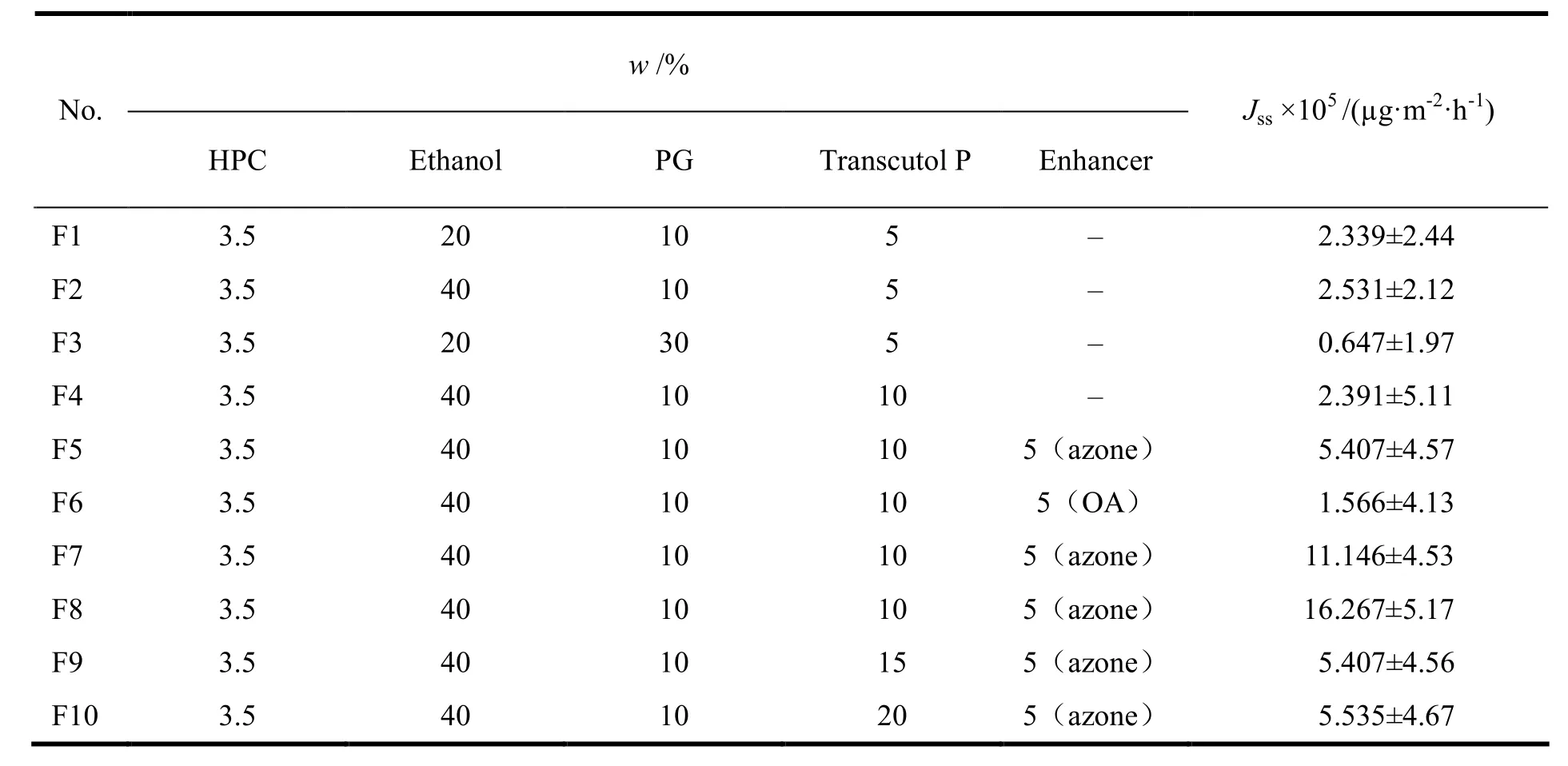
Table 2 The composition of the imidanafacin gels(n=4,±s)表2 咪达纳新凝胶剂的处方组成(n=4,±s)
Note: The drug contents(w)of all the gels were 0.2%, except those of F7 and F8 were 0.4%and 0.6%, respectively
w /% No. HPC Ethanol PG Transcutol P Enhancer Jss×105/(µg·m-2·h-1) F1 3.5 20 10 5 - 2.339±2.44 F2 3.5 40 10 5 - 2.531±2.12 F3 3.5 20 30 5 - 0.647±1.97 F4 3.5 40 10 10 - 2.391±5.11 F5 3.5 40 10 10 5(azone) 5.407±4.57 F6 3.5 40 10 10 5(OA) 1.566±4.13 F7 3.5 40 10 10 5(azone) 11.146±4.53 F8 3.5 40 10 10 5(azone) 16.267±5.17 F9 3.5 40 10 15 5(azone) 5.407±4.56 F10 3.5 40 10 20 5(azone) 5.535±4.67
通过分析比较各处方的经皮透过曲线,发现一定范围内改变处方中乙醇(图 3中 F1、F2)及Transcutol P(图3中F2、F4)的组成对制剂中的药物无明显促渗作用,这一结果也与通透促进剂筛选中实验结论一致,而处方中PG含量则对药物的皮肤透过性产生显著性的影响,见图3中F1、F3,实验初期,二者透皮曲线无显著性差异,但在5 h后,高PG含量处方F3的皮肤透过速率较F1有显著降低变缓的趋势,累积透过量显著性降低。此外考察了促渗剂对制剂中药物的透皮行为的影响,结果见图4。当制剂中加入azone,咪达纳新的经皮透过性明显得到改善,且azone的促渗能力明显优于OA。比较处方F5、F7、F8的经皮透过曲线(图5),制剂中咪达纳新的含量质量分数分别为0.2%、0.4%和0.6%的凝胶剂,其药物经皮透过的稳态流量Jss分别为5.4.×105、1.11×106和1.63×106µg·m-2·h-1,即在一定范围内,Jss与药物含量呈线性关系。实验进一步考察Transcutol P是否与azone存在协同效应,增加促渗效果,实验结果表明(图6),增加Transcutol P对药物的皮肤透过性不存在显著性的促渗作用,该处方中二者不存在协同作用。
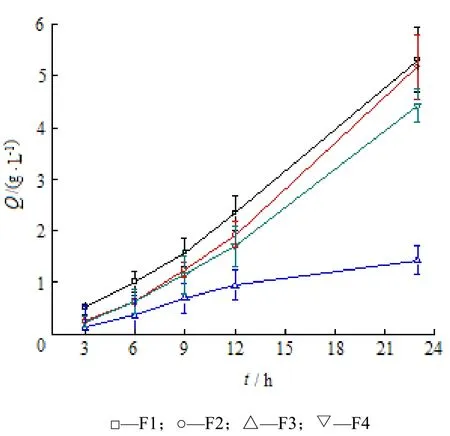
Fig. 3 The influence of the compositions of F1, F2, F3, F4 on the transdermal penetration of imidafenacin across rat skin (n=4,±s)图3 F1、F2、F3、F4中各组成成分对咪达纳新鼠皮透过性的影响考察(n=4,±s)

Fig. 4 The influence of the compositions of F4, F5, F6 on the transdermal penetration of imidafenacin across rat skin(n=4,±s)图4 F4、F5、F6中各组成成分对咪达纳新鼠皮透过性的影响考察(n=4,±s)
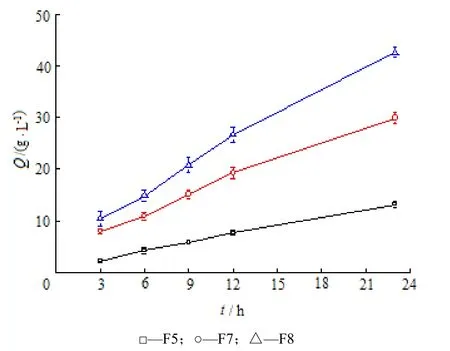
Fig. 5 The influence of the compositions of F5, F7, F8 on the transdermal penetration of imidafenacin across rat skin(n=4,±s)图5 F5、F7、F8中各组成成分对咪达纳新鼠皮透过性的影响考察(n=4,±s)
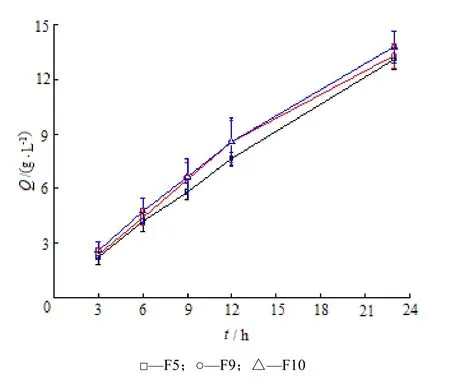
Fig. 6 The influence of the compositions of F5, F9, F10 on the transdermal penetration of imidafenacin across rat skin (n=4,±s)图6 F5、F9、F10中各组成成分对咪达纳新鼠皮透过性的影响考察(n=4,±s)
实验结果表明,与其他处方比较,F5中药物的皮肤累积透过量显著增加,azone对药物具有显著性的促渗作用。
2.4 咪达那新凝胶的释放度
释放度实验采用与凝胶剂经皮透过实验相同的立式扩散池装置和方法,但以0.45 µm孔径的微孔滤膜为渗透膜,分别于0.5、1.0、3.0、6.0、9.0和12.0 h取样,HPLC方法测定。表2中凝胶F1、F2、F3、F4、F5和F6的药物累积释放曲线见图7。
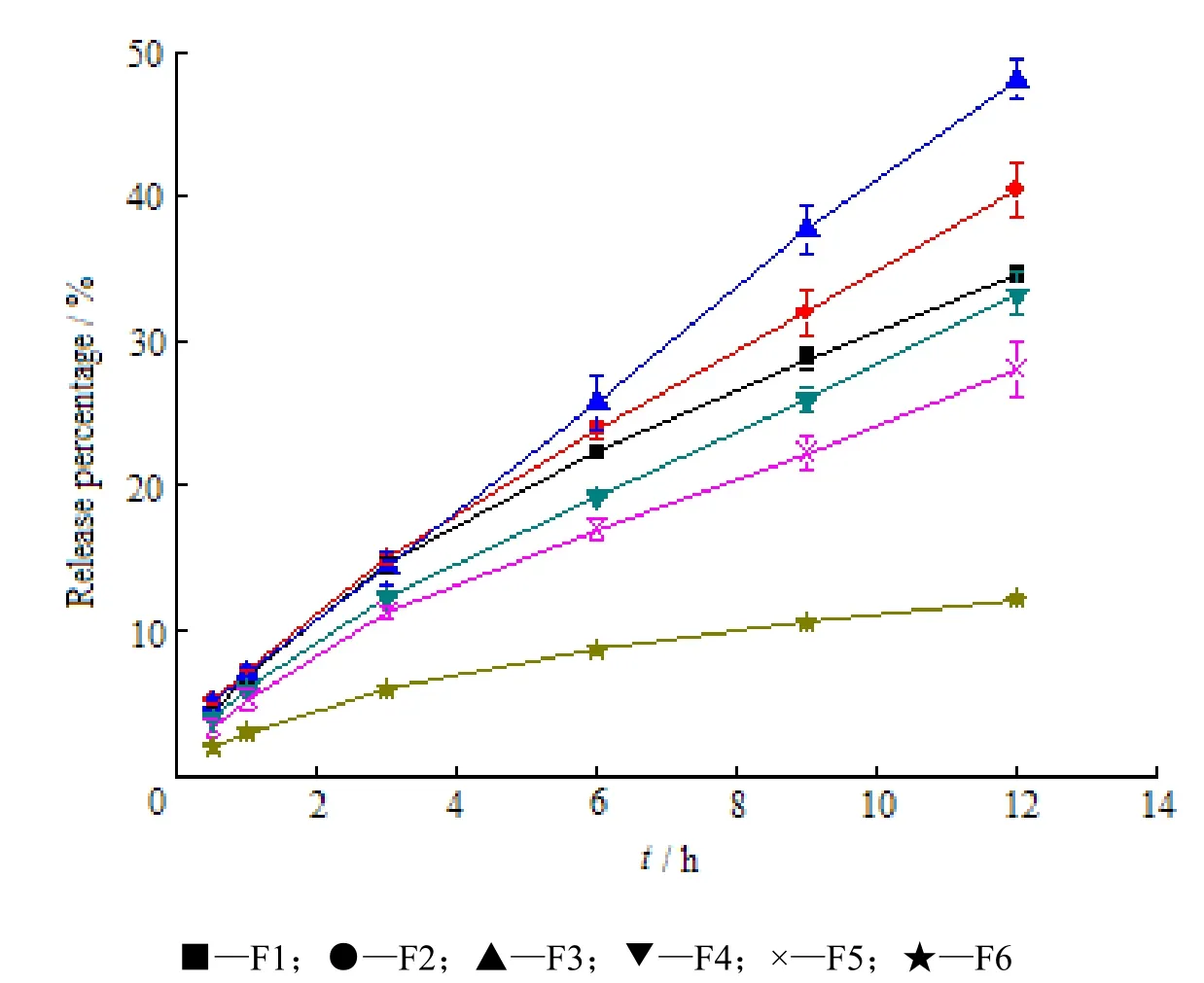
Fig. 7 The drug release profiles of typical imidafenacin gels (n=4,±s)图7 咪达那新凝胶剂的药物释放曲线(n=4,χ±s)
3 讨论
3.1 乙醇、PG和Transcutol P对药物经皮透过的影响
在制备含药凝胶时,处方中加入一定量的乙醇、PG或Transcutol P,主要是基于以下两方面的考虑:溶剂系统应保证药物和通透促渗剂在基质中呈溶解状态;促渗剂azone与PG间存在一定的协同作用,在适当的比例条件下产生更好的促渗效果[16]。
实验中考察了不同比例乙醇PGTranscutol P(F1、F2、F3、F4)对咪达纳新皮肤累积透过量的影响。
促渗剂筛选实验结果表明PG具有较好的促渗效果,故处方在进行筛选时尝试增加PG含量以期获得良好的皮肤透过性,但发现当处方中PG含量增加至30%时,药物的皮肤累积透过量显著性降低,基于两种相悖的实验结果,继而考察了该处方的体外释放行为,结果显示基质对药物具有良好的释放性能,说明影响制剂中药物透皮行为的关键因素并非药物的释放过程,更可能是药物的透皮过程。当PG在加入到凝胶中后,与 HPC-H及Transcutol P等存在复杂的相互作用,其存在形式,较在促渗剂筛选实验中的状态可能发生改变,对皮肤结构影响的程度也会存在一定的差异性。总的来说,在该给药系统中,PG不但不能显著性改善药物的皮肤透过性,同时,一味增加PG的量还可能导致药物皮肤累积透过量的降低,综合考虑PG的保湿作用及溶剂作用,确定质量分数为10% PG为最终处方用量。
处方中Transcutol P并不能有效改善药物的经皮通透性,但考虑到具有高乙醇含量的处方挥发性强,进而导致制剂在贮存过程中的释药行为及透皮行为发生改变;同时,Transcutol P,对药物及促渗剂均具有较好的增溶效用,因而在凝胶剂中加入适量Transcutol P以改善制剂中各组分的相容性及稳定性。
乙醇作为制剂中除水以外的最高含量的溶剂组分,增加其在制剂中的比例无法产生增渗作用(图3 中的F1、F2)。但事实上,乙醇在该给药系统中更多来承担是溶剂角色,以保证药物及促渗剂azone及OA的溶解状态;同时,过高的乙醇含量亦会影响制剂的最终稳定性,故质量分数为40%乙醇,刚好可溶解处方量的药物及促渗剂,作为乙醇的最终用量。
通常认为影响制剂中药物的皮肤累积透过量的主要因素包括:a.基质的释药能力;b.皮肤的屏障作用。对不含促渗剂的处方(F1、F2、F3、F4),仅通过改变PG、Transcutol P或者乙醇等有机溶剂的比例,虽可影响基质的释药能力(图 7),却无法显著性改善药物的经皮透过能力,换句话说,在此类处方中,影响药物的皮肤透过性的主要因素仍是皮肤的屏障作用。
3.2 促渗剂对药物经皮透过的影响
由促渗剂筛选实验结果表明,促渗剂azone、OA、NMP及IMP均具有良好促渗效果,因而从中选择azone、OA为促渗剂,进一步对制剂处方进行优化。
值得注意的是,azone的促透作用通常有较长的迟滞时间[14-16],通透促进剂筛选实验也得到同样的结果,而当azone加至凝胶剂(azone含量质量分数为5%)中,不仅药物的经皮透过性得到改善,其迟滞时间也相应变短;与之相比,以OA为促渗剂的制剂经皮累积透过量却未有显著性提升。
分析这一实验结果可能与azone,OA的存在形式有关。据相关文献报道,azone及OA都可以通过改变磷脂双分子层的相转变行为,打乱角质层中脂质结构的有序紧密排列,增加角质细胞间脂质的流动性,从而降低皮肤屏障作用,进而增加药物的累积皮肤通透量[14-15]。
对于OA,其脂溶性强于azone,在水溶性凝胶剂基质中的溶解度有限。一方面,通透促进剂筛选实验中,OA主要以分子形式存在乙醇溶液中,可渗入皮肤角质层,打乱紧密排列的磷脂双分子层结构;而在凝胶制剂中,OA作为一种脂溶性成分,在该凝胶基质中基本处于近饱和的状态,随着制剂中乙醇的挥发和扩散,OA达到饱和并以油滴的形式析出(可见凝胶呈不透明的乳胶状),非分子状态的OA渗入皮肤的量有限,因而改变其“砖块结构”的能力有限,对药物的促渗效果并不明显;另一方面,由咪达那新释放曲线(图7)结果可以看出,含OA的凝胶(F6)的药物释放速率明显低于含azone的处方(F5)及不含促渗剂的处方(F4),由于药物在OA中的溶解度更高,药物更易分配在含OA的基质中,导致药物的释放速率更低,药物释放缓慢可能是导致经皮通透性差的重要原因之一。
而对于含有azone的凝胶,体系的相容性较好,外观澄清透明;另外处方中所含有的PG可能在一定程度上增强azone的促渗作用。有文献报道,PG与azone合用可显著缩短azone的迟滞时间,存在协同促渗作用[16]。
[1] HENDERSON E, DRAKE M. Overactive bladder[J]. Maturitas, 2010, 66(3): 257-262.
[2] WEIN A J, ROVNER E S. Definition and epidemiology of overactive bladder[J]. Urology, 2002, 60(5): 7-12.
[3] AOKI Y, ISHIZAKI T, KAZAMA K, et al. Multiple unit oral sustained release preparation and production method thereof: US, 795792[P]. 2006-01-30.
[4] KURITA H. Percutaneously absorbed preparation: US, 881807[P]. 2011-10-26.
[5] 张惠芹, 袁秀红, 覃惠英. 老年人尿失禁易患因素及处理现状[J]. 现代临床护理, 2006, 5(5): 83-85.
[6] 崔福德. 药剂学[M]. 6版. 北京: 中国医药科技出版社, 2002: 469-472.
[7] DELGADO-CHARRO M B,RICHARD G. Effective use of transdermal drug delivery in children[J]. Adv Drug Deliv Rev, 2013, 73(30): 63-82.
[8] WIEDERSBERG S, RICHARD G. Transdermal drug delivery: 30+ years of war and still fighting[J]. J Control Release, 2014, 190(28): 150-156.
[9] SAKAKIBARA R, TATENO F, YANO H, et al. Effect of imidafenacin on urinary sensation and activity in prefrontal micturition area in patients with over-active bladder[J]. Autonomic Neuroscience, 2013, 179(1/2): 173-176.
[10] SANTOS P, MACHADO M, WATKINSON A C, et al. The effect of drug concentration on solvent activity in silicone membranes[J]. International Journal of Pharmaceutics, 2009, 377(1/2): 70-75.
[11] AARMA M V,KAUSHAL A M,GARG S. Influence of micro-environmental pH on the gel layer behavior and release of a basic drug from various hydrophilic matrices[J]. Journal of Controlled Release, 2005, 103(2): 499-510.
[12] EBERT C D,SANDERS S W. Compositions and methods for transdermal oxybutynin therapy: US, 8241662(B2)[P]. 2012-08-14.
[13] 王英姿, 任天池, 肖永庆. 不同透皮促进剂对高乌甲素凝胶体外透皮吸收的影响[J]. 中国中药杂志, 2005, 33(11): 665-668.
[14] MORIMOTO Y, SUGIBAYASHI K, KEN-ICHI H, et al. Penetration enhancing effect of Azone on the transport of 5-fluorouracil across the hairless rat skin[J]. International Journal of Pharmaceutics, 1986, 32(1): 31-38.
[15] BEASTALL J C, WASHINGTON C, HADGRAFT J, et al. Mechanism of action of Azone as a percutaneous penetration enhancer: Lipid bilayer fluidity and transition temperature effects[J]. International Journal of Pharmaceutics, 1988, 43(3): 207-213.
[16] 郑俊民. 经皮给药新剂型[M]. 北京: 人民卫生出版社, 2006: 45-46.
Preparation and in vitro transdermal penetration of imidafenacin gels
CAI Chen-chen,WANG Rong-xue,YU Hong-dan,WANG Jun-wei,HE Zhong-Gui,XU Hui*
( School of Pharmacy,Shenyang Pharmaceutical University,Shenyang 110016,China)
ObjectiveTo prepare imidafenacin gel, investigate the penetration of imidafenacin through rat skin in vitro, and discuss the potential of transdermal delivery of imidafenacin.MethodThe imidafenacinhydro-alcoholic gels were prepared using HPC as the gelling agent, and horizontal diffusion cell method was used to screen the permeation enhancer through full-thickness rat skin; The in vivo drug release and transdermal penetration of imidafenacin were investigated with Franz diffusion cells using microporous membrane and rat skin as the permeation membrane, respectively.ResultsThe Azone and oleic oil showed the optimum enhancement in penetration. The contents of ethanol, PG and Transcutol P in the gels had little influence on the permeation of imidafenacin, while Azone, as an enhancer, could promote the accumulated penetration remarkably.ConclusionOf the penetration enhancers investigated, Azone was found to improve notably the transdermal penetration of imidafenacin, and our studies indicated potential of transdermal delivery of imidafenacin.
pharmaceutics; gelling agent; permeation enhancer; transdermal; imidafenacin
R94
A
(本篇责任编辑:吕向一)
(2015)03-0097-10
10.14146/j.cnki.cjp.2015.03.003
2014-11-25
蔡晨辰( 1989-),女( 汉族),湖北襄樊人,硕士研究生,E-mail ccqqcw@163. Com;*通讯作者: 徐晖( 1972-),男( 汉族),辽宁法库人,副教授,博士,主要从事药物新剂型与药用高分子材料研究,Tel. 024-23986356,E-mail xuhui-lab@163.com。
