三氯生在水环境中的迁移及降解技术研究进展
2015-02-28王秀娟丘锦荣田应兵周建利刘清云
王秀娟,丘锦荣,田应兵,周建利,赵 涛,刘清云
(1.长江大学农学院,湖北荆州 434025;2.环境保护部华南环境科学研究所,广东广州 510642)
三氯生在水环境中的迁移及降解技术研究进展
王秀娟1,2,丘锦荣2*,田应兵1,周建利1,赵 涛2,刘清云2
(1.长江大学农学院,湖北荆州 434025;2.环境保护部华南环境科学研究所,广东广州 510642)
三氯生作为广谱抗菌剂被广泛使用,因其亲脂性容易被生物体富集并进入食物链中,因此,三氯生的生物毒性给生态环境带来的威胁是潜在和不可预测的。简述了国内外近年来对水体中三氯生的处理技术,比较了各种处理技术的优劣。结果表明,高级氧化技术具有反应快速、彻底、矿化度高等优点,但其处理费用较高,因此研发经济可行的高级氧化技术成为未来处理水环境中三氯生的研究方向。
三氯生; 毒性; 迁移转化; 降解
三氯生,学名二氯苯氧氯酚,又名“三氯新”、“三氯沙”等,作为抗菌素和抗菌剂被认为对人体无急性毒性和对眼睛、皮肤无刺激性而被广泛使用。具有广谱抗菌性,在0.1%~0.3%的质量浓度时就对革兰氏阳性菌、革兰氏阴性菌、霉菌和酵母菌有抑制效果[1]。其用于个人护理品至少已有50年的历史,早在20世纪60年代,美国就已经开始使用含三氯生的腋下除臭剂和除臭香皂,到了1972年,1%的三氯生开始作为医药工业的消毒液,1985年在欧洲开始使用含三氯生的牙膏[2]。到了2002年,欧洲每年用于商业产品的三氯生就达350 t[3]。在世界范围内,三氯生在抗菌剂中的使用每年以5.4%的速率递增[4]。如今,三氯生有着更加广泛的应用:个人护理类产品的抗菌霜、洗涤液、洗发水等,日用消费类产品的纤维织品、运动鞋袜类,医疗用品消毒等[5]。
过去人们一度认为三氯生是安全低毒的,因此尚未得到足够重视。但是随着其广泛使用,环境中检测到的含量越来越高。尽管三氯生的半衰期较短,但是由于长期大量输入环境中,使得三氯生呈现出一种“持续性存在的状态”。其生物毒性、类似于内分泌干扰物的特征、降解过程的中间和最终产物的高毒性等引起了研究者们的极大重视。
1 三氯生介绍
1.1 三氯生物理化学性质三氯生的化学结构式见图1。其最早是由瑞士的巴塞尔人Ciba-Geigy Co合成的,分子量为289.5,熔点为 (57±1)℃,米白色,无臭,无味,结晶性粉末,不易溶于水,易溶于有机溶剂,具有热稳定性,难挥发,能在150~200 ℃稳定加热2 h。三氯生是一种相对亲脂化合物,正辛醇/水分配常数lgKow为5.4[6]。其在水中溶解度较低,在20 ℃下其溶解度仅为10 mg/L[1]。
1.2 三氯生安全性由于污水处理厂出水是三氯生进入环境的主要途径,污水厂出水受纳河流的水生生物直接暴露于较高浓度的三氯生下。三氯生对水生生物的毒性效应已有许多报道:如严重影响河流的生物膜,使其大幅降低光合效率、细菌和硅藻的生存发育能力以及磷酸盐的吸收等[7]。Davidr Orvos等研究三氯生对活性污泥微生物、藻类、无脊椎动物和鱼的影响,其中藻类被认为是最容易受感染的生物[8]。有研究表明,0.42 μg/L的三氯生就会抑制水藻的光合作用[9],而青鳉鱼暴露于0.17 mg/L的三氯生下5~9 d游泳速度就会受影响[10]。Ximei Liang等用6个月的剑尾鱼做三氯生的急性试验,当雌性剑尾鱼暴露在三氯生时,其CYP1A、CYP3A、GST和P-gp的 mRNA表达量呈现剂量-效应关系[11]。Consuelo Riva等用斑马贻贝做三氯生毒性试验,结果证明三氯生会诱导产生氧化应激反应、引起斑马贻贝蛋白质表达谱的显著改变,并且三氯生对多种生物过程有显著的影响,特别是那些参与钙离子结合或应激反应[5]。
三氯生对土壤生物也有影响,Dasong Lin等证明三氯生毒性会引起蚯蚓的氧化应激反应,并且反应产生的物质会导致DNA损伤。成年蚯蚓暴露14 d,EC10(对存活无影响浓度)为32 mg/kg(干重土壤中含三氯生)[12]。同样,三氯生对植物也有影响,芜菁暴露21 d,EC50(对存活无影响浓度)为3 mg/kg[13]。此外,三氯生还具有潜在的雌激素效应[14],利用的酶也是双酚A(动物试验发现有模拟雌激素的效果)代谢和分泌的关键酶[15],是内分泌干扰物,会扰乱人类与动物体内正常的内分泌功能。
三氯生引起广泛关注的重要原因还有其降解中间或最终产物具有生物毒性。甲基三氯生(Me-三氯生)是有氧条件下三氯生生物降解产物[16-17],但是它比母体化合物的亲脂性更强,性质更加稳定,更容易在脂肪组织上富集,光稳定性更强[18-19]。另外,在饮用水处理消毒中的氯会与三氯生反应生成氯仿和醚类等有毒有害物质[20],直接危害人体健康。由于三氯生的化学结构与高毒物质二噁英很相似,其在光转化过程中会产生二噁英类物质[21-23](图1)。三氯生的光转化条件是一类比较温和的反应条件,有时只需自然光照射该过程便能完成。而产物二噁英类物质比母体化合物毒性更强,稳定性更高,具有强烈的致癌毒性、生殖毒性和遗传毒性。
2 迁移
三氯生作为一种新兴污染物,不同于持久性有机污染物(POPs)的“难降解”、“全球性循环”等特征,其挥发性较弱,不会像POPs通过“蒸发”进行全球范围内的迁移。三氯生在环境中的分布主要是通过水相传递和食物链扩散(图2)。
含三氯生的产品使用后,最终大部分会随污水进入污水处理厂。研究表明,超过95%的含三氯生的消费产品使用后随污水排放系统进入污水处理厂[24-25]。但是,目前的污水处理系统并未能让三氯生得到有效处理。有研究表明,在污水处理过程中只有2%~4%的三氯生随废水排出,30%~50%被污泥吸附,48%~65%通过生物和其他方式降解[4,26]。而且不同污水处理工艺对三氯生的去除效果影响巨大,采用活性污泥、氧化沟、串联氧化塘、生物反应器、滴滤等不同工艺净化污水,其污水处理厂出水口含三氯生浓度变化幅度为60.5~22 100.0 ng/L[4,16,18,21,23,26-28]。虽然只有少部分三氯生随污水厂出水进入环境中,但是由于污水处理厂出水频繁,使得这成为三氯生进入环境水体的重要方式。
此外,农业土地施用有机污泥是三氯生进入环境水体的又一方式。污泥施用于农用土地在世界上许多地方都是比较常见的。在加拿大安大略省,每年约有120万t(干重)污泥被应用到大约15 000 hm2的农业用地[29]。然而,在污泥施用后,三氯生的性质决定了其不会显著挥发,污泥中的三氯生通过淋溶渗滤等方式进入环境水体中[17,30]。
目前三氯生在环境中几乎无所不在。1999~2000年美国地质调查局对全国30个州139条河流进行调查,最常出现的7种化合物就包含三氯生,检测频率高达57.6%[31]。在中国、瑞士、印度、德国和加拿大地表水中,三氯生的浓度范围为0.008~944.000 ng/L[1,18,32-36]。在西班牙一个污水处理厂出水受纳海洋中测定海洋沉积物中三氯生含量,在离出水口20 m深度为20~40 m的海洋沉积物中,三氯生的质量浓度达0.27~130.70 μg/kg[21]。
由于三氯生的疏水亲脂性质,水生生物如水藻、紫贻贝、虹鳟鱼、斑马鱼、大西洋宽吻海豚[8,19,37-39]都会富集三氯生。三氯生还会通过食物链甚至通过人体皮肤直接接触吸收[40],最终在人体中存在和富集。目前人的母乳、血浆、脑、肝脏、脂肪组织都能检测到三氯生[37,41-42]。
3 三氯生处理技术
3.1 吸附一些常用的吸附剂如活性炭和粘土可以有效去除水中的三氯生。土壤对三氯生的吸附受pH和有机质含量的影响。在碱性条件下,三氯生分子电离,离子间产生排斥力,使得土壤对其吸附量下降。土壤有机质含量较少,三氯生的吸附量也减少,而且土壤对三氯生的吸附几乎是不可逆转的[43]。Shishir Kumar Behera等研究3种吸附剂(活性炭、高岭土和蒙脱石)在不同pH和离子强度下对三氯生的吸附能力。结果表明,活性炭对三氯生的吸附能力最强,吸附剂的吸附能力随着溶液离子强度增加而增加。对pH而言,在酸性范围的吸附能力较碱性高,高岭石和蒙脱石在pH为3时对三氯生的吸附量分别为6.4、19.3 mg/g,当pH为10时吸附量分别降到了1.5、3 mg/g[44]。琚丽婷用蒙脱石负载纳米铁镍处理三氯生,既提高了蒙脱石的比表面积,又能有效克服纳米铁易团聚和易氧化的特点。在28 ℃,pH=7时,三氯生(初始浓度为6 mg/L)去除率达63%[45]。
此外,沸石具有较大的比表面积和阳离子交换量也常被用作吸附剂,何敏祯以天然沸石为原料,用十六烷基三甲基溴化铵(HDTMA)溶液对天然沸石改性。改性沸石对三氯生的吸附效率远快于原沸石,前者在2 h内就达到吸附平衡,后者则需24 h。去除率也大幅度提高,改性沸石对三氯生的去除率达85.00%以上,而原沸石只有4.95%[46]。雷超以离子交换的方式将阳离子表面活性剂溴化十六烷基吡啶(CPB)负载在原沸石外表面制备改性沸石,证明用CPB负载的沸石对三氯生的吸附亲和力较原沸石增加。3种CPB 改性沸石 OZ 0.5,OZ 1.0,OZ 2.5(将初始浓度为0.5、1.0、2.5 mmol/L的10 ml CPB溶液加入10 mg原沸石中充分震荡,离心得到改性沸石OZ 0.5,OZ 1.0,OZ 2.5)对三氯生的吸附平衡容量分别达到了27.15、39.66、41.14 mg/g,而原沸石只有0.91 mg/g[47]。
用吸附法处理去除水中三氯生能耗低、反应过程不产生有毒物质,但是吸附剂大多数使用一次就废弃,处理费用较高,并且只是将三氯生从水体中转移,却不能将其彻底转化为无害物。
3.2 生物降解技术Young-Mo Kim等利用可以降解芳香族化合物的鞘氨醇单胞菌PH-07(Sphingomonassp. PH-07)降解与芳香族化合物结构相似的三氯生。结果表明,这种菌株能使三氯生分解代谢形成几种中间体,并且主要中间体2,4-二氯苯酚对鞘氨醇单胞菌PH-07的毒性比三氯生低。同时也表明,醚键断裂是三氯生对这种菌株毒性减少的主要原因[48]。Do Gyun Lee等用丙烷培养基上的母牛分枝杆菌JOB5(MycobacteriumvaccaeJOB5)在3 d内就降解了大约95%的三氯生(5 mg/L),初始降解速率为每天每毫克蛋白质(包括活的和坏死的细菌)降解(0.021±0.003)mg的三氯生,并且释放0.27 mg/L的氯化物[49]。Varima Bokare等使用纳米零价铁和漆酶作为氧化还原两步混合系统,使得三氯生完全转化为无毒产品[50]。徐海丽在污水厂的活性污泥样品中分离得到了一株能够以三氯生为唯一碳源和能源的鞘氨醇单胞杆菌,该菌株能在 24 h内降解三氯生[51]。
土壤中也有能降解三氯生的微生物且降解过程中需氧,Guang-Guo Ying等发现在有氧的土壤中三氯生可以被生物降解,实验室条件下在有氧土壤中三氯生的生物降解半衰期为18 d,在试验进行的70 d内,在缺氧的土壤中三氯生几乎不能被降解[52]。Butler等1年内在3种质地的土壤的3个不同土层深度下观测三氯生的浓度变化。结果表明,三氯生浓度降低主要是因为生物降解、淋溶、生物扰动和转换成不可萃取的形态。它们的变化有很强的季节性,与土壤温度、水分含量、排水强度有关[17]。
虽然三氯生是可以被生物降解的,但是三氯生作为抗菌剂对微生物生长代谢可能会有影响。Shujuan Wang等用小球藻来净化三氯生,将藻细胞暴露在浓度为100~800 μg/L(根据废水中的浓度设计)的三氯生中,在1 h内就有超过50%的三氯生通过藻细胞的吸收而被移除。4 d后,在除去三氯生的非生物损失后,由小球藻引起的三氯生去除率达77.2%。但是对藻细胞的亚显微结构观察表明其叶绿体被破坏,导致藻细胞生长时能量供给降低,这就对三氯生生物降解的有效性产生不利影响[53]。
使用生物法降解经济,但是对环境条件和微生物种类的要求严苛,在污水处理厂的生物降解速率要低于实验室报道的速率,并且降解周期长,在污水处理厂中污水处理时间较短,不能提供完全降解三氯生的时间[16]。再者对三氯生降解产物的生态安全性也还有待研究。
3.3 高级氧化降解技术高级氧化以产生具有强氧化能力的羟基自由基为特点,在高温高压、电、声、光辐照、催化剂等反应条件下,几乎使所有难降解的有机污染物氧化成低毒或无毒的小分子物质。且羟基自由基无选择地直接与污水中污染物反应,不会存在一种污染物质降解了另一种物质还基本不变的情况。根据产生羟基自由基的方式和反应条件的不同,目前用于降解三氯生的有臭氧氧化、Fenton氧化、Photo-Fenton氧化、光化学氧化、声化学/声电化学氧化等方法。
3.3.1臭氧氧化。臭氧在常温常压下是一种不稳定气体,具有强氧化性,标准电极电位为2.07 V,可以迅速氧化三氯生。Sonia Suarez等对两个污水处理厂的水样用臭氧氧化,4 mg/L(3×10-5mol/L)的臭氧就能把含7.5 mg/L DOC的废水里几乎100%的三氯生氧化,6 mg/L(1.3×10-4mol/L)的臭氧就能把含12.4 mg/L DOC的废水里三氯生氧化58%。并且他们还确定了三氯生与臭氧的二级反应速率,阴离子三氯生与臭氧的反应很快,速率常数为(5.1±0.1)×108L/(mol·s)。中性三氯生与臭氧反应的速率常数为(1.3±0.1)×103L/(mol·s)[54]。所以在pH接近中性时,三氯生能被迅速地氧化。
此外,利用臭氧氧化三氯生可以减少或消除其抗菌活性。在三氯生羟基的邻位和对位容易发生苯酚-臭氧反应[55]。而三氯生分子的抗菌活性主要是因为它的酚环通过范德华力和氢键与细菌脂烯酰基-酰基载体蛋白还原酶相互作用[56],因此通过臭氧产生氧加成到苯酚环上或者打开苯酚环使三氯生分子被氧化[55],这样就使得三氯生的抗菌活性减少或消除。
3.3.2Fenton氧化。1894年化学家Fenton 发现过氧化氢与二价铁离子的混合溶液具有强氧化性,可以将当时很多已知的有机化合物如羧酸、醇、酯类氧化为无机态,氧化效果十分显著。为了纪念这一发现,把Fe2+/H2O2命名为Fenton(芬顿)试剂。芬顿试剂的作用原理是基于H2O2和均相金属离子催化剂之间的电子传输[57],芬顿试剂氧化过程中会产生大量非常活泼的羟基自由基,其标准电极电位为2.80 V,仅次于氟(2.87 V),是降解污染物的主要氧化剂[58]。而羟基自由基可以将有机物降解为易降解的小分子物质甚至直接矿化为二氧化碳、水等无机物,不会产生二次污染[59]。由于芬顿试剂的这些优点,将其用于去除有机污染物得到了极大的关注。
在Fenton体系中完全降解所需要的时间与pH、催化剂(Fe2+)和H2O2的浓度密切相关。在一定范围内随着pH升高,降解速率会降低,原因可能是作为催化剂的溶解铁浓度会降低。降解速率会随着浓度的增加而增大,也会随着反应温度的增加而增加。Macarena Munoz等在25 ℃下用1 mg/L的Fe3+和H2O2在1 h内就能完全转化10 mg/L水溶液中的三氯生。反应物浓度不变,温度升高,转化速率增大,在50 ℃下完全转化大约需要20 min。而且在用这种方法降解三氯生时,只会产生几种芳香族中间产物和短链有机酸,芳香中间体的生态毒性远小于三氯生的毒性,并且产生的具有生物毒性的二噁英显著减少。
3.3.3Photo-Fenton氧化。Photo-Fenton 是当今最重要的高级氧化技术(AOP) 方法之一。紫外光能显著加快Fenton反应[61],反应产生羟基自由基,使有机物分解。但反应必须在pH<3进行,否则因析出Fe(OH)3沉淀而使加入的Fe2+或Fe3+失效[62]。但是当pH<3时,会出现大量的CO32-、HCO3-,作为有效的羟基自由基清除剂会降低光芬顿的降解速率,可以通过在光芬顿反应前将CO32-、HCO3-移除或使用大量的铁催化来解决这一问题[63]。
但是大多数高级氧化降解使用氧化剂或者辐射(O3/H2O2/TiO2)的组合,或使用催化剂和辐射(Fe2+/H2O2、UV/TiO2)装置需要高电能,这在经济上是不划算的,使用催化剂和太阳能可能会解决这个问题。Klamerth 等尝试使用太阳能来减少光芬顿降解成本,结果表明在300 nm的波长下,低剂量的芬顿试剂(铁:5 mg/L,过氧化氢:50 mg/L)就能将三氯生减少到几乎可以忽略的浓度[63]。
3.3.4光化学氧化。包括光激发氧化法(如O3/UV)和光催化氧化法(如TiO2/UV)。前者主要以O3、H2O2、O2和空气作为氧化剂,在光辐射作用下产生羟基自由基,后者则是在反应溶液中加入一定量的半导体催化剂,使其在紫外光的照射下产生羟基自由基。
在自然环境下,光降解是三氯生一个主要的去除途径[18,64]。Anton Lindström等证明解离的三氯生在阳光下很容易被分解,8月时在47° N的地方光降解的半衰期<1 h,他们认为夏季湖泊和河流中三氯生浓度之所以比冬季小是因为夏季三氯生的光降解较强[18]。
虽然在不同的光照或不同的降解体系中,三氯生有可能降解成不同的物质,但是大部分三氯生的光降解产物是远比三氯生毒性更强的含氯化合物。Kazushi等用低强度的人造白光源分别照射淡水与海水,在两种水样中均观测到三氯生的降解,前者三氯生的半衰期为8 d后者为4 d。并且,光照3 d后在两种水样中都发现了三氯生的光解反应产物 2,8-二氯二苯并-对-二噁英(DDCD)[65]。Jimmy等利用TiO2/UV光催化反应降解三氯生,在TiO2上光(波长<365 nm)催化6 h内就能降解95%的三氯生。加入少量的过氧化氢(0.001 25%~0.080 00%)能使大大增加三氯生的降解速率。反应结果表明,产物中只有2,4-二氯苯酚比较多,对苯二酚(氢醌)和醌比2,4-二氯苯酚至少少了10倍。产生的2,4-二氯苯酚说明三氯生降解过程中是醚键断裂[66]。
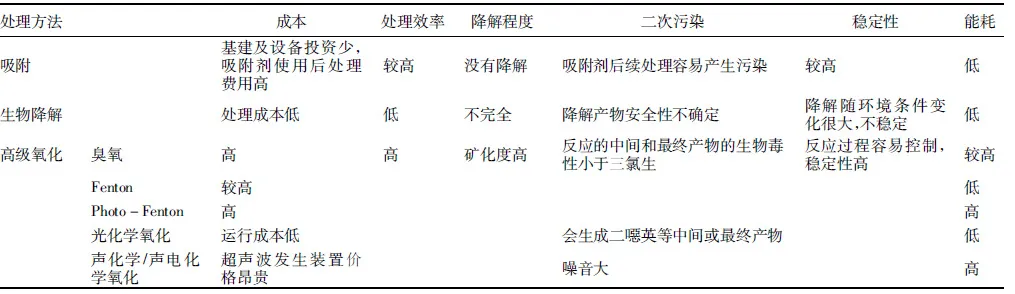
表1 三氯生处理方法比较
3.3.5声化学/声电化学氧化。目前,用超声波降解水中三氯生的报道还较少。Lucia Sanchez-Prado等利用超声降解不同类型水溶液中的三氯生(初始浓度为5 μg/L),废水在超声180 min后只有60%降解,而在海水中15 min就有95%的转化率。降解符合假一级动力学,速率常数(每分钟)分别是0.228 4(海水)>0.105 1(3.5%的NaCl去离子水)>0.059 7(离心城市径流)>0.052 3(未处理城市径流)>0.027 2(去离子水)>0.006 3(废水)。并且在试验条件下,降解过程没有伴随着有毒代谢产物的形成[67]。Yan-Ze Ren等研究在水溶液中用高频超声波(850 kHz)声电化学降解三氯生,以金刚石镀铌作为电极,15 min内,初始浓度为5 mg/L的三氯生,在酸性电解质(H2SO4)条件下(pH=2.5)降解82%;而以硫酸钠(pH=5.8)和氢氧化钠(pH=12.7)作为电解质,分别降解63%和41%。可见,酸性电解质有利于三氯生的声电化学降解。此外,不同的电源电压对三氯生的降解程度也有较大的影响,从5 V增加到10 V,三氯生降解从61%增加至82%,这主要是因为电压增加,溶液中的羟基自由基也会增加,所以在相同时间内对三氯生的降解速度变快了。但是在更高的电极电压(>10 V)时,观察到在电极表面形成气泡,会减小声电化学过程的效率[68]。
综上所述,用不同方法降解三氯生各有优劣,表1对几种处理方法进行归纳总结。
4 结论与展望
虽然三氯生的半衰期不长,但是由于广泛使用,长期持续性的进入环境中使其成为“假性持久性污染物”,对长期暴露在水环境中的生物产生副作用。加上三氯生的亲脂性质,容易被生物富集进入食物链中,给生态环境带来的威胁是潜在和不可预测的。因此研究三氯生的迁移、转化规律有重要意义。传统的水处理工艺不能完全去除三氯生,需要对其进行改进,已有许多针对三氯生降解、处理的研究,主要为吸附、生物和高级氧化法。高级氧化法尽管存在费用较高的问题,但是其反应快速、彻底、矿化度高等优点使其得到广泛的研究和应用。今后对高级氧化降解的研究重点是把握反应机理和反应的中间及最终化合物的毒性,以探索得到经济、环境友好的高级氧化法降解三氯生。
[1] CHAU W C,WU J L,CAI Z W.Investigation of levels and fate of triclosan in environmental waters from the analysis of gas chromatography coupled with ion trap mass spectrometry[J].Chemosphere,2008,73(1):13-17.
[2] JONES R D,JAMPANI H B,NEWMAN J L,et al.Triclosan:A review of effectiveness and safety in health care settings[J].AJIC Am J Infect Control,2000,28(2):184-196.
[3] SINGER H,MüLLIER S,TIXIER C,et al.Triclosan:Occurrence and Fate of Widely Used Biocide in the Aquatic Environment:Field Measurements in Wastewater Treatment Plants,Surface Waters,and Lake Sediments[J].Environ Sci Technol,2002,36(23):4998-5004.
[4] HEIDLER J,HALDEN R U.Mass balance assessment of triclosan removal during conventional sewage treatment[J].Chemosphere,2007,66(2):362-369.
[5] RIVA C,CRISTONI S,BINELLI A.Effects of triclosan in the freshwater mussel Dreissena polymorpha:A proteomic investigation[J].Aquatic Toxicology,2012,118/119:62-71.
[6] BHARGAVA H N,LEONARD P A.Triclosan:Applications and safety[J]. AJIC Am J Infect Control,1996,24(3):209-218.
[7] PROIA L,VILCHES C,BONINNEAU C,et al.Drought episode modulates the response of river biofilms to triclosan[J].Aquatic Toxicology,2013,127:36-45.
[8] ORVOS D,VERSTEEG D,INAUEN J,et al.Aquatic toxicity of triclosan[J].Environmental Toxicology and Chemistry,2002,21(7):1338-1349.
[9] RICART M,GUASCH H,ALBERCH M,et al.Triclosan persistence through wastewater treatment plants and its potential toxic effects on river biofilms[J].Aquatic Toxicology,2010,100(4):346-353.
[10] NASSEF M,MATSUMOTO S,SEKI M,et al.Acute effects of triclosan,diclofenac and carbamazepine on feeding performance of Japanese medaka fish (Oryzias latipes)[J].Chemosphere,2010,80(9):1095-1100.
[11] LIANG X M,NIE X P,YING G G,et al.Assessment of toxic effects of triclosan on the swordtail fish (Xiphophorus helleri) by a multi-biomarker approach[J].Chemosphere,2013,90(3):1281-1288.
[12] LIN D S,ZHOU Q X,XIE X J,et al.Potential biochemical and genetic toxicity of triclosan as an emerging pollutant on earthworms (Eisenia fetida)[J].Chemosphere,2010,81(10): 1328-1333.
[13] AMORIM M J B,OLIVEIRA E,SOARES A M V M,et al.Predicted No Effect Concentration (PNEC) for triclosan to terrestrial species(invertebrates and plants)[J].Environment International,2010,36(4):338-343.
[14] CRAWFORD B R,DECATANZARO D.Disruption of blastocyst implantation by triclosan in mice:Impacts of repeated and acute doses and combination with bisphenol-A[J].Reproductive Toxicology,2012,34(4):607-613.
[15] POLLOCK T,TANG B,DECATANZARO D.Triclosan exacerbates the presence of 14C-bisphenol A in tissues of female and male mice[J].Toxicology and Applied Pharmacology,2014,278(2):116-123.
[16] LOZANO N,RICE C P,RAMIREZ M,et al.Fate of Triclocarban,Triclosan and Methyltriclosan during wastewater and biosolids treatment processes[J]. Water Research,2013,47(13):4519-4527.
[17] BUTLER E,WHELAN M J,SAKRABANI R,et al.Fate of triclosan infield soils receiving sewage sludge[J].Environmental Pollution,2012,167:101-109.
[18] LINDSTRÖM A,BUERGE I J,POIGER T,et al.Occurrence and Environmental Behavior of the Bactericide Triclosan and Its Methyl Derivative n Surface Waters and in Wastewater[J].Environmental Science and Technology,2002,36(11):2322-2329.
[19] KOOKANA R S,SHAREEF A,FERNANDES M B,et al.Bioconcentration of triclosan and methyl-triclosan in marine mussels (Mytilus galloprovincialis) under laboratory conditions and in metropolitan waters of Gulf St Vincent,South Australia[J].Marine Pollution Bulletin,2013,74(1):66-72.
[20] RULE K,EBBETT V R,VIKESLAND P J.Formation of Chloroform and Chlorinated Organics by Free-Chlorine-Mediated Oxidation of Triclosan[J].Environ Sci Technol,2005,39(9):3176-3185.
[21] AGüERA A,FERNáNDEZ-ALBA A R,PIEDRA L,et al.Evaluation of triclosan and biphenylol in marine sediments and urban wastewaters by pressurized liquid extraction and solid phase extraction followed by gas chromatography mass spectrometry and liquid chromatography mass spectrometry [J].Analytica Chimica Acta,2003,480(2):193-205.
[22] 陈忠良.三氯生光降解产物分析[D].无锡:江南大学,2008.
[23] MEZCUA M,OSÉ GMEZ M,FERRER I,et al.Evidence of 2,7/2,8-dibenzodichloro-p-dioxin as a photodegradation product of triclosan in water and wastewater samples[J].Analytica Chimica Acta,2004,524(1/2):241-247.
[24] REISS R,MACKAY N,HABIG C,et al. Anecological risk assessment for triclosan in lotic systems following discharge fromwastewater treatment plants in the United States[J].Environmental Toxicology and Chemistry,2002,21(11):2483-2492.
[25] GAO Y P,JI Y M,LI G Y,et al.Mechanism,kinetics and toxicity assessment of OH-initiated transformation of triclosan in aquatic environments[J].Water Research,2014,49(1):360-370.
[26] BESTER K.Triclosan in a sewage treatment process-balances and monitoring data[J].Water Research,2003,37(16):3891-3896.
[27] YING G G,KOOKANA R S. Triclosan in wastewaters and biosolids from Australian wastewater treatment plants[J].Environment International,2007,33(2):199-205.
[28] SABALIUNAS D,WEBB S F,HAUK A,et al.Environmental fate of Triclosan in the River Aire Basin,UK[J].Water Research,2003,37(13):3145-3154.
[29] LAPEN D R,TOPP E,METCALFE C D,et al.Pharmaceutical and personal care products in tile drainage following land application of municipal biosolids[J].Science of The Total Environment,2008,399(1/3):50-65.
[30] TOPP E,MONTEIRO S C,BECK A,et al.Runoff of pharmaceuticals and personal care products following application of biosolids to an agricultural field[J].Science of The Total Environment,2008,396(1):52-59.
[31] KOLPIN D W,FURLONG E T,MEYER M T,et al.Pharmaceuticals,Hormones,and Other Organic Wastewater Contaminants in U.S.Streams,1999-2000:A National Reconnaissance[J].Environmental Science and Technology,2002,36(6):1202-1211.
[32] WU J L,LAM N P,MARTENS D.Triclosan determination in water related to wastewater treatment[J].Talanta,2007,72(5):1650-1654.
[33] ZHAO J L,ZHANG Q Q,CHEN F,et al.Evaluation of triclosan and triclocarban at river basin scale using monitoring and modeling tools:Implications for controlling of urban domestic sewage discharge[J].Water Research,2013,47(1):395-405.
[34] XIE Z Y,EBINGHAUS R,FLÖSER G,et al.Occurrence and distribution of triclosan in the German Bight (North Sea)[J].Environmental Pollution, 2008,156(3):1190-1195.
[35] RAMASWAMY B R,SHANMUGAM G,VELU G,et al.GC-MS analysis and ecotoxicological risk assessment of triclosan,carbamazepine and parabens in Indian rivers[J].Journal of Hazardous Materials,2011,186(2/3):1586-1593.
[36] HUA W Y,BENNETT E R,LETCHER R J.Triclosan in waste and surface waters from the upper Detroit River by liquid chromatography-electrospray-tandem quadrupole mass spectrometry[J].Environment International,2005,31(5):621-630.
[37] ADOLFSSON-ERICIA M,PETTERSSON M,PARKKONEN J,et al.Triclosan,a commonly used bactericide found in human milk and in the aquatic environment in Sweden[J].Chemosphere,2002,46(9):1485-1489.
[38] COOGAN M A,EDZIYIE R E,LA POINT T W,et al.Algal bioaccumulation of triclocarban,triclosan,and methyl-triclosan in a North Texas wastewater treatment plant receiving stream[J].Chemosphere,2007,67(10):1911-1918.
[39] FAIR P A,LEE H B,ADAMS J,et al.Occurrence of triclosan in plasma of wild Atlantic bottlenose dolphins(Tursiops truncatus) and in their environment[J].Environmental Pollution,2009,157(8):2248-2254.
[40] MOSS T,HOWES D,WILLIAMS F M.Percutaneous Penetration and Dermal Metabolism of Triclosan (2,4,4'-Trichloro-2'-hydroxydiphenyl Ether)[J].Food and Chemical Toxicology,2000,38(4):361-370.
[41] ALLMYRA M,ADOLFSSON-ERICI M,MCLACHLAN M S,et al.Triclosan in plasma and milk from Swedish nursing mothers and their exposure via personal care products[J].Science of the Total Environment,2006,372(1):87-93.
[42] GEENS T,NEELS H,COVACI A.Distribution of bisphenol-A,triclosan and n-nonylphenol in human adipose tissue,liver and brain[J].Chemosphere,2012,87(7):796-802.
[44] BEHERA S K,OH S Y,PARK H S.Sorption of triclosan onto activated carbon,kaolinite and montmorillonite:Effects of pH,ionic strength,and humic acid[J].Journal of Hazardous Materials,2010,179(1/3):684-691.
[45] 琚丽婷.蒙脱石负载零价纳米铁镍或纳米铁银双金属处理三氯生的研究[D].广州:华南理工大学,2013.
[46] 何敏祯.HDTMA改性沸石对三氯生的吸附行为与机理研究[D].广州:华南理工大学,2012.
[47] 雷超.表面活性剂改性分子筛吸附三氯生的性能及机理研究[D].广州:华南理工大学,2013.
[48] KIM Y M,MURUGESAN K,SCHMIDT S,et al.Triclosan susceptibility and co-metabolism-A comparison for three aerobic pollutant-degrading bacteria[J].Bioresource Technology,2011,102(3):2206-2212.
[49] LEE D G,CHU K H.Effects of growth substrate on triclosan biodegradation potential of oxygenase-expressing bacteria[J].Chemosphere,2013,93(9):1904-1911.
[50] BOKARE V,MURUGESAN K,KIM Y M,et al.Degradation of triclosan by an integrated nano-bio redox process[J].Bioresource Technology,2010,101(16):6354-6360.
[51] 徐海丽.一株三氯生高效降解菌的筛选及其降解特征的初步研究[D].厦门:华侨大学,2012.
[52] YING G G,YU X Y,KOOKANA R S.Biological degradation of triclocarban and triclosan in a soil under aerobic and anaerobic conditions and comparison with environmental fate modeling[J].Environmental Pollution, 2007,150(3):300-305.
[53] WANG S J,WANG X,POON K,et al.Removal and reductive dechlorination of triclosan byChlorella pyrenoidosa[J].Chemosphere,2013,92(11):1498-1505.
[54] SUAREZ S,DODD M C,OMIL F,et al.Kinetics of triclosan oxidation by aqueous ozone and consequent loss of antibacterial activity:Relevance to municipal wastewater ozonation[J].Water Research,2007,41(12):2481-2490.
[55] MVULA E,VON SONNTAG C. Ozonolysis of phenols in aqueous solution[J].Organic and Biomolecular Chemistry,2003,1(10):1749-1756.
[56] LEVY C W,ROUJEINIKOVA A,SEDELNIKOVA S,et al.Molecular basis of triclosan activity[J].Nature,1999,398(6726):383-384.
[57] CHALK A J,BECK B,CLARK T.A Temperature-Dependent Quantum Machanical/Neural Net Model for Vapor Pressure[J],Journal of Chemical Information and Computer Sciences,2001,41(4):1053-1059.
[58] BIGDA R J.Consider Fenton chemistry for wastewater treatment[J].Chemical Engineering Progress,1995, 91(12):62-66.
[59] 张德莉,黄应平,罗光富,等.Fenton及Photo- Fenton研究进展[J].环境化学,2006,25(2):121-127.
[60] MUNOZ M,DE PEDRO Z M,CASAS J A,et al.Triclosan breakdown by Fenton-like oxidation[J].Chemical Engineering Journal,2012,198/199:275-281.
[61] PIGNATELLO J J.Dark and photoassisted Fe3+-catalyzed degradation of chlorophenoxy herbicides by hydrogen-peroxide[J].Environmental Science and Technology,1992,26(5):944-951.
[62] 谢银德,陈锋,何建军,等.Photo - Fenton 反应研究进展[J].感光科学与光化学,2000,18(4):357-365.
[63] KLAMERTH N,MIRANDA N,MALATO S,et al.Degradation of emerging contaminants at low concentrations in MWTPs effluents with mild solar photo-Fenton and TiO2[J].Catalysis Today,2009,144(1):124-130.
[64] WILSON B,CHEN R F,CANTWELL M,et al.The partitioning of Triclosan between aqueous and particulate bound phases in the Hudson River Estuary[J].Marine Pollution Bulletin,2009,59(4/7):207-212.
[65] ARANAMI K,READMAN J W. Photolytic degradation of triclosan in fre-shwater and seawater[J].Chemosphere,2007,66(6):1052-1056.
[66] YU J C,KWONG T Y,LUO Q,et al.Photocatalytic oxidation of triclosan[J].Chemosphere,2006,65(3):390-399.
[67] SANCHEZ-PRADO L,BARRO R,GARCIA-JARES C,et al.Sonochemical degradation of triclosan in water and wastewater[J].Ultrasonics Sonochemistry,2008,15(5):689-694.
[68] REN Y Z,FRANKE M,ANSCHUETZ F,et al.Sonoelectrochemical degradation of triclosan in water[J].Ultrasonics Sonochemistry,2014,21(6):2020-2025.
Research Advance of Triclosan Transport and Transformation in Water Environment
WANG Xiu-juan1,2, QIU Jin-rong2*, TIAN Ying-bing1et al
(1. Agricultural College, Yangtze University, Jingzhou, Hubei 434025; 2. South China Institute of Environmental Sciences, Ministry of Environmental Protection, Guangzhou, Guangdong 510000)
Triclosan is widely used as broad spectrum antibacterial agent, it is easy to bioaccumulate and gather into the food chain for its lipotropy. Therefore, the biological toxicity of triclosan causes potential unpredictable threat of the ecological environment. This paper will make a brief introduction of current world-wide researches on treatment technology of triclosan in water, the advantages and disadvantages of various treatment technologies were compared. The results showed that advanced oxidation technology own the edges of fast response, thorough, high salinity,etc., but it is of higher processing costs. Therefore, developing economic feasible advanced oxidation technology tend to be a future research direction in dealing with the triclosan in water environment.
Triclosan; Toxicity; Transport and transformation; Degradation
国家重大科技专项(2014ZX0726001);环境保护部华南环境科学研究所中央级公益性科研院所基本科研业务专项(PM-zx021-201406-35)。
王秀娟(1991-),女,福建建阳人,硕士研究生,研究方向:水污染控制技术。*通讯作者,高级工程师,博士,从事水污染控制技术研究。
2014-12-03
S 181.3
A
0517-6611(2015)02-251-06
