腹主动脉瘤直型覆膜支架的生物力学分析
2015-02-20谷雪莲胡方遒祁勇翔李中华宋成利
谷雪莲 胡方遒 祁勇翔, 李中华 宋成利
1(上海理工大学教育部微创医疗器械工程研究中心,上海 200093)2(上海微创医疗器械(集团)有限公司,上海 201203)
腹主动脉瘤直型覆膜支架的生物力学分析
谷雪莲1*胡方遒1祁勇翔1,2李中华2宋成利1
1(上海理工大学教育部微创医疗器械工程研究中心,上海 200093)2(上海微创医疗器械(集团)有限公司,上海 201203)
应用数值模拟分析方法,研究腹主动脉瘤直型覆膜支架在径向压握、自膨胀释放及植入后平衡状态3种工况下的稳定性及各项生物力学指标。建立覆膜支架、压握工具以及目标血管的有限元模型。对圆柱状压握工具沿R轴负方向施加大小为6.50 mm的位移载荷,压握覆膜支架至外径为7.00 mm;将压握工具恢复到原始尺寸,建立血管/覆膜支架接触关系;支架完全释放后平衡状态下,对其内表面均匀施加50~150 mmHg动脉压。分析支架部分在压握与平衡状态下的最大主应变(MPS)峰值及分析后形态、释放状态下变形血管以及覆膜的等效应力峰值(VMS)。在径向压握过程中,金属支架最大压握主应变峰值为5.73%;在自膨胀释放过程中,造成血管壁应力集中的峰值为0.371 MPa,覆膜应力峰值为0.388 MPa;在植入后平衡状态下,支架平均应变为0.0859%,振荡应变为0.0486%,覆膜应力峰值为2.09 MPa,安全因子为8.23。支架部分在各工况下应变处于镍钛合金屈服强度之内,在圆角弯折处应变最为集中;覆膜部分在各工况下应力值也满足e-PTFE膜材料的屈服强度。该研究结果可以为覆膜支架的结构优化设计以及覆膜材料选择提供一种分析方法,可以提高覆膜支架的生物力学性能,并给工程设计和临床操作提供参考。
覆膜支架;腹主动脉瘤;生物力学;镍钛合金
引言
腹主动脉瘤(abdominal aortic aneurysm, AAA) 是由于动脉血管壁因疾病、损伤等因素引其的血管壁局部变薄,在承受血流的冲击下,血管壁的薄弱点向外突出而形成囊状膨大。腹主动脉瘤是一种存在潜在生命危险的疾病,病变处膨大易压迫周围器官及组织,动脉瘤破裂更会危及患者生命[1]。动脉瘤腔内修复术(endovascular aneurysm repair, EVAR)是通过在DSA动态监测下,经双侧股动脉的小切口,通过输送系统将覆膜支架植入腹主动脉瘤腔内,重建新的血流通道,以治愈动脉瘤。EVAR以其创伤小、并发症少、患者痛苦少等优势逐渐代替开腹手术成为治疗腹主动脉瘤的主要方法。Greenhalgh等曾统计临床手术结果,证明EVAR相较于传统手术能够很大程度上减少术后并发症和死亡率[2]。然而,长期以来临床数据表明EVAR术后病变部位存在一定的复发率,造成这些修复失败的原因主要包括支架移位、内漏、疲劳折损等[3-6]。而与之相联的覆膜支架特性尤为重要,如图1所示。覆膜支架是指金属支架外面或内面覆盖有膜性材料的介入医疗器械,分为直型与分叉型两种,它的耐用性与稳定性将直接影响到EVAR效果的好坏。

图1 覆膜支架外形图。(a)直型 (b)分叉型Fig.1 The structure of nitinol stent graft. (a) Cylindrical stent-graft, (b) Bifurcating stent-graft
覆膜支架从其生产到植入人体内的过程中,较常出现的现象包括:支架被压握入鞘时,局部大应变造成的微结构裂纹会最终导致结构断裂;自膨胀释放时,支架未能完全释放问题或者是支架部分强行撑开血管,撕裂划伤血管壁;植入体内后的平衡状态中,由于血压作用或随人体运动而弯折时局部大应变而造成支架断裂或覆膜撕裂等[3-6]。国内外对于腹主动脉瘤的生物力学研究较多,但是关于临床使用的腹主动脉瘤直型覆膜支架的生物力学研究文献却较为少见。Kleinstreuer等建立了镍钛合金支架的有限元模型,分析和评价了其植入体内前后生物力学性能[7]。然而,该研究所建立的支架模型为理想模型,其结构与尺寸皆与临床实际使用的覆膜支架差距较大,同时其研究重点在于金属支架的受力情况,而对于覆膜支架来说,金属支架所附着的膜材料在支架输送到释放的过程中的应力应变大小与分布同样重要。Demanget等运用数值模拟方法,研究分析了覆膜支架在弯折状态下支架与覆膜的应力应变情况,但是其所研究的弯折状态太过于极限并不符合腹主动脉瘤病变处的一般情况,无法给覆膜支架的设计与改进提供直接的参考[9]。针对上述问题,笔者以覆膜支架为研究对象,采用有限元分析技术,验证和研究其在模拟过程中对器械本身及血管壁造成的生物力学性能影响。
为了对覆膜支架结构设计提出较有意义的优化建议,以改善其生物力学性能,本研究建立了直型覆膜支架、压握工具和动脉瘤血管的有限元模型。分析该模型在3种加工及使用的模拟过程(径向压握、自膨胀释放、植入后平衡状态)中自身以及血管的变形和场输出情况。结合机构特点和后处理计算结果,对覆膜支架在接触载荷下的力学性能进行分析,提出覆膜支架结构的改进建议。
1 材料与方法
1.1 模型建立
笔者通过查阅文献以及参考现有的覆膜支架形状结构与参数,选取上海某公司的覆膜支架结构参数进行建模。考虑到计算效率与时间等因素,仅选取覆膜支架主体部分进行建模分析,如图2所示。覆膜支架模型整体为圆管状,其主体部分由一节节独立的类正弦线骨架单元组成。骨架外部附着一层圆筒状覆膜。表1为覆膜支架各部分尺寸参数。
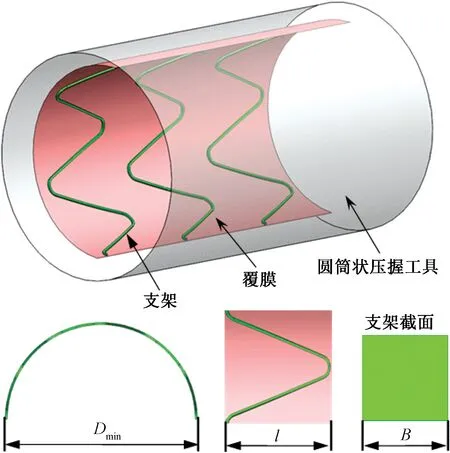
图2 覆膜支架装置结构Fig.2 Structure dimensions of nitinol stent graft

Dmin/mmL/mml/mmB/mm扩张状态200060001500020压握状态7006000≈1600020
注:L为覆膜支架模型轴向总长度;Dmin为支架外径;l为支架单元长度;B为支架单元厚度。
Notes:L: Length of stent graft;Dmin: External diameter of stent;l: Length of stent unit;B: Thickness of stent graft.
利用几何建模软件Solidworks 2010及Hyperme-sh v11.0,对直型覆膜支架、压握工具和动脉瘤血管建立几何模型与有限元模型。根据临床数据,模拟血管被建成一个外径为20.00 mm、壁厚为0.20 mm中部隆起的空心圆管,压握工具直接被建成为一个三维直管壳状体。有限元模型建立方法如表2所示。
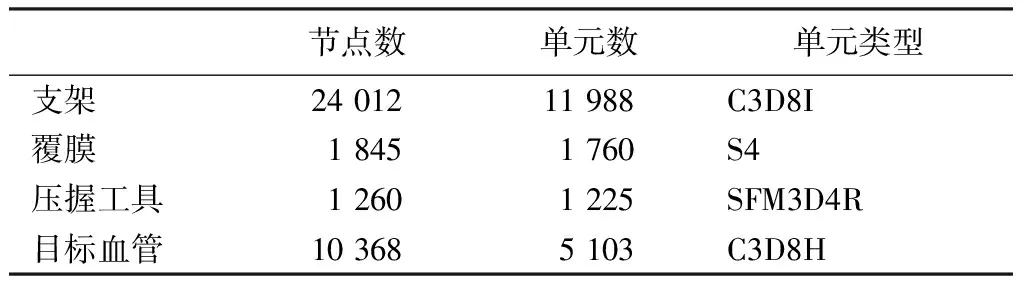
表2 有限单元模型参数
在建立覆膜支架的有限元模型时,支架及覆膜部分分别采用C3D8I和S4单元,可在保证计算精度的同时,可以减小计算周期,提高收敛性。目标血管在厚度方向上分布两层均匀等厚度实体单元,保证计算精度,降低计算成本。压握工具因被定义为刚性面,故而采用SFM3D4R单元。
1.2 本构模型
将建立好的模型导入到有限元分析软件Abaqus 6.10 CAE中进行各项定义及后续计算。所分析的覆膜支架模型金属支架部分采用了各向同性、均匀、不可压缩的镍钛合金材质。镍钛合金材料具有超弹性能、形状记忆性能、抗疲劳性能、抗腐蚀性能及良好的生物相容性[10],因而被广泛应用于医学领域,而在人体温度下镍钛合金材料的力学性能评价主要以最大主应变(maximum principal strain, MPS)为基础,用于覆膜支架分析的镍钛合金材料参数引用文献[7],各模拟过程均设置在人体内环境温度37℃的情况下。模拟分析后将处理结果中的MPS峰值与镍钛合金材料的马氏体转化应变阈值(6%)以及屈服应变阈值(12%)[7]进行比较,从而分析判断微结构中裂纹及断裂机率。覆膜支架附着的膜材料为膨化聚四氟乙烯(e-PTFE),定义为各向同性的壳体,并选用Lamina材料本构模型,其各项参数引用于文献[9]。压握工具则被定义为一层刚性面。为较好模拟动脉瘤血管,暂将模拟血管选定为Neo-Hookean solid超弹性材料本构模型, strain-energy方程为
(1)
式中,I1为应变不变量,J为体积比,C10与D1为两个常数。
通过翻阅文献与公式计算[7-8],确定两个参数分别为C10=648 MPa,D1=0.000 7。
1.3 边界条件与载荷
1.3.1 径向压握
径向压握过程是覆膜支架加工必须经历的一个过程。该过程中,将覆膜支架与定型模具的有限元模型均被转化到总体圆柱坐标系下。1、2、3自由度方向分别对应该坐标系的γ、θ和Z方向。对覆膜支架在轴向方向进行约束;对压握工具的轴向和周向方向上进行约束,同时对其施加径向位移UR=6.50 mm[7]。因覆膜支架产品中支架与覆膜之间是经细线紧密缝合的,故而在定义支架覆膜之间接触时,采用将支架外表面与覆膜内表面“Tie”住以保证在模拟过程中支架与覆膜之间不会发生相对移动[9]。设置主从接触对时,压握工具的内表面设置为主面,覆膜支架的外表面被设置为从面,接触对的摩擦系数设置为0[7]。结合接触分析的复杂性及材料属性的非线性,将分析步设置中的非线性分析开关打开,并设置较小的增量以提高计算收敛性。
1.3.2 自膨胀释放
自膨胀释放过程中,对模拟血管两端截面在轴向和周向进行约束,压握工具取消载荷,回复到初始状态,覆膜支架则凭借镍钛材料的超弹性回弹到初始尺寸。在新增的接触对中,目标血管内表面和覆膜支架外表面分别设置成主面和从面。其接触设置与压握过程一致,摩擦系数则改为0.25[7]。其余边界条件与接触属性设置都与压握过程相同。
1.3.3 植入后平衡状态
覆膜支架植入病患部位后,首尾分别依靠镍钛合金的超弹性释放于动脉瘤两端的正常血管中,使覆膜支架固定于患处,而支架主体则在动脉瘤腔内形成新的血流通道。Li[7,11]等人的研究结果表明,支架植入后动脉瘤壁所受压力大幅减小,但由于其本身膨化的状态及腔内残存液体,故而无法完全贴附于覆膜支架上。此时支架处于平衡状态,动脉瘤壁组织还未完全贴附覆膜并沿空隙长入,瘤壁及动脉瘤腔内残留血液对覆膜支架主体的作用力将远小于动脉血流对其的压力,几乎可忽略。本部分主要针对主体部分进行分析,因此,在平衡状态分析中略去了瘤壁与支架的接触关系。
基于上述,将自膨胀释放完全的覆膜支架后处理模型用于该工况分析。分析过程中覆膜支架接触定义及边界条件与压握过程相同。同时,在覆膜支架内表面施加50 mmHg(舒张压)至150 mmHg(收缩压)的动脉压[7]。
2 结果
2.1 径向压握
图3为覆膜支架在径向压握过程中变形后的最大主应变场输出云图。可以发现该覆膜支架模型最大应变集中在每支架单元的圆角弯折处,最大主应变峰值分别为5.73%。该覆膜支架最大压握主应变峰值小于12%的镍钛合金屈服强度[7],故而可以判断该覆膜支架模型在径向压握过程中不存在裂纹或断裂的危险。该过程中覆膜不会被拉伸,仅因支架压握使覆膜发生折叠而产生少量应力,对支架应变情况未造成影响。
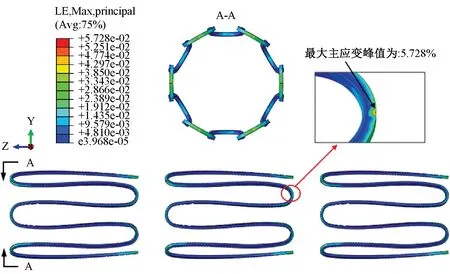
图3 覆膜支架径向压握最大主应变Fig.3 Maximum principal crimping strain field of stent
从覆膜支架压握后的横截面来看,可以发现支架的圆角弯折处均存在一定的径向偏移形变。该形变可能造成覆膜与支架接触区域发生局部撕裂,所以应对该弯折处做结构优化设计以降低风险。
2.2 自膨胀释放
通过数值模拟分析结果观察,在自膨胀释放末期,镍钛合金支架处最大主应变峰值为0.017 9%。图4所示为覆膜支架在自膨胀释放后血管壁的等效应力(Von Mises stress, VMS)分布,可以看出支架释放后的血管等效应力分布与支架形状相似,应力集中于血管与支架接触区域的变形处。由图4还可以看出,血管的等效应力峰值为0.371 MPa,与文献中所提到0.670 MPa[13]的血管屈服强度相比较,可知该覆膜支架模型的释放不会对血管造成撕裂等严重事故。
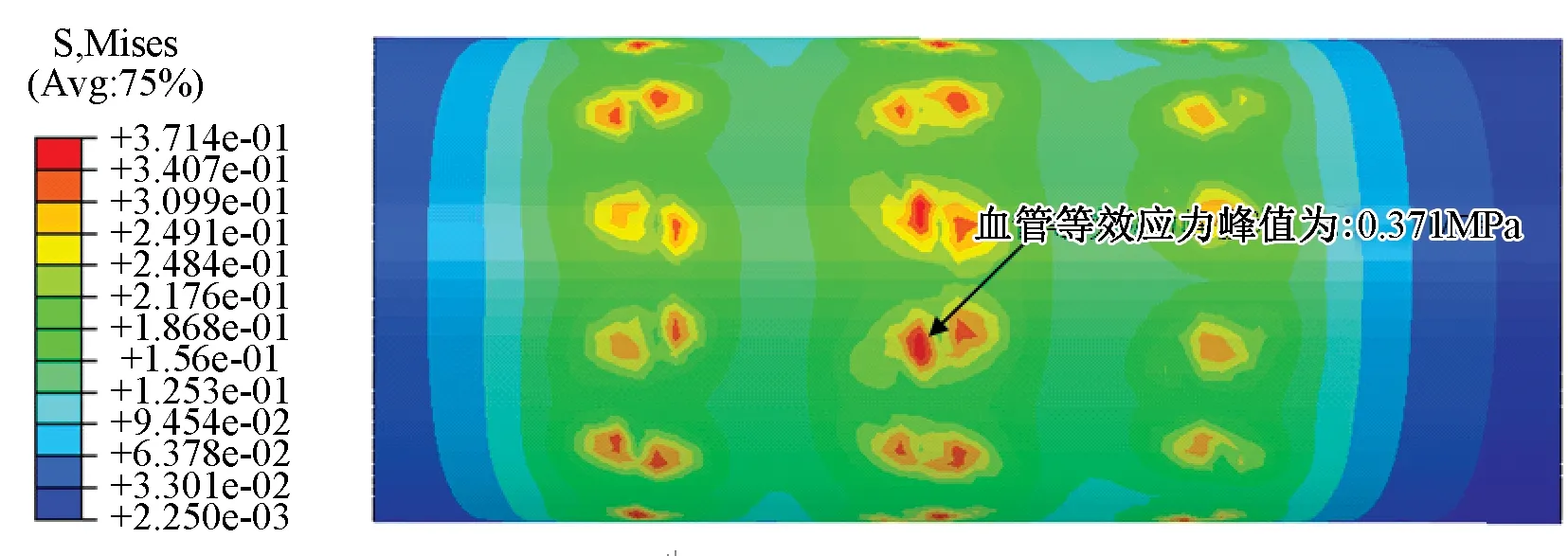
图4 覆膜支架造成血管变形等效应力分布Fig.4 VMS filed of deformed artery induced by stent
图5为覆膜支架释放时覆膜所受的等效应力分布。可以看出,覆膜与金属支架相接触的区域所受应力较大且较为集中,同样导致覆膜出现一定的形变。覆膜的等效应力峰值为0.388 MPa,该数据要远小于e-PTFE的6.60 MPa[7],说明e-PTFE膜在释放过程中不会因受支架作用力而出现破裂等情况。

图5 覆膜等效应力分布Fig.5 VMS filed of graft
2.3 植入后平衡状态
振荡应变相较于平均应力应变对镍钛合金支架疲劳寿命具有更大影响[12],故而将数值模拟分析结果进行整理及计算,如表3所示。从表格中可以看到,在(50~150)mmHg动脉压作用下镍钛合金支架的平均应变为0.085 9%,远小于镍钛合金12%的镍钛合金屈服强度[7],不会产生裂纹或断裂危险。镍钛合金支架的振荡应变为0.048 6%,同样小于0.4%的最低要求[12]。经计算得出安全因子为8.23,处于覆膜支架设计要求的安全范围之内。
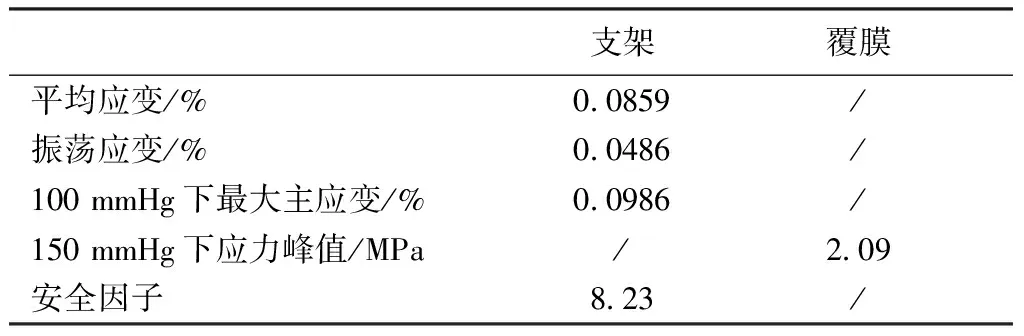
表3 在50~150 mmHg下支架的应力应变
注[7]:平均应变=0.5(最大主应变@150 mmHg+最大主应变@50 mmHg);振荡应变=0.5(最大主应变@150 mmHg-最大主应变@50 mmHg);安全因子=0.4%/振荡应变。
Notes[7]:Mean strain=0.5(strain@150 mmHg+strain@50 mmHg). Alternating strain=0.5(strain@150 mmHg-strain@50 mmHg). Safety factor=0.4%/alternating strain.
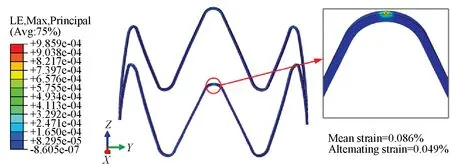
图6 在100 mmHg下覆膜支架的最大主应变Fig.6 Maximum principal strain of stent under a 100 mmHg mean pressure load
图6显示,覆膜支架发生疲劳折损可能性最大的地方处于支架每单元圆角弯折处的中部,因此为改善支架性能,可在该处进行适当的结构设计调整。
图7为在100 mmHg平均动脉压下覆膜的等效应力分布。可以看出,覆膜与支架相接触的区域应力值相对较小,而无支架牵制的区域如每个支架单元相邻区域所受的应力较大。由表3可知,在p=150 mmHg的情况下,覆膜所受的应力峰值为2.09 MPa,该数值小于e-PTFE膜的屈服强度6.60 MPa。因此,e-PTFE膜在该工况下是安全的。
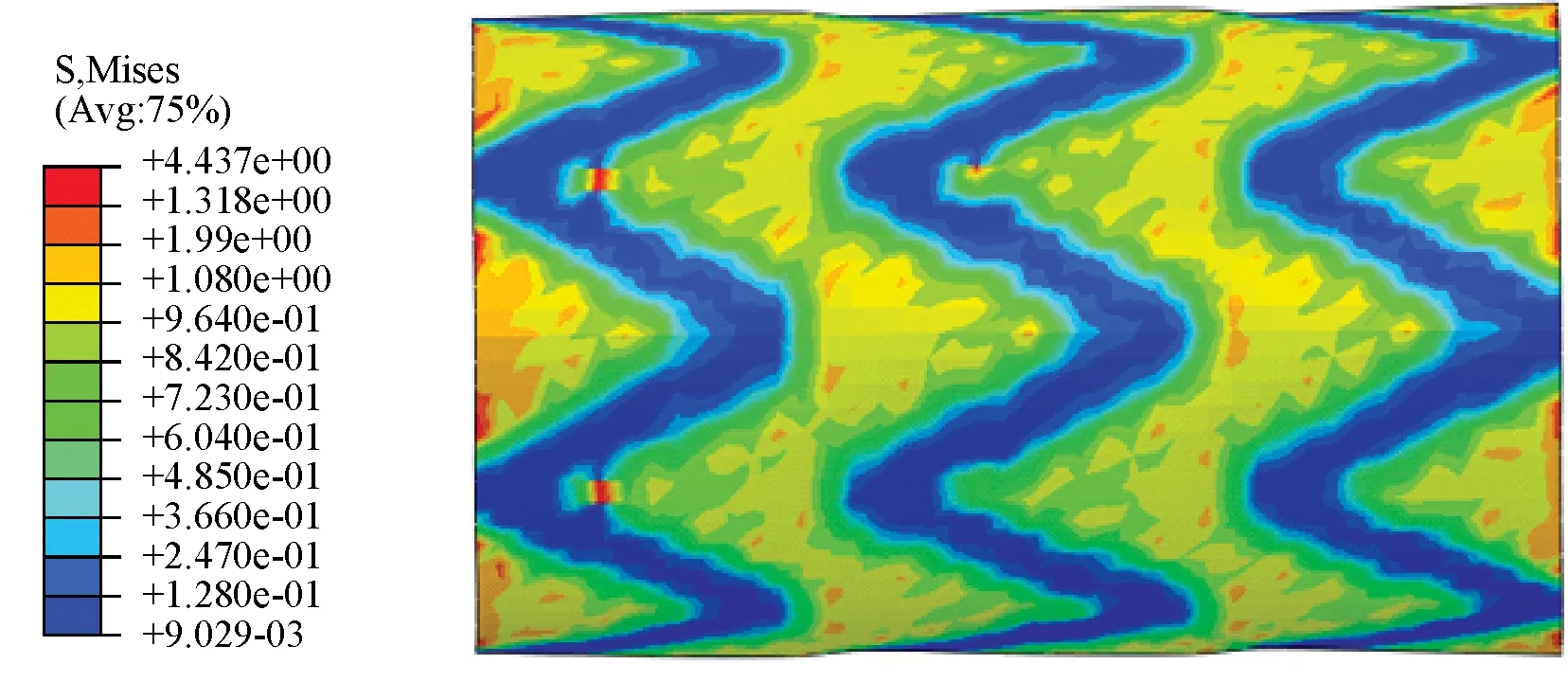
图7 在100 mmHg下覆膜的等效应力分布Fig.7 VMS filed of graft under a 100mmHg mean pressure load
3 讨论
目前,针对腹主动脉瘤直型覆膜支架模型从压握到植入的整体生物力学分析研究报道较少,而笔者研究提出了一种用于腹主动脉瘤直型覆膜支架的结构分析和优化设计的生物力学性能分析方法。建立了一款具有直型覆膜支架的有限元仿真模型,数值模拟并分析了覆膜支架在径向压握、自膨胀释放、植入后平衡状态下的生物力学性能。一方面,对于覆膜支架的结构设计而言,本方法将用于支架结构设计改进及覆膜材料的选用,根据不同的生物力学性能需求,准确有效地确定结构优化方案及覆膜材料的筛选;另一方面,对于临床应用而言,可为临床手术操作提供较为直观的技术性指导,提高覆膜支架植入前后的准确性与有效性,对其在介入治疗中的有效使用起到辅助作用。
通过该数值模拟分析可以看出,本研究所分析的覆膜支架模型最大应变集中在支架单元的圆角弯折处,而此处应变过大将对整个支架结构的稳定性造成一定隐患。此外,压握过程中支架的圆角弯折处均存在径向偏移形变,将造成覆膜与支架接触区域局部撕裂。而在自膨胀释放过程中,血管壁所受的应力峰值虽在正常范围,但应力集中且数值稍大,可能对血管壁造成损伤。植入后平衡状态中,覆膜支架所受应力应变值均在正常范围内。
本研究的模拟方法与结果可对覆膜支架的结构设计优化及覆膜材料的选择提供有效的参考意见。针对文章模拟分析的覆膜支架结构,可适当增大支架单元圆角处的曲率半径,降低在其压握过程中的应变,同时增加圆角弯折处的厚度与宽度,以降低在压握过程中支架产生的径向形变;可适当对支架尺寸变化进行改良,降低其径向支撑力,以减轻其在释放过程中对血管壁造成的损伤。
当然,本研究的模拟方法也存在一定的局限,如分析所定义血管模型为理想模型,在平衡状态分析时也未将血管与支架的接触关系考虑进去等。若对分析模型进行全面定义将增加模型复杂性及计算时间,故而在查阅文献及反复验证的基础上对上述问题进行了适当简化。
4 结论
本次研究完成了腹主动脉瘤直型覆膜支架在径向压握、自膨胀释放及植入后平衡状态下的生物力学性能分析,并针对不同阶段的数值模拟计算结果,分析与评价了该覆膜支架的应变、应力、安全因子等生物力学性能指标。针对分析结果,对该覆膜支架的结构提出了优化建议,为其结构设计改进提供参考。同时,针对腹主动脉瘤直型覆膜支架模型的整体生物力学分析研究,也将对覆膜材料的选择提供重要参考。
[1] Krupski W, Rutherford R. Update on open repair of abdominal aortic aneurysms: The challenges for endovascular repair [J]. Journal of the American College of Surgeons, 2004, 199(6):946-960.
[2] Greenhalgh R, Brown L, Kwong G,etal. Comparison of endovascular aneurysm repair with open repair in patients with abdominal aortic aneurysm (EVAR trial 1), 30-day operative mortality results: randomised controlled trial [J]. Lancet, 2004, 364(9437):843-848.
[3] Cochennec F, Becquemin J, Desgranges P,etal. Limb graft occlusion following EVAR: clinical pattern, outcomes and predictive factors of occurrence [J]. European Journal of Vascular and Endovascular Surgery, 2007, 34(1):59-65.
[4] Kleinstreuer C, Li Zhonghua. Analysis and computer program for rupture-risk prediction of abdominal aortic aneurysms[J]. Biomedical Engineering Online, 2006(5):19.
[5] Carroccio A, Faries P, Morrissey N,etal. Predicting iliac limb occlusions after bifurcated aortic stent grafting: Anatomic and device-related causes[J]. Journal of Vascular Surgery, 2002, 36(4):679-684.
[6] Zarins CK, Arko FR, Crabtree T,etal. Explant analysis of AneuRx stent grafts: relationship between structural findings and clinical outcome[J]. Journal of Vascular Surgery, 2004, 40(1):1-11.
[7] Kleinstreuer C, Li Zhonghua, Basciano CA,etal. Computational mechanics of Nitinol stent grafts [J]. Journal of Biomechanics, 2008, 41(11): 2370-2378.
[8] Zidi M, Cheref M. Mechanical analysis of a prototype of small diameter vascular prosthesis: numerical simulations [J]. Computers in Biology and Medicine, 2003, 33(1): 65-75.
[9] Demanget N, Avril S, Badel P,etal. Computational comparison of the bending behavior of aortic stent-grafts [J]. Journal of the Mechanical Behavior of Biomedical Materials, 2012,05(1):272-282.
[10] Azaouzi M, Makradi A, Belouettar S. Deployment of a self-expanding stent inside an artery: A finite element analysis [J]. Materials & Design, 2012, 41: 410-420.
[11] Li Zhonghua, Kleinstreuer C. Blood flow and structure interactions in a stented abdominal aortic aneurysm model [J]. Medical Engineering and Physics.2005,27:369-382.
[12] Pelton AR, Gong XY, Duerig TW. Fatigue testing of diamond-shaped specimens [C]//Pelton AR, Duerig TW, eds. SMST 2003: International Conference on Shape Memory and Superelastic Technologies. Pacific Grove: International Organization on SMST, 2004:293-302.
[13] Raghavan ML, Webster MW, Vorp DA.Exvivobiomechanical behavior of abdominal aortic aneurysm: assessment using a new mathematical model [J]. Annals of Biomedical Engineering, 1996, 24(5): 573-575.
Biomechanical Analysis for Cylindrical Abdominal Aortic Stent-Grafts
Gu Xuelian1*Hu Fangqiu1Qi Yongxiang1,2Li Zhonghua2Song Chengli1
1(ShanghaiInstituteforMinimallyInvasiveTherapy,UniversityofShanghaiforScienceandTechnology,Shanghai20093,China)2(ShanghaiMicroportMedical(Group)Co.,Ltd. (HQ),Shanghai201203,China)
stent-grafts; abdominal aortic aneurysm; biomechanics; nitinol alloy
10.3969/j.issn.0258-8021. 2015. 05.015
2014-09-17, 录用日期:2014-11-21
R318.01/R318.11
D
0258-8021(2015) 05-0623-06
*通信作者(Corresponding author), E-mail: guxuelianbest@126.com
