H5N6亚型禽流感病毒反向遗传疫苗株的构建及免疫保护试验
2015-02-11,,,,,
,,,,,
(中国动物卫生与流行病学中心,山东青岛 266032)
H5N6亚型禽流感病毒反向遗传疫苗株的构建及免疫保护试验
蒋文明,侯广宇,王素春,李金平,刘 朔,陈继明
(中国动物卫生与流行病学中心,山东青岛 266032)
为应对抗原性已发生变异的第2.3.4.6分支H5N6亚型禽流感病毒(AIV)引发的潜在流行,本研究利用反向遗传操作技术,以A/Puerto Rico/8/34(PR8)的内部基因为骨架,以H5N6亚型AIV A/Chicken/SC/6/2014(C6)的基因组为模板,经RT-PCR扩增其HA及NA基因,并对HA基因进行分子修饰,去除与H5亚型AIV致病力有关的HA蛋白裂解位点处的多个碱性氨基酸,使其获得低致病性AIV的分子特征(即将-PLRERRRKR-突变为-PQRETR-),成功构建了H5N6亚型AIV疫苗候选株rC6。免疫效力试验表明,rC6重组灭活疫苗可以诱导产生高水平的血凝抑制抗体。免疫攻毒保护试验表明,rC6重组灭活疫苗可以提供SPF鸡抵抗同源和异源H5N6病毒100%的保护,而针对第2.3.4分支的Re-5疫苗仅能提供大约10%的保护。利用反向遗传技术构建的rC6重组疫苗候选株为该分支病毒的防控提供了有益的尝试。
禽流感病毒;变异株;H5N6;反向遗传;疫苗
2003年以来,H5N1亚型高致病性禽流感(Avian inf uenza,AI)一直在多个国家和地区流行,不但给养禽业造成了严重的经济损失,还严重威胁着人类的健康。除了不断加强和完善流感监测以外,接种疫苗仍然是防控AI的重要手段。而疫苗的有效性则取决于疫苗株与流行株之间的抗原性匹配程度[1]。2005年,我国推出了针对第2.3.4分支的Re-5疫苗,有效地控制了该分支病毒的流行[2]。2014年,四川、黑龙江发生的由第2.3.4.6分支H5N6亚型抗原变异株引起的AI疫情表明,流行病毒的抗原性已发生较大变异。因此,有必要重新构建针对第2.3.4.6分支的疫苗候选株,以应对该分支病毒的流行和威胁。本研究以筛选出的第2.3.4.6分支的H5N6亚型代表株C6为表面基因供体,以PR8的内部基因为骨架,构建了疫苗候选株rC6,并进行了免疫效力和攻毒保护试验,为该分支禽流感病毒的防控提供参考。
1 材料与方法
1.1 病毒株、细胞、载体以及实验动物
A/Chicken/SC/6/2014(H5N6)(C6)、A/ Goose/SC/7/2014(H5N6)(G7)及A/Puerto Rico/8/34(PR8)均由本实验室分离和保存;双向表达载体pH205和293T细胞由本实验室构建保存;SPF鸡胚和SPF鸡购自北京梅里亚维通实验动物技术有限公司。
1.2 主要试剂
QIAamp Viral RNA mini Kit购自Qiagen公司;PrimeSTAR Max DNA Polymerase、PrimeScript Reverse Transcriptase、T4 DNA连接酶、pMD19-T、DNA Marker、质粒提取试剂盒、胶回收试剂盒购自TaKaRa公司;限制性内切酶BsmBI、BsaI购自NEB公司;转染试剂Lipofectamine 2000购自Invitrogen公司。
1.3 引物设计
扩增PR8内部基因全长的引物根据Hoffmann发表的文献合成[3]。扩增C6病毒株HA基因突变引物根据其HA的多个连续碱性氨基酸位点的特异性序列设计,从而使具有强毒株分子特征的HA裂解位点-PLRERRRKR-突变成弱毒株的HA裂解位点-PQRETR-(图1)。HA、NA和HA突变体(HAmut)的引物由生工生物公司合成(表1)。

图1 HA基因碱性氨基酸裂解位点处的分子修饰

表1扩增C6病毒株HA、HAmut、NA基因所用引物
1.4 病毒RNA的提取及基因扩增
按照QIAamp Viral RNA mini Kit说明书提取病毒RNA,利用PrimeScript Reverse Transcriptase进行反转录。以cDNA为模板,利用PrimeSTAR Max DNA Polymerase扩增病毒各基因片段。PCR产物经琼脂糖凝胶电泳后,利用DNA胶回收试剂盒纯化回收,然后与pMD19-T载体连接,阳性重组质粒送生工生物测序鉴定。
对于HAmut的构建,以鉴定正确的C6 HA阳性重组质粒为模板,以两对引物HA-F/HA-Mut-R和HA-Mut-F/HA-R分别扩增出HA1和HA2片段,然后以HA1和HA2的混合物为模板,HA-F/HA-R为引物,用PrimeSTAR Max DNA Polymerase进行重叠延伸PCR(SOE-PCR),扩增出HAmut片段。PCR产物经胶回收后,与pMD19-T载体连接,阳性重组质粒测序鉴定。
1.5 重组表达质粒的构建
将鉴定正确的C6 HAmut、NA重组质粒以及6个PR8内部基因片段重组质粒经相应的BsmBI或BsaI酶切,与BsmBI酶切的表达载体pH205相连,提取重组质粒,进行测序鉴定,并利用DNAStar7.0软件进行序列分析。
1.6 病毒拯救与鉴定
按照Lipofectamine 2000脂质体转染试剂盒说明进行。将6个PR8内部基因重组表达质粒和2个C6 HAmut和NA表面基因重组表达质粒各0.6μg混合共转染293T细胞,48h后将细胞悬液接种10日龄SPF鸡胚,0.2ml/枚,37℃继续孵化,72h后收集尿囊液,测定其血凝活性。取血凝阳性的尿囊液经10000倍稀释后接种10日龄的SPF鸡胚扩增病毒,0.1ml/枚,72h后收集尿囊液,于-70℃保存备用。重组病毒命名为rC6。提取救获病毒的RNA,用RT-PCR扩增病毒的全基因组并测序。1.7 免疫保护试验和免疫交叉保护试验
将40只21日龄的SPF鸡分成4组,每组10只,其中一组经颈部皮下接种rC6灭活油苗、一组接种Re-5灭活油苗,接种剂量各为0.3ml/只,一组为不接种疫苗直接攻毒组,一组为健康对照组。免疫后21天采血分离血清,分别用鸡源H5N6亚型C6株和鹅源H5N6亚型G7株作为抗原测定抗体效价,并用106EID50的C6病毒对各组鸡进行滴鼻攻毒,连续观察14天,统计排毒、发病和死亡情况。
免疫交叉保护试验方法同上。其中攻毒用的野毒株为鹅源G7株。
2 结果
2.1 表达PR8内部基因重组质粒的构建
PR8的6个内部基因片段PB2、PB1、PA、NP、M、NS经RT-PCR扩增后,与pMD19-T载体连接,测序正确后经酶切后分别与酶切处理好的pH205表达载体连接,构建表达6个内部基因的重组质粒。经PCR、测序鉴定重组质粒构建正确(图2)。
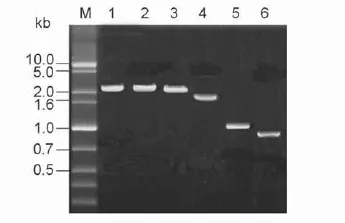
M. 1kb plus DNA Marker;1. PB2;2. PB1;3. PA;4. NP;5. M;6. NS图2 表达PR8内部基因重组载体的PCR鉴定
2.2 表达HAmut重组质粒的构建
采用SOE-PCR扩增C6株的HA基因,并将其克隆至pH205载体中,构建pH205-HAmut重组质粒。经PCR鉴定重组质粒构建正确(图3)。测序结果表明,HA裂解位点的氨基酸序列已由野生型病毒HA分子的-PLRERRRKR-突变为-PQRETR-,即被修饰为典型的H5亚型低致病性AIV HA分子特征。
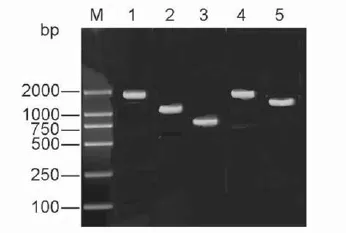
M. DL2000 DNA Marker;1. HA;2. HA1;3. HA2;4. HAmut;5. NA图3 表达C6病毒株HA、HAmut和NA重组质粒的PCR鉴定
2.3 重组病毒的拯救与鉴定
将构建成功的8个重组质粒转染293T细胞,利用反向遗传技术拯救出重组病毒rC6。在鸡胚繁殖一代后,提取病毒RNA、反转录,对拯救病毒的全基因组进行扩增、测序。测序结果表明,HA基因裂解位点已被突变为-PQRETR-,为低致病性AIV分子特征,其余7个片段均未发生突变,均与预期的病毒疫苗株一致。
2.4 SPF鸡的免疫保护试验和交叉免疫保护试验
rC6灭活油苗的免疫和交叉免疫保护试验见表2。免疫后21天,用鸡源H5N6亚型C6株作为抗原,测得rC6重组灭活油苗免疫鸡的平均抗体效价为29.4;用鹅源H5N6亚型AIV G7株做抗原,测得rC6重组灭活油苗免疫鸡的平均抗体效价为28.9;用Re-5作为抗原,测得rC6重组灭活油苗免疫鸡的平均抗体效价为22.9。Re-5灭活油苗免疫后21天,用Re-5作为抗原,测得Re-5重组灭活油苗免疫鸡的平均抗体效价为28.9,用C6株作为抗原测得的平均抗体效价为24.5;用G7株作为抗原测得的平均抗体效价为24.7。攻毒保护试验结果显示,rC6重组灭活疫苗为SPF鸡提供的针对同源病毒的免疫保护率为100%;用鹅源H5N6亚型AIV G7株攻毒,rC6重组灭活疫苗提供的交叉免疫保护率为100%。Re-5灭活疫苗对C6和G7株病毒提供的免疫保护率仅为10%。未免疫组经攻毒C6和G7后5天内全部死亡,健康对照组的鸡正常。
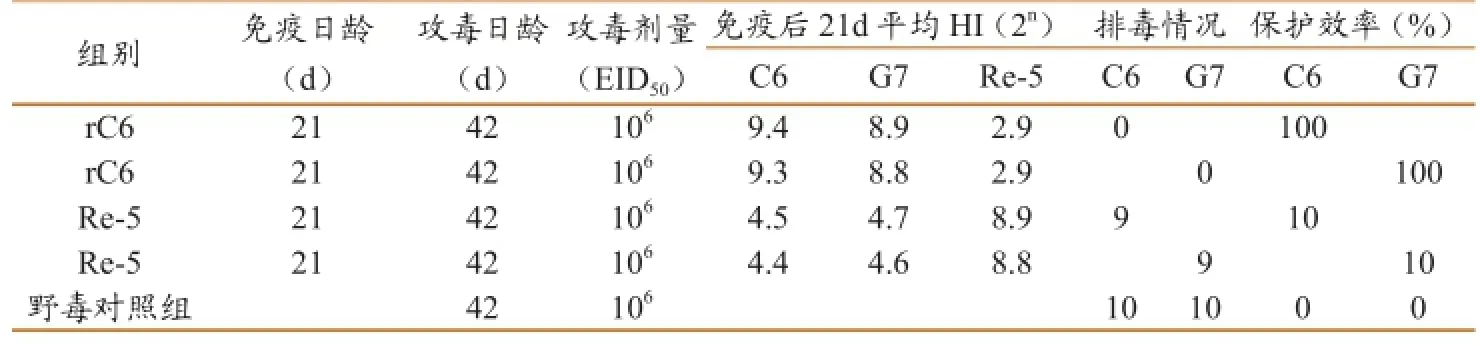
表2 rC6重组灭活疫苗对SPF鸡的免疫和交叉免疫保护试验
3 讨论
从cDNA克隆拯救出负链RNA病毒是90年代分子病毒学研究领域最振奋人心的技术,也为制备新型的禽流感疫苗开启了新的思路和方法。近年来,世界各地不断有禽流感事件发生,尤其是高致病性禽流感,给养禽业造成了巨大的经济损失,也严重危害着人类的健康。加之禽流感一直处于不断变异之中,这给禽流感的防控增加了难度。
2005年,我国开始实施针对禽流感的大规模免疫政策,随着病毒的不断变异,疫苗也从Re-1更新到Re-4和Re-5,到目前的Re-6和Re-7。从流行病学调查来看,Re-5对应的第2.3.4分支的病毒出现了一些变异毒株。抗原表位分析显示,与该分支的疫苗株Re-5相比,C6病毒株在Q131L、S139P、D140N、A143T、S145L、T156M、I167T、Q208K、K234Q、V281M等抗原位点出现了变化[4,5]。Re-5与C6之间的交叉HI相关系数R=0.39(R˜0.5),说明C6毒株与疫苗株之间的抗原性差异明显。
本研究采用反向遗传操作技术,以A/Puerto Rico/8/34(PR8)的内部基因为骨架,A/CK/ SC/6/2014(H5N6)的表面基因为供体,通过对其HA基因进行分子修饰,去除HA蛋白裂解位点处的多个连续碱性氨基酸,使其获得低致病性AIV的分子特征[6],同时又保证了重配病毒与流行株的抗原匹配性,成功构建了针对第2.3.4.6分支的H5N6亚型AIV疫苗候选株rC6。在用SPF鸡进行的免疫保护试验和交叉免疫保护试验中,rC6灭活油苗免疫21天的平均抗体效价为29.4,交叉免疫的平均抗体效价也有28.9,而用Re-5作为抗原测得的抗体效价只有22.9,说明这些新近流行的毒株与原有针对第2.3.4分支的Re-5疫苗在抗原性上已经差别很大。免疫攻毒保护试验也验证了这一结论,rC6重组灭活疫苗可以提供SPF鸡针对同源和异源H5N6病毒100%的保护,而Re-5疫苗只能提供大约10%的保护。本研究构建的rC6重组疫苗候选株为该分支病毒的防控提供了有益的探索和尝试。
H5亚型高致病性禽流感病毒的变异情况值得关注,第2.3.4分支的病毒出现了显著的变异,尤其是第2.3.4.6分支病毒的大量出现,应引起足够的重视。兽医主管部门应加强对禽流感疫苗的质量管控和临床应用效果的监测评估,并根据疫情的变化及时调整疫苗生产用种毒。并积极调整防控策略,由单纯依赖疫苗的防控方针,转向综合性的防控策略。
[1] Shi H,Liu X. Generation of an attenuated H5N1 avian inf uenza virus vaccine with all eight genes from avian viruses [J]. Vaccine,2007,25:7379-7384.
[2] Chen H. Avian influenza vaccination:the experience in China[J]. Rev Sci Tech,2009,28:267-274.
[3] Hoffmann E,Stech J,Guan Y,et al. Universal primer set for the full-length amplif cation of all inf uenza A viruses[J]. Arch Virol,2001,146:2275-2289.
[4] Kaverin N V,Rudneva I A,Govorkova E A,et al. Epitope mapping virus by using monoclonal antibodies[J]. J Virol,2007,81:12911-12917.
[5] Velkov T,Ong C,Baker M A,et al. The antigenic architecture of the hemagglutinin of inf uenza H5N1 viruses[J]. Mol Immunol,2013,56:705-719.
[6] Gohrbandt S,Veits J,Hundt J,et al. Amino acids adjacent to the haemagglutinin cleavage site are relevant for virulence of avian influenza viruses of subtype H5[J]. J Gen Virol,2011,92:51-59.
Construction of Reverse Genetic Vaccine Strain against Variant H5N6 Avian Inf uenza Virus and its Protective Eff cacy Test
Jiang Wenming,Hou Guangyu,Wang Suchun,Li Jinping,Liu Shuo,Chen Jiming
(China Animal Health and Epidemiology Center,Qingdao,Shandong 266032)
To control of H5N6 subtype highly pathogenic avian inf uenza viruses(HPAIVs) with antigenic changes(clade 2.3.4.6),and the potential pandemic threat to poultry,a reassortant virus,named rC6,was constructed using reverse genetics in the study. The virus contained modif ed HA and NA genes of an epidemic strain A/Chicken/SC/6/2014 with the internal genes derived from A/Puerto Rico/8/34(PR8). The reassortant virus was attenuated by removal of the multi-basic amino acid motif in the HA gene by mutation and deletion(from PLRERRRKR to PQRETR),thus resulting in a candidate vaccine virus. Immune eff cacy tests showed that the inactivated rC6 recombinant vaccine could induce high levels of hemagglutination inhibition antibody. Challenge tests showed that rC6 recombinant inactivated vaccines provided SPF chickens with 100% protection against homologous and heterologous H5N6 virus,and Re-5 vaccine against clade 2.3.4 viruses only provided about 10% protection. The rC6 recombinant vaccine candidate strains using reverse genetics technology provided a benef cial attempt for prevention and control of the virus of clade 2.3.4.6.
:avian inf uenza virus;variant;H5N6;reverse genetics;vaccine
S852.657
:A
:1005-944X(2015)01-0064-04
