正交试验优选白术中白术内酯Ⅰ和白术内酯Ⅲ提取工艺
2015-01-16梁志远甘秀海张君勇练小卫
梁志远, 甘秀海, 吴 坤, 张君勇, 练小卫
(1.贵州师范学院药用植物研究所,贵州贵阳550018;2.贵州师范学院化学与生命科学学院,贵州贵阳550018)
正交试验优选白术中白术内酯Ⅰ和白术内酯Ⅲ提取工艺
梁志远1,2, 甘秀海1,2, 吴 坤2, 张君勇2, 练小卫2
(1.贵州师范学院药用植物研究所,贵州贵阳550018;2.贵州师范学院化学与生命科学学院,贵州贵阳550018)
目的优选白术中白术内酯Ⅰ和Ⅲ提取工艺。方法以白术内酯Ⅰ和Ⅲ的含有量为评价指标,选取料液比、乙醇体积分数、提取温度、提取次数为考察因素,通过正交试验优选白术中白术内酯Ⅰ和Ⅲ的提取工艺。结果最佳提取工艺条件为85%乙醇,料液比1∶12,在50℃下提取2次,每次30 min。结论该提取工艺操作简单、方便、安全,稳定性好,为白术中白术内酯的进一步研究提供科学依据。
白术;白术内酯;超声波;正交试验;提取工艺
白术为菊科植物白术Atracttylodesmacrocephala koidz的干燥根茎,性味甘、苦、温,具有健脾、益气、燥湿利水、止汗安胎等功效[1]。现代药理学研究表明,白术还具有抗炎、抗肿瘤、调节胃肠道功能和促进营养物质吸收的作用。白术主要产于浙江、安徽、湖南、湖北、江西、福建等地,以浙江磐安、鄞县、新昌地区产量最大,于潜所产品质最佳[2]。白术内酯Ⅰ和Ⅲ是白术的有效成分,也是白术药材质量控制的主要指标[3-5]。由于白术中白术内酯Ⅰ和Ⅲ含有量较低,性质又不太稳定,如何对其进行提取,一直受到人们的关注。目前用于白术内酯的提取方法有:有机溶剂冷或热浸提法、渗漉法、索氏提取法、超声波提取法,水蒸气蒸馏法和超临界 CO2萃取法等[6-8],溶剂常用甲醇[9-11]。
超声波技术近年来发展非常迅速,具有省时、节能、高效等特点。该法是利用超声波产生的强烈振动、强烈的空化效应、搅拌等,造成植物组织细胞壁的破裂,增加溶剂渗入细胞组织,加快细胞内含物的释放,从而提高浸出率,缩短提取时间,同时可避免高温对提出成分的影响,被广泛用于中药有效成分的提取[12]。本研究以乙醇为溶媒,采用超声波辅助提取,考察了料液比、乙醇体积分数、提取温度、提取次数因素对提取率的影响。通过正交试验优化了白术内酯Ⅰ和Ⅲ的提取工艺,以期为白术内酯的进一步研究和开发利用提供实验依据。
1 仪器与材料
1.1 仪器 Agilent 1260高效液相色谱仪(美国惠普公司);BSA124S型电子天平 (北京慧龙环科环境仪器有限公司);KQ3200B型超声波清洗器 (昆山市超声仪器有限公司);RE-2000A型旋转蒸发仪 (上海亚荣生化仪器厂);SHB-Ⅲ循环水式多用真空泵 (郑州长城科工贸有限公司);XFB-200BC微型万能粉碎机 (长沙市雨花区中诚制药机械厂)。
1.2 材料 药材白术购于贵阳药材市场,经贵阳中医学院席先蓉教授鉴定为白术Atractylodesmacroeephala Koidz的根茎。白术内酯Ⅰ和Ⅲ对照品购于贵州省迪大科技有限责任公司(批号分别为GZ73069-12-3和GZ73030-71-4,纯度均大于99%);甲醇为色谱纯,水为娃哈哈纯净水,乙醇为食用级,其余试剂均为分析纯。
2 方法与结果
2.1 白术内酯Ⅰ和Ⅲ测定
2.1.1 对照品溶液的配制 分别精密称取白术内酯Ⅰ和Ⅲ对照品8.0 mg和10.0 mg,用甲醇溶解,置50 mL量瓶中并定容,制成白术内酯Ⅰ和Ⅲ质量浓度分别为160和200 μg/mL的混合对照品贮备液。
2.1.2 供试品溶液的制备 精密称取过40目的白术粉末(50℃衡重4 h)0.5 g,置100 mL具塞锥形瓶中,加入95%乙醇20mL,在40℃下超声提取30min,提取液过滤,减压除尽乙醇和水,甲醇溶解,取上清液过0.45μm滤膜,取续滤液作为供试品溶液。
2.1.3 色谱条件 ZORBAXSB.C18色谱柱(150 mm× 4.6mm,5μm);流动相为甲醇-水 (65∶35);体积流量1.0m L/m in;检测波长220 nm;柱温30℃;进样量10μL。色谱图见图1。
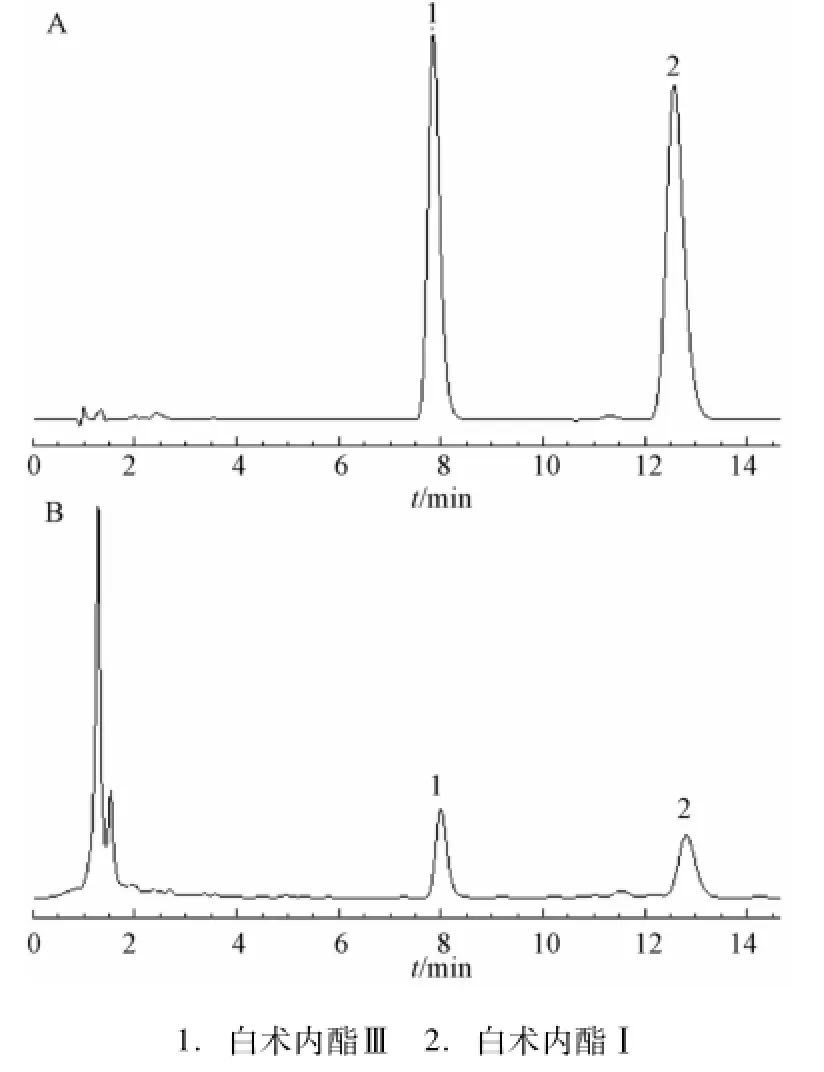
图1 白术内酯Ⅰ和Ⅲ对照品 (A)和供试品 (B)HPLC色谱图
2.1.4 线性关系考察 分别精密吸取白术内酯Ⅰ和III混合对照品贮备液1.0、2.0、4.0、6.0、8.0、10.0 mL置10 mL量瓶中,加甲醇至刻度,摇匀,得白术内酯I和III质量浓度分别为16、32、64、96、128、160μg/mL和20、40、80、120、160、200μg/mL的对照品溶液。在上述色谱条件下进行分析。以白术内酯对照品质量浓度 (μg/mL)为横坐标,峰面积为纵坐标,绘制标准工作曲线,并进行线性回归,求得两种内酯回归方程,白术内酯 I:Y= 40.94X+74.431,r=0.999 7;白术内酯 III:Y= 26.078X+49.741,r=0.999 9。结果表明白术内酯Ⅰ和Ⅲ分别在16~160μg/mL和20~200μg/mL范围内峰面积积分值与质量浓度呈良好线性关系。
2.1.5 精密度试验 精密吸取 “2.1.4”项下白术内酯Ⅰ和Ⅲ度分别为 64、80μg/m L混合对照品溶液,按“2.1.3”项下进行测定,重复进样5次,结果白术内酯Ⅰ和Ⅲ的RSD分别为0.77%和0.55%,表明仪器精密度良好。
2.1.6 稳定性试验 取同一供试品溶液分别在0、2、4、6、8 h进样,按 “2.1.3”项下测定,结果白术内酯Ⅰ和Ⅲ的RSD分别为1.63%和1.68%。表明供试品溶液在8 h内稳定。取一供试品溶液按 “2.1.3”项下测定,置于冰箱冷藏24 h后再测定,结果白术内酯Ⅰ和Ⅲ的RSD分别为1.72%和2.80%。表明供试品溶液置冰箱冷藏在24 h内仍能保持稳定。
2.1.7 重复性试验 精密称取药材5份,每份0.5 g,按“2.2.3”项下方法平行制备供试品溶液,按 “2.1.3”项下测定。结果白术内酯Ⅰ和Ⅲ的RSD分别为1.36%和1.40%,表明该方法重复性良好。
2.1.8 加样回收率试验 精密称取已知含有量的白术药材6份,每份0.25 g,3份分别精密加入白术内酯Ⅰ和Ⅲ对照品贮备液2 mL(即白术内酯Ⅰ和Ⅲ各加320μg和400 μg),3份分别精密加入白术内酯Ⅰ和Ⅲ对照品贮备液3 mL(即白术内酯Ⅰ和Ⅲ各加 480μg和 600μg),按“2.2.3”项下方法制备供试品溶液,按 “2.1.3”项下测定,结果见表1,结果表明方法的回收率较好。

表1 白术内酯Ⅰ和Ⅲ的加样回收率
2.2 白术内酯Ⅰ和Ⅲ最佳提取工艺的优选
2.2.1 超声提取单因素试验设计 以提取液中白术内酯Ⅰ和Ⅲ的含有量为评价指标,考察单因素对提取率影响。精密称取过40目的白术粉末 (50℃衡重4 h)0.5 g,在前期研究基础上,分别研究料液比1∶8、1∶10、1∶12、1∶14 4个水平,乙醇体积分数65%、75%、85%、95%4个水平,提取温度30、40、50、60℃4个水平,提取次数1、2、3次3个水平的单因素试验条件下,测定提取液中白术内酯Ⅰ和Ⅲ的含有量,得出各因素的最佳范围。
单因素试验显示,白术内酯Ⅰ和Ⅲ的提取率随料液比的增大有增高的趋势,当料液比达到1∶14时,白术内酯Ⅰ的提取率略有增加,但白术内酯Ⅲ的反而降低;随提取温度的升高白术内酯Ⅰ和Ⅲ的提取率也有增大的趋势,当提取温度达到60℃时,白术内酯Ⅰ和Ⅲ的提取率都降低。在考察超声时间对白术内酯Ⅰ和Ⅲ提取率的影响时,发现超声30 m in已基本提取完全。
2.2.2 正交试验设计 在单因素试验基础上,确定料液比、乙醇体积分数、提取温度和提取次数四个因素的3个水平,采用L9(34)正交试验表安排实验,因素与水平见表2。

表2 因素水平
2.2.3 正交试验方法与结果 精密称取过40目的白术粉末 (50℃衡重4 h)9份,每份0.5 g,置100mL具塞锥形瓶中,按 “2.2.2”项下的正交试验方法超声提取,提取液过滤,减压除尽乙醇和水,残余物用甲醇溶解,转移至10 mL量瓶并定容,0.45μm滤膜过滤,得供试品溶液1~9号,然后按 “2.1.3”项下测定白术内酯Ⅰ和Ⅲ的含有量,并进行极差和方差分析。结果见表3~5。

表3 L9(34)正交试验结果 (n=2)
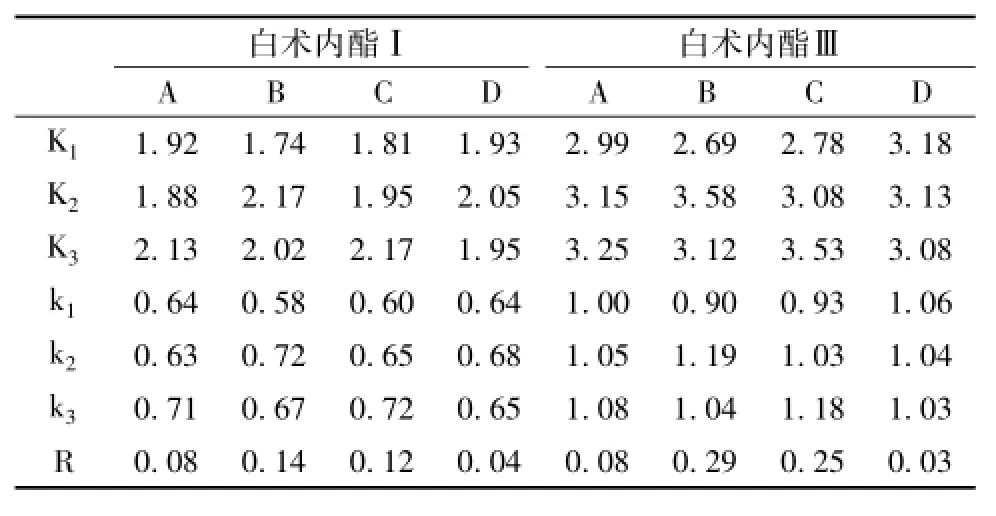
表4 L9(34)正交试验结果分析
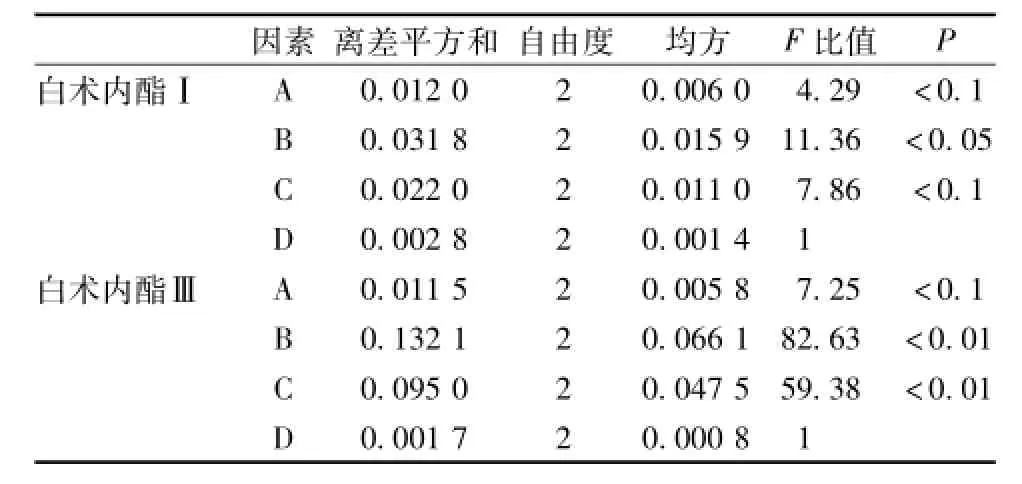
表5 方差分析
从表4极差R值看出,白术内酯Ⅰ和Ⅲ都是RB>RC>RA>RD,即影响因素主次顺序为:乙醇体积分数>提取温度>料液比>提取次数。从表4方差分析结果表明,对于白术内酯Ⅰ的提取:乙醇体积分数影响显著,料液比和提取温度有一定影响,提取次数影响甚微;对于白术内酯Ⅲ的提取:乙醇体积分数和提取温度影响非常显著,料液比有一定影响,提取次数影响甚微,即正交试验的极差分析和方差分析都显示,乙醇体积分数对两种内酯的提取结果有显著影响,为影响提取率的主要因素,提取温度和料液比为次要因素。综合考虑极差和方差分析结果,筛选出超声波辅助乙醇提取白术中白术内酯Ⅰ和Ⅲ的最佳工艺条件A3B2C3D2,即料液比1∶12、乙醇体积分数85%、提取温度50℃、提取2次,每次30 min。
2.2.4 验证试验 精密称取过40目的白术粉末 (50℃衡重4 h)6份,每份0.5 g,3份按优选出方法制备供试品溶液,3份按文献 [13]的方法制备供试品溶液,按“2.1.3”项下测定,优选方法的结果为白术中白术内酯Ⅰ和Ⅲ的平均含有量分别为0.75 mg/g和1.41mg/g,文献方法的平均含有量分别为0.77mg/g和1.40mg/g。本研究又将量扩大到5倍,即取2.5 g白术粉末,按上述方法重复实验,优选方法的结果为白术内酯Ⅰ和Ⅲ的平均值分别为0.71mg/g和1.38 mg/g,文献方法的平均值分别为0.75 mg/g和1.39 mg/g,表明两种方法提取效率相当。
3 讨论与结论
在文献 [9]的基础上,本研究考察了乙腈-水、乙腈-0.2%乙酸水、甲醇-水、甲醇-0.1%磷酸水等不同流动相系统,结果发现甲醇-水系统能获得分离度较好的色谱峰;进而探究了甲醇与水80∶20、70∶30、65∶35、60∶40,结果在甲醇与水65∶35的比列下,供试品溶液中白术内酯Ⅰ和Ⅲ峰间的分离度大于4,并能与杂质峰达到较好的基线分离,保留时间也较适合。
通过考察发现提取温度不宜过高,50℃比较合适,温度高于50℃提取率反而会降低。可能是两种白术内酯都不够稳定所致,因为白术内酯Ⅲ分子有个羟基,易发生分子内脱水生成白术内酯Ⅱ,另白术内酯Ⅲ与白术内酯Ⅰ可进行分子间脱水,生成双白术内酯[14-15]。
通过考察发现提取率随乙醇体积分数的降低而降低,乙醇体积分数为85%比较合适。可能是这两种内酯极性都不大,降低乙醇体积分数即增加溶媒的极性,导致它们在其中的溶解度降低。研究中还发现,随着乙醇体积分数的降低,极性杂质的溶出量增多,最后用甲醇定容时不溶物也随之增加,干扰测定。因此,乙醇体积分数相对高些,有利提高白术内酯Ⅰ和Ⅲ的提出率和纯度。
通过考察发现提取率随料液比的增大有增高的趋势,当料液比达到1∶14时,白术内酯Ⅰ的提取率略有增加,但白术内酯Ⅲ的反而降低。可能是料液比增加,相应水量增加,减压除去乙醇和水的时间延长,导致白术内酯Ⅲ发生分子内脱水转变成白术内酯Ⅱ。因此,料液比不宜太高。
本研究的方法与文献 [13]的相比,最大的不同是用食用级乙醇代替文献中的甲醇作溶媒,虽然在提取时间、提取次数和溶剂用量方面也随着改变,但安全性提高了。从植物中提取有效成分,乙醇和甲醇都是人们常用的溶媒,乙醇的极性比甲醇稍弱,往往通过加适量的水来增加其极性,甲醇的沸点相对较低,除去方便。因此,在用量不大时人们更喜欢使用甲醇。但甲醇毒性较大,不宜工业化生产。
本研究采用超声波辅助提取法,其优点之一为高效、快速,可避免白术内酯Ⅰ和Ⅲ长时间处于较高温度下导致结构发生变化。另外,采用食用级乙醇作溶媒,所筛选出超声波辅助乙醇提取白术中白术内酯Ⅰ和Ⅲ的最佳工艺,方法合理可行,结果稳定,提取率高;所需设备简单,操作方便安全;适宜大规模工业化生产。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:68.
[2]陈晓萍,张长林.白术不同化学成分的药理作用研究概况[J].中医药信息,2011,28(2):124-126.
[3]张程荣,曹 岗,丛晓东,等.白术化学成分和质量控制研究进展[J].中华中医药杂志,2011,26(10):2328-2331.
[4]丁永明,宋长义,贾天柱.白术炮制品的质量标准研究[J].中成药,2005,27(6):53-56.
[5]刘玉强,才 谦.50批不同来源白术药材及饮片中白术内酯Ⅰ和白术内酯Ⅲ含量的HPLC法测定[J].药物分析杂志,2012,32(7):1249-1252.
[6]王 芳.白术内酯Ⅲ提取工艺研究[J].陕西教育学院学报,2008,24(3):56-58.
[7]卫修来,陈 镇,夏 泉,等.索氏提取法提取白术内酯Ⅰ的工艺研究[J].时珍国医国药,2009,20(6):1427-1428.
[8]王天宝,贺清源.超声波提取两种白术内酯的溶剂选择[J].现代医药卫生,2009,25(5):755-756.
[9]刘伟祥,黎琼红,谢 晨,等.HPLC法测定白术中的白术内酯Ⅰ、Ⅱ、Ⅲ[J].中草药,2007,37(8):1261-1262.
[10]吴 佳,王艳平,刘湘丹,等.白术内酯Ⅰ和Ⅲ在不同白术样品中的比较研究[J].中国民族民间医药,2009,18(2):4-5.
[11]许祥君,陈 敏,宗 露,等.不同品规白术中白术内酯Ⅰ、Ⅲ的含量测定[J].中国医院药学杂志,2011,31(17):1421-1424.
[12]徐小燕.超声技术在中草药提取中的应用[J].中国药房,2007,18(18):1426-1429.
[13]李 鹏,陈琴华,李志浩,等.超声法提取白术中白术内酯Ⅰ和白术内酯Ⅲ的正交实验研究[J].中药材,2009,32(10):1615-1618.
[14]王小芳,王 芳,张亚环,等.白术挥发油中苍术酮氧化反应的动力学[J],应用化学,2007,24(3):31-35.
[15]李 伟,文红梅,崔小兵,等.白术的炮制机理及其倍半萜成分转化的研究[J].中国中药杂志,2006,31(19):1600-1603.
R284.2
:B
:1001-1528(2015)06-1356-05
10.3969/j.issn.1001-1528.2015.06.046
2014-03-18
贵阳市乌当区科技局基金资助项目 (乌科字 [2012]58号)
梁志远 (1959—),女,教授,主要从事有机化学教学和药用植物成分研究工作。Tel:(0851)85816647,E-mail:gzwh24000@ sina.com
