三水碘化锂制备工艺研究
2015-01-11郭举
郭 举
(瓮福(集团)有限责任公司,贵州福泉,550500)
三水碘化锂制备工艺研究
郭 举
(瓮福(集团)有限责任公司,贵州福泉,550500)
介绍了利用含碘溶液制备三水碘化锂的生产工艺,研究了反应条件对三水碘化锂纯度的影响。结果表明:反应温度为45℃,n(碳酸锂)/n(碘离子)=1.2∶1,反应时间为1 h,搅拌速度为200 r/min时,制备的产品纯度可达98.1%。
三水碘化锂;碘;磷矿
海相沉积岩类磷矿一般都伴有氟碘资源。美国、苏联等国家在20世纪50年代就开始从事磷矿石提碘研究,我国也从20世纪70年代开始研究从磷矿中提碘,但因为工艺复杂、成本高而没有实现工业化生产[1]。贵州某大型国有磷化工企业于2007年建成了世界上第一套磷矿提碘装置,产量达到100t/a。
三水碘化锂作为一种重要的基础化学试剂,在电解液(用于燃料电池)、药物合成、催化化学、无水碘化锂的制备、照相业及人工晶体合成等方面有着广泛的应用[2]。目前,国、内外制备三水碘化锂的方法主要有:硫化氢还原法、联胺法、液氨法及中和法[3]。
本文利用碘生产中间过程产物(含碘溶液)制备三水碘化锂,并对工艺条件进行了试验研究,探讨了反应时间、反应温度、搅拌速率、物料配比等因素对产品纯度的影响。该工艺具有过程简单、生产周期短、原材料利用率高、所制备的产品纯度高等优点。
1 实验部分
1.1 主要原料及仪器
碘溶液、亚硫酸、碳酸锂、丙酮,旋转蒸发仪、真空干燥箱、数显恒温水浴锅、循环水式真空泵、电动搅拌机。
2.2 试验原理
碘溶液的主要组成为:w(I-)=3%~5%,溶液呈强酸性。由于碘溶液中含有少量的单质碘,为提高碘利用率,实验先加入少量亚硫酸作还原剂,将碘单质还原为碘离子;然后加入一定量的无水碳酸锂,反应得到碘化锂与硫酸锂溶液;经真空浓缩后,得到的晶体为硫酸锂与碘化锂混合晶体;利用碘化锂易溶于丙酮而硫酸锂不溶于丙酮的特性,向混合晶体加入一定量丙酮(作为萃取剂),分离提纯碘化锂;最后,将萃取液低温结晶,即可制得高纯度的三水碘化锂产品。工艺流程如图1所示。
主要反应方程式为:


图1 三水碘化锂制备工艺流程图Fig.1 Flow chart for preparing lithium iodide trihydrate
2 结果及讨论
2.1 反应时间对产品纯度的影响
在反应温度45℃,搅拌速度200 r/min,n(碳酸锂)/n(碘离子)=1.2∶1时,研究不同反应时间对产品纯度的影响。结果见图2所示。

图2 反应时间对产品纯度的影响Fig.2 Effect of reaction time on product purity
由图2可知,反应时间对产品纯度影响较大:反应时间延长,有利于提高产品的纯度,但继续延长反应时间,产品纯度反而下降。反应时间超过2h后,溶液颜色略微变灰,有可能是部分碘离子被氧化所致,从而使得产品纯度降低,这也说明反应液不宜长时间暴露在空气中。因此,选择反应时间为1h比较适宜。
2.2 反应温度对产品纯度的影响
在反应时间为1 h,搅拌速度200 r/min,n(碳酸锂)/n(碘离子)=1.2∶1时,研究不同反应温度对产品纯度的影响。结果见图3所示。
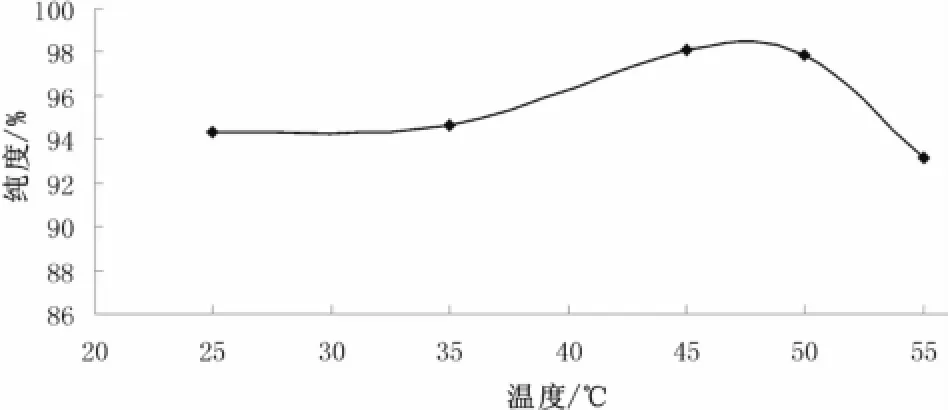
图3 反应温度对产品纯度的影响Fig.3 Effect of reaction temperature on the product purity
由图3可知,随着反应温度的升高,产品纯度呈先升后降的趋势。在一定时间内,温度越高越有利于反应的进行,即所得产品的纯度越高;但温度超过50℃后,继续升高温度,产品纯度则快速降低。在高温下,溶液表面会有一层淡淡的黄雾,这是由于单质碘在微热情况下升华造成的,这也说明碘离子在高温条件下被氧化成碘单质而挥发了,从而降低了产品的纯度。提高反应温度有利于反应的进行,但温度过高会降低产品纯度,因此,反应温度控制在45℃为宜。
2.3 搅拌速度对产品纯度的影响
在反应温度为45℃,反应时间1 h,n(碳酸锂)/n(碘离子)=1.2∶1时,研究不同搅拌速度对产品纯度的影响。结果见图4所示。
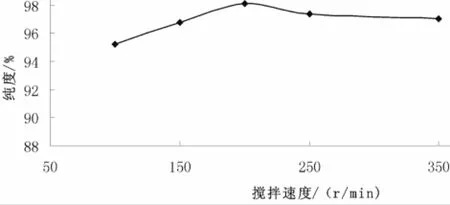
图4 搅拌速度对产品纯度的影响Fig.4 Effect of stirring speed on product purity
从图4可知,随着搅拌速度的增加,产品纯度有所增加,但搅拌速度大于200 r/min后,继续增大搅拌速度,产品纯度则会随之降低。这是由于当搅拌速度逐渐增加时,碳酸锂与氢碘酸之间的有效碰撞增加了,这利于碘化锂的生成;但继续增加搅拌速度时,还未参加反应的氢碘酸会在高速搅拌下挥发到空气中,使参加反应的氢碘酸的量减少,从而使产品纯度降低。综合考虑,选择搅拌速度为200 r/min为宜。
2.4 物料配比对产品纯度的影响
在反应温度45℃,搅拌速度200 r/min,反应时间1 h时,研究不同物料配比对产品纯度的影响。结果见图5所示。
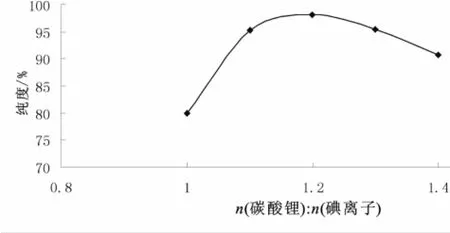
图5 物料配比对产品纯度的影响Fig.5 Effect of material ratio on product purity
在碳酸锂与氢碘酸的反应中,若碳酸锂加入量少于理论值,则反应溶液的 pH为2~3,浓缩结晶后所得白色产品很快变为红色,最后变为咖啡色。这可能是产品上附有高浓度的氢碘酸,并与空气大面积接触时被氧化为单质碘,从而影响了产品纯度。若碳酸锂加入量过多,则过量的碳酸锂溶解到溶液当中,并在浓缩结晶过程中与碘化锂一起结晶出来混杂在产品当中,从而降低了产品的纯度。因此,碳酸锂加入量应为溶液中碘离子含量的1.2倍为宜。
2.5 正交试验
为确定各反应因素影响的主次关系,结合单因素实验结果,本文确定了正交实验的因素和水平,如表1所示。正交实验结果及极差分析见表2。
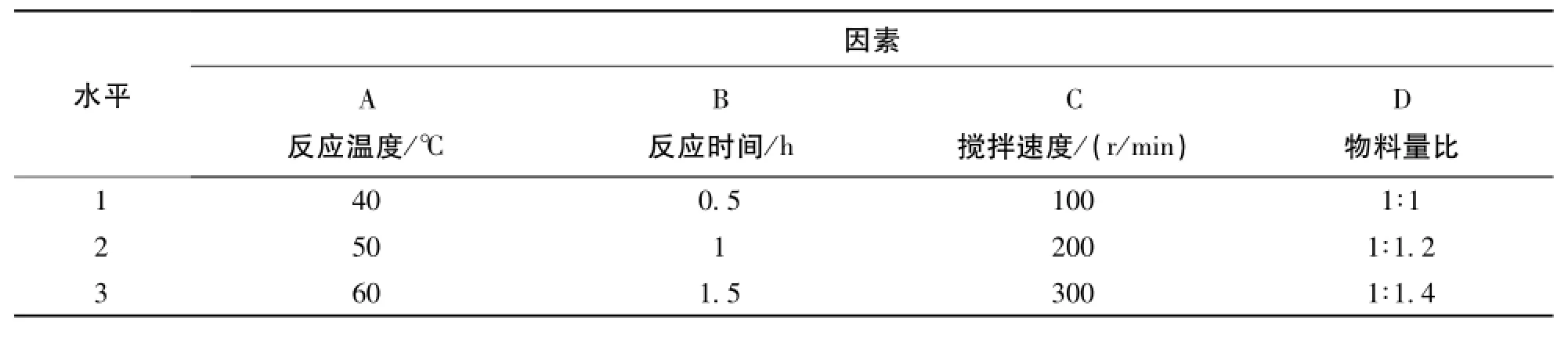
表1 正交实验因素水平表Table.1 Orthogonal factor level table

表2 正交实验结果及极差分析表Table.2 Orthogonal experiment results and range analysis table
以各因素的水平号为横坐标,相应的Kij为纵坐标,绘制正交实验的直观分析图,见图6。
通过比较各因素极差的大小,得出各因素对产品纯度影响的主次顺序为:反应温度>物料配比 >反应时间 >搅拌速度。
3 产品检测
取一定量的三水碘化锂产品,利用 XRD进行表征,见图7。图7与标准图谱对照,确定该产品为三水碘化锂。

图6 实验指标与因素、水平的关系Fig.6 Relationship among laboratory parameters,factors and the levels
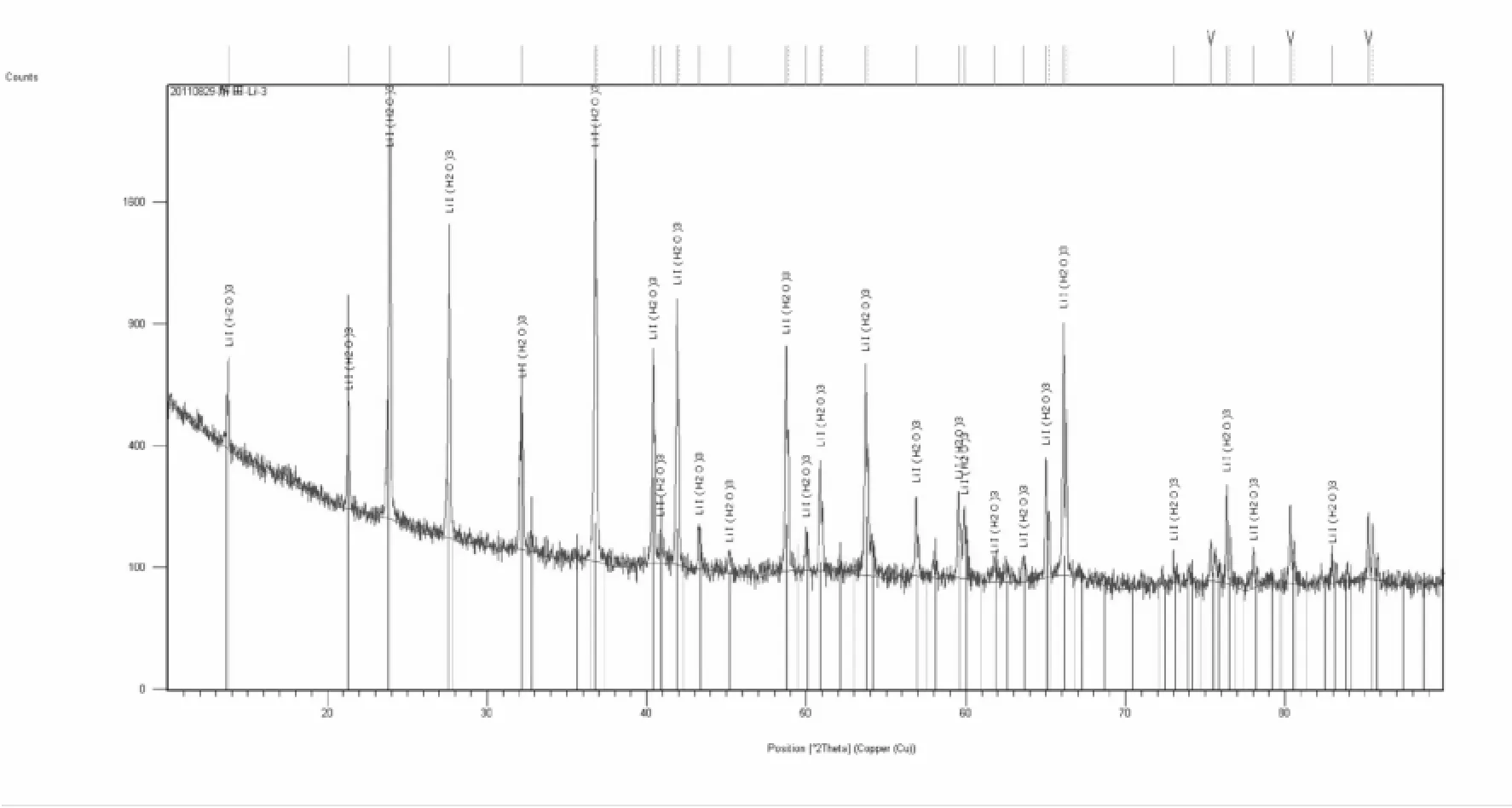
图7 三水碘化锂的 XRD谱图Fig.7 XRD pattern of lithium iodide trihydrate
4 结论
1)该方法制备三水碘化锂的最佳工艺条件为:反应温度45℃,n(碳酸锂)/n(碘离子)=1.2 ∶1,反应时间1 h,搅拌速度200 r/min。在最优条件下制备的产品纯度为98.1%。
2)该方法对产品纯度有影响的主次因素顺序为:反应温度>物料配比 >反应时间 >搅拌速度。
3)利用XRD对产品进行表征,证实产品是三水碘化锂。
[1]赵志刚,任光明.高纯碘化锂的制备[J].沂州师范专科学校学报,2000,16(2):64-65.
[2]魏太保,张有明.碘化锂在有机合成中的应用[J].西北师范大学学报:自然科学版,1996,32(1):106 -112.
[3]中国科学院近代物理研究所.碘化锂(铕)晶体的制备[J].原子能科学技术,1966,(3):165-167.
Study on Preparation of Lithium Iodide Trihydrate
GUO Ju
(Wengfu(Group)Co.,Ltd,Fuquan 550500,China)
This paper introduced the production process using an iodine solution for preparation of lithium iodide trihydrate,the effects of reaction conditions on the purity of the lithium iodide trihydrate was studied.The results showed that the control of reaction temperature as 45℃,the material ratio as 1.2:1,reaction time as 1h,stirring speed as 200r/min,the purity of the product can be reached 98.1%.
lithium iodide trihydrate;iodine;phosphatehosphate
TQ124.6
A
1004-275X(2015)04-0012-04
12.3969/j.issn.1004-275X.2015.04.004
收稿:2015-04-27
郭举(1983-),男,湖北潜江人,工程师,硕士研究生学历,主要从事磷化工研究工作。
