大鼠灌胃清热养心颗粒后血浆中咖啡酸、绿原酸药代动力学研究
2015-01-09磊陆超居文政
吴 磊陆 超居文政
(1.南京中医药大学附属医院,江苏南京210029;2.南京中医药大学,江苏南京210029)
大鼠灌胃清热养心颗粒后血浆中咖啡酸、绿原酸药代动力学研究
吴 磊1,2陆 超1居文政1
(1.南京中医药大学附属医院,江苏南京210029;2.南京中医药大学,江苏南京210029)
目的:建立大鼠灌胃清热养心颗粒后血浆中咖啡酸、绿原酸的UPLC-MS/MS测定方法,并用于其在大鼠体内的药代动力学研究。方法:SD大鼠6只,灌胃清热养心颗粒2g/kg,以阿魏酸为内标,用UPLC-MS/MS法测定给药后血浆中的药物浓度,并用DAS1.0软件计算药动学参数。结果:咖啡酸、绿原酸的线性范围分别为25~800ng/mL(r=0.9965)、11.25~1440ng/mL(r=0.9949)。方法学考察均符合要求。日内、日间变异系数(RSD)均小于9.8%,精密度和准确度等均符合生物样品分析的要求。大鼠体内咖啡酸药代动力学参数:T1/2β为(180.42±25.54)min,AUC0-t为(155397.53±3059.14)ng·min·mL-1,Cmax为(729.43±24.56)ng/mL;绿原酸药代动力学参数:T1/2β为(115.94±16.12)min,AUC0-t为(191710.99±7263.26)ng·min·mL-1,Cmax为(1110.32±115.33)ng/mL。结论:建立的UPLC-MS/MS分析方法准确灵敏,适于咖啡酸、绿原酸的药代动力学研究。
清热养心颗粒 绿原酸 咖啡酸 药代动力学 UPLC-MS/MS SD大鼠
清热养心颗粒是江苏省中医院的院内制剂,具有清热解毒、养心安神的功效。此方由金银花、黄连、酒黄精、百合、山豆根、甘草等组成,临床可用于治疗邪毒侵心型、心气虚弱型和气阴两虚型病毒性心肌炎[1-3]。酚酸类成分为清热养心颗粒中主要有效成分,现代药理研究表明,清热养心颗粒中咖啡酸、绿原酸等酚酸类成分有显著的抗炎、抗氧化、抗凝血等多种生物活性[4-6],且绿原酸也是该制剂的指标性成分[7]。但有关清热养心颗粒有效成分药代特性方面的研究还未见报道。为深入了解清热养心颗粒药代动力学行为,本研究建立了清热养心颗粒中酚酸类成分绿原酸和咖啡酸血药浓度检测方法,方法稳定、可靠,成功应用于药代动力学研究,现报道如下。
1 实验材料
1.1 试药 清热养心颗粒 (江苏省中医院医院制剂,批号:201203001、201207002、201307001);对照品咖啡酸(批号:110885-200102)、绿原酸(批号: 110753-200413)和阿魏酸(批号:110773-201313)均购于中国药品生物制品检定所。水为超纯水,甲酸、甲醇、乙腈为色谱纯,其他试剂均为分析纯。
1.2 仪器 Agilent 1290超高效液相色谱仪;Agilent G6430 LC-MS三重四级杆质谱仪,配有电喷雾化离子源(ESI);色谱工作站:MassHunter;AE240电子天平 (上海梅特勒-托利多有限公司);MICRO-17R冷冻离心机(美国Thermo公司);WH-2微型旋涡混合仪 (上海沪西分析仪器厂);Drict-Q5超纯水机(法国Millipore公司)。
1.3 动物 SD大鼠,雌雄各半,6只,体质量250~270g,由南京中医药大学实验动物中心提供,合格证号:SCXK(浙)2008-0033。
2 实验方法
2.1 色谱及质谱检测条件 Agilent ZOBAX SB C18色谱柱 (2.1mm×150mm,5μm);流动相:甲醇(2mmol/L)-醋酸铵水溶液(80∶20);流速:200μL/min;柱温:35℃。离子源:ESI;离子化模式:负离子;定量模式:多反应检测模式(MRM);毛细管电压:3500V;干燥气温度:400℃;绿原酸的Fragmentor及CE值分别为90V、10V;咖啡酸的Fragmentor及CE值分别为90V、10V;阿魏酸的 Fragmentor及 CE值分别为80V、10V;检测对象:绿原酸m/z 353→m/z 191;咖啡酸m/z 179→m/z 135;阿魏酸m/z 193.1→m/z 134.0。2.2 对照品溶液的配制 精密称取适量绿原酸对照品,用甲醇定容,配制成浓度为1.40mg/mL的储备液;精密吸取适量,用甲醇分别稀释成112.5、450、900、3600、14400ng/mL的系列标准溶液。精密称取适量咖啡酸对照品,用甲醇配制成浓度为1.60mg/mL的储备液;精密吸取适量,用甲醇分别稀释成250、500、2000、4000、8000ng/mL的系列标准溶液。以上溶液于4℃保存,备用。
2.3 内标物溶液的配制 精密称取适量阿魏酸对照品,用甲醇定容并稀释成550ng/mL,于4℃保存,备用。
2.4 血浆样品处理 取血浆样品100μL,加入550ng/mL阿魏酸溶液(内标)20μL,1mol/L盐酸溶液50μL,涡旋30s,再加入乙酸乙酯800μL,涡旋振摇3min,12000r/min离心5min。取上清液750μL,40℃氮气流吹干,加100μL50%甲醇复溶,12000r/min离心5min,取上清液2μL进样分析。
2.5 给药剂量的确定 清热养心颗粒临床给药剂量为每次10~20g,2次/d。人的平均体重按60kg计算,则其临床给药剂量为0.33~0.67g/kg。按大鼠每千克体重的临床等效量是人的6倍计算,则清热养心颗粒大鼠灌胃剂量为2~4g/kg,经预实验,确定大鼠给药剂量为2g/kg。
2.6 药代动力学研究 SD大鼠6只,给药前12h禁食不禁水,分别口服清热养心颗粒2g/kg。于给药前及给药后 10min、20min、30min、1h、1.5h、2h、3h、4h、6h、8h、10h和 12h经眼眶后静脉丛取血约0.3mL,置于肝素化试管中,以 4000r/min离心10min,取上层血浆于-40℃保存待测。
2.7 数据处理 大鼠静脉给药后测得的血药浓度(C)-时间(T)数据应用DAS 1.0软件进行处理。选择适宜的数学模型拟合,计算药代动力学参数。
3 实验结果
3.1 专属性实验 在本实验所采用的UPLC-MS/ MS条件下,咖啡酸、绿原酸和阿魏酸的保留时间分别为1.14min、1.06min、1.16min。咖啡酸、绿原酸和内标互不干扰,峰形良好,无杂峰干扰,基线平稳,见图1。
3.2 标准曲线制备 取空白血浆100μL,分别加入绿原酸、咖啡酸对照品系列标准溶液各10μL,配制成相当于绿原酸及咖啡酸血浆质量浓度分别为11.25、45、90、360、1440ng/mL和25、50、200、400、800ng/mL的血浆样品。按“血浆样品处理”项下操作,取2μL进样分析。以各成分峰面积与内标峰面积的比值Y对血浆质量浓度X进行线性回归运算,求得的回归方程即为标准曲线。绿原酸回归方程: Y=2.3419X+0.0442(r=0.9949),定量下限为10.9ng/mL。咖啡酸回归方程:Y=4.5936X+0.3382(r=0.9965),定量下限为25ng/mL。
3.3 准确度和精密度 取空白血浆100μL,按“血浆样品处理”项下制备绿原酸和咖啡酸低、中、高3个浓度(绿原酸血浆质量浓度为45、90、360ng/mL;咖啡酸血浆质量浓度为50、200、400ng/mL)的质量控制(QC)样品,每个浓度平行做5份,连续测定3d。根据随性标准曲线求得实测浓度。实测浓度的RSD即为精密度,加入浓度和实测浓度的比值即为准确度。结果表明,绿原酸日内、日间准确度分别为95.2%~103.7%(RSD≤7.4%,n= 5)和92.5%~105.7%(RSD≤9.4%,n=15);咖啡酸日内、日间准确度分别为94.5%~107.2%(RSD≤7.9%,n=5)和98.2%~108.1%(RSD≤9.8%,n=15)。实验结果符合生物样品分析方法的要求。
3.4 提取回收率 取空白血浆100μL,配制“准确度和精密度”项下低、中、高3个不同浓度含药血浆质控样品,按上述“血浆样品处理”项下操作后进样分析,以血浆中绿原酸、咖啡酸的峰面积与相应质量浓度对照品溶液中绿原酸、咖啡酸峰面积的比值计算出上述3种质量浓度的提取回收率,每个浓度平行做5份。经UPLC-MS/MS测定后,低、中、高3种浓度下的提取回收率分别为:绿原酸,(86.1± 3.9)%、(87.2±5.2)%和 (90.8±8.4)%;咖啡酸,(84.4±4.4)%、(87.9±5.0)%和(85.6±5.3)%。采用同样的方法考察了内标的提取回收率为 (84.3± 4.6)%。
3.5 稳定性考察 取空白血浆100μL,配制“准确度和精密度”项下低、中、高3个不同浓度含药血浆质控样品,按“血浆样品处理”项下操作方法处理样品。考察含药血浆样品处理好后溶液中分析物在室温放置24h、含药血浆样品-20℃反复冻融3次、含药血浆样品-40℃长期冷冻28d的稳定性,每个浓度平行3份。结果表明,经处理后的血浆样品室温放置24h后绿原酸及咖啡酸血药浓度的RSD均小于9.7%,-40℃保存 28d血药浓度的 RSD均小于10.9%,经过3个冻融周期后两个分析物的血药浓度RSD均小于8.7%。

图1 样品的液-质联用离子流图(A.空白血浆样品;B.混合对照品;C.血浆样品;1.绿原酸;2.阿魏酸;3.咖啡酸)
3.6 介质效应考察 取离心管数只,分别精密加入低、中、高3个浓度绿原酸对照品标准溶液(450,900,3600ng/mL)及咖啡酸对照品标准溶液(500,2000,4000ng/mL)各10μL,再分别加入内标替硝唑溶液20μL,水60μL,旋涡1min,于12000r/min离心5min,进行UPLC-MS/MS分析,进样量2μL,记录峰面积A1。除不加内标外,另按“血浆样品处理”项下操作提取空白血浆数管,挥干后同上操作,记录峰面积A2。A1和A2的比值(A2/A1×100%)即为介质效应ME(%)。绿原酸及咖啡酸血浆样品低、中、高3种浓度LC-MS/MS介质效应 (n=3)分别为88.43% 、83.93% 、90.76% 和 91.36% 、93.22% 、89.46%,内标阿魏酸介质效应(n=9)为84.17%。
3.7 大鼠体内药代动力学 大鼠单剂量(2g/kg)灌胃清热养心颗粒后绿原酸和咖啡酸的血药浓度-时间曲线见图2。所测数据使用DAS 1.0软件进行处理,主要药动学参数见表1。由结果分析可知,绿原酸和咖啡酸在大鼠体内的药动学符合二室开放模型。
表1 大鼠灌胃清热养心颗粒后咖啡酸和绿原酸的药动学参数(±s,n=6)
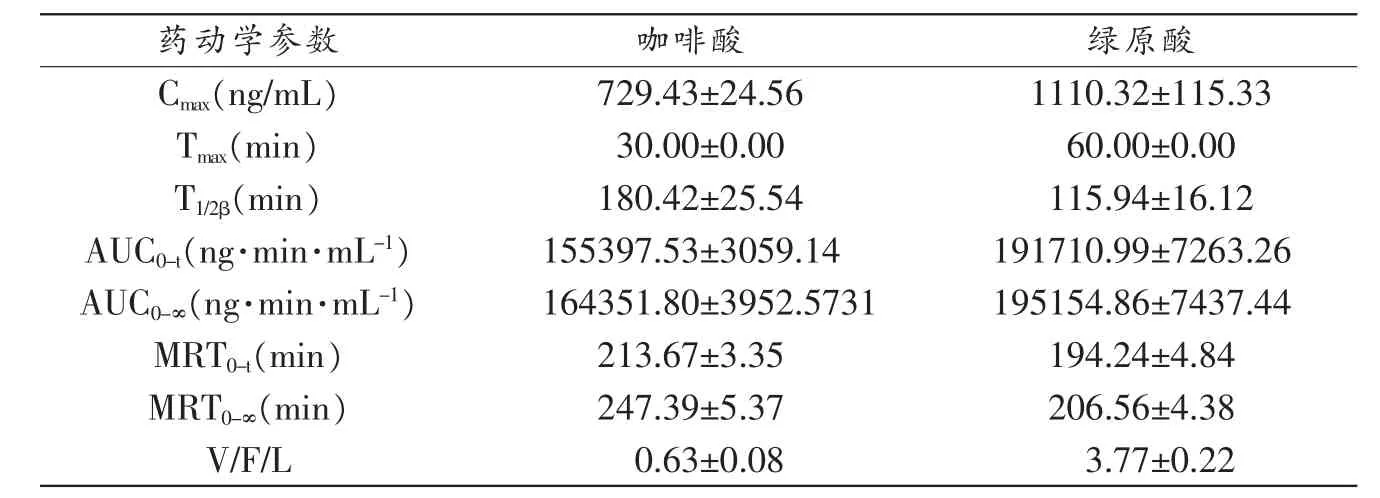
表1 大鼠灌胃清热养心颗粒后咖啡酸和绿原酸的药动学参数(±s,n=6)
药动学参数 咖啡酸 绿原酸Cmax(ng/mL)729.43±24.561110.32±115.33 Tmax(min) 30.00±0.00 60.00±0.00 T1/2β(min) 180.42±25.54 115.94±16.12 AUC0-t(ng·min·mL-1) 155397.53±3059.14 191710.99±7263.26 AUC0-∞(ng·min·mL-1) 164351.80±3952.5731 195154.86±7437.44 MRT0-t(min) 213.67±3.35 194.24±4.84 MRT0-∞(min) 247.39±5.37 206.56±4.38 V/F/L 0.63±0.08 3.77±0.22
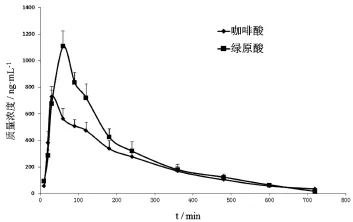
图2 大鼠体内绿原酸和咖啡酸的平均血药浓度-时间曲线(n=6)
4 讨论
4.1 本文对血样中酚酸类成分的提取方法进行了考察:甲醇沉淀、乙腈沉淀、乙酸乙酯提取、乙酸乙酯/乙醚(3∶1)提取,每个提取或沉淀条件考察了不同的酸化条件 (加不同量的 1mol/L盐酸:10、20、30、50、100μL),结果发现50μL,1mol/L盐酸酸化后乙酸乙酯的提取回收率高,无内源性物质干扰,重现性好。
4.2 在绿原酸和咖啡酸的测定及药代动力学研究中,目前文献多数使用HPLC和LC-MS/MS方法[8-12],但分析时间多数在5~20min之间。本实验建立大鼠血浆中咖啡酸、绿原酸的UPLC-MS/MS测定方法,并用于其在大鼠体内的药代动力学研究,分析时间为2min。实验表明所建立的方法迅速、准确、稳定、可靠。通过药代动力学研究,获得主要成分比较全面的药代动力学参数,为临床药代动力学研究提供了参考。
[1] 王昃睿,王晓东,刘中华,等.清心解毒汤治疗邪毒侵心型病毒性心肌炎.吉林中医药,2014,34(8):789
[2] 皇甫海全,于海睿,张文钊,等.养心汤临床应用研究进展.辽宁中医药大学学报,2014,16(7):129
[3] 张秀华.病毒性心肌炎的临床治疗效果分析.中国医药指南,2014,12(18):219
[4] Park W H,Kim S H,Kim C H.A new matrix metalloproteinase-9 inhibitor 3,4-dihydroxycinnamic acid(caffeic acid) from methanol extract of Euonymus alatus:isolation and structure determina-tion. Toxicology,2005,207(3):383
[5] Jang D S,Yoo N H,Kim N H,et al.3,5-Di-O-caffeoyl-epiquinic acid from the leaves and stems of Erigeron annuus inhibits protein glycation,aldose reductase,and cataractogenesis.Biol Pharm Bull,2010,33(2):329
[6] 张鞍灵,马琼,高锦明,等.绿原酸及其类似物与生物活性.中草药,2001,32(2):173
[7] 邹小娟,刘志辉,钱芳.清热养心颗粒的鉴别及其绿原酸含量测定.中国医药导报,2008,10(6):908
[8] 李淼,王永香,孟谨,等.HPLC法测定金银花中新绿原酸等8种成分的量.中草药,2014,45(7):1006
[9] 陈芳,邓雁如,郭利平.HPLC法同时测定金银花及金芪降糖片中9种成分的含量.天津中医药,2014,31(3):168
[10] 谢丽艳,徐洁,戴国梁,等.HPLC同时测定消癌平注射液中7种主要成分的含量.中国实验方剂学杂志,2013,19(21):86
[11] 陈婷,唐跃年,胡燕锋.HPLC法同时测定金银花中4种主要成分的含量.中国药师,2012,15(12):1721
[12] 班丽娜,徐远金.HPLC/MS同时测定双黄连口服液中的4种有效成分.中成药,2012,34(2):265
编辑:吴 宁
R289.5
A
1672-397X(2015)05-0074-03
吴磊(1983—),男,硕士,主管中药师,研究方向:中药临床药代动力学。
居文政,主任中药师,博士,博士生导师。wzhju333@163.com
2015-02-07
