Cocktail法评价清热养心颗粒对大鼠体内P450酶活性的影响研究
2015-01-02戴国梁
吴 磊, 陆 超, 戴国梁, 王 珂
(1.南京中医药大学附属医院;2.南京中医药大学,江苏 南京 210029;3.徐州市中心医院,江苏 徐州 221009)
细胞色素P450酶(CYP450)是机体内最重要的代谢酶系统,可催化多种内源性、外源性化合物的氧化反应,在药物和致癌物代谢活化过程中具有非常重要的作用.有些药物经CYP450酶系代谢后,转化为活性代谢物,药效增强;有些药物经CYP450代谢后,药效降低或消失[1,2].肝脏是药物代谢的主要场所,因此,评价外源物对肝脏药物代谢酶的诱导或抑制作用尤为重要[3,4],已有大量实验报道化学合成药物诱导或抑制CYP450酶活性,而有关中药对CYP450影响的报道并不多见[5].
清热养心颗粒由金银花、黄连、酒黄精、百合、山豆根和甘草组方而成,全方具有清热解毒,养心安神之功效,是新型的治疗病毒性心肌炎药物[6].临床广泛用于治疗热毒侵心、气阴两伤、心神失宁的病毒性心肌炎以及合并心律失常、心悸胸闷等.
本实验采用"Cocktail"探针药物法,通过考察清热养心颗粒对大鼠体内CYP450酶5种亚型(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1)的影响,提示与相关药物存在相互作用的可能性,指导那些有多重代谢途径的药物的剂量设计,降低和避免临床联合用药时由于相互作用引起的不良反应发生.
1 材料
1.1 药品与试剂
清热养心颗粒(江苏省中医院制剂,批号1307001,规格:10g/袋),注射用奥美拉唑钠(江苏奥赛康药业股份有限公司委托杭州澳亚生物技术有限公司生产,批号14010126,规格:含奥美拉唑40mg/支),甲苯磺丁脲(Tolbutamide)对照品(Sigma,017K1025),氯唑沙宗(chlorzoxazone)对照品(Sigma,017K1385),茶碱 (theophylline)对照品(Sigma,T1633),奥美拉唑(omeprazole)对照品(中国药品生物制品检定所,批号:100367-201104),右美沙芬(dextromethorphan)对照品(Sigma,097K11348),内标吡罗昔康(中国药品生物制品检定所,批号:100177-200603),替硝唑(中国药品生物制品检定所,批号:100336-200402),甲醇、乙腈为色谱纯(Merck Company),二氯甲烷为分析纯,实验用水为超纯水.
1.2 仪器
Waters Quattro Micro液质联用仪(美国Waters公司),色谱工作站:Masslynx 4.0;Mettler AE240电子天平(梅特勒-托利多 (上海)有限公司);Micro-17R冷冻离心机 (美国 Thermo公司);Drict-Q5超纯水机 (法国Millipore公司);WH-2微型旋涡混合仪(上海沪西分析仪器厂);KQ3200型超声波清洗器(昆山市超声仪器有限公司).
1.3 动物
雄性 SD大鼠,12只,体重(240±40)g,由南京中医药大学实验动物中心提供,合格证号:SCXK(浙)2008-0033.
2 方法
2.1 溶液的配制
2.1.1 混合探针的配制
称取甲苯磺丁脲20mg,氯唑沙宗60mg,茶碱25mg,右美沙芬30mg,固体用0.5%CMC-Na研磨混匀后后,全部转移至10mL容量瓶中,注射用奥美拉唑钠粉针剂1支(40mg),用生理盐水定容.混合探针临用前配制,现配现用.
2.1.2 混合标准溶液及质控溶液的配制
精密称取甲苯磺丁脲、氯唑沙宗、茶碱、奥美拉唑、右美沙芬各对照品适量,分别溶于10mL容量瓶中,加甲醇稀释至刻度,摇匀,即得各对照品储备液,备用.另精密移取各储备液适量于同一10mL容量瓶中,甲醇定容至刻度,摇匀,即得浓度分别为76.8、112.64、28.672、2.048、1.536μg·mL-1的 混 合对照品储备溶液.取该混合对照品储备溶液适量,倍比稀释成系列不同浓度的混合标准溶液,冷藏于-4℃备用.
吸取上述甲苯磺丁脲、氯唑沙宗、茶碱、奥美拉唑、右美沙芬混合标准溶液适量,得质控高浓度混合标液,浓度分别为 38.4、56.32、14.336、1.024、0.768μg·mL-1;质控中浓度标液,浓度分别为 4.8、7.04、1.792、0.128、0.096μg·mL-1;质控中浓度标液,浓度分别为 0.3、0.44、0.112、0.008、0.006μg·mL-1,所有标液冷藏于-4℃备用.
2.1.3 混合内标的配制
精密称取替硝唑和吡罗昔康各对照品适量,分别溶于10mL容量瓶中,甲醇定容,摇匀,得各对照品储备液.另精密移取各储备液适量于同一10mL容量瓶中,甲醇定容至刻度,摇匀,使得替硝唑和吡罗昔康的终浓度分别为1.2、10.6μg·mL-1.冷藏于-4℃冰箱备用.
2.2 色谱条件
色谱柱:Agilent Zorbax SB C18(2.1×150mm,5μm)(美国Agilent公司);保护柱:Agilent EclipaseXDB2C8(2.1mm×12.5mm,5μm);流动相:乙腈(A):0.1%甲酸 -4mmol/L甲酸铵(B)=75:25;流速 0.2mL·min-1;进样量:5μL;柱温:23℃.
2.3 质谱检测条件
离子化方式为电喷雾 (ESI);多反应监测(MRM);正负离子同时检测.检测电压:3.5kV;离子源温度:120℃;脱溶剂温度:350℃;脱溶剂气体流速:500L·h-1.各成分的检测离子,质核比,锥孔电压及碰撞气能量见表1.

表1 5种探针药物及内标质谱参数
2.4 动物给药方法
12只大鼠随机平均分为两组,即实验组和对照组,实验组每天上午灌胃清热养心颗粒4g·kg-1,连续给药10天,对照组正常饲养.第10天晚上,大鼠禁食不禁水,于第11天早晨两组大鼠均灌胃给予混合探针药物10mL·kg-1,于给药前和给药后5、10、20、40min和 1、1.5、2、2.5、3、5、8、12、24h从 眼底静脉丛采血约0.4mL,置肝素抗凝试管.全血4000r·min-1离心10min后,吸取上层血浆于-20℃保存待用.整个实验过程尽量避光.
2.5 大鼠血浆样品处理
精密吸取血浆样品100μL,加入1.3.3项下配制的混合内标20μl,漩涡30s混匀,加入800μL二氯甲烷,漩涡3min,于4℃,12000r·min-1离心10min,吸取下层有机层 700μl,N2气吹干,用 75%乙腈 100μL复溶,12000r·min-1离心 5min,吸取5μL进样分析.
2.6 数据处理
药动学参数采用DAS1.0软件计算,给药前后各探针药动学参数的差异用SPSS 11.5统计,以配对t检验进行分析,P<0.05表示差异有统计学意义.
3 结果
3.1 色谱行为
本色谱条件下,甲苯磺丁脲、氯唑沙宗、茶碱、奥美拉唑、右美沙芬和内标替硝唑、吡罗昔康的保留 时 间 分 别 在 2.53、2.42、2.04、2.31、3.26、2.08、2.64min.5种探针药物与2种内标分离良好,互不干扰且血浆中内源性杂质不影响分析物的测定,基线平稳(见图1).本方法具有良好的特异性和分离度能准确测定血浆中各探针药物的浓度,重现性好.
3.2 标准曲线
取空白血浆100μL,加入2.1.2项下配制的不同浓度的混合标液10μL,再加入2.1.3项下混合内标20μL,按“2.5大鼠血浆样品处理方法”处理.分别计算各成分的峰面积(Ai)与相应内标的峰面积(As)的比值Y,以比值Y对探针药物的进样质量浓度进行线性回归,得回归方程.见表2.
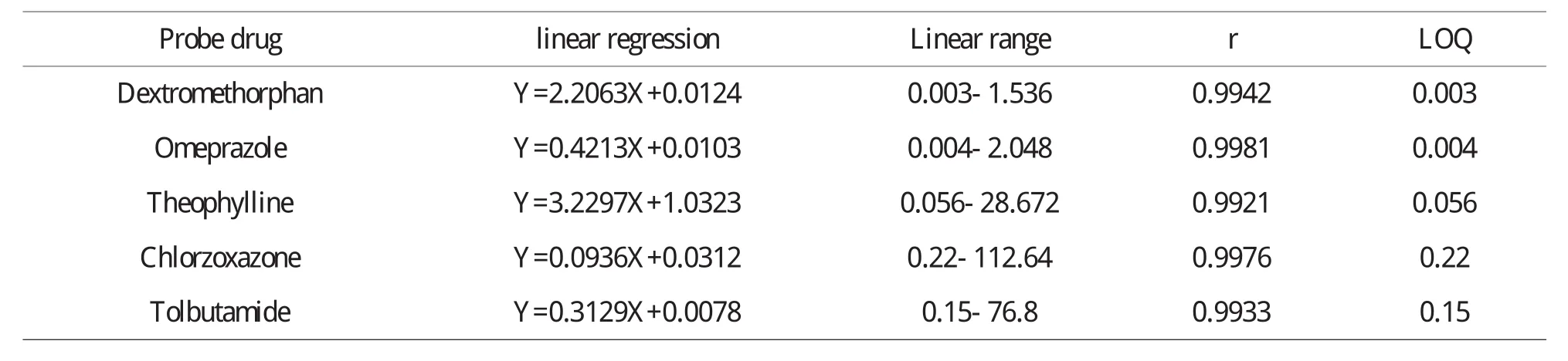
表2 5种探针药物的线性关系及灵敏度考察(μg·mL-1,n=5)

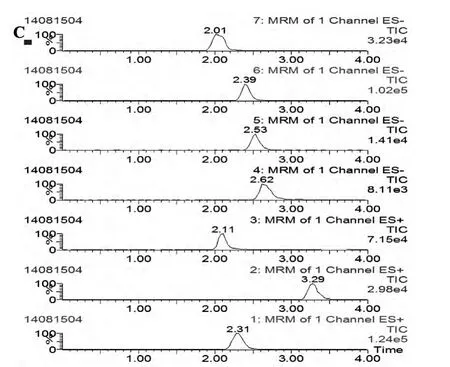
图1 各分析物及内标的LC-MS/MS图谱
3.3 精密度
考察日内精密度与日间精密度.取大鼠血浆100μL,分别加入10μL高、中、低质控标液,每个浓度平行5份,按“2.5血浆样品处理”方法处理样品,取5μL进样分析,根据随行标准曲线计算各分析物检测值,日内重复测定5次,平行测定3天.结果表明其日内和日间精密度均小于10%,准确度均在90%~115%之间.
3.4 提取回收率
按取大鼠血浆100μL,同上配制高、中、低3个不同浓度含药血浆质控样品,按“2.5血浆样品处理方法”处理样品,记录分析物峰面积Ax.另以流动相配制相同进样浓度的含药溶液,记录分析物峰面积As.提取回收率计算公式如下:R(%)=Ax/As×8/7×100%,各成分提取回收率(Recoveries)结果见表3.
3.5 介质效应
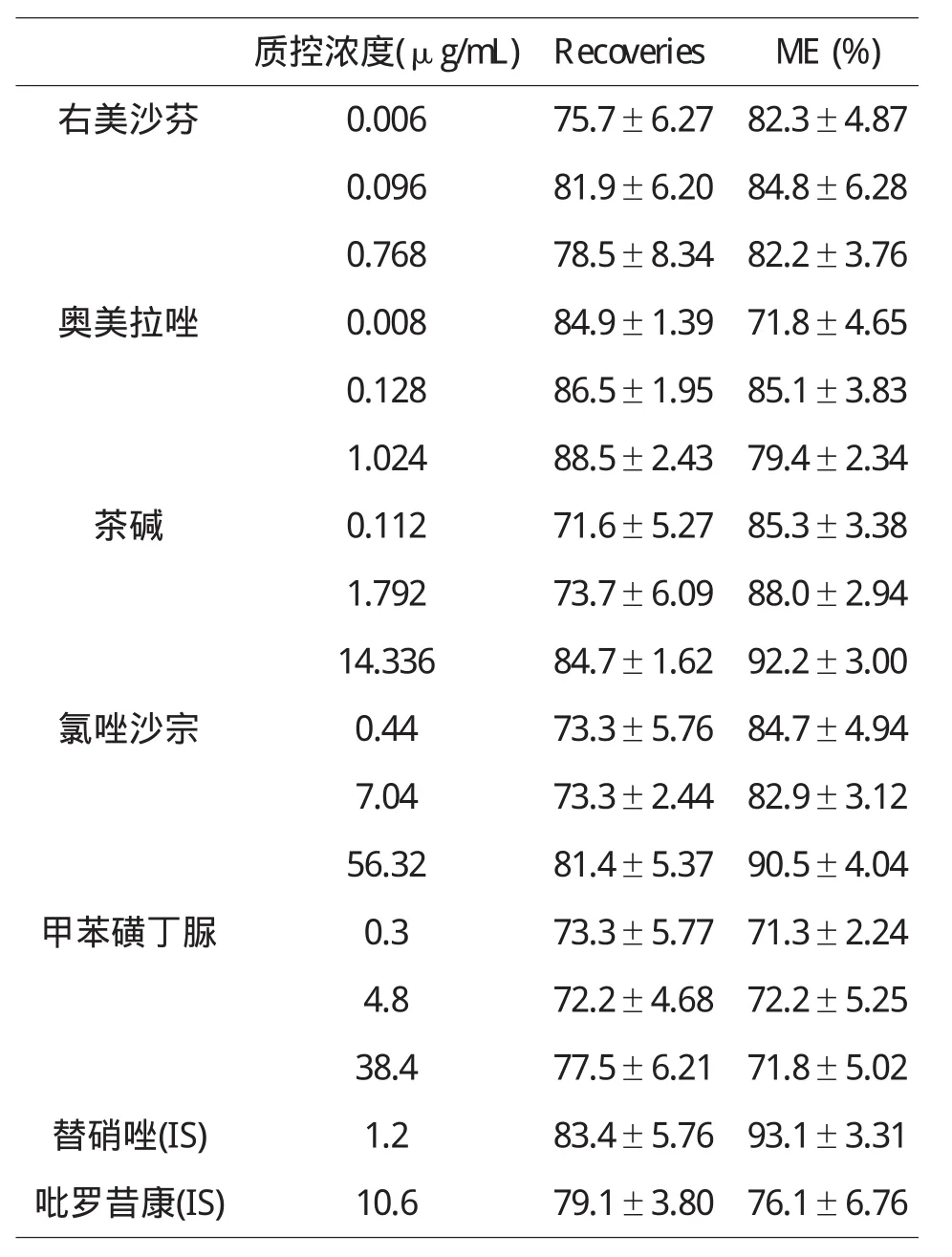
表3 各检测成分的提取回收率及介质效应(n=3)
取空白血浆加入800μL二氯甲烷,旋涡振荡3min,4℃,12000r/min离心10min,吸取下层有机层700μL,N2气吹干,分别精密加入3个浓度混合质控标液混合标液10μL,再加入2.1.3项下混合内标20μL,N2气吹干,用75%乙腈100μL复溶,12000r/min离心5min,吸取5μL进样分析,计算介质效应ME(%).介质效应结果见表3.
3.6 样品稳定性考察
考察5种探针药物标品及含药血浆在不同保存条件下的稳定性.标准品的甲醇溶液可在4℃冰箱保存2个月以上.含药血浆样品在-40℃冰箱内冷冻保存一个月样品稳定.血浆样品在室温(避光保存)12h内稳定.血浆样品反复冻融3次后测定,实验结果稳定.
3.7 药动学参数
3.7.1 5种探针药物的药-时曲线
实验组和对照组大鼠分别灌胃混合探针药物,按1.5项方法操作,测得5种探针药物的血药浓度,结果见图2.

图2 5种探针药物给药前后的药-时曲线
3.7.2 6种探针药物的药动学参数
各种成分的药代动力学数据经中国药理学会推荐的DAS1.0程序处理,分别按单室、二室、三室模型以最小二乘法拟合,结果表明甲苯磺丁脲符合一室模型(W=1/CC),其他均符合二室模型(W=1/CC),5种探针药物的生物半衰期(T1/2)、表观分布容积(Vd/F)、机体总清除率(CL/F)、达峰时间(Tmax)、最大血药浓度(Cmax)、药时曲线下面积(AUC)见表4.
表4 5种探针药物在大鼠体内的药动学参数(±S,n=6)

表4 5种探针药物在大鼠体内的药动学参数(±S,n=6)
探针 参数 给药前 给药后甲苯磺丁脲 T1/2(h) 5.38±1.21 4.26±0.87 Vd/F(L·kg-1)0.009±0.001 0.007±0.002 Tmax(h) 3.21±0.92 2.82±1.02 Cmax(mg·L-1) 31.61±2.35 27.12±12.a AUC0-t(mg·L-1·h)429.11±41.72 330.67±44.32a AUC0-∞(mg?L-1·h)471.48±42.56 347.30±46.45a氯唑沙宗 T1/2(h) 2.37±0.76 2.04±0.63 Vd/F(L·kg-1) 4.27±1.23 5.41±1.92 CL/F(L·h-1·kg-1)1.49±0.38 2.05±0.74 Tmax(h) 0.67 0.67 Cmax(mg·L-1) 17.93±1.32 12.19±2.03a AUC0-t(mg·L-1·h)45.91±9.81 32.46±10.23 AUC0-∞(mg·L-1·h)46.93±10.76 33.49±11.51
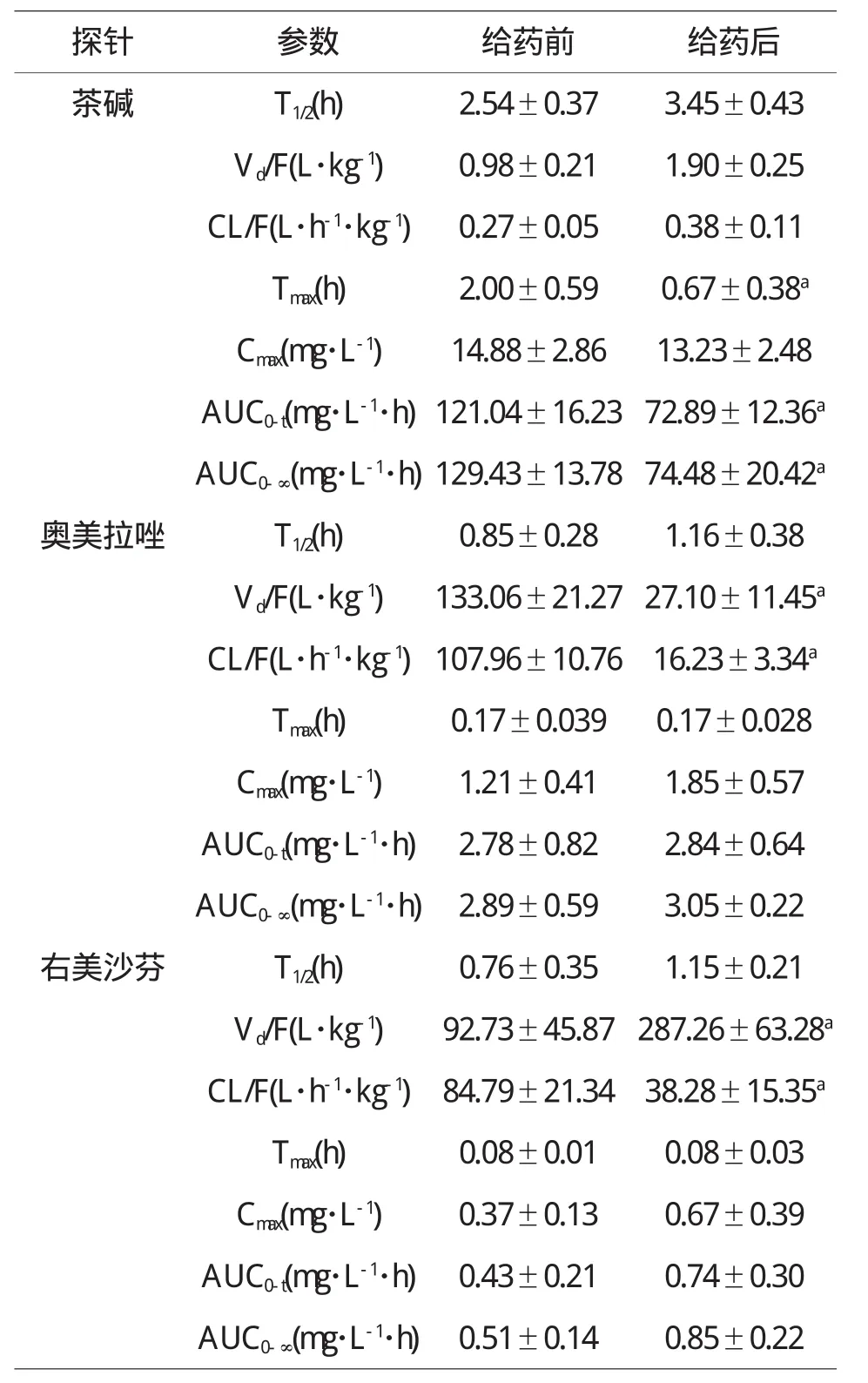
与给药前比aP<0.05
4 讨论
本实验采用“Cocktail”法考察清热养心颗粒对大鼠体内CYP450酶5种亚型的影响,“Cocktail”方法的建立首先应排除同时使用的各种探针底物在体内的代谢性相互作用,保持其作用的专属性;另外为有效评估各种探针底物在给药前后的药动学参数变化,必须保证每种探针底物有选择地作用于一种酶,且具有高度敏感性[7-9].在本实验采用自身对照的方法,将试验用动物个体间的遗传代谢性差异降到最低,同时参考文献[7,10-11]并验证排除了5种探针药物(甲苯磺丁脲、氯唑沙宗、茶碱、奥美拉唑、右美沙芬)在体内存在潜在代谢性相互作用的可能性,实验设计基本符合“Cocktail”法的条件,因此可以同时给予此5种探针底物以评估艾迪注射液对大鼠体内P450酶活性的影响.
由表4可以看出,连续给予清热养心颗粒10天后,氯唑沙宗、奥美拉唑和右美沙芬的药动学行为无显著性变化,提示清热养心颗粒对大鼠CYP2E1、CYP2C19及CYP2D6活性基本无影响;而清热养心颗粒能使甲苯磺丁脲和茶碱的AUC显著降低(P<0.05),分别降低至给药前的0.77和0.60倍,提示艾迪注射液能诱导大鼠CYP2C9和CYP1A2酶的活性.
因此在临床上使用清热养心颗粒的同时,合并使用经CYP2C9和CYP1A2代谢的药物,应充分考虑两者合并用药的给药剂量对合用药物代谢的影响,必要时应注意调整合用药物的给药剂量,为临床合理用药提供依据,确保临床疗效,同时将可能出现的不良代谢性药物相互作用降到最低程度.
〔1〕施畅,吴纯启,马华智,廖明阳.复方丹参滴丸对大鼠肝CYP450酶系诱导作用的研究[J].解放军药学学报,2003,19(5):344-346.
〔2〕张沂,鲍燕燕,王洪武,王大鹏.左旋氧氟沙星对大鼠肝重、肝微粒体蛋白质及细胞色素P450的影响[J].海军总医院学报,2004,17(1):6-8.
〔3〕李文东,马辰.药物体外肝代谢研究进展[J].中国药学杂志,2003,38(10):737-740.
〔4〕王佳,代百东.药物体外肝代谢研究方法[J].亚太传统医药,2008,4(3):48-49.
〔5〕张锦楠,李亚伟,徐艳霞,等.大鼠肝微粒体 CYP 450诱导作用的研究 [J].中国药学杂志,2002(37):424.
〔6〕邹小娟,刘志辉,钱芳.清热养心颗粒的鉴别及其绿原酸含量测定 [J].中国医药导报,2008,10(6):908-10.
〔7〕Zhu B,Ou-Yang DS,Chen XP,et al.Assessment of cytochrome P450 activity by a fivedrug cocktail approach[J].Clin Pharmacol Ther 2001,70:455-461.
〔8〕Paolini M,Biagi GL.Cocktail strategy.com lications and lim itations.J Clin Pharmacol 1993,33:1011-2.
〔9〕Brockmoller J,Roots I.Assensement of liver metabolic function:clinical implications[J].Clin Pharmacokinet,1994,27(3):216-248.
〔10〕刘史佳,刘子修,周玲,等.雷公藤活性成分对大鼠体内P450酶活性的影响[J].中国药理学通报,2011,27(2):276-280.
〔11〕王丹,刘萍霞,张振清,等.L C-MS/MS 同时测定6种CYP450探针药物及快速评价小鼠CYP450同工酶活性[J].军事医学科学院院刊,2008,32(6):545-549.
