胃癌患者新辅助化疗后术前营养状态的评估
2014-12-02章左艳
李 梅,章左艳
(上海交通大学附属第六人民医院,上海 200233)
胃癌是我国最常见的恶性肿瘤之一,进展期胃癌营养不良的发生率在70% ~80%[1]。研究发现,营养不良可能增加胃癌术后并发症[2-3]。近年来,新辅助化疗或称为术前化疗因其能够增加进展期胃癌的根治切除率而逐渐成为研究的热点[4-5]。但新辅助化疗所产生的毒副作用,例如呕吐、腹泻及纳差等消化道症状可能加重患者原有的营养不良,从而为后续手术及术后恢复带来不利的影响[6]。欧洲营养学会指出,营养支持不能延误患者获得根治切除的时间窗。因此,对于新辅助化疗的胃癌患者,既要通过适当的营养支持来降低围手术期的风险,又不能做过于漫长的营养支持而使患者失去最好的根治切除机会。解决这一矛盾的首要办法是如何快速便捷的了解患者的营养状况,即营养评估[7]。我们用营养风险筛查方法NRS2002来评估我院普外科2011年2月—2012年12月收治的接受新辅助治疗的进展期胃癌患者的营养状况。
1 对象与方法
1.1 对象 选择我院普外科2011年2月—2012年12月新入院的已接受新辅助治疗的患者63例,男40例,占63.49%,女23 例,占36.51%;年龄28 ~76 岁,平均年龄36.1岁。63例患者均经胃镜病理确诊为进展期胃癌,采用多烯紫杉醇(TAT)联合5-氟尿嘧啶(5-Fu)及顺铂(DDP)方案行新辅助化疗:TAT 75 mg/m2第1天;5-Fu 600 mg/m2第1 ~5天;DDP 25 mg/m2第1 ~3天,均静脉滴注,21 d为1个周期,一般进行3个周期化疗。化疗后4~6周行手术治疗。
1.2.1 评估内容 采用TCS-200-RT型电子体重身高计测定患者身高体重,计算出患者的体重指数 (body mass index,BMI)=体重(kg)/身高(m)2。咨询表格记录患者近3个月体重变化,1周的饮食变化,疾病与营养状态等。同时收集患者入院时的实验室指标:血常规,白蛋白、前白蛋白、血红蛋白、白细胞及淋巴细胞计数。
1.2.2 营养状况评估 应用欧洲肠外肠内营养学会于2002年推荐的营养风险筛查方法NRS2002对入选的患者进行营养状况评估,NRS2002包括:①原发疾病对营养状态影响的严重程度;②近3个月体重的变化;③近1周饮食摄入量的变化;④BMI指数;⑤70岁以上判定营养风险程度为1分。将评分≥3,作为评定存在营养风险的指标,<3分表示不存在营养风险。
1.2.3 营养支持 正常饮食外联合肠内营养支持,制剂为整蛋白型肠内营养粉剂(安素),2~4次/d,总能量供给为500 kcal/d。不能正常饮食予以经鼻胃管肠内营养支持,总能量供给大于1 500 kcal/d。
1.3 统计学方法 采用SPSS 19.0软件,计数资料采用卡方检验,计量资料采用t检验。
2 结果
2.1 营养评估情况 63例患者中,NRS≥3分23例占36.5%;NRS<3分40例,占63.5%。评分≥3者平均BMI为(21.29 ±3.31)kg/m2,评分 <3 者平均 BMI为(24.28 ±3.75)kg/m2,两者比较差异有统计学意义(P <0.05)。
2.2 不同NRS 2002评分实验室检查情况 见表1。
2.3 不同NRS 2002评分者前白蛋白情况 以前白蛋白为指标,前白蛋白<180 mg/L的患者中,NRS 2002≥3分者18例,NRS 2002<3分者4例;前白蛋白≥180 mg/L的患者中,NRS 2002≥3分者5例,NRS 2002<3分者36例。NRS 2002特异度为87.8%;灵敏度为81.8%;准确率为85.7%。

表1 不同NRS 2002评分实验室检查情况(n=63)
2.4 不同评分患者术后情况 见表2。
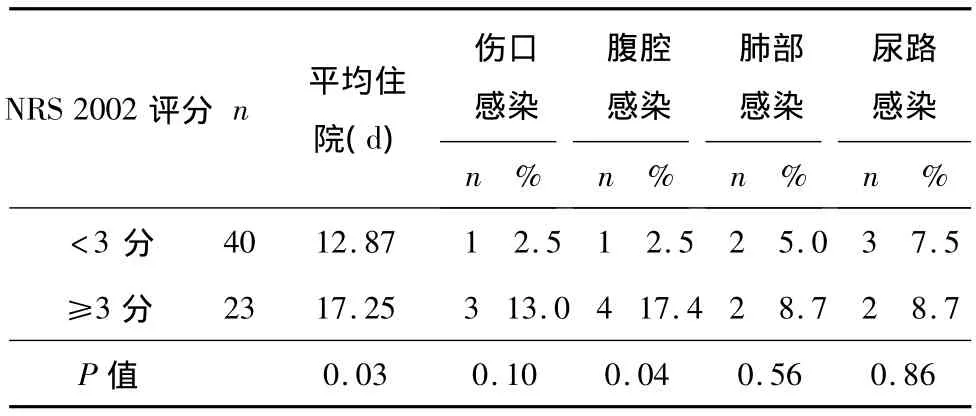
表2 不同评分患者术后情况 (n=63)
3 讨论
3.1 营养不良和营养风险 营养不良和营养风险是临床营养问题上常用术语,但二者有着不同定义。营养不良一般指蛋白质、热量或其他营养素缺乏或过量而导致的一种营养状态,住院患者的营养不良一般指蛋白质能量营养不良。营养风险是指现存的或潜在的营养和代谢状况影响疾病预后或手术后临床结局的风险。营养风险概念包含2层含义:①有营养风险的患者可能由于营养状况问题导致临床预后不佳。②对有营养风险的患者给予营养支持可能改善临床预后。营养风险的概念外延要大于营养不良。
3.2 胃癌患者新辅助化疗后营养风险 胃癌新辅助化疗能够有效控制病情发展,使患者获得根治性切除的机会,但是由于胃癌患者本身存在较高的营养不良发生率,营养不良的发生率可达70% ~80%,并且广泛存在免疫功能低下的情况[8]。加上化疗本身引起的消化道并发症如恶心、呕吐、食欲下降、腹泻会引起患者摄食降低,从而加重营养不良,如这部分患者行手术治疗,可能引起较高的感染并发症,甚至影响肿瘤综合治疗的整体效果和预后[9]。此类有营养风险的患者予以营养支持可能对患者的临床预后有较大改善。
3.3 营养评估是营养支持的前提和基础 营养支持是有适应证的,没有营养不良风险的患者营养支持并不能改善临床预后,甚至会导致感染并发症的发生。选择快速方便准确的营养评估工具,是营养治疗的最初步骤[10]。因此,针对胃癌新辅助化疗患者进行适当营养支持前需要进行有效营养风险评估。经NRS2002筛查后,63例接受新辅助化疗的胃癌患者中有23例患者存在营养风险,与无营养风险患者在性别、年龄、化疗周期及肿瘤部位方面差异无统计学差异,但是化疗-手术间期在4周内的患者营养不良的风险高于无营养风险患者,这可能解释为间期越长,患者越能从化疗的毒性反应中恢复,能够更多的摄入含有营养的食物,改善自身的营养状态,所以部分国外研究推荐6~8周的间期可能也是出于相同的考虑。从人体测量指标及血常规及生化指标来看,除了白细胞计数外,经NRS2002筛选的营养风险患者均低于无营养风险患者,说明NRS2002评分与临床指标存在相关性,间接提示NRS2002能够初步筛选出营养不良的患者。根据NRS 2002的结果,我们对患者的住院时间及术后感染并发症做了统计,结果发现,NRS 2002≥3分患者的住院时间较<3分者长,腹腔感染的并发症发生率也高,可以看出NRS2002对于本组病例的风险筛查具有较好的应用价值,能够在一定程度上预测临床具有营养风险患者的术后感染发生率及术后住院时间。Bozzetti等[11]的研究发现,营养不良与消化道肿瘤术后感染并发症呈正相关。
3.4 营养支持和护理宣教 NRS 2002≥3分患者存在营养风险,营养支持的早期应以纠正电解质、维生素、微量元素失衡为主[12]。遵医嘱给予肠内外营养支持,服用配方营养制剂,予以脂肪乳剂、氨基酸和电解质等肠外营养改善患者营养状况。如合并低蛋白血症,贫血,可以输注人血白蛋白支持和成分输血支持。本组患者均予以整蛋白型肠内营养粉剂(安素)肠内营养支持,同时护士予以护理营养宣教,指导此类患者充足营养和水分的摄入,注意合理的饮食结构,鼓励患者摄入高蛋白质食物,如瘦肉、鱼肉、鸡肉、鸡蛋等,少吃肥肉和动物油。多食用高纤维素食品,如富含膳食纤维的蔬菜、水果和薯类。对食欲减退、厌食患者,可以建议少食多餐,食物品种多样化,努力营造安静舒适的进食环境。告知患者戒酒戒烟,养成健康规律的饮食习惯,不吃变质食物和不洁食物。鼓励进食后适量运动,养成定时排便习惯,保证大便通畅。针对不同的营养风险患者可以制定个体化宣教计划予以营养支持宣教,以降低患者营养风险从而改善患者营养不良状况。
4 小结
胃癌新辅助治疗后存在一定的营养不良风险发生率。对于经过新辅助治疗后入院接受手术的患者,护士在营养风险评估中扮演重要角色。有效的营养评估有利于患者顺利进行治疗,减少相关并发症,对患者康复有积极的推动作用。
[1]李守淼,刘志强,李保中,等.进展期胃癌根治术后早期肠内营养的临床应用研究[J].内科急危重症杂志,2010,16(2):84-85.
[2]黎介寿.临床营养支持的发展趋势[J].肠外与肠内营养,2010,17(1):1-4.
[3]周成富,李世宽,周岩冰,等.代谢综合征对胃癌术后并发症短期结局影响的多因素分析[J].中国实用外科杂志,2010,30(8):687-690.
[4]De Vita F,Giuliani F,Galizia G,et al.Neo-adjuvant and adjuvant chemotherapy of gastric cancer[J].Ann Oncol,2007,18 Suppl 6:vi120-vi123.
[5]李子禹,季鑫,季加孚.新辅助化疗对胃癌手术并发症的影响[J].中国实用外科杂志,2013,33(4):275-278.
[6]Schattner M.Enteral nutritional support of the patient with cancer:route and role[J].J Clin Gastroenterol,2003,36(4):297-302.
[7]潘玲,毛德强.NRS-2002评估473例首诊恶性肿瘤患者营养状况[J].重庆医学,2013,42(10):1117-1118,1121.
[8]江志伟,李宁,刘福坤.肠内免疫营养对胃癌手术病人免疫功能和急性炎性反应的调理作用[J].肠外与肠内营养,2000,7(4):202-203.
[9 ]Arends J,Bodoky G,Bozzetti F,et al.ESPEN Guidelines on Enteral Nutrition:Non-surgical oncology[J].Clin Nutr,2006,25(2):245-259.
[10]Bozzetti F,Arends J,Lundholm K,et al.ESPEN Guidelines on Parenteral Nutrition:non-surgical oncology[J].Clin Nutr,2009,28(4):445-454.
[11]Bozzetti F,Gianotti L,Braga M,et al.Postoperative complications in gastrointestinal cancer patients:the joint role of the nutritional status and the nutritional support[J].Clin Nutr,2007,26(6):698-709.
[12]徐仁应.恶性肿瘤患者营养评估与营养支持[J].上海护理,2011,11(4):93-96.
