新一代抗菌药物替加环素的研究进展
2014-11-26孙桂凤陈頔孙钊
孙桂凤,陈頔,孙钊
北京医院药学部,北京 100730
近日,国际上陆续报道在印度、巴基斯坦、英国等地发现产NDM-1(I型新德里金属细菌β-内酰胺酶)泛耐药肠杆菌科细菌,引发社会广泛关注,媒体称之为“超级细菌”。此类细菌能够产生可水解β-内酰胺类抗菌药物的酶,对青霉素类、头孢菌素类和碳青霉烯类药物广泛耐药,但对替加环素敏感。替加环素是继多西环素、米诺环素、美他环素后开发的新一代四环素类抗生素。2005年6月17日美国FDA批准其用于治疗成人复杂皮肤及其软组织感染(cSSSIs)和成人复杂的腹腔内感染(cIAIs),包括复杂阑尾炎、烧伤感染、腹内脓肿、深部软组织感染及溃疡感染。与四环素相比,在中央的骨架的侧链上,在第9位以D环甘氨酰环代替了N2烷基2甘氨酰氨基,使抗菌谱更广,抗菌活性更强,而且使它得以能克服大多数细菌对四环素耐药机制的产生。因而,在临床上具有良好的应用前景。本文综述了近年来替加环素的研究进展。
1 药理作用
1.1 作用机制 替加环素的作用机制与四环素类药物相似,与细菌核糖体30s亚基的A位点结合,阻止细菌转录从而抑制蛋白质合成[1,2]。研究显示,替加环素与核糖体的结合模型说明替加环素在与核糖体30 s亚基A位结合的同时与核糖体的剩余部分H34结合,所以与核糖体结合的更加牢固。替加环素与核糖体的结合能力比米诺环素、四环素强,抑制细菌蛋白合成的能力是米诺环素3倍、四环素的20倍。
1.2 对抗细菌耐药的机制 四环素产生耐药是后天获得性的,主要由耐药基因传播,这些耐药基因在质粒、整合子及接合转座子内被发现[3]。通过化学实验研究,确定了替加环素的立体结构对于其耐药性的作用,证明在第9位上一个大的取代基产生的空间位阻可以克服四环素的耐药机制 。
2 药代动力学
替加环素的血浆蛋白结合率为71%~89% ,与其他四环素类药物相比较,分布容积大,达到7~9 L/kg,血清峰浓度一般在0.6~1.5mg/L范围内,谷浓度可低至0.13mg/L,AUC可为5mg/h/L,半衰期长达36小时。替加环素,不受细胞色素P450酶系统的影响,也不影响由这些酶代谢的其他药物[6,7]。只有很少部分经葡萄糖醛酸结合代谢,59%以原型通过胆道排泄,22%经尿液排泄。在胆囊,肺和结肠的药物浓度比血清高,而在骨和关节液中的浓度比血清低。
药代动力学研究表明,不同年龄、性别和人种无需调整剂量[8,9]。与正常对照比较,其药代动力学性质在肝功能轻度损害的患者中没有改变;在中度肝功能损害者中,其半衰期延长23%;在重度肝损害的患者中,其半衰期延长43%,清除率降低55%。因此,有轻中度肝功能损害患者无需调整剂量;而对重度肝功能损害的患者,可首次给予100mg负荷剂量,然后为维持在25mgq12h。与健康对照比较,肌酐清除率<30 mL/min患者,替加环素的AUC可增加40%,而峰浓度(Cmax)不受影响。与之不同的是,接受血液透析的晚期肾衰竭患者替加环素的Cmax可升高60% ,而AUC仅增加20%。因此,二者均不需要调整剂量。
3 体外抗菌活性
多项研究表明,替加环素对G+菌、G-菌、厌氧菌有广泛的抗菌活性,包括万古霉素耐药肠球菌(VRE)、甲氧西林耐药的金黄色葡萄球菌(MRSA)、青霉素耐药的肺炎链球菌(PRSP)等,仍有很好抗菌效果,见表1。
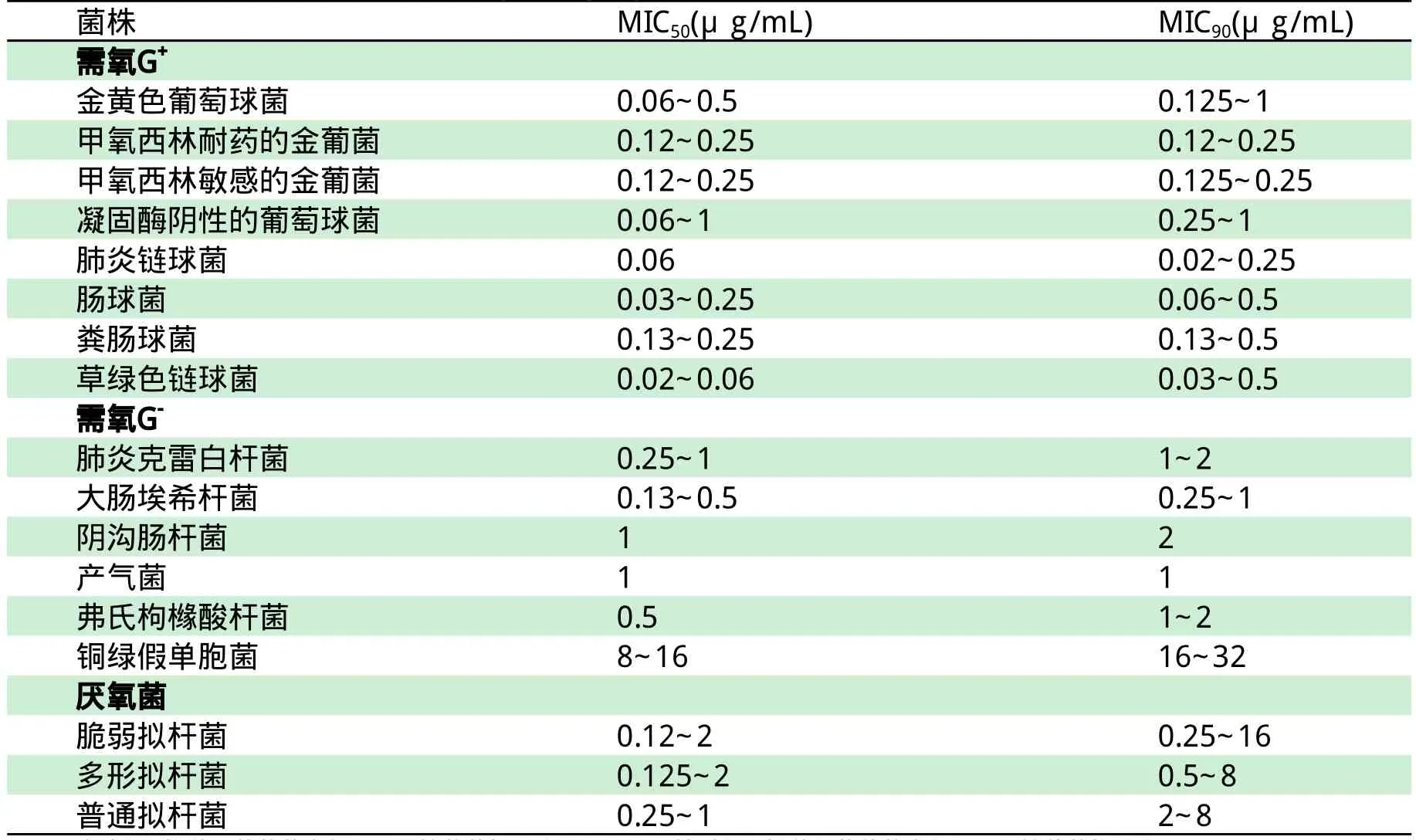
表1 替加环素的体外抗菌活性Tab 1 In vitro antimicrobial activity of tigecycline
另一项研究对比了替加环素与碳青霉烯类的抗菌能力[17],研究显示,在临床分离的碳青霉烯类敏感的肠杆菌属菌株中,78%对替加环素敏感,9%中等敏感,有13%对替加环素耐药。而耐碳青霉烯类肠杆菌属的菌株中,有49%对替加环素敏感20%中等敏感,31%耐药菌。替加环素对碳青霉烯类敏感克雷伯菌属的敏感率为67%,对碳青霉烯类耐药株的克雷伯菌属敏感率为60%,两者之间差异无统计学意义(P=0.27)。
2000~2005年在北美、拉丁美洲和欧洲的医学中心开展了一项较大规模的研究[18],共收集了104株产碳青霉烯酶(丝氨酸和金属β内酰胺酶)的肠杆菌科细菌,采用微量稀释法测定替加环素和其他25种抗菌药物的抗菌活性。其中产KPC22和KPC2373株,VIM2114株,IMP2111株,SME215株,NMC241株。产碳青霉烯酶的菌株中,依次排序分别为肺炎克雷伯菌(53株)、阴沟肠杆菌(22株)和弗劳地柠檬酸杆菌(9株) 。产碳青霉烯酶的肠杆菌科细菌对多数抗菌药物耐药率高。测试药物对这些菌株的抑菌率依次为:替加环素(100%)>多黏菌素B(88.1%)>阿米卡星(73.0%)>亚胺培南(37.5%)。替加环素对这些菌株的抗菌活性最高,与多黏菌素一样(MIC90,1mg/L),可能作为治疗多重耐药的肠杆菌科细菌引起感染的另一种选择,但需有更多的临床资料证实。
4 临床研究
4.1 对于皮肤和皮肤组织感染的治疗[19-22]复杂性皮肤和皮肤组织感染往往会产生很严重的后果,常常需要采用外科手术进行治疗。在美国,每年有250万cSSSI感染者,其中约40万患者需要住院治疗,其治疗方法主要为使用高剂量的抗菌药物,且通常需要每日多次给药。目前对于复杂的皮肤和皮肤组织感染的常规治疗方法为万古霉素和氨曲南的联用。替加环素的Ⅲ期临床试验共有546名患者参与,比较了替加环素组与万古霉素-氨曲南联合应用组,用于成年人cSSSI的疗效。主要治疗终点是定为试验治疗结束后12~92天随访的临床反应,两组的临床治愈率无明显差异。使用替加环素根治MRSA的有效率分别为78.1%,使用万古霉素和氨曲南联合治疗的有效率为75.8%。研究结果显示,单独使用替加环素与联合使用万古霉素和氨曲南的疗效相同。
4.2 对于复杂的腹腔内感染的治疗 复杂的腹腔内感染是由多种微生物包括多重耐药的细菌引起,因此对于临床治疗仍是挑战。从2002年11月到2004年8月,惠氏研究中心在全世界17个国家96个地区,对834名患者进行了多中心双盲的临床试验[23],旨在比较替加环素与亚安培南/西司他丁治疗复杂腹腔内感染的疗效。非劣效试验和有效性试验均证明,替加环素与亚安培南/西司他丁对于复杂的腹腔内感染(复杂阑尾炎、肠穿孔、腹膜炎、十二指肠穿孔、复杂胆囊炎等)有同样的疗效。其他同样设计的Ⅲ期临床试验也显示了类似的结果[24,25],这些试验同样比较了替加环素与亚胺培南/西司他丁治疗成年CIAI患者(最常见为复杂的阑尾炎)的效果。结果显示,替加环素和亚胺培南/西司他丁的临床治愈率分别为80.6%和82.4%。由此可见,替加环素与亚胺培南/西司他丁在治疗复杂性腹腔内感染时,疗效相当。
4.3 呼吸道感染的治疗 替加环素除用于FDA已批准的cSSSIs和cIAIs外,也用于可用于治疗呼吸道感染。在2005年,一项研究在全球范围评估了替加环素对病原体的抗菌效力[26],包括社区获得性感染菌株和医院获得性肺炎感染菌株。社区获得性感染的病原体中,流感嗜血杆菌占52.9%(21%为氨苄西林耐药的菌株),肺炎链球菌占39.2%(23.7%为青霉素耐药),以及摩拉克(氏)菌占7.9%。结果显示,替加环素临床上可100%有效抑制这3种菌株的活动。对于医院获得性肺炎,94.3%的患者由最常见的10个病原体产生,包括:金黄色葡萄球菌占48.5%(其中49.4%为苯唑西林耐药),铜绿假单胞菌占15.6%,克雷伯菌占5.6%,肺炎链球菌占4.6%,不动杆菌占4.5%,肠杆菌占4.0%,大肠埃希氏菌占3.8%,粘质沙雷菌占2.5%,肠球菌占2.3%,嗜麦芽菌和β-溶血性链球菌分别占1.1%。替加环素对这些病原体的抑制率大于96%(除外铜绿假单胞菌)。2007年的另一项研究对25例呼吸道相关的感染患者,单独使用替加环素或者联合应用其它抗菌药物进行治疗。结果显示,替加环素的有效率最高[27]。Ⅲ期的随机、对照临床试验显示,对于社区获得性肺炎的治疗,替加环素的疗效不亚于左氧氟沙星[28]。目前,临床研究还正在进一步评估替加环素治疗严重呼吸道感染的效果。
4.4 其它感染的治疗 目前用于治疗其它感染的大规模临床研究还较少。研究显示替加环素可有效治疗严重的败血症感染性,显著降低外科重症监护的严重的败血症患者的死亡率[29]。在治疗尿路感染方面,已证明替加环素可以有效的治疗经常性尿脓毒症[30]。
5 药物相互作用
有研究显示,替加环素不抑制或诱导肝细胞色素P450酶系统[31]。同样,作用于P450的药物也不改变替加环素的清除率。但替加环素有可能降低避孕药物的作用;在评估地高辛和替加环素相互作用的试验中,替加环素仅使地高辛的Cmax增加了13%,并未改变清除率和AUC,替加环素的药代动力学也未改变。所以在两种药物同时使用时不用改变各自剂量。与华法林合用时,根据国际标准化比率,替加环素可引起后者血药浓度升高,而替加环素的药代动力学曲线也不受华法林影响,两药合用时临床还应注意监视凝血时间。
6 不良反应
一项临床对照试验显示,与接受万古霉素和氨曲南的对照组比较,替加环素组恶心、呕吐的发生率较高,注射部位疼痛、静脉炎、皮肤瘙痒和皮疹等不良反应也较多。其药物安全性为D类,孕妇忌用。由于与四环素的结构相似,对骨和牙齿可能会有影响,因此也不宜应用于儿童[32,33]。
7 结语
替加环素的已经在2005年1月28日被FDA批准用于治疗复杂的皮肤和皮肤组织感染和复杂的腹腔内感染,越来越多的临床研究显示,替加环素可有效治疗其他感染。与其它种类的抗菌药物不同,替加环素单独使用时能同时覆盖如甲氧西林耐药金黄色葡萄球菌、链球菌和厌氧菌等病原体。对于近期发现的、大多数抗菌药物耐药的“超级细菌”替加环素也有一定的疗效,但是目前还缺乏相关的体外研究和临床评价数据。可见替加环素在临床抗感染治疗中可应用的范围相当宽,其临床地位因此显得非常重要。
[1] Olson MW, Ruzin A, Feyfant E, et al. Functional, biophysical,and structural bases for antibacterial activity oftigecycline.[J].
[2] Gemmell CG, Edwards DI, Fraise AP, et al. Warren Guidelinesfor the p rophylaxis and treatment of methicillin2resistan t Staphylococcus aureus (MRSA) infections in the UK[J].Antimicrobial Chemotherapy, 2006,57:589-608.
[3] Curcio J. Treatment of recurrent urosepsis with tigecycline: A pharmacological perspective[J]. J ClinMicrobiol 2008,46:1892-1893.
[4] Zhanel GG, Homenuik K, Nichol K, et al. The glycylcyclines:acomparative review with the tetracyclines[J]. Drugs, 2004, 64:63-88
[5] Projan SJ. Preclinicalpharmacology of GAR-936, a novel glycylcycline antibacterial agent[J]. Pharmacotherapy,2000,20:219S-228S
[6] Kasbekar N. Tigecycline: a new glycylcycline antimicrobial agent[J]. Am J HealthSystPharm , 2006, 63 (13) : 1235-1243.
[7] Pankey GA. Tigecycline[J]. J AntimicrobChem other, 2005, 56(3):470-480.
[8] Bauer G, Berens C, Projan SJ, et al. Comparison of tetracyclineand tigecycline binding to ribosomesmapped by dimethylsulphateand drug2directed Fe2+ cleavage of 16S rRNA[J]. J AntimicrobChem other, 2004, 53 (4) : 592-599.
[9] Meagher AK, Ambrose PG, Grasela TH, et al. The pharmacokinetic and pharmacodynamic profile of tigecycline[J]. Clin InfectDis,2005, 41 (Suppl5) : S333-S340.
[10] Wyeth Pharmaceutics. Tygacil( Tigecycline) for Injection[packageinsert] [M]. Philadelphia, PA:Wyeth Pharmaceuticals Inc,2005.
[11] Athwani D. Tigecycline: clinical evidence and formulary positioning[J]. Int J Antimicrob Agents, 2005, 25 (3) : 185-92.
[12] Bouch S, Stevens T, Johnson B, et al. Tigecyclineevaluation Surveillance Trial (TEST):globalin vitro antibacterial activity against 13, 669 Grampositive and Gram2negativepathogens [J].Clin M icrob Infect, 2005, 11 (2): 241-242.
[13] Bouch S, Hoban DJ, Johnson BM, et al. In vitroevaluation of tigecycline and comparative agents in 3049 clinicalisolates 2001 to 2002 [J]. D iagn M icrobiol Infect D is, 2005, 51(4): 291-295.
[14] Sader HS, Jones RN, Stilwellmg, et al. Tigecycline activity tested against 26, 474 blood stream infection isolates: a collection from 6 continents [J]. DiagnMicrobiol Infect Dis, 2005,52 (3) : 181-186.
[15] Simona B, Pooja T, Usha K, et al. CarbapenemaseproducingKleb siellapneumoniae in Brooklyn, NY: molecular epidemiology and invitro activity of polymyxin B and other agents[J]. Antimicrobial Chemotherapy, 2005; 56 (1) : 128-132
[16] Betriu C, Culebras E, Gomez M, et al. Invitro activity of tigecycline against bacteroidesspecies[J]. Journal of Antimicrobial Chemotherapy, 2005; 56 (2) : 349-352
[17] Woodford N, Hill RL, Livermore DM. In vitro activity of tigecycline against carbapenem susceptible and resistant isolates of Klebsiellasppand Enterobacterspp[J]. J AntimicrobChemother ,2007 ,59 (3) :582-583.
[18] Castanheira M, Sader HS , Deshpande LM , et al .Antimicrobialactivities of tigecycline and other broad-spect rum antimicrobials tested against serine carbapenemase and metallo-βlactamase2producingEnterobacteriaceae: report from the SENTRY Antimicrobial Surveillance Program[J].Antimicrob Agent s Chemother, 2008, 52 ( 2 ) :570-573.
[19] Breedt J, Teras J, Gardovskis J, et al . Safety and efficacy of tigecycline in treatment of skin and skin structure infections: Results of a double-blind Phase 3 comparison study with vancomycinaztreonam[J]. Antimicrob Agents Chemother 2005,49: 4658-4666.
[20] Sacchidanand S, Penn RL, Embil JM, et al . Efficacy and safety of tigecyclinemonotherapy compared with vancomycin plus aztreonam in patients with complicated skin and skin structure infections:Results from a Phase 3 randomised double-blind trial[J]. Int J Infect Dis 2005,9:251-261.
[21] Postier RG, Green SL, Klein SR, et al. Results of a multicenter,randomized, open-label efficacy and safety study of two doses of tigecycline for complicated skin and skin-structure infections in hospitalized patients[J]. ClinTher 2004, 26:704-14.
[22] Grosse EJ, Babinchank T, Dartois N, et al. The Efficacy and Safety of Tigecycline in the Treatment of Skin and Skin-Structure Infections: Results of 2 Double-Blind Phase 3 Comparison Studies with Vancomycin-Aztreonam[J]. Clin Infect Dis 2005,41:S341-53.
[23] Olson MW, Ruzin A, Feyfant E, et al.Functional, biophysical, and structural bases for antibacterial activity oftigecycline. Antimicrob Agents Chemother[J].Antimicrobial Agents and Chemotherapy,2006, 6: 2156-2166.
[24] Oliva ME, Rekha A, Yellin A, et al . A multicentric trial of the efficacy and safety of tigecycline vs. imipenem/cilastatin in patients with complicated intra-abdominal infections[J]. BMC Infect Dis 2005,5: 88-95.
[25] Kuti JL, Dowzicky M, Nicolau DP. A pharmacodynamic simulation to assess tigecycline efficacy for hospital-acquired pneumonia compared with other common intravenous antibiotics[J]. J Chemother 2008, 20:69-76.
[26] Fritsche TR, Sader HS, Stilwellmg, et al. Antimicrobial activity of tigecycline tested against organisms causing communityacquired respiratory tract infection and nosocomial pneumonia[J].DiagnMicrobiol Infect Dis 2005,52:187-193.
[27] Schafer JJ, Goff DA, Stevenson KB, et al. Early experience with tigecycline for ventilator-associated pneumonia and bacteremia caused by multidrug-resistant Acinetobacterbaumannii[J].Pharmacotherapy 2007,27:980-987.
[28] Tanaseanu C, Bergallo C, Teglia O, et al . Integrated results of phase 3 studies comparing tigecycline and levofloxacin in community-acquired pneumonia[J]. DiagnMicrobiol Infect Dis 2008, 61:329-338.
[29] Swoboda S, Ober M, Hainer C, et al .Tigecycline for the treatment of patients with severe sepsis or septic shock: A drug use evaluation in a surgical intensive care unit[J]. J AntimicrobChemother 2008,61:729-733.
[30] Curcio J. Treatment of recurrent urosepsis with tigecycline: A pharmacological perspective[J]. J ClinMicrobiol 2008,46:1892-1893.
[31] Wyeth Pharmaceutics. Tygacil( Tigecycline) for Injection[packageinsert] [M]. Philadelphia, PA:Wyeth Pharmaceuticals Inc,2005.
[32] Kasbekar N. Tigecycline: a new glycylcycline antimicrobial agent[J]. Am J HealthSystPharm , 2006, 63 (13) : 1235 - 1243.
[33] Rubinstein E, Vaughan D. Tigecycline: a novel glycylcycline[J].Drugs, 2005, 65 (10): 1317 - 1336.
