多西他赛联合顺铂治疗晚期胃癌的临床观察
2014-11-25邓文静余更生吕华珠李春鸣
邓文静,余更生,吕华珠,李春鸣
(江门市中山大学附属江门中心医院肿瘤科,广东江门 529000)
胃癌是我国最常见的恶性肿瘤之一,合理的手术联合放化疗是其主要治疗手段。不同期别的胃癌生存差异较大,早期患者根治性手术后5 年生存率可达90%以上,而晚期患者则不到10%。因大部分早期患者缺乏特异性临床症状与体征,多数患者发现时已为晚期,失去手术治疗机会[1]。姑息性化疗成为此类患者的主要治疗手段。与最佳支持治疗相比,它可缓解临床症状、提高生活质量、延长生存时间等[2]。多西他赛作为新一代半合成紫杉类药物,可单药或联合应用于晚期胃癌中,其总反应率可达17%~24%[3]。迄今,对于晚期胃癌的化疗目前无公认、统一的方案推荐,本研究拟探讨多西他赛联合顺铂治疗晚期胃癌的疗效及毒副反应,明确其在临床实践中的可行性。
1 资料与方法
1.1 临床资料 选择2011 年1 月至2012 年12 月在我院治疗的17 例均经手术和病理证实的晚期胃癌患者,5 例主要为粘液腺癌、部分为印戒细胞癌,1 例为管状腺癌,11 例为粘液腺癌,中位年龄为53.2 (31~72)岁,所有患者均接受过FOLFOX 或者THP +希罗达的一线治疗,但既往未使用过紫杉类及铂类化疗。所有患者KPS 评分≥80,肝肾及骨髓功能基本正常,有明确可测量病灶。观察指标为总反应率(overall response rate,ORR)、有效率及毒副反应。
1.2 治疗方法 所有患者均接受多西他赛+顺铂的治疗方案:多西他赛75 mg/m2+生理盐水250mL 静脉滴注,第1 天,1 小时后静脉滴注顺铂20 mg/m2+生理盐水500 mL,第1~4 天,每21 天重复1 次。多西他赛治疗前1 天、治疗当天及治疗后第1 天均口服地塞米松处理(7.5 mg/次,2 次/天)。每化疗2 疗程后进行疗效评价:若进展则化疗终止;若有效则继续2~4 程。对每个疗程急性不良反应均进行客观评价,化疗后如出现白细胞或血小板减少者予粒细胞集落刺激因子或粒细胞一巨噬细胞集落刺激因子支持,若出现Ⅲ~Ⅳ度急性毒性反应则剂量减量至原剂量75%。减量超过原剂量25%则终止该方案。所有化疗的总疗程数为2~6 个。
1.3 评定标准 近期疗效评价标准参照1999 年世界卫生组织制定的实体瘤客观疗效评价标准进行,完全缓解 (complete response,CR)+部分缓解(partial response,PR)为总反应率(ORR),CR+PR+稳定(stable disease,SD)为有效率。急性毒副反应的标准参照2006 年版美国CTC3.0 进行。
1.4 统计方法 采用SPSS17.0 统计软件进行统计分析,计数资料比较采用χ2检验,检验水准α=0.05。
2 结 果
2.1 疗效 17 例患者均完成≥2 疗程化疗(7 例接受2 程化疗,7 例接受了6 程,3 例接受了4程),1 例患者因2 程化疗后出现4 级白细胞下降将后续剂量降为初始剂量的75%。所有患者均可行近期疗效评价。其总反应率 (CR+PR)为17.6%,有效率(CR+PR +SD)为58.8%,1 例达CR (5.9%),2 例PR (11.7%),7 例SD(41.2%),7 例PD (41.2%)。
2.2 不良反应 所有化疗病例均可进行不良反应评价,主要为白细胞下降、恶心呕吐及脱发。偶有轻度的手足综合症、神经毒性及肝功能损害等。所有毒副反应经对症处理均可缓解,无治疗相关死亡事件发生。具体结果详见表1。
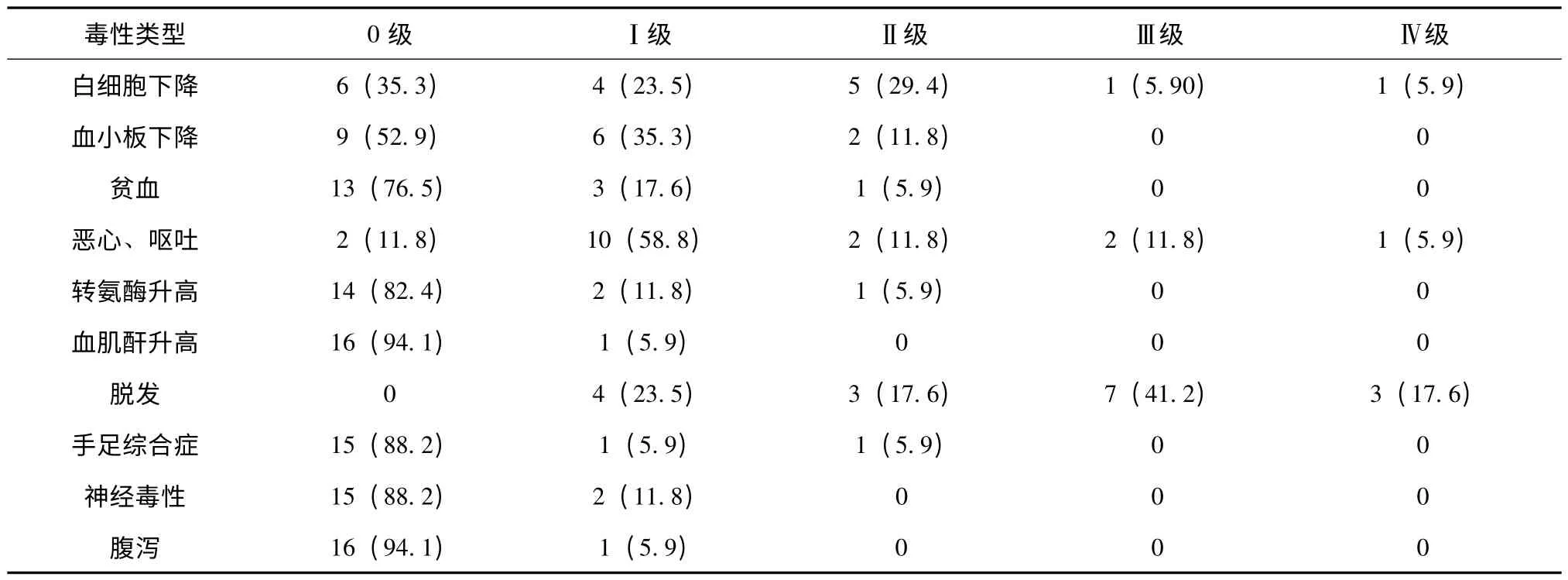
表1 多西他赛联合顺铂化疗期间的急性毒副反应(n,%)
3 讨 论
胃癌的发病率及死亡率在全世界范围内均较高,因早期难以发现,确诊时大部分为中晚期病变。对于此类患者,化疗是主要的治疗手段,尤其是联合化疗,其近期有效率可达50%以上,生存期也得以一定程度改善。部分研究显示,接受最佳支持治疗的晚期胃癌患者其中位生存时间仅3~5个月,而接受化疗者则可达9~11 个月。基于前瞻性临床试验的荟萃分析显示[4-5]:对于不可手术切除的晚期胃癌患者,姑息化疗与单纯支持治疗相比,前者的1 年生存率(20% vs.8%,RR 2.14,95%CI 1.00~4.57,P=0.05)、半年无症状期(30% vs.12%,RR 2.33,95%CI 1.41~3.87,P<0.001)、治疗后4 个月的生活质量评价 (RR 2.07,95%CI 1.31~3.28,P <0.001)均明显优于后者。然而,对于晚期甚至是局部进展期胃癌患者而言,至今无标准的、最优化疗方案推荐[6]。多西他赛是一种半合成的紫杉类药物,在多种实体肿瘤包括胃癌中显示了较好的抗肿瘤活性。来自多个地区的单药多西他赛应用于晚期胃癌临床研究显示:总反应率均接近20%[7]。它通过与微管蛋白β-亚单位结合,抑制细胞内微管蛋白解聚、促进微管蛋白聚合最终导致细胞死亡发挥抗肿瘤作用。体外研究发现多西他赛可通过抑制多药耐药相关蛋白-1 (multidrug resistance-associated protein-1,MRP-1)增强顺铂的抗肿瘤活性[8]。多个小样本的Ⅱ期临床试验显示多西他赛联合顺铂用于局部进展期或晚期胃癌是可行的,最高ORR 可达56%,而毒副反应可耐受[9]。Ridwelski K[10]等采用多西他赛(75 mg/m2)联合顺铂(75 mg/m2)用于43例局部进展期或晚期胃癌的治疗,结果发现其ORR 为37.2%,3~4 级白细胞减少18.6%,3 级腹泻、脱发、恶心与呕吐发生率分别为9%、7%、7%。Ajani JA 等[11]在一前瞻性多中心Ⅱ期临床试验中探讨了多西他赛联合顺铂(DC 方案)与多西他赛联合顺铂及5-氟尿嘧啶(DCF 方案)用于转移性或局部复发性胃癌/胃食管结合部腺癌的疗效及毒副反应,结果发现,两者的ORR 分别为26%与43%,3~4 级白细胞减少发生率分别为87%与86%,3~4 级腹泻、恶心与呕吐分别为5%vs.19%,23% vs.28%。在随后的Ⅲ期临床试验中发现:与CF 方案(顺铂100 mg/m2d1 +5-氟尿嘧啶1000 mg/m2d1-5)相比,DCF 方案(多西他赛75 mg/m2d1 +顺铂75 mg/m2+5-氟尿嘧啶750 mg/m2d1-5)可延长总生存(死亡风险下降23%,P=0.02)、提高总反应率(37% vs.25%,P=0.01)。但治疗相关毒副反应增加,主要表现为:3~4 级中性粒细胞减少、口腔炎、腹泻发生率分别为82% vs.57%,21% vs.27%,19%vs.8%。生活质量方面,接受DCF 方案的患者明显优于CF。最近研究发现,适当减少DCF 方案中三药的剂量可明显降低3~4 级中性粒细胞减少、恶心、呕吐的发生率,而疗效并不明显降低。
本研究中共17 例患者经多西他赛联合顺铂治疗后总反应率为17.6%,有效率为58.8%,相应结果与单药多西他赛用于晚期胃癌的结果相似,但低于部分小样本的Ⅱ期临床试验及Ⅲ期临床试验V-325 的结果。治疗毒副反应方面,3~4 级白细胞下降、恶心与呕吐等发生率分别为11.8%、17.6%,低于相关研究结果。究其原因可能与以下因素相关:(1)化疗疗程数偏低。在上述相应的临床研究中,接受多西他赛联合顺铂最多的疗程数达8 个,而本研究中只59% (10/17)的患者接受了4~6 程化疗,41% (7/17)患者因疾病进展只接受了2 程化疗。化疗强度的降低可能一定程度降低ORR;(2)病例数偏少。本研究中病例数仅17例,这与本地区居民的就医习惯存在一定关联,因为一旦确诊为晚期有的患者及其家属就选择放弃诊治或直接转入上级医院治疗,这为病例的收集造成一定困难;(3)所选择病例均为晚期病例。本研究中所有患者均为合并远处转移病变,体内肿瘤负荷较大,而相关类似研究中包含了很大部分局部复发后进展期病变患者,临床分期相对偏早。
综上所述,多西他赛联合顺铂的化疗方案治疗晚期胃癌,疗效肯定,不良反应轻,患者耐受性良好。但临床进一步广泛推广有赖于前瞻性Ⅲ期临床试验的验证。
[1]李建璜,李斌,钟美佐.不同化疗方案治疗晚期胃癌的疗效评价[J].中国肿瘤临床,2009,36 (8):205-207.
[2]Takiuchi H,Goto M,Kawabe S,et al.Second-fine chemomerapy in gastricancer [J].Gan To Kagaku Ryoho,2005,32 (1):19-23.
[3]Giuliani F,Gebbia V,De Vita F,et al.Docetaxel as salvage therapy in advanced gastric cancer:a phase II study of the GruppoOncologico Italia Meridionale (G.O.I.M.)[J].Anticancer Res,2003,23 (5b):4219-4222.
[4]秦叔逵,龚新雷.晚期胃癌化疗的现状和新进展[J].临床肿瘤学杂志,2006,11 (9):641-652.
[5]Casaretto L,Sousa PL,Mari JJ.Chemotherapy versus support cancer treatment in advanced gastric cancer:a meta-analysis[J].Braz J Med Biol Res,2006,39 (4):431-440.
[6]Taketa T,Sudo K,Wadhawa R,et al.Adjuvant therapy in gastric cancer:what is the optimal approach [J].Curr Oncol Rep,2013,15 (2):146-151.
[7]Khokhar NZ,Jiang Y,Benson AB 3rd,et al.Refining docetaxel-containing therapy for gastric cancer [J].Gastrointest Cancer Res,2011,4 (3):96-105.
[8]Maeda S,Sugiura T,Saikawa Y,et al.Docetaxel enhances the cytotoxicity of cisplatin to gastric cancer cells by modification of intracellular platinum metabolism [J].Cancer Sci,2004,95 (8):679-684.
[9]Roth AD,Maibach R,Martinelli G,et al.Docetaxel (Taxotere)-cisplatin (TC):an effective drug combination in gastric carcinoma.Swiss Group for Clinical Cancer Research (SAKK),and the European Institute of Oncology (EIO) [J].Ann Oncol,2000,11 (3):301-306.
[10]Ridwelski K,Gebauer T,Fahlke J,et al.Combination chemotherapy with docetaxel and cisplatin for locally advanced and metastatic gastric cancer [J].Ann Oncol,2001,12(1):47-51.
[11]Ajani JA,Fodor MB,Tjulandin SA,et al.Phase II multi-institutional randomized trial of docetaxel plus cisplatin with or without fluorouracil in patients with untreated,advanced gastric,or gastroesophageal adenocarcinoma [J].J Clin Oncol,2005,23 (24):5660-5667.
