碱性体系下萃取钒的研究
2014-11-16陈金清熊家任林凯
陈金清 , 熊家任 , 林凯
(1.江西理工大学,a.工程研究院;b.冶金与化学工程学院,江西 赣州341000;2.国家钨与稀土产品质量监督检验中心,江西 赣州341000)
钒是一种非常重要的稀有金属,被广泛应用于冶金[1]、化工[2]、电子[3]等领域中,因此其价格出现逐年攀升趋势.钒在自然界的分布相当分散[4],一般都不会形成单独的矿床,而主要是以伴生矿的形式存在[5],因而钒主要是在各种冶金过程中作为副产品进行回收.从氧化铝生产和石煤中提钒便是生产钒的一种重要途径.
氧化铝生产用的铝土矿中通常都有一定量的含钒矿物,这些矿物在高压溶出过程中大约有30%左右进入铝酸钠溶液中[6],它可以在生产流程中循环积累达到一定的浓度.铝酸钠溶液中的钒对分解过程具有不利的影响[7],它可使产品氢氧化铝颗粒变细并进入晶格中,以至于在焙烧氢氧化铝时造成氧化铝的强烈细化,这对生产砂状氧化铝是非常不利的.因此,从氧化铝生产过程中回收钒,不但可以降低钒对氧化铝产品的不利影响,还可以创造更多的经济价值,因此是非常必要的.近年来,石煤提钒已成为石煤资源综合利用的重要方面,其中氧化焙烧——碱浸工艺越来越受青睐[8].现有的文献中,在碱性介质中萃取钒的研究都是用N263作为萃取剂,而且都是在pH<10的条件下进行[9-11],有很高的萃取率.如能在更强的碱性条件下有效地萃取钒,对于碱性条件下提取钒有重要的参考价值,因此有必要对此进行深入研究.
在水溶液中,钒在不同pH值和不同浓度条件下存在的状态不同,Clark等总结过这方面的资料[12].在一定浓度下,随着溶液由酸性至碱性的转变,钒在溶液中的存在形式依次为VO2+、V2O5(沉淀)、H2V10O284-、HV10O285-、V10O286-、V3O93-、VO3(OH)2-、VO43-.钒只有在较强酸性条件下,以VO2+或V2O5沉淀形式存在,在弱酸性和碱性条件下,都是以阴离子形式存在.能用来萃取阴离子的萃取剂主要是季铵盐和胺类萃取剂.季铵盐可以直接与被萃取物发生阴离子交换反应,如柯兆华等用季铵盐在碱性条件下萃取钨[13],刘波等用N263萃取钒[10],盖会法等用 N263萃取铼[14],杨项军等用CTAB萃取金[15]等.胺类则需要在酸性条件或者经过酸化后才能萃取阴离子,如伯胺N1923萃取钼[16]、萃取钨[17]、萃取金[18],N503[19]萃取金等.在筛选萃取剂过程中,笔者用酸化(酸过量)的胺类萃取剂和季铵盐萃取剂做对比试验,不管是用硫酸酸化或是用盐酸酸化,萃余液都呈酸性,与本文的初衷有出入,所以选用季铵盐做为萃取剂,本研究用MTOAC做为萃取剂.
1 实验部分
1.1 实验方法
有机相采用分析纯MTOAC与工业纯的仲辛醇和磺化煤油按照一定质量比配制,水相采用分析纯的偏钒酸铵配制成含五氧化二钒浓度为2 g/L的溶液,用分析纯的氢氧化钠调节pH,在环境温度30℃左右,按一定相比(有机相与水相的体积比,下同)混合于梨形分液漏斗中,于康氏振荡器上震荡一定时间,静置10 min后,分液分析.
1.2 分析及数据处理
水相中的钒,采用硫酸亚铁铵容量法滴定,实验中萃取率和反萃率分别按以下公式计算:
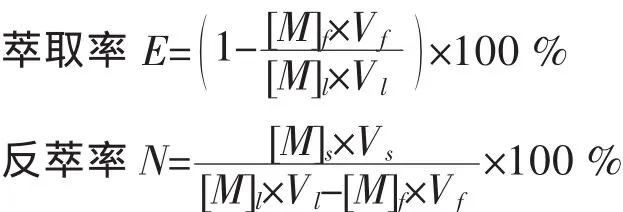
[M]l,[M]f,[M]s——分别为料液、萃余液和反萃液中钒的浓度,g/L;
Vl,Vf,Vs——分别为料液、 萃余液和反萃液的体积,L.
2 结果与讨论
2.1 有机相组分对萃取的影响
2.1.1 萃取剂浓度对萃取的影响
有机相按照萃取剂+0.3倍萃取剂的仲辛醇+磺化煤油的质量比配制.萃取剂质量分数为5%,10%,15%,20%,25%,分别与水相pH值为9.67、11.14和11.7按相比为1混合震荡反应10 min.考察萃取剂不同浓度对萃取的影响,结果见图1.
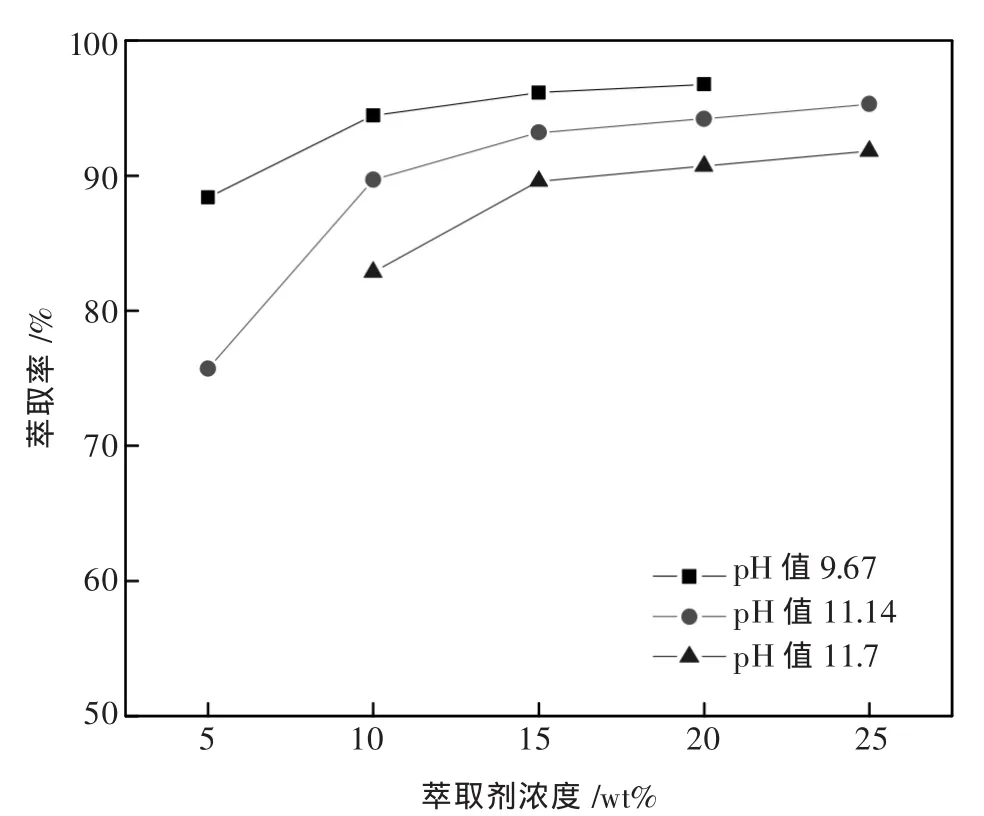
图1 萃取剂浓度对萃取钒的影响
由图1可知,在一定pH值条件下,随着萃取剂浓度的升高,萃取率也随之升高;在同一萃取剂浓度条件下,随着pH值的升高,萃取率降低.在pH值为9.67时,萃取剂的浓度从5%升高到10%时,萃取率升高得比较快,从88%升高到94%,再增加萃取剂浓度,萃取率升高则不明显,出现缓坡.pH值为11.14和11.7时,萃取剂浓度从5%升高到10%再到15%,萃取率明显升高,再升高萃取剂浓度,萃取率升高趋势变缓.当萃取剂浓度的升高,萃取率的升高趋势变缓以后,继续升高萃取剂浓度,萃取剂的未饱和度也越大,不利于萃取剂的有效使用.选择萃取剂的质量浓度为15%,同时考察仲辛醇的添加量对混合相分相的影响.
2.1.2 仲辛醇的作用
在胺类萃取剂的萃取过程中通常会添加醇类防止出现第三相[20],本实验添加了仲辛醇.另外在配制有机相的过程中,由于MTOAC吸水性很强,当它直接与磺化煤油混合,搅拌后会出现浑浊,静置10 min左右后,明显分成两层.此时稍添加仲辛醇,分层的两相又很快溶于一相,而且清澈透明.分别取仲辛醇的质量分数为2.0%、3.5%、4.5%、6%和10%配制有机相,按相比为1,分别在pH值为11.14和11.7的条件下震荡反应10 min,考察不同仲辛醇浓度条件下萃取钒的影响,结果见表1.
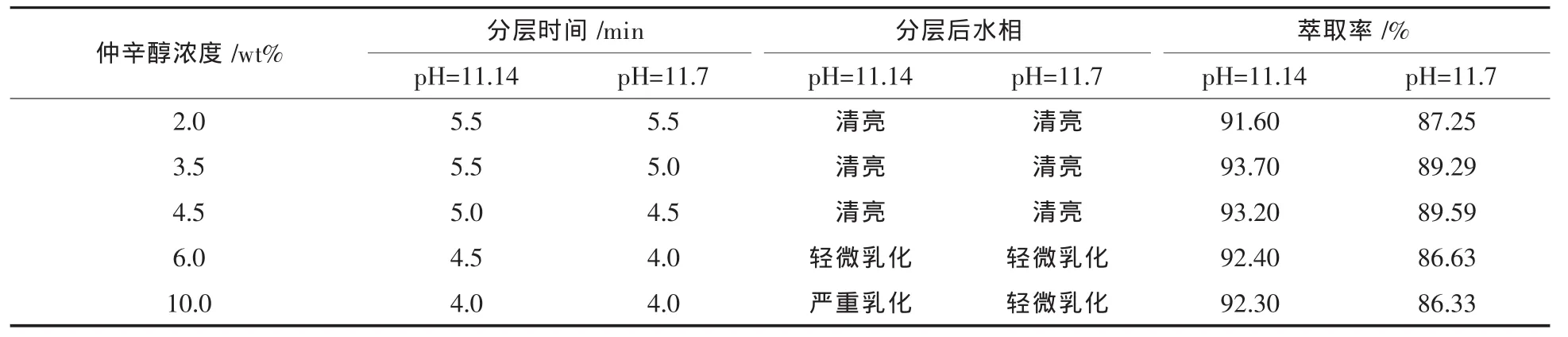
表1 不同仲辛醇浓度分别在2种p H值条件下萃取钒的结果
由表1可知,随着仲辛醇的浓度增加,混合液更容易分层;分层后水相的乳化程度也有所增加.仲辛醇的添加量为4.5%及以下时,混合液分层后水相清亮透明;添加量为6%时有轻微乳化,静置4 h,乳化消失;添加量为10%则严重乳化,需要静置十多个小时才能变得澄清.添加量为3.5%到4.5%时,萃取率最高,添加量为2%或者添加量高达6%和10%时,萃取率都有所下降.因为添加量为2%时,添加量太少,影响萃取剂的活性,使得萃取率降低;添加量增加,水相容易乳化,影响萃取效果.由此可见,有机相中仲辛醇的含量为3.5%或4.5%较为合适,本文选择仲辛醇的添加量为3.5%.
通过单因素实验,分别考察萃取剂和仲辛醇的浓度,得到有机相的最佳配比为15%MTOAC+3.5%仲辛醇+81.5%磺化煤油.通过图1和表1,在相同条件下,pH值越高,得到的萃取率则越低.
2.2 水相p H值对萃取的影响
有机相为最佳配比与不同pH值的水相按相比为1∶1震荡反应10 min.考察水相pH对钒萃取率的影响,结果见图2.
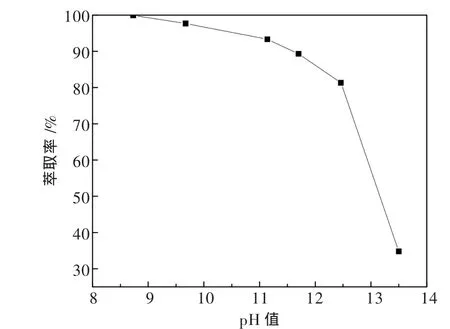
图2 水相p H值对萃取钒的影响
由图2可知,水相pH对萃取的影响很明显.随着pH值的升高,萃取率逐渐降低.根据Clark等总结的资料[12],在溶液中V2O5的浓度为2 g/L时,随着碱性的增强,钒的主要存在形态从 V3O93-到 VO3(OH)2-再到VO43-.发生的反应为:
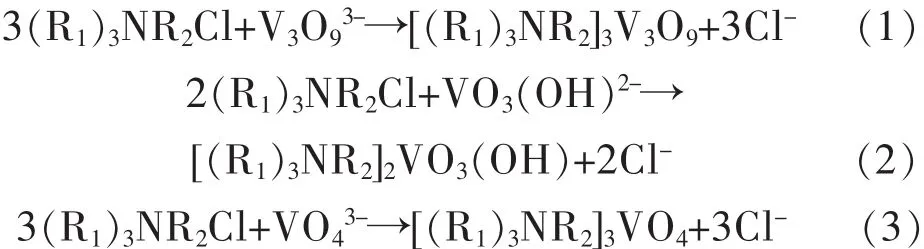
其中 R1为 C8H17,R2为 CH3,下同.
pH值为9左右,萃取反应主要按式(1)进行;pH值为9.5到12.5时,萃取反应主要按式(2)进行;pH值为13以上,萃取反应主要按式(3)进行.离子中的钒原子数n与离子价态z的比值从1∶1到1∶2再到1∶3,逐渐变小,理论被萃取量也逐渐变小[21],在相同条件下越难被萃取.所以随着碱性的增强,萃取率呈明显下降趋势.本文主要考察在一定碱性条件下萃取钒,并有较高(90%)的萃取率,所以在后续的实验中,水相pH值定为11.5左右,主要被萃阴离子为VO3(OH)2-.
2.3 震荡时间对萃取的影响
在有机相配比不变,水相pH值为11.46,相比为 1 的条件下, 分别震荡 1、3、5、10、15 min 进行试验.考察不同震荡时间对萃取钒的影响,结果见图3.
由图3可知,震荡反应1 min时,就有89.7%的萃取率,但是反应尚未平衡;继续震荡至3 min,萃取率明显上升,达到91.9%,反应则基本达到平衡;震荡反应时间升至5 min,萃取率稍有升高,达到92.1%,;震荡反应时间为10 min和15 min,萃取率较震荡5 min的几乎不变.故取震荡时间5 min为宜.
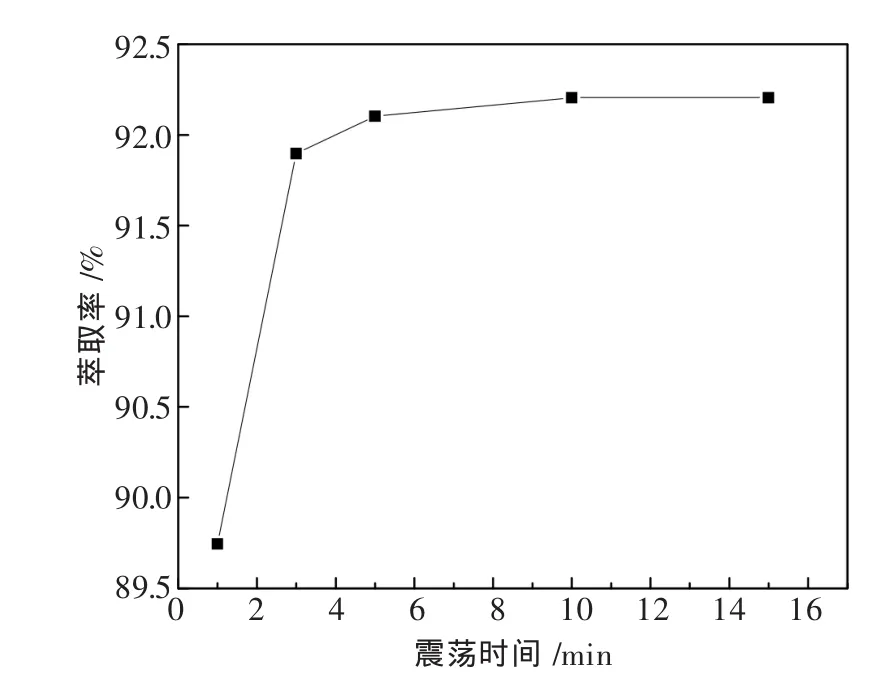
图3 震荡时间对萃取钒的影响
2.4 相比对萃取的影响
在有机相配比不变,水相pH值为11.46,按照不同相比(有机相与水相的体积比,下同),震荡反应5 min考察相比对萃取的影响,结果见图4.
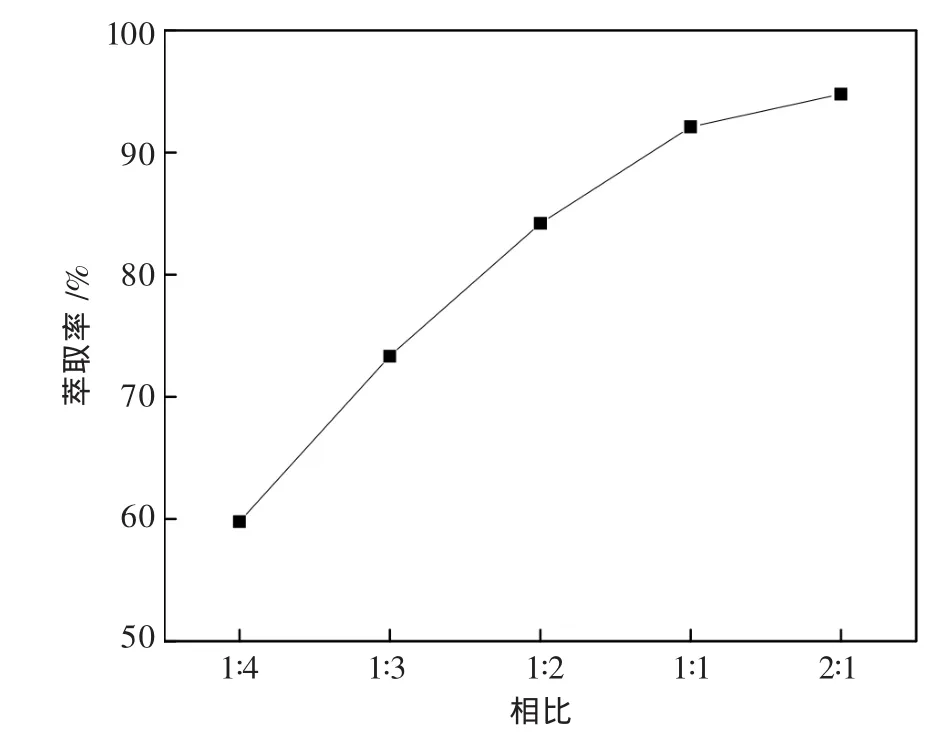
图4 相比对钒萃取的影响
由图4可知,钒的萃取率随着相比的不断增大而增大.在萃取过程中,当相比小于 1,如 1∶4、1∶3 和 1∶2时,能够在一定程度上富集水溶液中的钒,但是有机相和水相混合震荡后容易发生乳化,需要静置几个甚至十几个小时,水相才能澄清,不利于萃取的连续性;当相比为 1∶1 和 2∶1 时,分层后水相很清亮.相比为 2∶1或更高时,不利于溶液中钒的富集.综合考虑,为了获得较高浓度的富钒有机相,又要获得高的钒萃取率这2个因素,选择相比为1较适宜,钒的一级萃取率达到了92.1%.
2.5 反 萃
根据上面的分析,萃取反应为阴离子交换反应,而且强碱性条件下萃取率更低,尝试用不同的钠盐在强碱性条件下进行反萃实验.在环境温度下对负载有机相进行反萃,在0.5 mol/L NaOH的碱性条件下分别用 NaCl、NaNO3、Na2SO4和 Na2CO3作为反萃剂按相比为1∶1进行反萃试验.可能发生反应的化学方程式为:
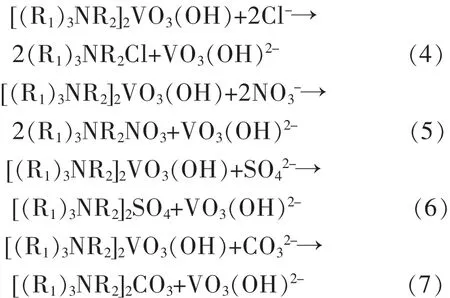
VO3(OH)2-被反萃下来后跟溶液中的 OH-结合,发生如下反应:

不同反萃剂对负载有机相反萃的效果如表2.

表2 不同反萃体系对负载有机相的反萃结果
由表2可知,负载有机相可用含NaCl或NaNO3的反萃体系进行反萃,反萃率都在90%以上,特别是用NaNO3时,其反萃率达到96.36%,应选为反萃剂.但是实验中发现用NaNO3反萃后,有机相分成清晰的两层,不能再生,会造成有机相的浪费.故实验中选用NaCl作为反萃剂.
经过实验筛选,反萃体系为0.5 mol/LNaCl+1.0mol/L NaOH,反萃效果最佳.与负载有机相混合震荡10 min,静置10 min后分液,单级反萃率可得到97.72%.
3 结 论
(1)以质量分数为15%三辛基甲基氯化铵+3.5%仲辛醇+81.5%磺化煤油为萃取体系的有机相,与水相中pH为11.46,V2O5的浓度为2 g/L的水溶液,按照相比为1∶1反应,单级萃取率能达到92%以上.
(2)负载有机相用0.5 mol/L NaCl+1.0 mol/L NaOH混合溶液反萃,可得到97.72%的单级反萃率.
[1]邓杰博.钒在冶金中的应用及研究进展[J].铁合金,2011(2):45-48.
[2]杨绍利,彭富昌,潘复生,等.钒系催化剂的研究与应用[J].材料导报,2008(4):53-56.
[3]崔艳华,孟凡明.钒电池储能系统的发展现状及其应用前景[J].电源技术,2005(11):77-81.
[4]杨守志.钒冶金[M].北京:冶金工业出版社,2010.
[5]廖世明,柏谈论.国外钒冶金[M].北京:冶金工业出版社,1985.
[6]赵卓.氧化铝生产流程中钒的提取研究[D].长沙:中南大学,2010.
[7]杨重愚.氧化铝生产工艺[M].北京:冶金工业出版社,1982:132-133.
[8]史玲,王娟,谢建宏.钠化法提钒工艺条件的研究[J].矿冶工程,2008,28(1):58-61.
[9]EI-Nadi Y A,Awwad N S,Nayl A A.A comparative study of vanadium extraction by Aliquat-336 from acidic and alkaline media with application tospent catalyst[J].International Journal of Mineral Processing, 2009, 92(3/4):115-120.
[10]肖超,肖连生,成宝海,等.石煤钒矿碱性浸出液提取钒新工艺[J].稀有金属与硬质合金, 2011,39(1):4-7.
[11]刘波,冯光熙,黄祥玉,等.用N263从钒溶液中回收钒[J].化学研究与应用,2003,15(1):54-57.
[12]Clark R J H, Brown D.The chemistry of vanadium,niobium and tantalum[M].London: Oxford Pergamon Press,1975:261~302.
[13]柯兆华,张贵清,关文娟,等.季铵盐从碱性钨酸钠溶液中萃取钨的研究[J].稀有金属与硬质合金,2012,40(6):1-4.
[14]盖会法,高自立,孙思修,等.季铵盐N263和叔胺TOA萃取铼(Ⅶ)的研究[J].应用化学,1987(5):20-24.
[15]杨项军,陈景,韦群燕,等.用CTAB/TBP体系从碱性氰化液中萃取低浓度 Au(Ⅰ)[J].中国有色金属学报,2004,14(11):1958-1962.
[16]李文华,杨永会,孙思修.伯胺N1923萃取钼(Ⅵ)的研究[J].稀有金属与硬质合金,1998(2):1-4.
[17]曾平,王玉鑫,王韧.伯胺N1923萃取钨的机理研究[J].湘潭大学自然科学学报,1991(2):79-84.
[18]姜键准,周维金,高宏成,等.N1923从碱性氰化物中萃取金(Ⅰ)的研究[J].无机化学学报,2001,17(3):343-348.
[19]周扬,李学玲,顾烁玥,等.用N503/TBP从碱性氰化液中萃取低浓度金[J].中国有色金属学报,2009,19(7):1345-1349.
[20]杨佼庸,刘大星.萃取[M].北京:冶金工业出版社,1988:140.
[21]曾添文,戴文灿,张志,等.离子交换树脂对钒(V)交换性能的研究[J].离子交换与吸附,2002,18(5):453-458.
