丙泊酚和异氟烷对颅内肿瘤患者炎性细胞因子的影响比较*
2014-11-07徐鲁峰潘雯宫建郭凤封瑞崔文瑶吕福斌高成杰
徐鲁峰,潘雯,宫建,郭凤,封瑞,崔文瑶,吕福斌,高成杰
(1.济南军区总医院麻醉科,济南 250031;2.辽宁省疾病预防控制中心,沈阳 110005;3.沈阳药科大学生命科学与生物制药学院临床药学教研室,沈阳 110016;4.中国医科大学药学院药物毒理学教研室,沈阳 110001;5.中国医科大学附属第一医院麻醉科,沈阳 110001)
颅内肿瘤是中枢神经系统最常见的疾病之一,严重危害人类的健康。原发性颅内肿瘤在成年人全身各系统肿瘤中居第11位,在儿童全身各系统肿瘤中居第2位,近年来其发病率呈明显上升趋势。颅内肿瘤对神经组织破坏性大,手术、放射治疗、化学治疗等综合治疗后仍有复发的可能,预后较差;因此,探讨脑保护作用药物对治疗颅内肿瘤具有重要的临床应用价值。异氟烷和丙泊酚均是临床常用的麻醉药物,均对脑组织起保护性作用[1]。2012年1月至2013年8月,笔者在前期研究的基础上[2-3],通过观察使用异氟烷和丙泊酚的颅内肿瘤患者手术后炎性细胞因子肿瘤坏死因子(tumor necrosis factor,TNF)-α、白细胞介素-1(interleukin-1,IL-1)和细胞黏附分子-1(intercellular adhesion molecular-1,ICAM-1)的改变,探讨这两种麻醉药物的临床使用价值。
1 资料与方法
1.1 临床资料 中国医科大学附属第一医院择期颅内肿瘤手术患者168例,男80例,女88例,随机分为丙泊酚组和异氟烷组,各84例。患者排除标准为:各种急性、慢性炎症,细菌及病毒感染,免疫系统疾病、结缔组织病,创伤及手术后1个月内再次手术等。丙泊酚组和异氟烷组患者基本资料间均差异无统计学意义(均P>0.05)。所有病例均获得医院伦理道德委员会的批准,且获得患者或其家属签署的知情同意书。
1.2 麻醉方法 患者于手术前30 min肌内注射苯巴比妥钠和东莨菪碱,以咪达唑仑、芬太尼和维库溴铵行麻醉诱导,气管插管后控制呼吸。分别以丙泊酚(意大利 AstraZeneca S.P.A,批准文号:H20080488)和异氟烷(英国雅培制药有限公司,批准文号:H20059911)行手术中麻醉维持,其中丙泊酚组行血浆靶控输注丙泊酚 3 ~ 6μg·mL-1,异氟烷组以低剂量异氟烷(1%~2%)持续吸入。丙泊酚组和异氟烷组均按需给予芬太尼和维库溴铵,手术结束前5 min,停止使用丙泊酚和异氟烷。麻醉操作由同一位经验丰富的麻醉科医师进行。患者分别于麻醉诱导前(t0)、手术后0 h(t1)、手术后 24 h(t2)、48 h(t3)抽取静脉血 5mL,并置于预冷的抗凝试管中,采血后即刻于4℃离心10 min(3000 r·min-1,r=10 cm),血清分离后于-70℃深冻冰箱中保存,待测。TNF-α、IL-1和ICAM-1含量的测定采用放射酶联免疫吸附法(中国晶美生物工程有限公司原装试剂盒)。
1.3 统计学方法 数据库建立使用SPSS 16.0版统计软件,计量资料以均数±标准差表示,同一时间点的组间数据比较采用两独立样本t检验或 t'检验(方差不齐时);不同时间点的组间数据比较采用重复测量方差分析,若资料不满足Mauchly球形检验假设,则使用Greenhouse-Geisser ε校正系数校正自由度;以P<0.05为差异有统计学意义。
2 结果
2.1 组间比较 丙泊酚组与异氟烷组比较,芬太尼用量分别为(291.34 ±27.92)和(297.05 ±34.26)μg,差异无统计学意义(t= -0.94,P=0.42);t0时,TNF-α、IL-1和ICAM-1的含量差异无统计学意义(P>0.05);t1时,TNF-α 和 ICAM-1的差异无统计学意义(P>0.05),丙泊酚组IL-1的含量明显低于异氟烷组;t2、t3时,丙泊酚组 TNF-α、IL-1 和 ICAM-1 的含量均明显低于异氟烷组,见表1。
2.2 组内比较 两组患者血清TNF-α、IL-1和ICAM-1的含量自t0~t2时逐渐上升,t2时两组各指标均较t0、t1时明显增高,t3时两组各指标均较t2时明显下降,见表1。
表1 两组患者血清TNF-α、IL-1和ICAM-1含量比较Tab.1 Comparison of the serum level of TNF-α,IL-1 and ICAM-1 between two groups of patients
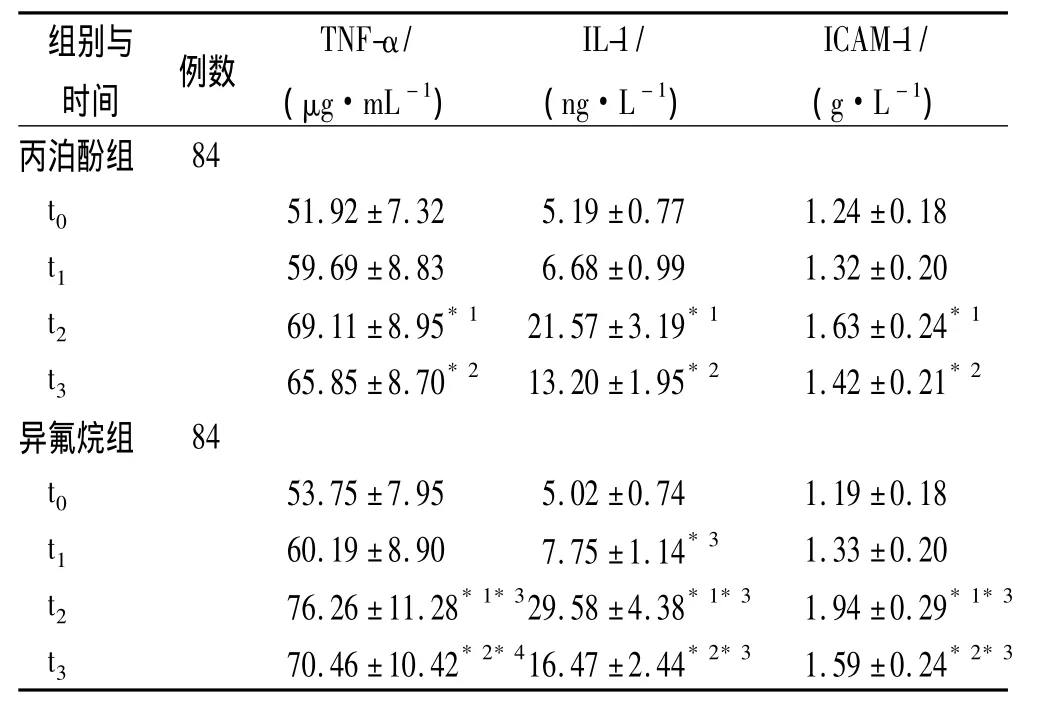
表1 两组患者血清TNF-α、IL-1和ICAM-1含量比较Tab.1 Comparison of the serum level of TNF-α,IL-1 and ICAM-1 between two groups of patients
与本组 t0、t1时比较,*1 P <0.05;与本组 t2时比较,*2 P <0.05;与丙泊酚组同时间点比较,*3 P <0.01,*4 P <0.05Compared with its own at t0,t1,*1 P <0.05;compared with its own at t2,*2 P < 0.05;compared with propofol group at the same time point,*3 P <0.01,*4 P <0.05
组别与时间 例数TNF-α/(μg·mL-1)IL-1/(ng·L -1)ICAM-1/(g·L -1)丙泊酚组84 t0 51.92 ±7.32 5.19 ±0.77 1.24 ±0.18 t1 59.69 ±8.83 6.68 ±0.99 1.32 ±0.20 t2 69.11 ±8.95*1 21.57 ±3.19*1 1.63 ±0.24*1 t3 65.85 ±8.70*2 13.20 ±1.95*2 1.42 ±0.21*2异氟烷组 84 t0 53.75 ±7.95 5.02 ±0.74 1.19 ±0.18 t1 60.19 ±8.90 7.75 ±1.14*3 1.33 ±0.20 t2 76.26 ±11.28*1*3 29.58 ±4.38*1*3 1.94 ±0.29*1*3 t3 70.46 ±10.42*2*4 16.47 ±2.44*2*3 1.59 ±0.24*2*3
3 讨论
近年来,炎症反应被认为是肿瘤发生发展的特征之一[4],其对肿瘤的病理改变起重要作用:一方面,机体的炎症状态促进肿瘤的发生发展,如炎性细胞因子IL-1、TNF-α等含量的改变,诱导肿瘤细胞表面化学因子受体发生变化,使肿瘤细胞侵袭力增强;另一方面,癌基因的活化促进炎性细胞因子的表达,如诱发ICAM-1和TNF-α等含量增多,进而改变炎症微环境,其中TNF-α是启动炎症反应的关键因子,可诱导IL-1的释放,IL-1随后又刺激产生其他细胞因子的生物合成,如加强ICAM-1的表达,进而诱导炎性瀑布,放大炎性反应[5-6]。因此,探讨颅内肿瘤患者炎性细胞因子的变化,不仅可明确肿瘤微环境的改变,而且可为药物干预靶点提供参考依据,指导临床用药[7]。
本研究分析两组患者手术前及手术后炎性细胞因子含量的改变,结果表明两组患者血清炎性细胞因子TNF-α、IL-1和ICAM-1水平均较麻醉诱导前升高,提示炎症微环境发生改变,即炎症反应在颅内肿瘤患者手术后脑损伤的发生机制中发挥一定的作用;丙泊酚组患者手术后24及48 h血清TNF-α、IL-1和ICAM-1水平均低于异氟烷组,说明两种麻醉方法对炎性细胞因子分泌的影响不同,提示颅内肿瘤患者采用丙泊酚静脉麻醉的抗炎效果要优于异氟烷吸入麻醉[2,8],即丙泊酚较异氟烷对颅脑肿瘤患者脑保护作用好。炎性细胞因子和抗炎性细胞因子共同组成炎性细胞因子交互网络,二者常处在平衡/失衡相互对立统一的变化过程中,进而调整机体的炎症微环境[2]。丙泊酚可能通过以下途径抑制炎性细胞因子的分泌:一是直接扩张内脏血管,改善肠道的低氧和血液灌注,进而减少炎性细胞因子的分泌[9];二是抑制白细胞的迁移能力,间接减少炎性细胞因子的分泌[10];三是丙泊酚发挥钙离子通道阻滞剂[11]和自由基清除剂[12]的作用,抑制炎性细胞因子的分泌。笔者前期研究[2-3]表明,使用丙泊酚的颅内肿瘤患者手术后内源性抗炎性细胞因子IL-4、IL-10和IL-13均较使用异氟烷的患者含量高,本研究进一步证实丙泊酚和异氟烷从多个环节调节炎症微环境的改变,发挥抗炎和细胞保护作用。
综上所述,丙泊酚可降低颅内肿瘤患者手术后炎症反应的强度,比低剂量异氟烷(1% ~2%)吸入麻醉具有更广阔的应用前景。
[1]CUI W,GONG J,WANG Q,et al.Myocardial protectionwith sevoflurane in coronary artery bypass grafting surgery[J].Pak J Med Sci,2012,8(4):761 -766.
[2]王昆鹏,宫建,白宇.丙泊酚和异氟醚对颅内肿瘤患者抗炎性因子的影响[J].天津医药,2012,40(8):831 -832.
[3]徐鲁峰,于金贵,高成杰,等.不同麻醉方法对颅内肿瘤患者抗炎症因子的影响[J].沈阳药科大学学报,2012,29(2):139-142.
[4]COLOTTA F,ALLAVENA P,SICA A,et al.Cancer-related inflammation,the seventh hallmark of cancer:links to genetic instability [J].Carcinogenesis,2009,30(7):1073-1081.
[5]KAKIASHVILI E,SPEIGHT P,WAHEED F,et al.GEF-H1 mediates tumor necrosis factor-alpha-induced Rho activation and myosin phosphorylation:role in the regulation of tubular paracellular permeability[J].J Biol Chem,2009,284(17):11454-11466.
[6]胡晓芳,杨智,安殿梅,等.急性脑出血患者炎症状态与hs-IL-1和NO 变化[J].中国公共卫生,2012,28(7):981-982.
[7]MANTOVANI A.Molecular pathways linking inflammation and cancer[J].Curr Mol Med,2010,10(4):369 -373.
[8]CEYLAN B G,YILMAZ F,EROGLU F,et al.Oxidant and antioxidant activities of different anesthetic techniques.Propofol versus desflurane[J].Saudi Med J,2009,30(3):371-376.
[9]KUMAKURA S,YAMAGUCHI K,SUGASAWA Y,et al.Effects of nitrous oxide on the production of cytokines and chemokines by the airway epithelium during anesthesia with sevoflurane and propofol[J].Mol Med Rep,2013,8(6):1643-1648.
[10]INADA T,UESHIMA H,SHINGU K.Intravenous anesthetic propofol suppresses leukotriene production in murine dendritic cells[J].J Immunotoxicol,2013,10(3):262 -269.
[11]MIGITA T,MUKAIDA K,HAMADA H,et al.Effects of propofol on calcium homeostasis in human skeletal muscle[J].Anaesth Intensive Care,2009,37(3):415 -425.
[12]YUMOTO M,NISHIDA O,NAKAMURA F,et al.Propofol attenuates oxidant-induced acute lung injury in an isolated perfused rabbit-lung model[J].J Anesth,2005,19(4):287-294.
