交联透明质酸衍生物的研究进展
2014-10-24薛茹胡立娜
薛茹 胡立娜
(河北常山生化药业有限公司 河北石家庄 050800)
1 前言
透明质酸(H A)是广泛存在于皮肤、韧带、关节液和眼睛的玻璃体等组织中的一种粘多糖,它是由(β-l-4)D-葡萄糖醛酸和(β-l-3)N-乙酰基-D-氨基葡萄糖双糖单位重复连接组成的一种线状聚阴离子粘多糖,是构成皮肤、玻璃体、关节滑液和软骨组织的重要成分,具有独特的理化性质和广泛的生物学功能,在临床上被广泛应用于眼科手术、骨科手术、骨性关节炎和类风湿性关节炎、预防术后粘连以及作为眼科和皮肤外用药物载体。但是由于天然H A在体内易于降解,无法在体内长期存留,难以发挥其优异的物理化学特性,往往会限制其疗效的发挥,应用受到了很大局限。尤其是近年来在预防粘连和软组织填充等方面的应用,要求H A在人体内应具有较长的存留时间,有时甚至要求在体内长期存留。长期以来研究者通过对天然透明质酸进行结构改造和修饰,以期获得具有更优异的物理化学特性,同时保留透明质酸原有良好生物相容性的透明质酸衍生物。
目前,国内外大都是通过对交联剂的种类和特性、交联方法、交联工艺等的研究与综合分析,再利用H A多糖链中含羟基、羧基和乙酰氨基三种能被衍生的官能团特性,用不同化学试剂和这些官能团反应得到不同的H A衍生物,由此决定了这些H A衍生物在医学领域中应用的广泛性。
2 HA的交联改性
HA分子中羟基、羧基、N-乙酰氨基以及还原末端是可被化学修饰的四个部位,主要修饰方法有酯化、交联、接枝等。H A的化学结构和H A两个最常用的共价修饰部位—羧基和功能羟基如图1所示[1]。
2.1 羟基改性
2.1.1 与环氧化合物交联
HA羟基和环氧化合物、反应可以制备H A的交联材料。Malson和Lindqvist首先利用1,4-丁二醇二环氧醚(BDDE)作为交联剂,将H A进行了交联。反应机理是环氧化合物的环氧基在一定条件下打开,然后与H A的部分N-乙酰基-D-氨基葡萄糖上的6位碳上的羟基反应。凌沛学[2]等人在此基础上将反应物按一定比例在50℃下反应交联,随后纯化。而魏长征[3]等人则改良性在温度降为4℃时进行交联反应。
HA与BDDE交联产物比天然的H A在体内更稳定,作为组织生物材料其机械性能更好。目前,该产品已经在市场上得到广泛的应用。
2.1.2 与二乙基烯砜交联
二乙烯基砜(DVS)在室温下可与HA的羟基快速反应,得到性质变化很大的HA凝胶。产物在水中的膨胀率取决于凝胶交联度,交联度可由H A相对分子质量、HA浓度、反应介质pH值、HA/DVS比率来控制。HA初始浓度可为0.25%~50%,与DVS反应成凝胶后,用pH≤4的水溶液清洗,所得产物具有高度黏弹性,可作注射剂、器官移植配件及药物缓释系统。
未经修饰的H A凝胶表面光滑,其带阴离子特性不适合联合用药。而D V S交联H A制备的水凝胶具有微孔结构,在水和水溶液中平衡吸附容量明显高于普通H A,可应用于预防术后粘连。DVS-H A作麻醉药物缓释基质,也可延长麻醉药物持久作用时间。
2.1.3 与酸酐交联
HA的羟基可以与酸酐或者酰氯进行酰化反应生成酯类化合物。Takashi[4]报道了利用乙酸酐作为酰化试剂合成乙酰化透明质酸(AcHA)的方法。这种物质的物理化学性质因乙酰基的取代度不同而不同。乙酰取代度越高AcHA的疏水性越强。与H A相比,当取代度为3.0时AcHA类化合物表现出来超强的保湿和极好的柔肤作用。由于AcHA可溶于有机溶剂中,如90%的乙醇溶液,作为超强保湿剂不但可以用在水性基底的化妆品中,也可以用在油性基底的化妆品中。
2.2 羧基交联
2.2.1 与醇类化合物交联
HA羧基在一定条件下均可进行酯化反应,通过酯化反应,HA的理化性质及生物活性得到一定程度的改变。H A的酯化衍生物已广泛应用于生物和医药领域。
对醇类化合物研究反应经历了四个阶段,第一阶段:酯化产物无生物活性,主要提高了HA的稳定性;第二阶段:HA主要与具有药物活性的甾醇类化合物的羟基反应,生成的产物保留了药物原有的药理活性,但具有作用持久、规律的特点,有明显的缓释作用;第三阶段:控制HA分子中部分羧基与药物的羟基反应,其他羧基与无药物活性的物质酯化,提高了产物的稳定性,所得到的产物既具有第二阶段产物的特点,又具有第一阶段产物的特点。第四阶段:HA的羧基同时与两种或两种以上的具有不同药理活性的物质酯化反应。
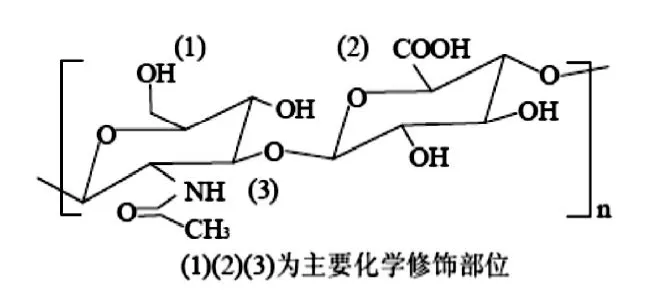
图1 HA的化学结构及主要化学修饰部位
Kana等[5]用酸性H A或HA-TBA在二甲基亚砜(DMSO)和甲醇存在下与三甲基硅重氮甲烷反应,生成透明质酸甲酯,HA经甲酯化后抗透明质酸酶的降解能力增强。HA甲酯的酯化程度不同,它的应用领域也不同,它可以用到化妆品、生物医药、伤口愈合、各种形式的组织工程支架如敷料、薄膜、纤维等其他更广的领域。
2.2.2 与酰肼化合物交联
酰肼化合物(Adipic acid dihydrazideADH)与HA连接后,剩余的一个N H2可与HA分子中其他羧基在连接,使H A分子内或分子间交联,在溶剂挥发后,可把柔软可流动的凝胶改性为机械硬度更大,可溶胀且具有良好的生物相容性和生物可降解性的H A水凝胶膜。另外,贺艳丽等[6]也对H A-A D H薄膜进行了生物相容性的研究,得出其具有良好的抗酶解性和生物相容性。
2.2.3 与氨基化合物交联
HA的酰胺化反应的溶剂一般是水或二甲基(DMSO),Danishefsky和Siskovic首先利用1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)将HA的羧基进行活化,在pH4.75时水溶液里进行了酰胺化反应。反应机理:羧基首先被EDC活化,生成不稳定的活性中间体,活性中间体与氨基化合物反应,生成酰胺化合物。而活性中间体很容易与水反应生成副产物N-酰基脲。为了避免这种副产物的产生,研究了其他活化羧酸基的方法,例如:利用EDC和1-羟基苯并三唑(HOBT)或EDC和N-羟基丁二酰亚胺(NHS)反应,得到比较稳定的活性中间体。人们也考察了在有机溶剂如DMF、DMSO中合成H A的酰胺化合物,H A钠盐首先转化为溶于有机溶剂的H A-TBA。Bellini和Topai就是利用HA-TBA在无水的DMSO中和1,1’-羰基二咪唑反应,得到比较稳定的H A-咪唑中间体,然后再与胺类化合物反应生成酰胺类化合物[7]。
2.2.4 与二硫化物交联
在酸催化作用下,二硫化物在乙醇中回流变成二酯,二酯肼解变成相应的二肼。SHU等[8]以H A溶于适量水中,搅拌同时加入一定量肼解的3,3’-二硫代丙酸(DTP)或4,4’-二硫代丁酸(DTB);用一定浓度的HCl调节pH,并使它保持在p H4.75,加入适量脱水剂碳二亚胺(EDC),反应一段时间后加Na OH调节pH至8.5,停止交联。继续搅拌24h,调节pH至3.5,将此酸性溶液用稀HCl进行透析,离心分离,冻干提纯得HA-DTBH和HA-DTPH。Shu等利用HA与二硫化物交联制得的凝胶薄膜,经性能测试后,显示其在伤口愈合和组织修复等临床应用方面有较大的潜在价值。
2.2.5 与壳聚糖交联
Lim等[9]利用壳聚糖作交联剂,溶解质量分数0.5%的透明质酸,调pH 3.6,加入一定质量的EDCI,保持p H不变,加入等体积的2%壳聚糖醋酸溶液,快速搅拌一段时间,50℃环境中烘4h,取出浸没于1mol/L的Na OH溶液中10min,中和其酸性,并用蒸馏水冲洗,烘干成膜。
姚子昂等[10]将壳聚糖与透明质酸以较低比例混合,由于透明质酸是一种带有负电荷的非晶物质,它能通过静电作用,增强壳聚糖分子之间是相互作用,分子间排列更加规整,且能提高膜的相对结晶度,因此能提高壳聚糖膜的结晶性。壳聚糖与透明质酸以较低比例混合时,两种分子相容性较好,膜表面结构均一,且透明质酸的混入可以提高共混膜的力学特性、透光性以及对葡萄糖的渗透速率。且共混膜与角膜细胞相容性好,可以支持细胞在膜上长成密集单层,能扩展它在组织工程中的应用。
3 展望
本综述报导的交联透明质酸改性方法简单易行,条件容易控制,具有良好的生物相容性和生物可降解性,是较理想的生物材料和药物载体,可用于药物的缓控释放。但交联产物的低毒性以及其他性质还亟待解决,且HA自身除交联改性外,还有许多其他性能有待进一步开发利用。今后将重点对制备HA衍生物的交联基团以及交联剂种类、交联机制进行研究。随着新型、天然交联剂的不断开发研究,HA衍生物种类会更加丰富,其性能会更加完善,新型交联HA产品会上市,进一步开拓H A的新用途。
[1]胡帼颖.透明质酸化学交联修饰及其衍生物的体外降解研究[D].天津:天津医科大学生物医学工程,2004.
[2]凌沛学,陈建英,贺艳丽,郭学平,汪敏,刘杰,刘建建,荣晓花.一种注射用交联透明质酸钠凝胶及其制备方法:中国,CN101502677B[P].2008-02-04.
[3]魏长征,奚宏伟,朱琳,蒋丽霞,吴剑英,王文斌.一种低温二次交联透明质酸钠凝胶的制备方法:中国,CN103146003A[P].2013-03-06.
[4]Oka T.Low molecular weight acetylhyaluronate,skin-softing composition,method of manufacturing the same,and method of purifying the same.US5679657,1997.
[5]Hirano K.Preparation of the methyl ester of hyaluronan and its enzymatic degr— adation.Carbohydrate Research,2005,340(14):2297-2304.
[6]陈建英,宋海波,贺艳丽,等.交联透明质酸凝胶膜的制备及其生物
相容性的研究[J].生物医学工程研究,2009,28(2):104-107.
[7]Bellini,D,&Topai,A.W O200001733,2000.
[8]Shu X Z.Disulfide cross-linkedhydrogels[J].Biomacro-molecules,2002,3:1304-1311.
[9]Lim S T.Preparation and evaluation of the in vitro drug release properties and mucoadhesion of novel microspheres of hyaluronic acid and chitosan[J].Journal of controlled release,2000,66:281-292.
[10]姚子昂,吴海歌,韩宝芹,等.壳聚糖-透明质酸共混膜性质的研究[J].高技术通讯,2004,14(9):97-99.