编写标准结构要素中的问题剖析
2014-10-10孙金莲
孙金莲
(湖南千山制药机械股份有限公司,湖南 长沙 410100)
1 标准的结构要素
通常标准的结构要素由资料性要素和规范性要素组成。
按要素的性质以及它们在标准中的具体位置可分为:
(1)资料性概述要素:封面、目次、前言、引言;
(2)规范性一般要素:名称、范围、规范性引用文件;
(3)规范性技术要素:术语和定义、符号、要求、规范性附录;
(4)资料性补充要素:资料性附录、参考文献、索引等。
在上述要素中,封面、前言、名称、范围为必备要素,其余为可选要素。
2 编写标准结构要素中容易出错的问题分析
2.1 目次(可选要素)
目次的作用是表明标准的层次结构、引导阅读、便于检索。注意事项:
(1)目次虽然是可选要素,但是一般建议列入标准。
(2)目次中的条目号、标题与文本中的条目号、标题应该一致。另外,要求章的条目标题与实验方法章的条目标题应该一致。错误案例:
(目次中)分类与标记——(文本中)标记
(目次中)术语和定义——(文本中)无此章
材料(要求)——材质试验(试验方法);表面质量(要求)——外观试验(试验方法);电气安全(要求)——电气系统试验(试验方法)
……
(3)“术语和定义”章的术语不应在目次中列出。错误案例:
3 术语和定义
3.1 真空乳化Vacuum emulsification
3.2 水相罐Water phase tank
3.3 油相罐Oil phase tank
3.4 乳化罐Emulsiftication tank
3.5 均质器Homogenizer
分析:术语条目的编号在形式上虽与章、条的编号相似,但章、条的编号具有隶属性,下脚点后面的数字隶属于下脚点前面的数字,1个层次中有2个及以上的条时才可设条;而术语的条目编号是一种代号,其作用是为了提及和查找方便。所以,即使只有一个术语,也应编条目号。
2.2 前言(必备要素)
前言由特定部分和基本部分组成。
2.2.1 制定标准前言和修订标准前言的范例
例1:制定标准前言
本标准依据《药品生产质量管理规范》(2010年修订版)、GB 28670—2012《制药机械(设备)实施药品生产质量管理规范的通则》的相关要求和GB/T 1.1—2009《标准化工作导则 第一部分:标准的结构和编写》给出的规则而制定。(这属于前言的特定部分)
本标准由中国制药装备行业协会提出。
本标准由全国制药装备标准化技术委员会(SAC/TC356)归口。
本标准主要起草单位:……。
本标准参加起草单位:(有才写)。
本标准主要起草人:……。
(这些属前言的基本部分)
例2:修订标准前言
本标准依据《药品生产质量管理规范》(2010年修订版)、GB 28670—2012《制药机械(设备)实施药品生产质量管理规范的通则》的相关要求和GB/T 1.1—2009《标准化工作导则第一部分:标准的结构和编写》给出的规则而修订。
本标准发布后代替JB/TXXXX—2004《XXXXXX》。
本标准与JB/TXXXX—2004相比,除编辑性修改外主要技术变化如下:
删除了原标准的XXX、XX、XXX……。修改了原标准的下列条款:
标准名称修改为:XXXXXXX。
4.1 XXXXXXX(见4.1条(本标准),2004版XX条)。
4.3.2 XXXXXXX(见4.3.2条(本标准),2004版XXX条)。
……
增加了下列条款:
(增加条款全部抄录下来)
本标准由中国制药装备行业协会提出。
本标准由全国制药装备标准化技术委员会(SAC/TC356)归口。
本标准主要起草单位:……。
本标准参加起草单位:(有才写)。
本标准主要起草人:……。
本标准所代替标准的历次版本发布情况为:
YY XXXX—1995
JB/T XXXX—2004
2.2.2 错误分析
上述示例中的错误分析如下:
(1)前言中说明标准中的附录哪些是规范性附录,哪些是资料性附录。GB/T 1.1—2009规定“前言”不描述附录性质,因目次内容已经标识,故不重复。
(2)把产品的营销宣传资料或编制说明中的资料写进前言(如产品研制过程、专利技术、用户反映和企业形象等)。起草人是想为自己的产品和企业做宣传,这不符合编写规则。
(3)把企业标准的发布当成行标的第1次发布(如新制订的标准写成第2次发布)。因标准的封面有发布时间和实施时间,修订标准的前言有本标准历次发布情况介绍,故标准编写规则规定,无论第1次,还是第2次发布都不应写。
(4)规定标准使用期限(如本标准自发布之日起有效期3年,到期复审)。乱作规定,不符合编写规则。
(5)本标准规定规范性引用文件中的推荐性标准使用年代号,强制性标准不使用年代号。注日期的标准表示只引用标准的该版本或其中的条款;不注日期的标准是跟踪引用。
(6)“本标准由全国制药装备行业标准化技术委员会(SAC/TC356)归口管理 。”此标委会名称书写不正确。
(7)修订标准中的修订条款一定要与原标准做比较,详见前言范例2的编写格式。
编者建议标委会秘书处在制定或修订标准发布实施后,给标委会委员、起草单位、制造单位各赠送1份,便于标准的贯彻执行和5年后的修订对比。
2.3 名称(必备要素)
名称要准确(概括标准主题)、简练(不涉及不必要的细节)、术语统一(先查看相关术语标准)。
2.3.1 举例说明
(1)中药矿物药及其煅制品、密度与松脆度测定方法——中药矿物药及其煅制品视密度测定方法
前面名称是起草单位的命名,破折号后的名称是审查确定的名称。标准中测定的是视密度而不是密度,松脆度是通过矿物药煅制前后视密度测定值计算判断,并非测定出来的,修订正确。
(2)中药汤剂煎煮机——中药煎药机
审查会上,专家提出,民间的“煎”和“煮”是不同的概念,“煎”是炒熟的意思,“煮”是加水烧熟的意思,因此“煎”、“煮”放一起是矛盾的。中药煎药机的定义:中药饮片加入适量的水,经加热提取制成汤剂的机器。因此,原名称中的“汤剂”、“煮”都去除了,保存“煎”是采用民间的习惯称谓。
(3)PP塑料输液瓶吹塑成型机——聚丙烯输液瓶吹塑成型机
PP塑料输液瓶在包材标准中称作“聚丙烯输液瓶”,审查会上确定应与包材标准用词一致。
(4)非鼓泡传氧生物反应器——非鼓泡传氧细胞培养罐
《制药机械术语》标准规定:利用培养基使动植物细胞增殖的设备叫培养罐,隶属于原料药设备中的发酵设备类;而生物反应器是隶属于原料药设备中的反应设备。修订与术语标准一致。
(5)高效包衣机——滚筒式包衣机
依据《制药机械术语》标准4.2.5.2而修订。
2.3.2 标准名称三要素的体现
名称中主体要素必不可少。示例中带下划线的部分是主体要素。
例1:只有主体要素——中药液体制剂包装机
例2:主体要素+补充要素——机械电气安全 机械电气设备 第1部分:通用技术条件
例3:引导要素+主体要素——制药机械 术语
例4:引导要素+主体要素+补充要素——农业机械和设备 散装物料机械 装载尺寸
2.4 范围(必备要素)
范围的文字应简洁,以便能作内容提要使用。
2.4.1 一般格式
本标准规定了……(即为标准中章的标题内容)。本标准适用于……(以下简称XXX机)。不适用于……。
2.4.2 存在的问题分析
规定的内容与文本中章标题不一致;适用范围中需要限制的条件表述不确切。在此规定了标准名称的简称后,以下的章、条内容提及标准名称一律使用简称。
2.5 规范性引用文件(可选要素)
2.5.1 示例分析(正确示例)
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件;凡是不注日期的引用文件,其最新版本(包括所有的修改清单)适用于本文件。
GB/T 191 包装储运图示标志
GB/T 1184—1996 形状和位置公差未注公差值GB/T 3766—2001 液压系统通用技术条件
GB 5226.1—2008 机械电气安全 机械电气设备第1部分:通用技术条件
GB 6388—1986 运输包装收发货标志
GB/T 9969 工业产品使用说明书总则
GB/T 10111 随机数的产生及其在产品质量抽样检验中的应用程序
GB/T 13306标牌
GB/T 13384 机电产品包装通用技术条件
GB/T 16769 金属切削机床噪声声压级测量方法
GB 23820—2009 机械安全偶然性与产品接触的润滑剂卫生条件
GB/T 24342—2009 工业机械电气设备 保护接地电路连续性试验规范
GB/T 28671 制药机械(设备)验证导则
《中华人民共和国药典》(2010年版 二部)国家药典委员会
2.5.2 注意事项
(1)编排格式:标准代号不顶格,缩进2个字;标准编号与标准代号空半个字;标准名称与编号或年代号空一个字。
(2)引用的要求:引用文件中不包含非公开的文件;前言、引言、资料性引用文件中出现的标准、文件;标准编制过程中的参考文件。
(3)标准条文中出现的引用标准应不写标准名称,是否写年代号应与规范性引用文件一致。
(4)引用的范围:标准条文(即分类和标记、要求、试验方法、检验规则、包装、规范性附录……)中出现的所有国标、行标、地标、国内有关文件等。
(5)排列顺序:国标、行标、地标、国内有关文件、ISO标准、IEC标准、ISO或IEC有关文件、其他国际标准或其他国际有关文件。GB、ISO、IEC按标准顺序号排列,由小到大。行业标准、其他国际标准先按标准代号的拉丁字母顺序排列,再按标准顺序号排列。例如,JB应排在YB的前面;拉丁字母J在Y之前。
(6)引用的方式:注日期引用和不注日期引用2种。注日期引用的情况:只适用本版本;只适用本版本的某些条款。不注日期引用:跟踪引用,即无论如何更新都适用。
(7)引用原则:原则上,上一级标准不能引用下一级标准,即起草国标不引用行标及以下标准,起草行标不应引用地标及企标。
(8)引用文件之后不加标点符号。
(9)起草单位应该对所引用的标准进行认真研究,特别是关系到成品质量的标准,如药典、包材标准等。
(10)有些标准包括范围很广,引用时研究具体引用的条款和相应的试验方法,要体现可操作性,如压力容器、电气、气动、易燃易爆标准等。
(11)要求条款是引用的XX标准,试验方法最好也引用或参考XX标准中对应的试验方法。
出错情况分析:
(1)起草标准参考过的标准、文件(如前言中提及的GMP、GB 27680通则等)引入规范性引用文件;
(2)标准条文中提及过的文件引入规范性引用文件;
(3)标准条文中的注、图注、表注中提及的文件引入规范性引用文件;
(4)标准中资料性附录提及的文件引入规范性引用文件;
(5)标准中的示例所使用或提及的文件引入规范性引用文件;
(6)在“术语和定义”一章中,标示术语所出自的标准引入规范性引用文件。如“GB/T 16952界定的术语及下列术语适用于本文件”,这里的GB/T 16952就不应引用。
2.5.3 错误示例
例1:引用标准的排列顺序,先按强制性标准顺序,后按推荐性标准顺序排列。
GB 5226.1—2008 机械电气安全 机械电气设备第1部分:通用技术条件
GB 6388—1986 运输包装收发货标志
GB 23820—2009 机械安全偶然性与产品接触的润滑剂卫生条件
GB/T 19 包装储运图示标志
GB/T 1184—1996 形状和位置公差未注公差值
GB/T 3766—2001 液压系统通用技术条件
……
例2:推荐性标准使用年代号,强制性标准不使用年代号。
GB/T 191—2008 包装储运图示标志
GB/T 1184—1996 形状和位置公差未注公差值
GB/T 3766—2001 液压系统通用技术条件
GB 5226.1 机械电气安全 机械电气设备 第1部分:通用技术条件
GB 6388 运输包装收发货标志
GB 23820 机械安全偶然性与产品接触的润滑剂卫生条件
……
例3:引用操作手册、规程、指南、购销合同。
《中国药品检验标准操作规范(2010版)》中国药品生物制品检定所中国药品检验总所编写
上述既不是标准,也不是文件,不能引用。
例4:条文中引用了标准名称。框中的内容表示删除。
微波设备的辐射卫生标准应符合GB 10436—89《作业场所微波辐射卫生标准》中第2条的规定。
例5:引用文件中的标示与国际文件存在一致性程度的标识。
GB/T 191 包装储运图示标志(eqv ISO 780:1997)。
说明:框中的部分为不符合GB/T 1.1—2009的编写规则。GB/T 1.1—2009版规定了在规范性引用文件清单所列的标准中标示与国际文件的对应关系的标示方法,只有正在起草的与国际文件存在一致性程度的我国标准,才需按GB/T 20000.2的规定标示。
例6:引用过时的标准,造成注日期引用的文件条款全然不对。
GB 5226.1—2002 机械安全 机械电气设备 第1部分:通用技术条件
应该是:GB 5226.1—2008 机械电气安全机械电气设备第1部分:通用技术条件
2.6 术语和定义(可选要素)
“术语和定义”的给出是为理解标准中易产生困惑、歧义、误解、混淆的专用词所必须的定义,引导人们正确理解和执行标准,也是对同一事物或客体形成一致的概念。定义应用言简意明的文字(包括图、公式等辅助说明内容)进行描述。
常见问题分析如下:
(1)本文件没有术语硬要拼几个凑数。
(2)术语编排格式不对。
(3)术语也可分级排列。
(4)只有一个术语也要编条号;术语不列入目次。
(5)术语定义要准确、简洁,做到言简意明。
例1:半自动硬胶囊充填机semi-automatic hard capsule filling machine
自动完成空心胶囊送囊、定向播囊、真空分囊、定量充填药物、人工辅助完成合囊的机器。
分析:自动硬胶囊充填机已有定义,这个术语的核心是定义“半自动”。
例2:储液桶liquid reservoir
连接于药液输送管路上的用于储备药液的容器。
包容物Fill material
封装在软胶囊壳内的液体(含混悬性药液)、稠膏、颗粉粒状或片状固态物料等。
说明:以上术语的定义框出部分表示删除,删除后定义简练、确切。
(6)术语定义时应查明在其他标准中是否已经定义,避免重复和矛盾。建议对制药机械产品名称及相关术语定义时请先查看《制药机械术语》标准,从中得到借鉴和启发。
(7)文件中引用了其他术语标准中的术语的编辑格式。
例1:双管板换热器double tube heat exchanger
两端各有两块管板的列管式换热设备。
[引自GB/T 15692—2008 制药机械术语3.6.2.5]。
例2:管程数Nt系指介质沿换热管长度方向往、返的次数。
[引自GB 151—1999 管壳式换热器3.9.3]。
2.7 分类和标记(可选要素)
产品分类和标记一般按YY/T 0216—1995制药机械产品型号编制方法进行。
2.7.1 产品分类和标记的正确范例
1 分类
抗生素玻璃瓶粉剂分装机按分装型式可分为气流分装和螺杆分装。
2 标记
(1)型号编制
抗生素玻璃瓶粉剂分装机型号编制按YY/T 0216—1995的规定,如图1所示。

图1 抗生素玻璃瓶粉剂分装机型号的编制
(2)标记示例
示例1:KFQ 5/30型:表示适用5~30 ml规格的抗生素玻璃瓶粉剂气流分装机。
示例2:KFG 5/30型:表示适用5~30 ml规格的抗生素玻璃瓶粉剂螺杆分装机。
2.7.2 易出现的问题
在产品分类和标记中容易出现的问题有:
(1)把产品的基本参数编入分类章。
例:三效逆流降膜蒸发器标准的分类与标记摘抄。
1 分类与标记
1.1 规格系列
规格系列有:500;1 000;1 500;2 000;4 000。
1.2 基本参数
基本参数如表1所示。
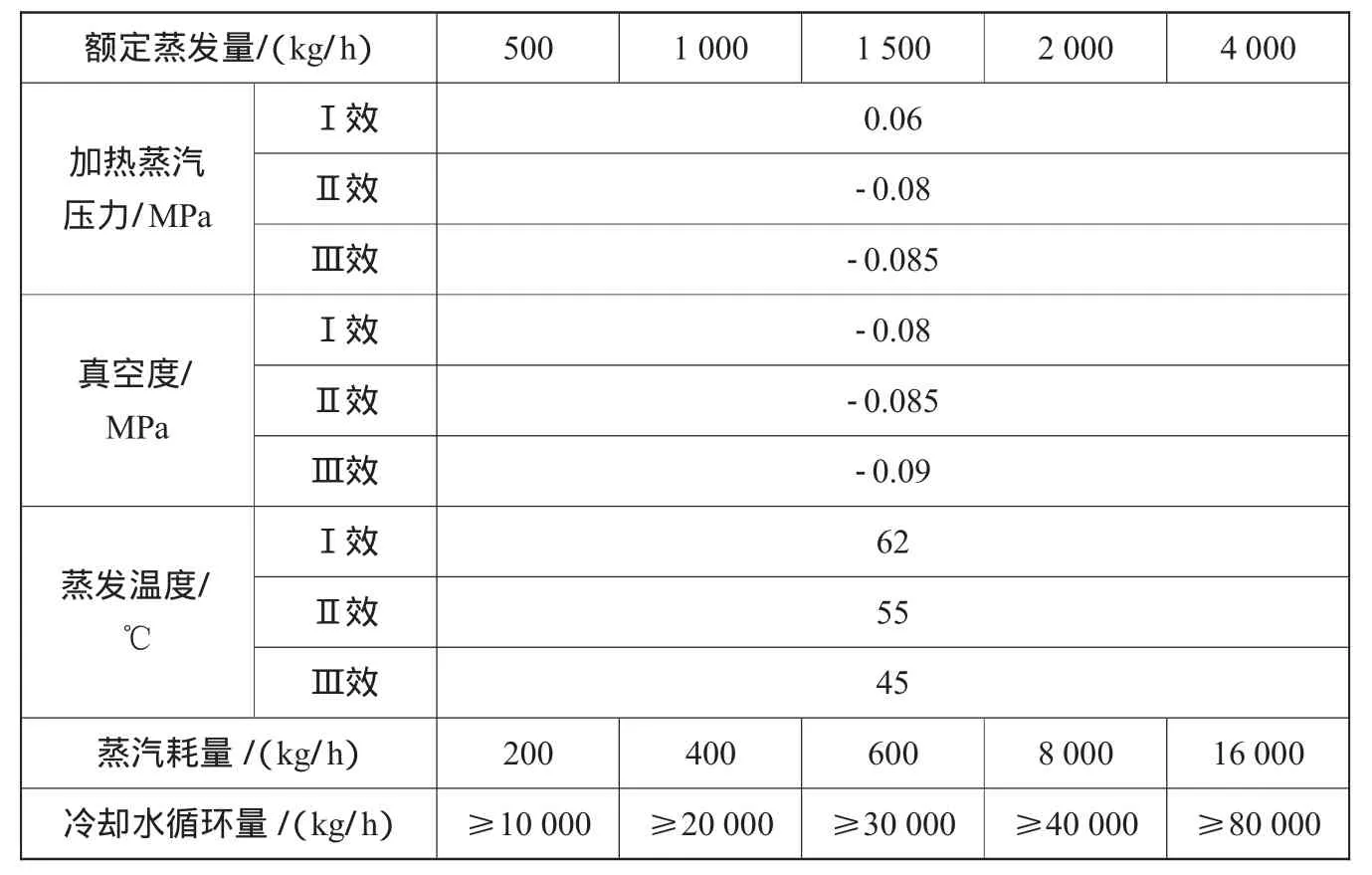
表1 基本参数
1.3 标记
1.3.1 型号标记
蒸发器型号编制应符合YY/T 0216的规定。
1.3.2 标记示例
JZN1000型表示蒸发量为1 000 kg/h的三效逆流降膜蒸发器。
分析:示例中1.1和1.2与章的内容不符,应该写分类,没有分类就不写。重要参数可编入“要求”章。
(2)把机器结构的组成部分当成分类。
例:产品分类
分装机类型为由分装孔真空吸取定量的药粉,再经净化干燥压缩空气将药粉吹入抗生素玻璃瓶内的机器。
分析:编辑的是分装机的工作原理,不是分类。产品没有分类就省略。
(3)引用了YY/T 0216—1995标准,而型号编制又不按其执行。
(4)分类过细。既按结构形式分类,又按功能分类,甚至还按模具种类分类。一种机器应该只选择一项主要特征进行分类。
(5)标准章题命名错误。如果机器没有分类,标题应该是“标记”,不应写成“型号与标记”。
2.8 要求(可选要素)
本要素是规范性技术要素的核心内容。在产品标准中以单独一章列出。其主要包括3个方面的内容:(1)给出标准所涉及的产品、过程或服务方面的所有特性。(2)可量化特性所要求的极限值。(3)对每个要求,可引用测定或检验特性值的试验方法和测量方法,或者直接规定试验方法和测量方法。
2.8.1 选择技术要素
选择技术要素的3个原则:目的性原则、性能特性原则、可证实性原则。
2.8.1.1 目的性原则
此原则为保证产品的适用性,促进相互了解。不同的时期有不同的目的原则:(1)开发期。验证设计标准,要求是全方位的。(2)制造期。工艺、工装,即作业指导书。(3)销售期。使用性能,即设备功能是否达到。
2.8.1.2 性能特性原则
此原则应该用性能参数来表述,而不是根据设计或描述性的特性来表述。性能特性是与产品的使用功能有关的特性,是产品在使用中才能体现出来的特性;描述性特性是与产品的结构、设计相关的具体特性,是在实物或图纸显示出来的特征(如机械产品在图纸中描述的尺寸、形状、表面粗糙度等)。因此,设计和工艺(制造)要求不写入标准。压力容器产品除外。
例1:吹瓶用气体管路焊接应采用氩弧焊,管路连接应便于拆卸。
分析:用描述性的特性来表述。这是制造过程要求不应列入标准。
例2:安瓿一体机自身应带A级空气风淋装置。
分析:用设计特性来表述,不可取,且2010版GMP规范已经规定吹灌封设备自身应带A级空气风淋装置。标准就应该用性能参数表述。应修改为:
安瓿一体机自带的A级空气风淋装置应符合《药品生产质量管理规范》规定的A级技术指标。
2.8.1.3 可证实性原则
标准中所有“要求”都要能写出试验方法,没有试验方法的“要求”不可写入标准。
产品标准“要求”章节的内容:着重规定产品的性能技术指标要求,产品标准的要求内容是以“结果”居多。所以产品标准中的产成品质量是重中之重。
2.8.2 通常编制产品标准的要求章节的内容
(1)材料:一般材料不列入产品标准。为了保证产品质量和安全要求时才列入,如为符合GMP或压力容器制造指定的材料。
(2)外观(或表面质量):对整机表面缺陷、颜色以及味觉、嗅觉、视觉、手感等做出的规定。不应把零部件的表面粗糙度值或管道的泄漏要求包括在内。
(3)性能:包括设备性能、产成品质量2个内容,一般设备性能编前,产成品性能编后,层次分明,条理清晰。
(4)设备(使用)性能:生产能力、功率、效率、运转率、速度、灵敏度、寿命、接口和互换性等。
(5)设备性能内容如下(不是每项标准全选,根据实际需要选取):
1)压力容器(管道):对产品的设计、制造、验收的标准依据和设计制造资质做出规定(属于压力容器产品才有)。
2)结构性能:保证产品质量和安全的必备结构做出特性值的规定。注意不要编成设计描述。
3)运转性能:空运转平稳、无异常声响;负荷运转程序控制正确、介质温度、压力、转数等控制正确;噪声、破损率等达标。
4)密封性能:气(汽)、液、润滑系统不泄漏。
5)控制和显示:产量、批次、速度、时间、温度、压力、灭菌值、工作周期等。
6)安全互锁:保证设备、环境、成品质量和人身安全的联锁控制。
7)健康、安全、环境保护:对电气安全、气动安全、防爆安全、防污染、防辐射、排污等要求做出规定,并规定极限值。遵守有关法规和强制性标准。
8)能耗指标:直接消耗能源的产品才做规定。
(6)产成品质量:产成品是设备功能的结果,也是设备服务的最终对象。其质量指标应该是商业型标准的精髓,缺了它就不成其为标准。制造设备的成败就由产成品是否合格来决定。因此,产成品的质量指标应做到先进、可靠、可验证。
2.8.3 编写“要求”章应注意的问题
编写“要求”章应注意的问题如下:
(1)每一条要求内容只对应一个试验方法,如一条内容需多个试验方法的尽量把要求内容分几条编写;如果一个内容有多种试验方法,只提倡选择其中最可靠的一种试验方法。
(2)要求的条款中不应包含有关合同的条款,如索赔、担保、费用计算、售后服务等内容。
(3)要求的编排程序与质量评定(即试验方法)程序尽可能协调一致。
(4)性能条款的排列应便于试验方法而编写。建议按结构特性值条款、空载试验中完成检验的条款、负载试验中完成检验的条款、安全要求条款、产成品质量条款的顺序排列。
(5)要求中的各项指标一般应给出定量数值,便于验证。
(6)其他章的内容有属要求章内容的还应在该章中列出,不能遗漏。
(7)制造过程的要求一般不列入。
(8)一般的原材料要求应不列入。
(9)一般产品的制造工艺要求应不列入。
(10)没有验证方法的要求不列入。
(11)不需验证的要求不列入。
(12)不能量化的要求不列入。
(13)不要把负载试验中完成的要求条款编入产成品质量条款,这样限制了这些要求条款的试验范围,也提高了试验的条件。
例1:国标旋转式压片机送审稿摘抄
1 压片质量
(1)压片机的压片力应连续可调,主压片力应显示。
(2)有自动控制片重的压片机应有单剔或群剔的功能,每次群剔中从不合格片通道中流出的合格片数应不大于不合格片数的4倍。
(3)压片机应有冲模超载保护功能。
(4)片剂重量差异限度应符合表1规定。
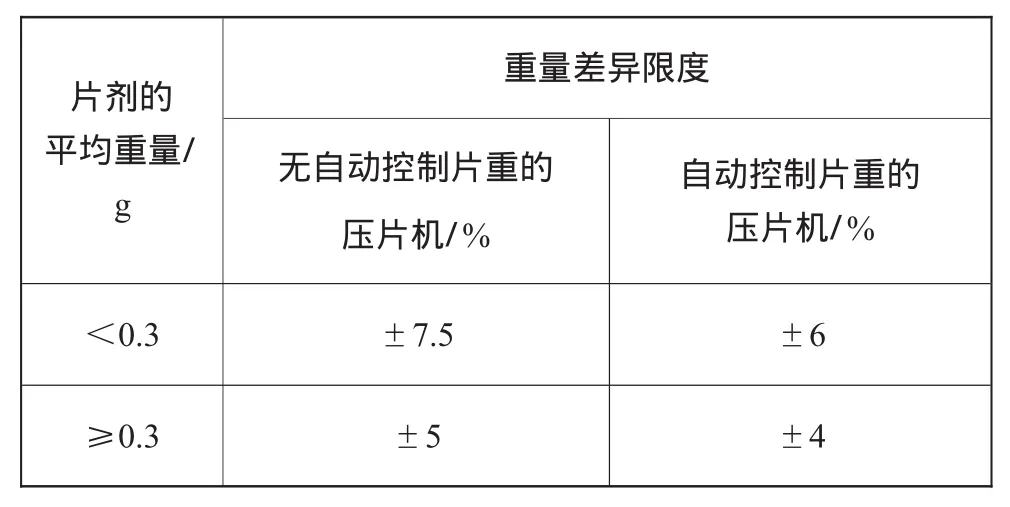
表1 片剂重量差异限度
(5)物料损耗率应不大于0.5%。
分析:(1)前3条并非属于压片质量,它是压片机的性能,不应与压片质量条款编辑在一起;(2)压片质量的试验条件比较苛刻,要用专门指定的试验物料,而前3条只要在负载试验情况下都能验证,限制了其试验范围。
例2:抗生素玻璃瓶粉剂气流分装机标准征求意见稿摘抄
5.4.12 分装、加塞质量
5.4.1 2.1 分装量差异应符合 《中华人民共和国药典》(2010年版二部)附录ⅠB《注射剂》中的规定。
5.4.1 2.2 加塞后胶塞的T型平面应与瓶口平面紧贴,合格率应不小于99.5%。
5.4.1 2.3 玻璃瓶破损率应不大于0.1%。
分析:最后一项不属分装、加塞质量,它是分装机的性能,不应与分装、加塞质量编辑在一起,它在任何负载试验下都能进行破损率试验。
2.9 试验方法(可选要素)
2.9.1 试验方法
试验方法是测定标准化对象特性值是否符合规定要求的方法。试验中要对测试的条件、设施、方法、顺序、步骤以及抽样和结果进行数据统计处理做出统一的规定。
2.9.2 成品质量试验的内容和格式
成品质量试验的内容和格式如下:
(1)试验条件:水、电、气、环境要求。
(2)试验介质:指定试验介质及要求。
(3)包装材料:符合的包材标准或指定的要求。
(4)试验设施:辅助设施或设备。
(5)试验物料名称、质量、配比要求。
(6)试验仪器、设备、检验器具名称和精度要求。
(7)针对试验物料确定具体(不是参数范围)工艺参数(如转数、温度、时间等)。
(8)操作步骤:包括开机、投入试验物料、运行程序等。
(9)取样规则,即取样位置、取样时间、取样次数、每次取样量、保存方法等。
(10)检测方法、计算公式及判定规则。
产成品质量试验的方法是指定一种价廉、易采集、通过负荷试验能达到产成品质量指标的原料,根据选定的原料规定确切的工艺参数和操作步骤、取样规则、检测方法、计算公式,也就是说能指导第三方按照标准中的产成品质量试验方法操作,能得出合格的检测报告,证明该产品能达到标准规定的产成品质量指标。
2.9.3 工作条件编入负荷试验条件的重要性
试验条件、试验介质、包装材料、试验设施这些“工作条件”是供需双方的一个接口,配合不好,影响机器使用性能。也是设备要达到使用性能必须具备的外部条件,其重要性可能成为影响设备能否正常使用的决定因素,因此,它将成为供需双方对产成品质量仲裁的依据之一。其次,是制约制造单位与使用单位的相互配合,达到产品使用的最佳状态的接口和设备安装确认时验证的主要内容之一。它能指导设计人员的设计,即设计时如何选用和设置介质进入设备的接口和管道连接方式;确定介质通过的腔室是否属于压力容器部件,并按相关规范设计;正确布局主机与辅助设施的位置;同时根据包装材料的规格尺寸、形状等设计传送、定位、装夹包装容器的合理结构。综上所述,试验方法中的“工作条件”内容必须引起起草人的重视,做到准确无误。
2.9.4 编写“试验方法”的注意事项
编写“试验方法”的注意事项如下:
(1)试验方法一般都应设条题,便于与要求的内容对照,以免漏检项。
(2)有专门标准规定的试验方法直接采用。
(3)“要求”章中的每条要求均应有相应的试验方法。试验编排顺序应尽可能与要求条款的顺序相同。
(4)一项要求内容原则上只规定一种试验方法。(5)试验仪器、设备只规定精度和性能要求,有效检定周期内使用。不要规定制造厂或其商标名称。
(6)试验结果数据应与技术要求量值的有效位数一致。
(7)对有害物质的试样和有某种危险的试验应加以说明并规定防范措施。
(8)对试验用的标准样品应提出检定和保存方法的规定。
(9)试验方法的描述不应采用要求型条款形式。错误示例:
例1:试验结果应达到XX条的要求。
例2:灌封机的负载噪声应按GB/T 16769的规定测试。
例3:液压系统在1.25倍额定压力下保压4 h,查验系统压降应不大于1 MPa。
(10)试验方法中不应引用合同、使用说明书、操作规程,引用了标准规定的方法就无需重复抄袭其内容。举例说明:
例1:装量差异按《中国药品检验标准操作规范(2010版)》“注射剂”中的“装量差异”检查法试验。
分析:引用的操作规范既不是标准,又不是文件,不能引用。确实可行就从操作规范中摘录下来,要么直接引用药典。
例2:按《中华人民共和国药典》(2010年版 二部)附录IA的重量差异检查法,每一袋随机抽取供试品20片,精密称取总重量,求得平均片重后,再分别精密称取每片的重量,每片重量与平均片重相比较,按表2的规定,超出重量差异限度的不得大于2片,并不得有1片超出限度的1倍。
分析:框去部分是重复药典规定的方法,已经引用了无需重复抄袭。应该修改为:
按《中华人民共和国药典》(2010年版 二部)附录I A《重量差异检查法》依次检查4袋样品,全部合格。
2.1 0 附录(可选要素)
规范性附录是技术要素,属标准的一部分。
资料性附录是给出对理解或使用标准起辅助作用的附加信息,属参考资料。
编写附录注意的问题:
(1)所有附录的排列顺序均按正文中出现的先后顺序给出,资料性和规范性不分开排列。每个附录均应另起一页编辑,不能接排。
(2)所有附录均应在标准正文中提及,即指明它的去处或服务的对象。
(3)正文中提及的方式:资料性附录是“参见附录A”,而规范性附录是“按或见附录A”。
最近笔者在上海审定了2项国标,其中的附录编辑都不理想,举一例来剖析。
例:矿物药材及其煅制品视密度测定方法……
3.4 计算方法
3.4.1 矿物药材及其煅制品视密度按式(1)计算

式中 ρ——样品的密度,kg/m3;
m——样品质量,kg;
m1——样品封蜡后排开水的质量,kg;
m2——样品封蜡后质量,kg;
ρ蜡——石蜡的密度,0.9 kg/m3;
ρ水——测定温度下水的密度,kg/m3。
3.4.2 数据修约
试验结果按照GB/T 8170规定修约至小数点后一位。
3.5 试验报告
试验报告包括以下内容:
(1)样品名称、来源、产地;
(2)批号;
(3)依据标准;
(4)试验人员;
(5)校审人员;
(6)试验环境;
(7)试验结果;
(8)试验日期;
(9)备注。
附录A
视密度相对变化率计算

式中 SC—煅制药物的视密度相对变化率;
ρ0—矿物药材煅制前的密度,g/cm3;
ρ1—矿物药材煅制后的密度,g/cm3。
分析:附录A原本是属于3.4条中的内容,而在3.4条中没有提及,另外编辑格式也不对。解决的办法是直接编入正文,因为3.4主要内容是计算方法,可以编成:
3.4.1 矿物药材及其煅制品视密度按式(1)计算:
3.4.2 视密度相对变化率计算(或是视密度相对变化率计算见附录A)
3.4.3 数据修约
附录A
(规范性附录)
视密度相对变化率计算
附录B
试验报告格式(供参考)
分析:附录B是属于3.5条的附加内容,应该在3.5条中增加3.5.2试验报告编写格式参见附录B,附录B的编写格式应为:
附录B
(资料性附录)
试验报告编写格式
B.1 试验报告表格
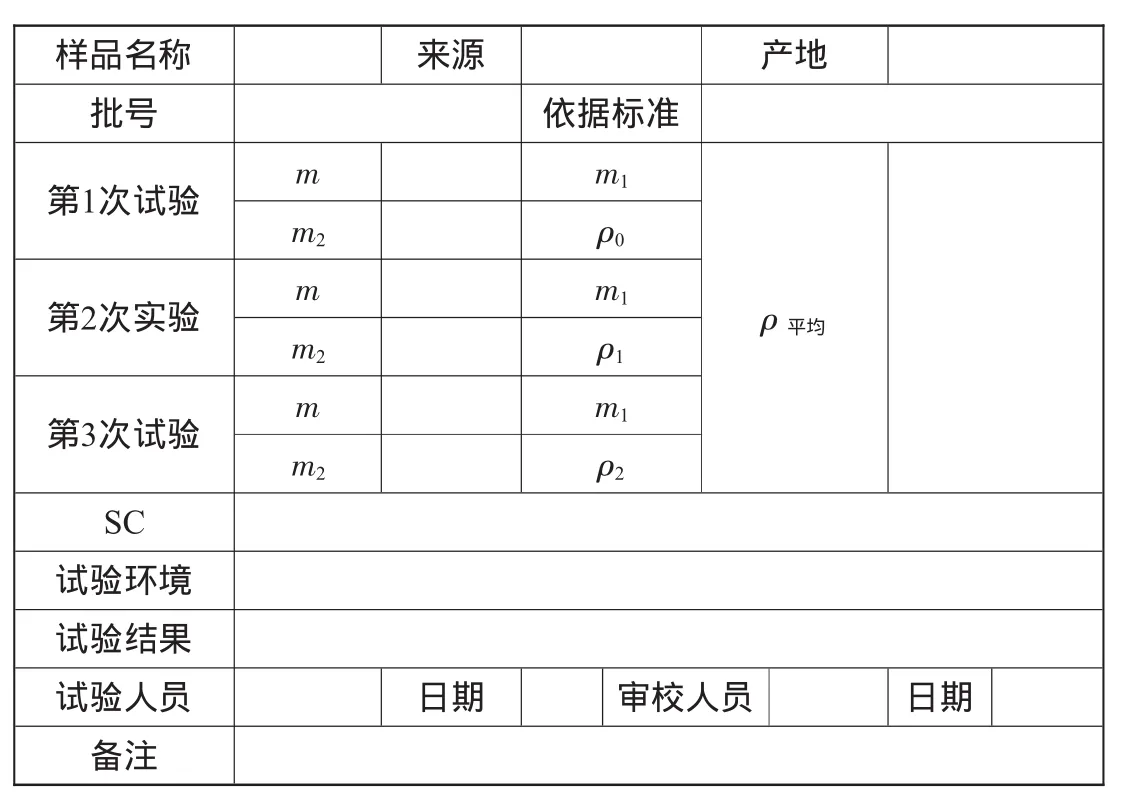
表B.1 试验报告
2.1 1 标准的层次及章、条、项、段的编排
2.1 1.1 部分
部分的排序是按阿拉伯数字1、2、3……顺序进行。部分的引导要素和主体要素是相同的,而补充要素应不同。部分不应再分部分。
2.1 1.2 章
章是标准内容划分的基本单元。按阿拉伯数字1、2、3……顺序编号,编号从“范围”开始。每一章应有标题。
2.1 1.3 条
条是章的细分。条在章的基础上可增加5个层次:如5.1.1.1.1.1,也最多只能增加5个层次。同一层次中有2个及2个以上的条时才设条。如5.1、5.2……。没有5.2就不能设5.1。第1层次的条宜给出标题。在某一章或某一条中,同一层次的条,有无标题应统一。无标题的条下面不能再分条。如果是由一段后跟冒号的文字引出的项,也就是说没有条题的条下面只能分项。无标题的条中可用黑体字强调关键术语或短语,有代替条题的作用。列项条款中也可用黑体字强调关键术语或短语来代替条题内容。
2.1 1.4 项
列项应由一段后跟冒号的文字引出。列项的各项之前应使用列项符号(破折号或圆点),同一层次的列项符号应统一。如果需要识别列项,应在各项之前使用小写拉丁字母编号(即不再使用破折号或圆点),后带半圆括号。
具体的情况有:(1)有条题的条,由一段后跟冒号的文字引出项;(2)由有条题的条下面直接引出项;(3)无条题的条,由一段后跟冒号的文字引出项;(4)如果在字母列项的某项中进一步细分成需要识别的若干分项,则使用阿拉伯数字编号,后带半圆括号。
2.1 1.5 段
段是章或条的细分,段不需要编号。当有标题的条下面再分条时,其下不能出现悬置段。应该将其内容编入分条款中。
2.1 2 其他值得注意的问题
2.1 2.1 标准中的同一用语前后不一致
例1:灭菌时间FH出现3种命名法。
1)要求中:冷点当量灭菌时间FH≥100 min。
2)附录标题:热穿透性指标FH值的确认。
3)计算方法:干燥灭菌的杀菌热力强度F(Hmin)。
例2:提取罐名称出现下列3种称谓。
提取设备、提取容器、提取罐。
例3:灌装系统出现下面3种称谓。
灌装、灌液、灌注。
例4:试验方法中的条题有3种表示方法:“5.1 材料检测、5.2 外观检验、5.3 性能试验”。
分析:检测、检验、试验3个词的意思基本一致,但标准强调同一概念的用词应一致,应该都称试验。
例5:电气安全试验中的用词不统一的表现形式。
1 电气系统的保护联结电路连续性试验按GB 5226.1—2008中18.2和GB/T 24342—2009中6.2规定进行检查。
2 电气系统的绝缘电阻试验按GB 5226.1—2008中18.3规定进行检查。
3 电气系统的耐压试验按GB 5226.1—2008中18.4规定进行检查。
4 电气系统的按钮按GB 5226.1—2008中10.2规定检查验。
5 电气系统的指示灯和显示器按GB 5226.1—2008中10.3规定检查检验。
6 查验压片机的急停功能,急停器件按GB 5226.1—2008中10.7规定检查验。
7 电气系统的配线按GB 5226.1—2008中第13章中13.1.1、13.2.1、13.2.2、13.3和13.4.1规定检查验。
8 电气系统的标记、警告标志和参照代号按GB 5226.1—2008中第16章规定检查验。
2.1 2.2 公式
公式的正确表示方法如下:
(1)公式应以正确的数学形式表示,由字母符号表示的变量应随公式对其含义进行解释。
例1,减速器的温升计算式:

式中 Δt——温升,℃;
t——实测部位的温度,℃;
t0——实测环境温度,℃。
(2)公式只能用量的符号来表达,不应使用量的名称或描述量的术语表示。
例2,物体密度计算公式:

(3)公式的编号不是必须的,如果为了提及和引用方便,需要对标准中的公式进行编号时,则应使用从“1”开始的带圆括号的阿拉伯数字。
(4)公式的编号应从引言开始一直连续到附录之前,并与章、条、图和表的编号无关。附录中公式的编号应前缀附录编号中表明附录顺序的大写字母,字母后跟下脚点(如A.1、A.2等)。
2.1 2.3 物理量和数值
物理量和数值的正确表示法举例如下:
例1:机器外形尺寸:100 mm×150 mm×200 mm,不能用(100×150×200)mm和100×150×200 mm3表示。
例2:电压误差为380(1±10%)V,不能用380 V±10%V表示。
例3:温度范围为18℃~25℃,不能用18~25℃表示。
2.1 2.4 汉字和符号
汉字不用符号连接。
(1)“噪声≤75 dB(A)”应改为“噪声不大于75 dB(A)”;
(2)“粗糙度≤0.8 μm”应改为“粗糙度值Ra≤0.8μm”。
2.1 2.5 数值和单位符号
数值和单位符号应结合使用,不应单独使用。
(1)不应将单位符号和单位名称混合使用。如“km/h”或“千米每小时”不能表示为“每小时km”、“千米/h”或“千米/小时”;又如“7 mL”不用“7 ml”或“7亳升”表示。
(2)单位符号应写在全部数值之后,并与数值之间留适当的空隙。例:“2 h”不用“2小时”表示,且数值和单位符号之间空1/4个汉字距离。唯一例外的是,平面角的单位“度”、“分”、“秒”的单位符号和数值之间不留空隙,例:20°5′7″不表示为20 °5′7″。
(3)不要将单位符号与其他符号或文字混合使用。如含水量“20 mL/kg”不应表示为“20 ml H2O/kg”或“20 ml水/kg”。
(4)不应通过附加下标或其他信息修改法制定计量单位的符号。如Umax=500V,不应表示为U=500Vmax。
3 结语
本文从审查国家标准、行业标准的过程中所发现的编写标准结构要素不规范现象入手,以GB/T 1.1—2009规定的编写规则给予纠正,并对征求意见稿和送审稿中的不符合编写规则的例句进行了分析,以使广大标准化编写人员受到启发,推动制药机械行业标准化工作向前发展。 (兴业杯参赛论文)
