La1-xSrxFeO3-δ复合材料的制备及其性能研究
2014-09-15韩尚宁
韩尚宁
(河南师范大学新联学院,河南 新乡 453007)
张丽敏
(山西师范大学化学与材料科学学院,山西 临汾 041004)
La1-xSrxFeO3-δ(LSF)系钙钛矿结构 (ABO3)复合氧化物是一种离子-电子混合导体材料,具有较大的氧渗透通量、较高的电子导电性和良好的催化活性,因而被作为氧分离膜材料 (应用于氧分离)和中温固体氧化物燃料电池的阳极材料[1]。LSF电导率受制备工艺及掺杂离子的影响,为提高其电导率,改善电极性能,一方面可以优化材料的制备方法,常用的合成方法有固相法、水热合成法、共沉淀法和溶胶-凝胶法等[2];另一方面可以通过改变掺杂离子的含量,寻找最佳配比的优良材料。
柠檬酸法,又称Pechini法,是Pechini于1967年发明的一种合成陶瓷粉体的方法[3]。该方法的优点是通过控制化学计量比保证溶液在分子尺度上的混合均匀性,能实现成分复杂分体的制备。同时为了克服柠檬酸络合能力的限制,避免pH值控制不当导致浓缩时水解析出金属离子,国内外许多学者研究并提出了改进柠檬酸法的有效方法[4-6],即向柠檬酸溶液中加入乙二胺四乙酸 (EDTA),EDTA酸和柠檬酸共同对金属离子络合,用氨水调节pH值,经过络合、凝胶化、干燥、燃烧得到粉体的方法—EDTA-柠檬酸联合络合法。下面,笔者采用该方法合成了La1-xSrxFeO3-δ(x=0.1~0.7)一系列的复合材料,并且探究了掺杂离子的含量对电导率的影响。
1 试验部分
1.1 试剂和仪器
1)试剂 La2O3(上海跃龙,高纯99.99% )、Fe(NO3)3·9H2O、Sr(NO3)2(天津科密欧化学试剂有限公司,分析纯)、氨水、乙二胺四乙酸 (EDTA)(天津申泰化学试剂有限公司,分析纯)、柠檬酸 (天津市风船化学试剂科技公司,分析纯)、HNO3(洛阳化学试剂厂,分析纯)、Ag浆 (贵研铂业有限公司)。
2)仪器 台式手动粉末压片机 (YP-24T,天津金孚伦科技有限公司)、坩埚电阻炉 (SG2-3-10,上海实验电炉厂)、高温箱型电阻炉 (SRJX-4-13,江苏省东台县电器厂)、数字万用表 (KEI-2000,美国KEITHLEY公司)、程序温度控制仪 (AT-808PAK5L1-40A-D2,厦门宇电自动化科技有限公司)、扫描电子显微镜 (Scanning Electron Microscopy,SEM) (JFC-1600,日本JEOL公司)、热重分析仪(TGA-DSC1,瑞士梅特勒-多利多公司)、X 射线衍射仪 (X-ray Refractory Diffractometer,XRD)(D8-ADVANCE,CuKα光源,德国布鲁克公司)。
1.2 LSF粉体的制备和LSF样条压制
1)LSF粉体的制备 La1-xSrxFeO3-δ(x=0.1~0.7)合成的原料是La2O3、Fe (NO3)3·9H2O及Sr(NO3)2。按照目标产物的化学计量比将La2O3溶于稀硝酸Sr(NO3)2、Fe(NO3)3·9H2O分别溶于去离子水中。将上述硝酸盐溶液混合均匀,加热搅拌,加入EDTA的氨水溶液,然后加入柠檬酸,(EDTA酸、柠檬酸与所有金属离子的摩尔比是1∶1.5∶1),调节PH值大约为6左右,用磁力搅拌器加热 (温度70℃左右)搅拌至凝胶状。将其转移到500ml的陶瓷蒸发皿中,放置电子万用炉上加热至燃烧,得到初次粉体。用玛瑙研钵其充分研磨后,转移到坩埚中放入马弗炉中焙烧5h(温度设为850℃),得到LSF纯相黑色粉体[7]。
2)LSF样条的压制 取约2.2g La1-xSrxFeO3-δ粉体在玛瑙研钵中充分研磨,红外灯烘干后,在不锈钢模具中5MPa左右的压力下压制成大约 (29mm×6.8mm×2.2mm)的阳极样条,将其放在高温电阻箱中1180℃烧结5h,得到具有一定机械强度、致密的阳极体。
1.3 LST材料结构表征及电化学性能测试
合成的粉体采用德国布鲁克公司D8-ADVANCE型X射线衍射仪进行结构表征 (采用CuKα光源,波长1.5418Å,管电压40kV,管电流40mA,扫描范围为20-80°,扫描速度为1.2°/min)。利用日本JEOL公司JFC-1600型号的扫描电子显微镜 (SEM)和瑞士梅特勒-多利多公司TGA-DSC1型号的热重分析仪分别对材料进行致密性和微观形貌进行分析。通过KEI-2000数字万用表及SG2-3-10坩埚电阻炉、WLS数字恒流电源等组成的测试系统利用四探针法对样条进行高温导电性能测试。
2 结果与讨论
2.1 LSF粉体的XRD表征
图1是 La1-xSrxFeO3-δ(x=0.1~0.7)在850℃的温度下焙烧5h制备的粉体的XRD图谱,可以看出粉体的衍射峰和ABO3钙钛矿的标准衍射峰相近,并且没有出现杂峰,说明LSF粉体中所有组分均为单一的立方钙钛矿结构。
随着Sr含量的增加,衍射峰向2θ角增大的方向偏移,但是晶体结构没有改变 (见表1)。由于Sr2+取代了铁酸镧结构中部分的La3+,为了保持电中性,使得B位的离子由Fe3+向Fe4+转变进行电荷补偿,由于Fe4+比Fe3+半径小造成晶包体积减小;虽然Sr2+比La3+的半径略大,会使晶包体积增大,但是前者的影响较大,因此出现晶格收缩导致了衍射峰向2θ角增大的方向偏移。Sr2+取代了部分的La3+后,B位的离子由Fe3+向Fe4+转变进行电荷补偿,同时出现氧空位,随着Fe4+离子浓度和氧空位浓度的增大导致晶体对称性降低,从而使晶格常数减小导致了衍射峰向2θ角增大的方向偏移[8-9]。
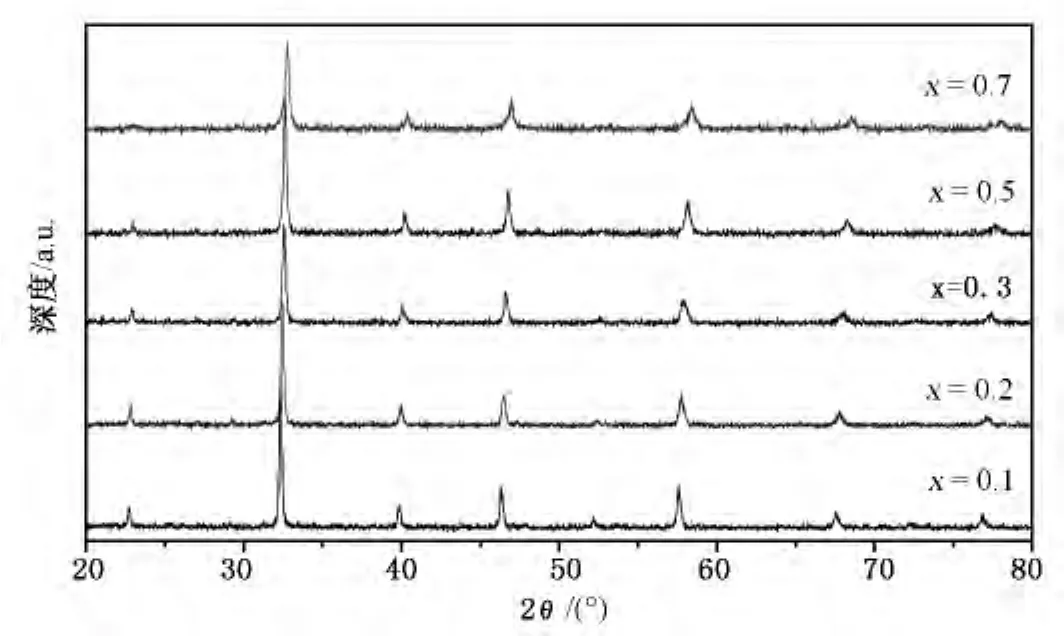
图1 LSF在850℃,5h粉体的XRD图谱

表1 La1-xSrxFeO3-δ (x=0.1~0.7)粉体晶面的2θ角的比较
2.2 LSF热重 (TG)分析
LSF粉体的TG-DSC曲线如图2所示。从图2中DSC(差示扫描量热法)曲线可以看出,LSF样条在400~800℃之间烧结时有一个较大的放热峰。这个放热过程是由于样条在压制时形成很大的界面压应力,随着温度的升高压应力逐渐的释放所引起的[10]。另外在1100℃时出现一个较强的放热峰,这是样条烧结的中期阶段,也是晶粒长大,烧结致密度迅速增大的过程。为防止样条分层或是断裂,烧结的程序可设为:室温~800℃为缓慢升温阶段,速率为1.2℃/min。1000~1180℃为LST样条快速收缩阶段,升温速率可以适当提高,设为1.6℃/min,并在1180℃恒温5h。
2.3 LSF样条的形貌表征
图3是LSF在1180℃烧结5h后截面的形貌照片,从图3(a)中可以看出,LST材料具有较好的空隙结构,晶粒分布较均匀,能够明显的看出晶粒间界面。与图3(a)相比,图3(b)气孔明显较少,而且部分晶面已经模糊不清,说明有固溶体的形成。图3(c)、图3(d)分别是x=0.5、x=0.7时LSF样品的断面照片,可以看出,LSF已经转化为固溶体,看不到晶粒间的界面,仍有气孔存在,但是其致密度相对较高。由此证明了在烧结温度相同的情况下,随着Sr含量的增加,样品烧结性能增大,致密度相对较高。

图2 LSF粉体的TG-DSC曲线
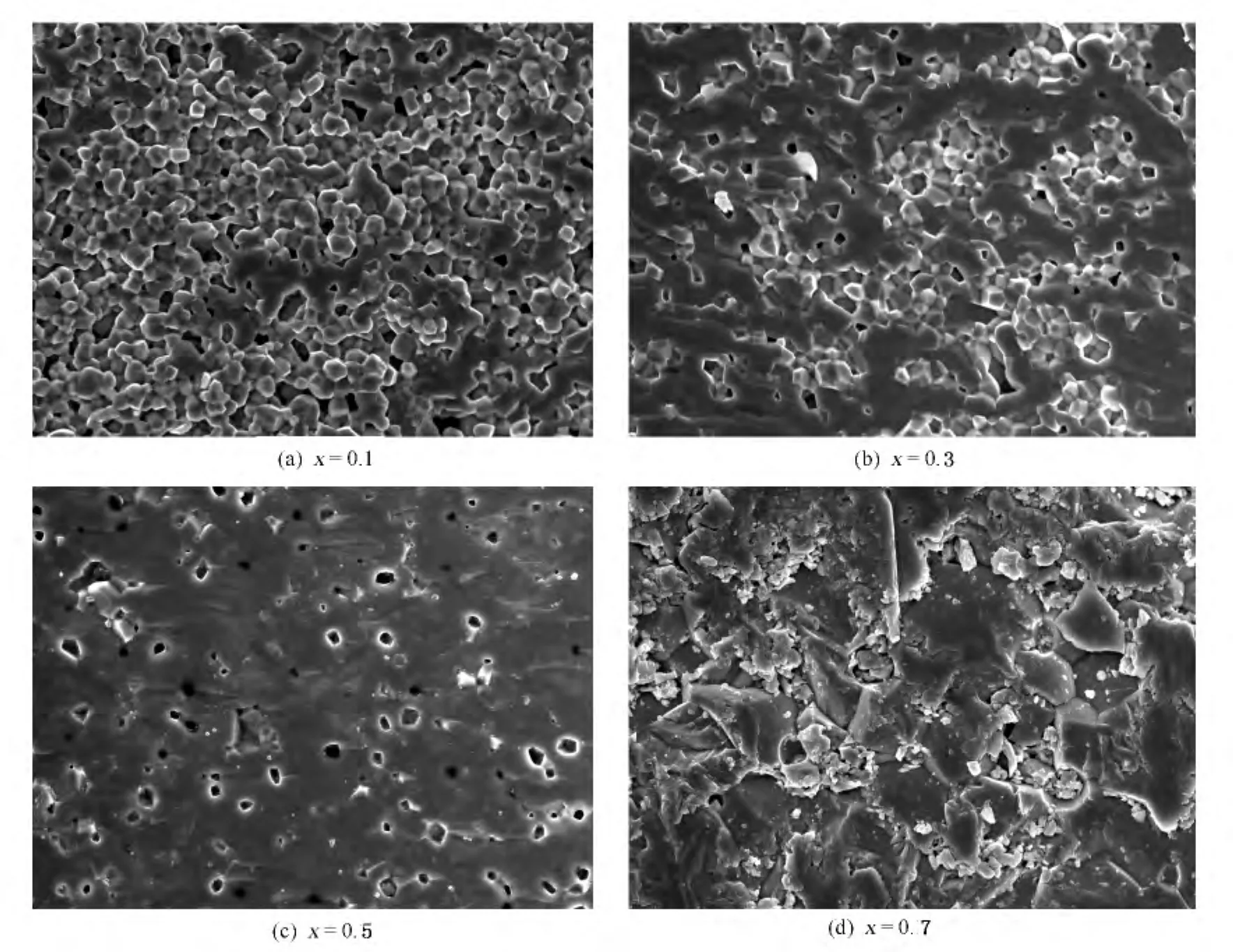
图3 LSF样品烧结温度为1180℃时断面的SEM图
2.4 LSF电导率的测试
在升温的过程中使用KEI-2000在空气气氛下对LST材料进行电导率测量,测试温度范围在300~900°C之间,每间隔50°C取一个点,升降温速率设为1.2°C/min。空气气氛下LSF的电导率与温度及Sr含量的关系曲线如图4所示。可以看出,在整个温度范围内,LSF的电导率基本上是随着Sr含量的增加而增大。特别是随着Sr含量的增加,其低温阶段电导率大大增加了,当x=0.7时,电导率在550°C出现最大值,达到327.38S/cm。这是中低温固体氧化物燃料电池所期望得到的,有利于降低电池运行温度,进而降低成本加速其商业化进程。
由图4还可以看出,LSF材料在空气中750°C时Sr含量x=0.5时电导率达到最大。这是因为当Sr含量较小时 (如x=0.1),形成的氧空位数很少,很难形成氧离子传输通道,这时主要是电子电导起作用,由图中可看出其电导率随温度的升高而增大。随着Sr含量的增加,形成的氧空位数增加,氧空位浓度逐渐增大,氧离子传输通道也随之形成,氧离子导电性逐渐增加,这时是电子-离子混合导电共同作用。但是当Sr含量过高时,氧空位浓度较大,高温下就会发生缔结形成势阱,使得离子或是电子陷入势阱而跃迁的几率减小,从而使电导率降低。
图5是LSF粉体电导率的阿伦尼乌斯曲线图,其中,σ的表达式为:


图4 空气中LSF电导率与温度、Sr含量的关系

图5 LSF粉体电导率的阿伦尼乌斯曲线
其中,σ为样品的电导率,S/cm;C0为常数(载流子浓度);T为绝对温度,K;k为Boltzmann常数;Ea 为电导活化能,kJ/mol[4-5]。
由图5可见,ln(σT)与1/T在低温阶段近似呈直线关系,符合小极化子导电机理[11-13]。这是因为在 La1-xSrxFeO3-δ(LSF) 钙钛矿型(ABO3)材料的结构中,部分低价Sr2+取代La3+导致了电荷的不平衡,使得B位离子为保持电中性由Fe3+向Fe4+转变进行电荷补偿同时产生氧空位。另外,Fe3+向Fe4+转变导致这2种离子周围晶格偏离平衡位置的位移不同产生畸变场。在固体理论中,由电子 (或是d电子空位)与周围的晶格畸变场组成的区域称为极化子[14-16]。在LSF材料中,由于Fe3+-O-Fe4+这样的小的极化子的形成,使得电子在Fe3+、Fe4+之间跃迁而导电。高温时LSF材料中由于氧空位缔结产生的势阱束缚电子迁移而导致电导率降低。
3 结论
1)采用EDTA-柠檬酸法合成的La1-xSrxFeO3-δ(LSF,x=0.1~0.7)材料均显示了单一的立方钙钛矿型结构,并不含有其他相物质。并且随着Sr含量的增加,衍射峰向2θ角增大的方向偏移,但是晶体结构没有改变。
2)在整个温度范围内,LSF的电导率基本上是随着Sr含量的增加而增大,当x=0.5时达到最大值;当测试温度为750℃、x>0.5时,过多的Sr掺入会引起氧空位浓度过大而导致其缔结成势阱,使得电导率降低。
3)所有组分在低温时电导率随温度的升高而增大,符合小极化子导电原理。达到一定温度 (各组分不同)后材料的电导率随着温度升高而降低,这是由氧空位缔结成势阱束缚电子迁移从而导致电导率下降。
[1]Boukamp B A.The amazing perovskite anode [J].Nature Mater,2003,2:294-296.
[2]Richard J B.Proceeding of Ceramics[J].Mater Sci Technology,2005,17A:71-72.
[3]Shao Z P,Yang WS,Cong Y,et al.Investigation of the permeation behavior and stability of a Ba0.5Sr0.5Co0.8Fe0.2O3-δoxygen membrane [J].Journal of Membrane Science,2000,172(1):177-188.
[4]段枣树 .新型阴极材料在IT-SOFC中的应用 [D].大连:中国科学院大连化学物理研究所,2005,21-26.
[5]马文广 .中温固体氧化物燃料电池新型阴极材料的制备及性能研究 [D].长春:吉林大学,2008.
[6]阎景旺 .中温固体氧化物燃料电池的研制与电极过程的研究 [D].大连:中国科学院大连化学物理研究所,2002.
[7]韩尚宁,张丽敏 .钙钛矿型复合材料La0.7Sr0.3-xMxFeO3(M=Ca、K)的制备及性能 [J].河南师范大学学报 (自然科学版),2011,39(2):76-79.
[8]Li XM,Su WH,Lu Z,et al.Mixed valence state and electrical conductivity of La1-xSrxCrO3[J].Journal of Alloys and Comdopounds,2000,305 (1-2):21-23.
[9]陈尚冰,张璐,戴向东,等 .钙钛矿型复合氧化物的制备及结构测试 [J].江汉石油学院学报,1995,17(4):61-64.
[10]刘伟明,李胜利,李士刚,等 .掺Sr铬酸镧粉体的合成及低温烧结行为研究 [J].无机材料学报,2007,22(6):1061-1064.
[11]Dasgupta N,Krishnamoorthy R,Jacob K T.Crystal structure,thermal expansion and electrical conductivity of Nd0.7Sr0.3Fe1-xCoxO3(0≤x≤0.8)[J].Materials Science and Engineering B,2002,90 (3):278-286.
[12]Roosmalen J A M,Huijsmans J P P,Plom L,Electrical conductivity in La1-xSrxMnO3+δ[J].Solid State Ionics,1993,66 (3-4):279-284.
[13]Cox P A.The Electronic Structure and Chemistry of Solid[M].New York:Oxford University Press,1987:179.
[14]江金国,崔崇 .La1-xSrxCo0.2Fe0.8O3系阴极材料导电机理研究 [J].材料科学与工艺,2007(4):576-577.
[15]江金国,崔崇 .La1-xSrxCo0.2Fe0.8O3系阴极材料制备及表征 [J].材料科学与工程学报,2004(3):382-385.
[16]夏正才,唐超群 .La1-xSrxMnO3阴极材料的导电机理研究 [J].物理学报,1999(8):1518-1521.
