突破光学显微镜的极限
2014-09-10
本刊记者


瑞典皇家科学院宣布,将2014年诺贝尔化学奖授予美国科学家埃里克·贝齐格、威廉·莫纳和德国科学家斯特凡·黑尔,以表彰他们为发展超高分辨率荧光显微镜做出的贡献。长期以来,光学显微镜的分辨率都被认为是有极限的,即不可能超过光波波长的一半,这被称为“阿贝极限”。然而,获奖的3位科学家打破了这一极限,使光学显微镜步入了纳米时代。
为什么说光学显微镜是有极限的?
显微镜的发明打开了通往微观世界的大门。显微镜的最早起源可追溯至1590年的荷兰,当一位眼镜商人的儿子在玩弄镜片时,偶然发现两块透镜在一定距离观察物体时,物像显得格外大。把两块透镜固定在直径不同的圆筒上,并使小圆筒能在大圆筒内自由滑动,这便成了今天显微镜的原始雏形。1665年,英国人罗伯特·胡克用他制作的显微镜观察树皮切片,看到一些密集排列的小孔,他称之为“cell”,现在我们沿用了这个名称,中文翻译为“细胞”。作为细胞的命名人,胡克当时所看到的其实并不是真正意义上的细胞。与胡克同时代的荷兰人列文虎克凭借他精心磨制的镜片制成了更精密的显微镜,第一次发现了血液里的细胞以及土壤中各种各样的微生物。
前面提到的显微镜是光学显微镜,也就是利用可见光,将微小物体形成放大影像的光学仪器。经过不断的改进,光学显微镜已经可以达到放大1600倍的效果了,这意味着科学家们可以辨别完整细胞,以及其中比较大的细胞器(如叶绿体、线粒体)的轮廓结构,但却无法分辨一个正常大小的病毒或者单个蛋白分子。那么,光学显微镜的放大效果有没有可能继续甚至是无限提高呢?
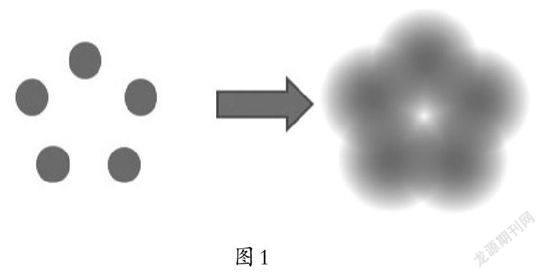
很遗憾,答案是否定的。光学显微镜的分辨率是有一个极限的,也就是说,用光学显微镜永远无法看到小于光波长一半的物体。这个极限被称为“阿贝极限”,它是德国物理学家、光学家恩斯特·阿贝于19世纪70年代提出来的。阿贝发现,可见光由于其波动特性,会发生衍射,因而光束不能聚焦到无限小。可见光波长范围为400纳米~780纳米,以可见光中波长最短的蓝紫光来说,其波长在400纳米左右,因此,如果两点之间的距离小于200纳米,我们将无法分辨出这两个点(如图1)。
一个多世纪以来,200纳米的“阿贝极限”一直被认为是光学显微镜理论上的分辨率极限,小于这个尺寸的物体必须借助电子显微镜才能观察。
电子显微镜是20世纪二三十年代发展起来的成像技术,它利用高能短波长电子束代替可见光作为光源,通过电子束与物体衍射作用工作,放大倍数可高达数十万倍。既然有了分辨率极高的电子显微镜,科学家是不是就没有必要再纠结于光学显微镜的分辨率极限了呢?并不是这样的。因为电子显微镜需要在真空条件下工作,还要经过复杂的标本处理过程,所以很难观察活的样本,而且电子束的照射也会使生物样品受到辐照损伤。对于生物学家而言,还有什么比让细胞活生生地出现在眼前更令人激动的呢?
突破“阿贝极限”的两种方案
荧光显微镜也是一种光学显微镜,故同样跳不出“阿贝极限”,只不过利用荧光分子为细小的物体“标记”,科学家可以更有针对性地观察和追踪他们感兴趣的内容。在突破“阿贝极限”的方案中,有两种各自独立发展出来的技术方法。
如图1所示,光源一次把处于这个半径里面的粒子照亮,看起来模糊一片,根本无法分辨每一个粒子。斯特凡·黑尔想到一个绝妙的点子:既然一次都亮起来看不清,那我就分两步。简单来说,就是用两束激光,一束激光激发荧光分子发光(图2左),这个光斑已达分辨率的极限,不能再小了;另一束激光则比较特殊(图2中),就把它想象成一个“面包圈”吧!当两束光聚焦到同一个点上,第二束光就把第一束光给灭了,只有中间那个点没有灭掉(图2右),这更小的点便突破了分辨率的极限。这就是斯特凡·黑尔开发出的STED显微镜的原理,STED全名是Stimulated Emission Depletion,意为受激发射损耗。斯特凡·黑尔正是利用这个原理,通过巧妙的设计,将STED显微镜的光斑尺寸变得非常小,然后用它一小点一小点地去扫描整个观察区域,就得到了分辨率高于传统光学显微镜的图像。
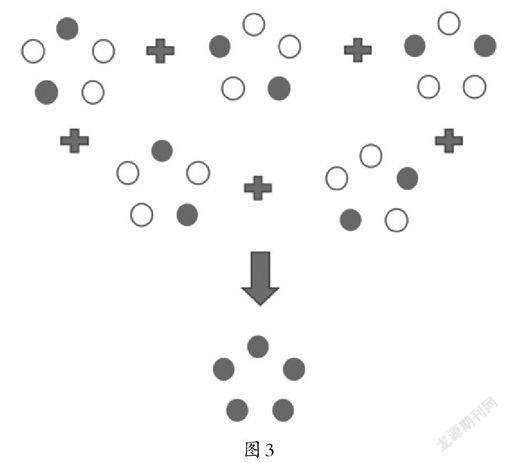
贝齐格和莫纳则通过各自的独立研究,为另一种显微镜技术——单分子荧光显微成像技术的发展奠定了基础。与STED不同,这种方法不是在显微镜的光斑尺寸上做文章,也不必先“点亮”再“熄灭”,而通过类似图像叠加的原理,巧妙地摆脱了“阿贝极限”的束缚。如图3示意,不是相邻两点之间的距离小于200纳米就无法分辨吗?那么,我们就依靠“开关”单个荧光分子,分别让不相邻且间距大于200纳米的两点发光,这样不就可以把它们区分开来吗?然后,再把每一次得到的图像叠加,用一定的数学方法加以处理,同样能得到分辨率高于传统光学显微镜的图像。
光学显微镜步入纳米时代
虽然这些新的光学显微技术可以使我们看到更小的物体,但并不意味着“阿贝极限”被推翻了,科学家们只是另辟蹊径地绕过了这个障碍。一旦挣脱了极限的束缚,光学显微成像技术便向纳米尺度大幅迈进,并将为疾病研究和药物研发带来革命性变化。
以STED技术为例,它在理论上已经可以达到40纳米~50纳米的分辨率。从此以后,科学家们就能在显微镜下“实时”观察活体生物细胞内单个分子的运动情况了。他们可以观测分子如何在脑神经细胞之间建立突触,可以研究与帕金森氏症、阿尔茨海默氏症和亨廷顿氏症有关的蛋白质变化情况,还可以追踪胚胎内部细胞的分裂过程。这也正是3位获奖者以及其他许多科学家们目前所从事的工作。
3位获奖者的简介如下:
斯特凡·黑尔:1962年生于罗马尼亚,目前任职于德国马克斯·普朗克生物物理化学研究所和德国癌症研究所。
埃里克·贝齐格:1960年生于美国,目前任职于美国霍华德·休斯医学研究所。
威廉·莫纳:1953年生于美国,目前任职于美国斯坦福大学。
【责任编辑】庞 云
