TLC-SERS联用法检测降糖中成药中添加的格列类药品
2014-08-06秦剑红解放军169医院药械科湖南衡阳421001
秦剑红 (解放军169医院药械科,湖南 衡阳 421001)
一直以来,中药制剂掺假现象屡禁不止,其种类繁多,作用机制不明,且相应的检测质量标准尚不完善,使得不法分子有机可乘。对于中药掺杂化学成分的检测,常用方法有薄层色谱法(TLC)[1,2]、高效液相色谱法(HPLC)[3,4]、液质联用法(LC-MS)[5,6]等。传统的TLC法操作简单,但存在较高的假阳性;HPLC、LC-MS法灵敏度高且准确性好,但其样品前处理过程复杂,且需要特定规格的试剂和色谱柱,检测成本较高,不易于基层推广。随着便携式拉曼光谱仪的普及,表面增强拉曼光谱技术逐渐在分析检测领域得到较多应用[7,8]。表面增强拉曼散射光谱(surfcae enhanced Raman scattering,SERS)能够提供分子能级的指纹图谱,且信号强度好,通常为常规拉曼光谱的104~106倍。将其与TLC方法相结合,先对复杂样品进行初步分离,然后采用SERS技术检测,获得待测物的特征指纹图谱,从而进行更准确的定性判别。目前,SERS技术已用于水污染的现场监控[9]、中药成分非法添加西药成分的检测[10]、生物尿样中可卡因代谢产物的定量分析[11]、中草药中结构相似生物碱成分的鉴别[12]等。
本研究采用TLC与SERS联用方法对降糖中成药中添加的格列类药物(格列喹酮、格列本脲、格列美脲、格列吡嗪、格列齐特)进行检测,首次采用有机相银溶胶获得了5种格列类化学降糖药的SERS图谱,可用于中药中非法添加该类化学药成分的快速检测。
1 材料与仪器
1.1 材料 格列齐特(批号:100296-201004)、格列本脲(批号:100135-200404)、格列美脲(批号:100674-201102)、格列吡嗪(批号:100281-200602)、格列喹酮(批号:100280-201002)对照品均购自中国药品生物制品检定所;硝酸银、柠檬酸三钠、N,N-二甲基甲酰胺(DMF)、聚乙烯吡咯烷酮(PVP-K30)等试剂均为分析纯,购自国药集团化学试剂有限公司;薄层板HSGF254(烟台江友硅胶开发有限公司);实验用水为二次蒸馏水;实验中所用的降糖中药阴性样品(不含非法添加成分)由山东省食品药品检验所提供。
1.2 仪器 BWS415-785H型便携式拉曼光谱仪(必达泰克),配有BAC151视频显微拉曼检测系统,激发光源785 nm,分辨率3.5 cm-1@912 nm,光谱范围175~2 700 cm-1;TG16-WS型高速离心机(上海卢湘仪);KQ-250DB型数控超声波清洗机(昆山市超声仪器有限公司);WFH-203B型紫外分析仪(精科实业);普析通用TU-1901双光束紫外可见分光光度计。
2 方法
2.1 银胶溶液的配制 将10 ml AgNO3与PVP(摩尔比10:1)的混合溶液加入100 ml沸腾的DMF中,其中AgNO31×10-3mol/L,继续加热1 min,见溶液由无色变为黄绿色,最终变为黄棕色的银胶溶液,冷却备用。
2.2 样品溶液的配制
2.2.1 对照品溶液 称取格列本脲、格列齐特、格列美脲、格列喹酮、格列吡嗪对照品适量,加甲醇-氯仿(1:1)溶解,分别制成每1 ml含1 mg的溶液,作为对照品溶液备用。
2.2.2 模拟阳性样品溶液 取降糖类中药阴性样品(不含非法添加成分)适量,研细,另精密称取适量降糖药对照品加入其中,使各个成分添加量均为1%(W/W),加甲醇-氯仿(1:1)溶解,超声10 min,离心后取上清液,作为降糖药的模拟阳性样品溶液。
2.2.3 真实样品溶液 取降糖类中成药样品各1.5 mg,研细,加甲醇1 ml溶解,超声15 min,以10 000 r/min离心5 min后取上清液,作为真实样品溶液备用。
2.3 检测方法 吸取对照品溶液和模拟阳性样品溶液各1 μl,点于同一硅胶板上,以环己烷-乙酸乙酯-冰醋酸(9:5:1)展开后取出,晾干,置于紫外灯(254 nm)下检视定位,于阳性样品色谱条带中与对照品Rf值相同位置处,滴加纳米银溶胶5 μl,对滴加银胶的位置进行检测,放大20倍,积分时间20 s,激光功率100 mW,将所得图谱与对照品的SERS谱进行对比分析,得出结果。
2.4 数据预处理方法 采用软件Matlab 7.6对所得光谱进行谱段选取( 300~1 700 cm-1)、Savitzky-Golay(Sgolay)法平滑、adaptive iteratively reweighted Penalized Least Squares(airPLS)法基线校正和归一化等预处理;制图软件使用Origin 7.5。
3 结果与讨论
3.1 薄层色谱条件的优选 参照国家药品标准[13]和相关文献方法[2,14],对薄层色谱展开条件进行比较。实验中考察了(a)氯仿-环己烷-乙醇-冰醋酸(8:13:1:1);(b)环己烷-乙酸乙酯-甲醇-冰醋酸(14:6:1:0.1);(c)环己烷-乙酸乙酯-冰醋酸(5:5:1)的展开情况。结果(a)、(b)体系下,分离效果均不理想,选择较简单的(c)体系进行调节,三者比例为9:5:1时效果较佳,格列喹酮、格列齐特、格列美脲、格列本脲、格列吡嗪的Rf值分别为0.72、0.66、0.56、0.47、0.35。
3.2 不同银溶胶的检测结果
3.2.1 银溶胶的选择与制备 采用传统的柠檬酸钠还原法制备所得银溶胶[15,16]进行实验时,增强效果均较差,几乎无增强信号;尝试使用氯化钠、硝酸钾等凝聚剂,并换用不同浓度的银溶胶,效果仍不理想。可能由于检测物均为水不溶性,难以与水溶性的纳米银粒子结合形成SERS“热点”,故无法产生较好的增强效应。因此,对于这种疏水性物质, 考虑采用有机溶剂制备的有机相的银溶胶进行检测。在制备有机相纳米银溶胶时,参照文献[17]、[18],尝试采用甲醇、乙腈、聚乙二醇、N,N-二甲基甲酰胺、四氢呋喃等溶剂制备纳米银溶胶,最终选择以N,N-二甲基甲酰胺(DMF)作为溶剂制备纳米银颗粒。DMF在整个反应过程中作为溶剂与还原剂,此外,为防止纳米银粒子的团聚,可在制备过程中加入PVP作为保护剂,达到延缓银离子还原的效果。
3.2.2 银溶胶的紫外表征 采用DMF作为还原剂,以PVP作为保护剂制备所得纳米银溶胶的紫外吸收光谱如图1。其最大吸收位置只有一个,说明所制纳米银溶胶为球型,且其最大吸收峰位于408 nm,根据文献[15]推测,此处制得的纳米银直径在50 nm左右,且半峰宽较窄,说明纳米颗粒分布较均匀。
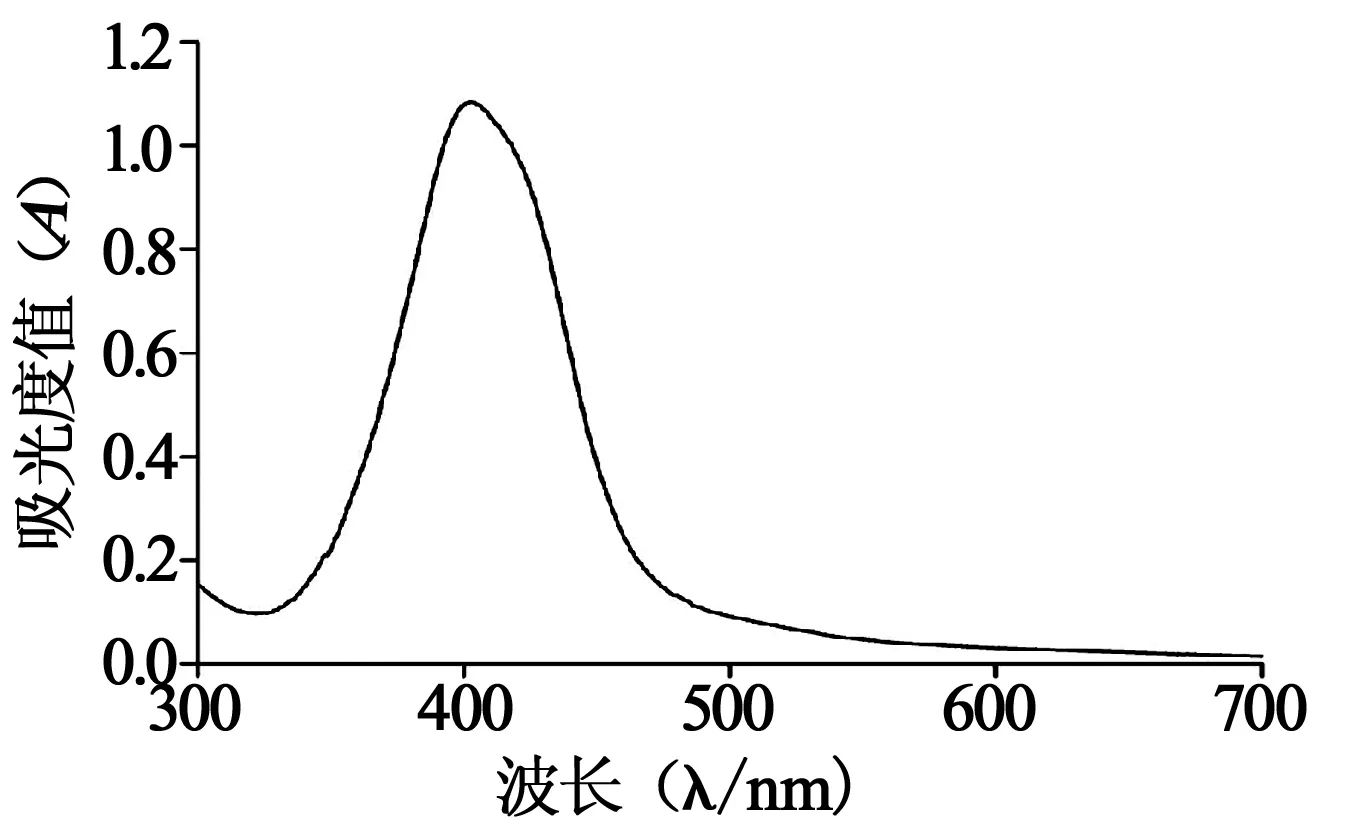
图1 银溶胶的紫外表征图谱
3.3 模拟阳性样品检测 将实验室自行制备的模拟降糖中药阳性样品按照“1.4项”下的方法进行检测,得到结果如图2所示。以格列喹酮为例,其SERS谱中出现的特征峰476, 499, 527, 610, 634, 663, 679, 743, 783, 808, 821, 834, 1004, 1029, 1090, 1125, 1164, 1188, 1205, 1275, 1349, 1442, 1600, 1615 cm-1(409, 865 cm-1除外),均可对应于其固体样品的拉曼光谱中的特征信号(图3),其中409、865 cm-1处特征信号来自于银胶溶剂DMF(图4)。
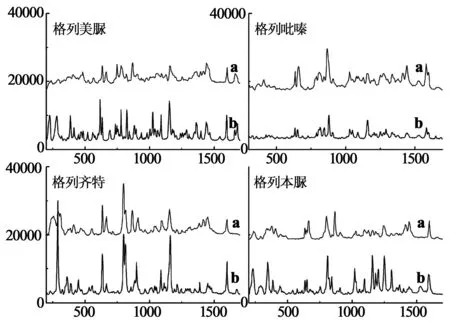
图2 格列类药物的SERS谱(a)及其常规拉曼光谱(b)
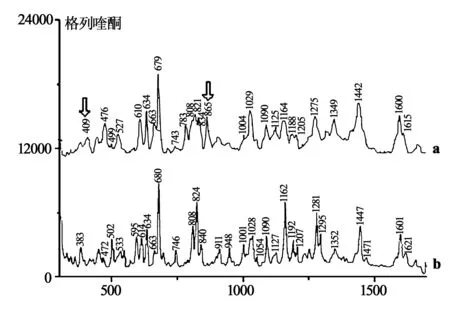
图3 格列喹酮的SERS谱(a)及其常规拉曼光谱(b)
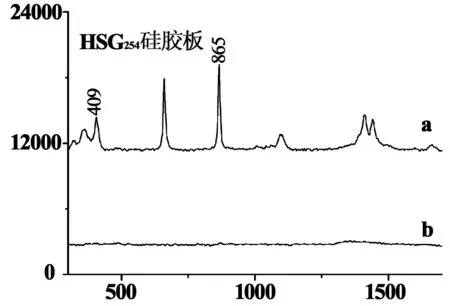
图4 空白硅胶板滴加银溶胶的SERS谱(a)及其常规拉曼信号(b)
采用有机相银溶胶获得的格列类降糖药的SERS图谱,含有丰富的特征信息,用于定性鉴别时准确性较高,进一步提高了本方法用于中药掺杂该类物质检测的专属性。
3.4 真实样品检测 利用建立的方法对7种真实的降糖中药样品进行检测,结果发现6号样品中非法添加了格列美脲,与山东省食品药品检验所提供的检测结果一致。
4 结论
本研究所建立的检测方法用于降糖类中成药中非法添加格列类化学药品的快速检测时,具有灵敏度高、专属性强、操作简单快速、检测成本低等优点,在中药掺杂快速检测、食品安全监控、农药残留检测等领域具有较好的应用前景。
【参考文献】
[1] 王铁松,仝 禹,郑 洁,等.薄层色谱法快速筛查降脂、降压、止咳平喘类中药制剂中的29种添加化学药物[J]. 中国药学杂志,2010, 45(11): 857-861.
[2] 陈玉武,张夙萍,高晓昱.薄层色谱法初筛少数中药制剂中添加降糖类化学药物[J]. 药物分析杂志,2010,30(7): 1298-1300.
[3] 吕情花,李永华. HPLC法测定中成药通宣理肺胶囊(颗粒、片)中非法添加的化学药品[J]. 中国现代药物应用, 2013, 7(21): 225-226.
[4] 钟伟新,王 平,曾 凡.HPLC法测定中成药和保健食品中违法添加的6种肾上腺皮质激素[J]. 今日药学,2012,22(5): 282-284.
[5] 李 丹,文红梅,崔福春,等. LC-MS/MS法快速测定中成药、保健食品中非法添加的36种化学成分[J]. 药物分析杂志, 2010, 30(8): 1527-1532.
[6] Chen Y,Zhao L,Lu F,etal. Determination of synthetic drugs used to adulterate botanical dietary supplements using QTRAP LC-MS/MS[J]. Food Addit Contam Part A, 2009, 26(5): 595-603.
[7] 陈 斌,余岳林,张少敏,等.中成药和保健食品中非法添加西药成分检测方法的探索[J]. 药物分析杂志,2009, 29(10): 1677-1680.
[8] 颜 杰,刘志强,程振田.中成药及中药保健食品中非法添加化学药品现状与对策[J]. 中国医疗前沿, 2007, 42(9):716-718.
[9] Li D,Qu LL,Zhai WL,etal. Facile on-site detection of substituted aromatic pollutants in water using thin layer chromatography combined with surface-enhanced Raman spectroscopy[J]. Environ Sci Technol,2011, 45(9): 4046-4052.
[10] Zhu QX,Cao YB,Chai YY,etal. Rapid on-site TLC-SERS detection of four antidiabetes drugs used as adulterants in botanical dietary supplements[J]. Anal Bioanal Chem, 2014, 406:1877.
[11] Huang RF,Han S,Li XS.Detection of tobacco-related biomarkers in urine samples by surface-enhanced Raman spectroscopy coupled with thin-layer chromatography[J]. Anal Bioanal Chem,2013, 405(21):6815.
[12] Federica P,Nobuko SB,Marco L,etal. TLC-SERS study of Syrian rue (Peganum harmala) and its main alkaloid constituents[J]. J Raman Spectrosc, 2013, 44(1): 102.
[13] 国家药典委员会.中华人民共和国药典2010年版二部[S]. 北京:中国医药科技出版社, 2010: 附录210.
[14] 汪 泉,李 翔,许 威,等.TLC法快速鉴别保健品中非法添加的7种降糖类药物[J]. 安徽医药,2012,16(4): 464-466.
[15] 尹利辉,张 雁.正电性纳米银胶的表征及加入不同凝聚剂后的表面增强拉曼散射光谱[J]. 药物分析杂志, 2010, 30(12): 2352-2355.
[16] Lee PC,Meisel D. Adsorption and surface-enhanced Raman of dyes on silver and gold sols[J]. J Phys Chem, 1982, 86(17): 3391-3395.
[17] Robin L,Garrel L,Richard H. Surface-enhanced Raman spectroscopy using nonaqueous[J]. J Colloid Interf Sci, 1985, 105(2): 483.
[18] Isabel PS,Luis ML. Synthesis of silver nanoprisms in DMF[J]. Nano Lett, 2002, 2(8): 903-905.
