高压静电喷雾法制备再生纤维素磁性微球
2014-08-03周冠成吴伟兵徐朝阳龚木荣戴红旗
周冠成 谷 军 吴伟兵,* 徐朝阳 龚木荣 戴红旗
(1.南京林业大学江苏省制浆造纸科学与技术重点实验室,江苏南京,210037;2.南京林业大学材料科学与工程学院,江苏南京,210037)
磁性高分子微球是将磁性材料与高分子材料以适当的方法复合而成的具有磁性和其他优异性能的微球型功能材料[1-3]。磁性高分子微球不但保留了比表面积大、水力性能好、可进行表面改性等高分子微球的优点,而且具备磁响应性能,使其在外加电场下可与其他介质迅速有效地分离。磁性高分子微球在水处理[4]、有机与生化合成[5]、环境与食品检测、酶的固定化[6]和免疫分析[7- 8]等领域有着广泛的应用前景。用作磁性高分子微球基材的原料种类众多。其中,天然纤维素来源广泛,廉价易得且可再生,以其为基材制备的磁性高分子微球生物可相容、可降解,还可利用纤维素分子中众多羟基对其进行各种化学改性。
高压静电喷雾法是一种利用电流体动力学射流技术将聚合物溶液或熔体制备成高分子微粒的方法[9]。其基本原理可简略表述为:在高压静电场中,以一定流速流出的聚合物溶液或熔体因受到电场的诱导而荷电。荷电液体在表面张力、黏弹力、静电斥力和重力等的共同作用下于喷嘴出口处形成“泰勒锥”。随静电斥力的增大,黏度合适的液体以小液滴的形式从“泰勒锥”中喷射而出形成高分子微粒产品。高压静电喷雾法是一种能够得到具有单分散性微粒的成形方法[10],利用该方法制备的高分子微粒粒径及形态可控。相较于其他方法,如沉淀法[11-12]、反相悬浮交联法[13]、喷雾干燥法[14]等,利用高压静电喷雾法制备磁性高分子微球工艺简单、磁性粒子与微球可控性强,喷雾过程属物理过程,绿色环保,无需使用大量乳化剂。吕昂等[15]用绿色环保的碱/尿素/水溶剂体系直接溶解天然纤维素,得到纤维素碱脲溶液。本实验将具有超顺磁性的Fe3O4纳米颗粒与纤维素碱脲溶液混合,利用高压静电喷雾法制备了具有单分散性的再生纤维素磁性微球(M-RCMS),并与未负载Fe3O4纳米颗粒的再生纤维素微球(RCMS)进行了比较。
1 实 验
1.1 材料及设备
材料:棉短绒浆板(纤维素样品使用前在真空干燥箱中于55℃下真空干燥24 h),聚合度500,湖北化纤集团有限公司;NaOH、尿素、H2SO4、Na2SO4,南京化学试剂有限公司;三氯化铁(FeCl3·6H2O),国药集团化学试剂有限公司;氯化亚铁(FeCl2·4H2O),台山市粤侨试剂有限公司。
设备:微量注射泵(LSP01-1A),保定兰格恒流泵有限公司;DPS-高压电源,大连鼎通科技发展有限公司。
1.2 Fe3O4纳米颗粒的制备
采用化学共沉淀法制备Fe3O4纳米颗粒。将摩尔比为2∶1的FeCl3·6H2O和FeCl2·4H2O溶解于水中(通N2保护),用搅拌机在500 r/min转速下搅拌0.5 h,再将浓氨水以约2 s滴1滴的速度与上述溶液混合,当pH值为9时停止滴加浓氨水。继续熟化2 h后,停止加热和搅拌,保持通N2使其冷却,磁化分离产物与上层清液。
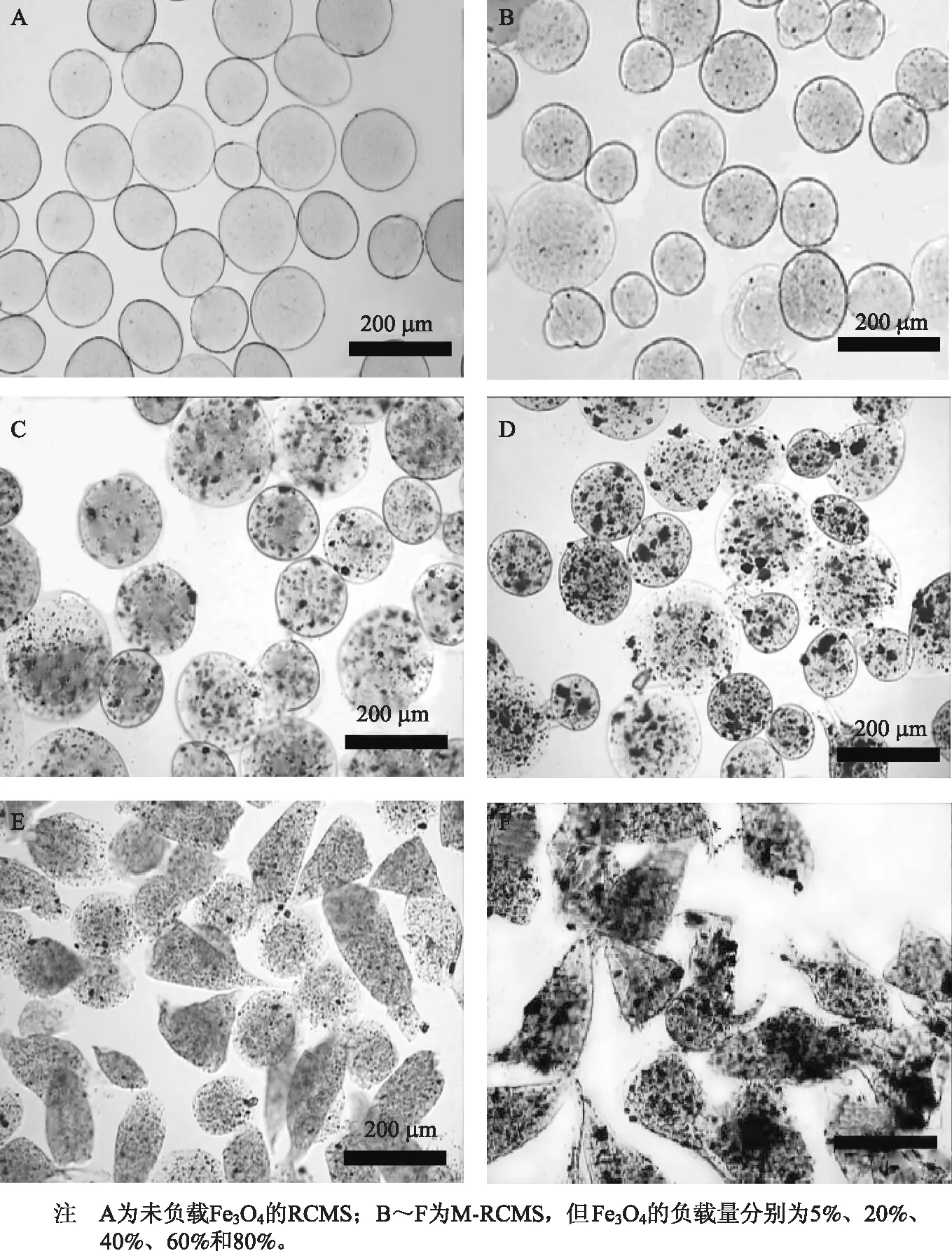
图2 RCMS与Fe3O4负载量不同的M-RCMS的光学显微镜照片
1.3 微球的制备
将质量分数为2%的纤维素碱脲溶液(m(NaOH)∶m(尿素)∶m(水)=7∶12∶81)以及其与Fe3O4纳米颗粒的混合液分别注入到10 mL针管内,用内径为1.2 mm的针头将针管安装于注射泵上,定液间距为15 cm,流量为10 μL/min,电压为10 kV。以硫酸和硫酸钠水溶液(m(H2SO4)∶m(Na2SO4)∶m(水)=5∶5∶90)为凝固浴。按图1所示,利用高压静电法喷雾制备RCMS和M-RCMS。M-RCMS中,Fe3O4的负载量(Fe3O4与纤维素的绝干质量比)分别为5%、20%、40%、60%、80%。
1.4 产品表征
用光学显微镜(BX41,OLYMPUS)观察并记录微球的湿态和表面结构;用扫描电镜(Hitachi S- 4800,日本)拍摄微球的表面结构;微球的物理性质,如湿真密度、含水率、收缩率、孔容、孔度、基质的比表面积、平均孔径、平均粒径的测定参考文献[16-20];利用DS-Advance型X射线衍射仪(Bruker,USA)测定微球和Fe3O4的X射线衍射(XRD)图谱;利用热重分析仪(DTG- 60AH)检测微球和天然纤维素的热稳定性;利用振动样品磁强计(Lake Shore 7407)检测M-RCMS和Fe3O4的磁性能;利用透射电镜(JEOL 2100EX)拍摄Fe3O4纳米颗粒的照片。
2 结果与讨论
2.1 Fe3O4负载量对高压静电喷雾的影响
RCMS与Fe3O4负载量不同的M-RCMS的光学显微镜照片如图2所示。从图2可以看出,RCMS粒径约为150 μm,M-RCMS粒径与RCMS的基本相同。随Fe3O4负载量的增加,M-RCMS的球形度和均一性受到一定程度的影响。当Fe3O4负载量为5%和20%时,M-RCMS的球形度和均一性都与

图1 静电喷雾过程原理图
RCMS相近。当Fe3O4负载量为40%时,M-RCMS均一性略有下降,个别M-RCMS有扁圆、拖尾的情况。进一步增加Fe3O4负载量至60%,大部分M-RCMS拖尾变形,呈锥状,但仍可观察到少许球形的M-RCMS。当Fe3O4负载量为80%时,M-RCMS已完全失去球形,均一性也几乎丧失。液流的均匀性是影响静电场中液体雾化的关键因素,直接关系到雾滴最终成形的均一性[21]。单纯的纤维素碱脲溶液是均相体系,以其作为前驱液喷雾得到的RCMS呈较为均一的球形(见图2A)。Fe3O4并不能溶解于纤维素碱脲溶液中,而是以另一相的形式分散于该体系中,体系的物理化学性质存在差异,又由于NaOH等电解质的存在,Fe3O4更易团聚,相比于单纯的纤维素碱脲溶液,该体系的均匀性大大降低。故利用该体系进行高压静电喷雾制备得到的M-RCMS无论是球形度还是均一性都逊于RCMS。随Fe3O4负载量的提高,这种不均一性逐渐严重。
2.2 M-RCMS的理化性质
2.2.1表面形态和物理性质
图3为RCMS和代表性的M-RCMS(Fe3O4负载量为20%,下同)的SEM照片。如图3所示,M-RCMS表面与孔隙中可见大量微细的Fe3O4颗粒。与RCMS相比,负载Fe3O4后,M-RCMS孔隙结构遭到一定程度的破坏。

图3 RCMS和M-RCMS的SEM照片
RCMS和M-RCMS的湿真密度等物理性质如表1所示。由表1可知,M-RCMS的湿真密度随Fe3O4负载量的增加而变大,这是由于Fe3O4的密度大于纤维素和水的密度。M-RCMS的含水率、收缩率、孔容和孔度均较大,但随Fe3O4负载量的增加而减小,这是由于Fe3O4附着于M-RCMS的内外表面,减小了纤维素与水的接触面积和孔隙体积,使得M-RCMS保水能力下降,孔隙结构变差。其中,孔容的减小还与湿真密度的增大有关。从表1还可看出,随Fe3O4负载量的增加,M-RCMS的比表面积不断增大,这是因为化学共沉淀法制备的Fe3O4粒径很小,具有很大的比表面积,虽然Fe3O4遮蔽了一部分M-RCMS表面,但正是由于这部分Fe3O4自身的裸露面积使M-RCMS获得了更大的比表面积[22]。

表1 RCMS和Fe3O4负载量不同的M-RCMS的物理性质
2.2.2XRD和热稳定性分析
图4为Fe3O4、RCMS及M-RCMS的XRD图谱。由图4可知,M-RCMS除了在2θ为22°处有一个纤维素的固有峰外,在2θ为30°、35°、43°、58°、62°处的衍射峰与Fe3O4立体晶面的相对应,表明Fe3O4已经成功负载于微球中,且负载过程中Fe3O4的晶体结构并未发生改变。
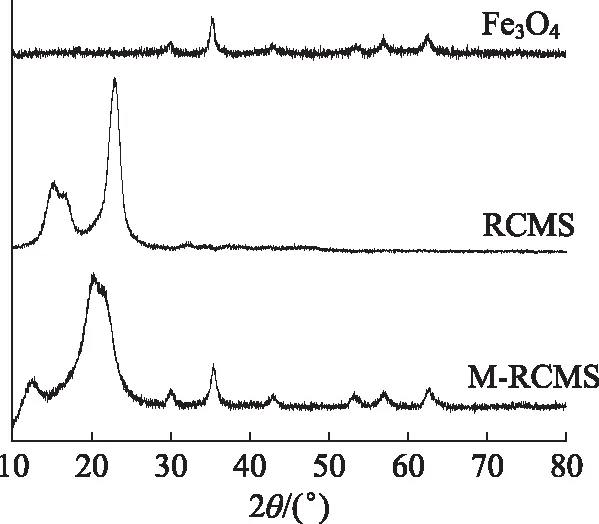
图4 M-RCMS、RCMS和Fe3O4 的XRD图谱
M-RCMS、RCMS和天然纤维素的TGA和DTGA图如图5所示。由图5a可知,300℃之前,各物质的质量损失很少,这一阶段主要是各类水的损失;但300℃之后三者的质量损失较大,这是纤维素分解气化所致。由图5b可知,M-RCMS和RCMS最大质量损失速率分别出现在346.6℃和339.8℃,均低于天然纤维素的352.6℃。这是由于纤维素的热分解是由无定形区向结晶区逐步进行的且无定形区较易分解[23];而M-RCMS和RCMS中的纤维素在再生过程中结晶度下降,无定形区的比例增加,所以其最大分解速率时的温度有所降低。M-RCMS质量损失速率最大时的温度高于RCMS的,可能是因为Fe3O4与纤维素间的结合屏蔽了少量活性基团,使得纤维素的氧化、脱氢和脱氮等反应相对滞后造成的。负载于M-RCMS的Fe3O4在高温下也难以分解,故在质量趋于稳定时,M-RCMS的质量高于RCMS和天然纤维素的质量。因此,M-RCMS热稳定性优于RCMS热稳定性,但略低于天然纤维素热稳定性。
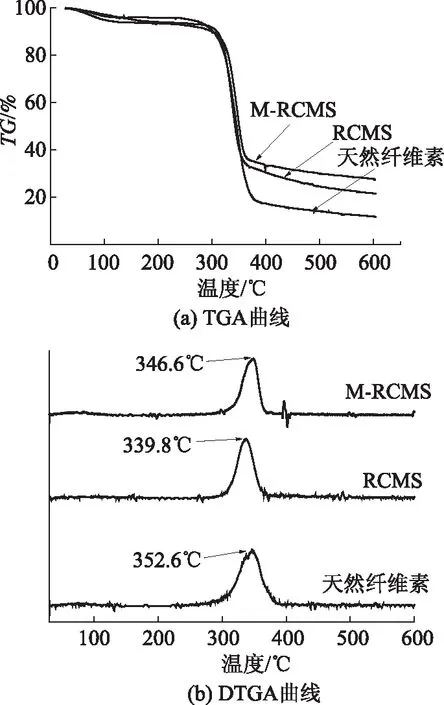
图5 天然纤维素、RCMS和M-RCMS的TGA和DTGA曲线
2.2.3磁性能分析
Fe3O4和M-RCMS的磁滞回线如图6所示。由图6a可知,M-RCMS的比磁化强度明显低于Fe3O4,这是因为M-RCMS中含有无磁性的纤维素,而且,Fe3O4含量较少。Fe3O4和M-RCMS的磁滞回线几乎无剩磁和矫顽力,这是超顺磁性的特征。磁性物质的尺寸影响产品的磁性能,Fe3O4的单畴理论临界尺寸为25 nm[24]。若制备得到的Fe3O4的粒径小于这一尺寸,则单个Fe3O3颗粒内部只拥有一个磁畴,磁畴内部原子磁矩方向一致,在外加磁场的作用下,所有磁畴取向顺着外磁场方向达到饱和,撤去外加磁场,又会恢复杂乱无序的状态,故无任何的剩磁和矫顽力。由图6b可知,本实验制备的Fe3O4颗粒的粒径小于25 nm,当其负载于微球中时,粒径与晶体结构并未发生明显变化,这使得M-RCMS具备了超顺磁性和有效的磁响应分离性能。
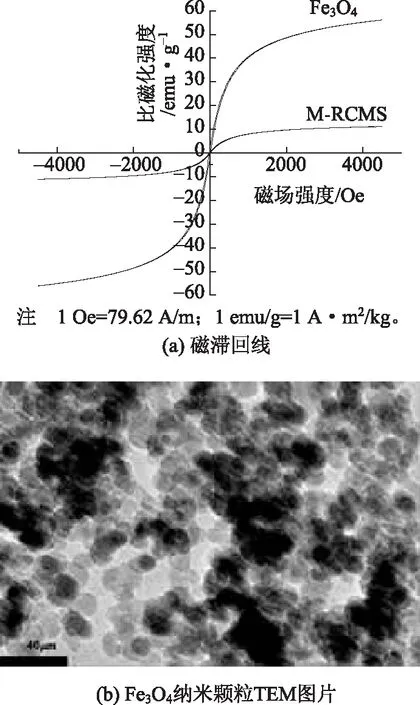
图6 Fe3O4 和M-RCMS的磁滞回线与Fe3O4 纳米颗粒的TEM图片
3 结 语
利用高压静电喷雾法制备再生纤维素磁性微球(M-RCMS)的工艺简单,在一定程度上实现了喷雾过程中M-RCMS的粒径和形态的可控。制备的M-RCMS具有良好的孔隙结构和较大的比表面积,保水能力强,热稳定性良好。负载过程中,Fe3O4的晶体结构与粒径并未发生改变,这使得M-RCMS具备良好的超顺磁性和有效的磁响应分离性能。
参 考 文 献
[1] Li Z, Cao M, Zhang W. Affinity adsorption of lysozyme with reactive red 120 modified magnetic chitosan microspheres [J]. Food Chemistry, 2014, 145: 749.
[2] Dong S, Xu M, Wei J, et al. The preparation and wide frequency microwave absorbing properties of tri-substituted-bisphthalonitrile/Fe3O4magnetic hybrid microspheres[J]. Journal of Magnetism and Magnetic Materials, 2014, 349: 15.
[3] Zhang H, Li X, He G, et al. Preparation of Magnetic Composite Hollow Microsphere and Its Adsorption Capacity for Basic Dyes[J]. Industrial & Engineering Chemistey, 2013, 52(47): 16902.
[4] 李保强, 贺全志, 罗 阳, 等. 磁性壳聚糖微球制备及在放射性水污染应用研究进展[J]. 水处理技术, 2010, 36(6): 10.
[5] Chang Y, Su Z X. Preparation and characterization of thermosensitive magnetic particles[J]. Materials Science and Engineering, 2002, 333(1/2): 155.
[6] 赵 敏, 王 玮, 李昕芯, 等. 海藻酸钠磁性微粒的制备及对漆酶的固定化[J]. 中国造纸学报, 2008, 23(4): 94.
[7] Reymond F, Vollet C, Plichta Z, et al. Fabrication and characterization of tosyl-activated magnetic and nonmagnetic monodisperse microspheres for use in microfluic-based ferritin immunoassay[J]. Biotechnology Progress, 2013, 29(2): 532.
[8] Hu F, Chen S, Yuan R, et al. Application of magnetic core-shell microspheres on reagentless immunosensor based on direct electrochemistry of glucose oxidase for detection of carbohydrate antigen 19-9[J]. Sensors and Actuators B: Chemical, 2013, 176: 713.
[9] Jaworek A. Micro- and nanoparticle production by electrospraying[J]. Powder Technology, 2007, 176(1): 18.
[10] Widiyandari H, Hogan Jr C J, Yun K M, et al. Production of narrow-size-distribution polymer-pigment-nanoparticle composites via electrohydrodynamic atomization[J]. Macromolecular Materials and Engineering, 2007, 292(4): 495.
[11] Zhou Y T, Niea H L, Christopher Branford-White, et al. Removal of Cu2+from aqueous solution by chitosan-coated magneticnanoparticles modified with alpha-ketoglutaric acid[J]. Journal of Colloidand Interface Science, 2009, 330(1): 29.
[12] 唐爱民, 张宏伟, 陈 港, 等. 原位复合法制备纤维素/磁性纳米复合材料的初步研究[J]. 中国造纸学报, 2006, 21(4): 66.
[13] Li G Y, Jiang Y R, Huang K R, et al. Preparation and properties of magnetic Fe3O4-chitosan nanoparticles[J]. Journal of Alloys and Compounds, 2008, 466(1/2): 451.
[14] Donadel K, Felisberto M D V, Fávere V T, et al.Synthesis andcharacterization of the iron oxide magnetic particles coated with chitosan biopolymer [J].Materials Science and Engineering C, 2008, 28(4): 509.
[15] 吕 昂, 张俐娜. 纤维素溶剂研究进展[J]. 高分子学报, 2007, (10): 937.
[16] 全国塑料标准化技术委员会通用方法和产品分会. GB/T 8330—2008离子交换树脂湿真密度测定方法[S]. 北京: 中国标准出版社, 2009.
[17] 全国塑料标准化技术委员会通用方法和产品分会. GB/T 5757—2008 离子交换树脂含水量测定方法[S]. 北京: 中国标准出版社, 2009.
[18] 李 欣, 李朝兴, 何炳林. 磁性珠状纤维素的性能表征[J]. 离子交换与吸附, 1997, 13(5): 496.
[19] Kaew Prasit C, Hequet E, Abidi N, et al. Quality measurements-application of methyleneblue adsorption to cottonfiber specifie surface area measurement: Part1.Methodology[J]. J of Cotton Sci, 1998(2): 164.
[20] Ewandow Ski Z L. Application of a linear synthetic polymer to improved the properties of cellulose fibers made by the NMMO process[J]. J of Applied Polym Sci, 2002, 83(13): 2762.
[21] 汪朝晖, 廖振方, 赵健新, 等. 静电场对不同液体介质的雾化效果试验研究[J]. 应用基础与工程科学学报, 2010, 18(1): 149.
[22] 谷 军, 吴伟兵, 王 飞, 等. 多孔性再生纤维素磁性微球的制备及性质[J]. 南京林业大学学报: 自然科学版, 2012, 36(3): 111.
[23] Mandal A, Chakrabarty D. Isolation of nanocellulose from waste sugarcane bagasse (SCB) and its characterization[J]. Carbohydrate Polymers, 2011, 86(3): 1291.
[24] Lee D K, Kang Y S, Lee C S. Structure and characterization of nanocomposite Langmuir-blodgett films of poly(maleic monoester)/Fe3O4nanoparticle complexes[J]. Phys Chem B, 2002, 106(29): 7267.
