氯菊酯在沙土表面的光降解
2014-07-24刘芃岩田磊陈艳杰
刘芃岩,田磊,陈艳杰
(河北大学 化学与环境科学学院,河北 保定 071002)
氯菊酯是一种拟除虫菊酯类高效杀虫剂,具有性质稳定、杀虫能力强、残效时间长、安全系数高等优点,常用于农业和家庭防虫,与含氰基结构的菊酯相比,氯菊酯对高等动物毒性更低,同等使用条件下害虫抗性发展相对较慢[1],但是随着大量使用,它在环境介质中的残留量不断累积,仍然可能对生态环境和人体健康造成威胁.Carloni发现在小鼠幼年时对氯菊酯摄入量即使在无明显损害作用水平(NOAEL)也会减少其大脑皮层的成长[2].另外,与人体皮肤接触后氯菊酯会长时间残留并被吸收[3-4].目前对于氯菊酯的研究多为在农业产品中的检测研究[5-6],但是氯菊酯水溶性低,亲脂,决定了环境中的氯菊酯大部分会被吸附在土壤中,少部分进入水体[7],本实验选用沙土做基质研究其光降解情况,对其在土壤中的迁移转化具有重要的理论指导作用.
光化学降解是拟除虫菊酯类农药在环境中迁移转化的一个重要环节,已有一些相关报道,涉及的种类包括:苯醚菊酯、胺菊酯、氰戊菊酯、溴氰菊酯、氯氰菊酯等[8-11].同时,研究农药的光化学降解能够促进开发更为安全和有效的农药使用技术,并且光化学降解已被作为评价农药生态安全性的指标之一,EPA 等机构规定,新农药注册登记时必须提供该农药的光化学降解资料[12-13],中国也颁布了相关的规定[14].目前关于氯菊酯光降解的研究很少,而其他农药光降解的研究也多用丙酮、正己烷、水等溶剂作为介质[15-16],氯菊酯在土壤表面的光降解情况尚不清楚,本研究对于其光化学降解资料的完善具有重要意义.
为了研究氯菊酯在沙土表面的光降解规律,本文通过对样品与光源的距离、沙土厚度、不同光源、不同的pH、含水量、不同添加物等因素的研究,总结了氯菊酯随研究因素的变化规律,分析了氯菊酯在沙土中可能的降解过程,为氯菊酯在复杂的实际环境中的迁移和降解条件的筛选提供了理论依据.
1 材料与方法
1.1 主要仪器与试剂
Agilent 7890A-5975C气相色谱-质谱联用仪(美国安捷伦公司);XPA-2型光化学反应仪(南京胥江机电厂);BF-2000M 型氮气吹干仪(北京八方世纪科技有限公司);KQ-250B 型超声仪(昆山市超声仪器有限公司);LG10-2.4A 离心机(北京雷勃尔离心机有限公司);PHS-2CW 型酸度计(上海理达仪器厂);氯菊酯(纯度>95%,中山市凯达精细化工股份有限公司);腐殖酸(分析纯,天津光复精细化工研究所);正己烷和丙酮(HPLC,J&K);沙土(普通建筑用沙,过0.15~0.20mm 筛网,水洗后烘干);缓冲溶液(由磷酸二氢钾和磷酸氢二钠配置);硝酸钠、硫酸铜、硫酸锰,硫酸铁均为分析纯,本文用水均为超纯水.
1.2 气相色谱-质谱条件
色谱条件:HP-5毛细管色谱柱(30m×0.32mm×0.25μm),进样口温度:220 ℃;模式:不分流;载气:高纯氦气(质量分数≥99.999%);流量:1.0 mL/min;进样量:1μL;升温程序:
质谱条件:离子源,EI源,能量70eV,温度230 ℃,四级杆温度为150 ℃,辅助通道温度为280 ℃.扫描模式,全扫描测定,溶剂延迟4min.
1.3 实验方法
储备液的制备:准确称取5.0mg氯菊酯,溶解在25mL正己烷中制成质量浓度为200mg/L 的氯菊酯储备液,使用时取一定量按需要稀释.
含氯菊酯的沙土样品制备:将200mg/L氯菊酯储备液稀释成5.0mg/L,按沙土与储备液质量(g)和体积(mL)的比例为1:1加入沙土中混合均匀并自然晾干,制成含5.0mg/kg氯菊酯的沙土样品,样品浓度选择根据一般农药大致用量确定,样品可避光、阴凉保存7d.
光降解:按需要称取含氯菊酯的沙土样品均匀铺开放在玻璃板上,面积恒定为2cm×7cm,放入光降解仪中,调整好样品与光源的距离,定时取样进行处理分析.
样品的处理:将沙土和正己烷-丙酮(体积比7:3)混合溶剂按照质量(g)和体积(mL)的比例为1:1混合,超声提取20min,2 500r/min离心10min,用玻璃注射器移取上清液,重复提取3次,合并所得溶液,氮吹浓缩后定容至1mL,用微量注射器取1μL进气质联用仪进行分析.
2 结果与讨论
2.1 标准曲线的制作
按实验方法1.3中所述沙土样品制备方法制备氯菊酯质量分数为0.1,0.5,1.0,2.0,5.0,10.0mg/kg的沙土样品,并提取测定,以峰面积y 为纵坐标,以质量分数x(mg/kg)为横坐标作标准曲线,标准曲线方程为y =17 907x-911.82,R2=0.999 8.
2.2 提取效率的研究
在20g沙土样品中,加入10.0mg/L氯菊酯标准溶液5mL 混匀自然阴干,按实验方法1.3中所述方法处理测定7次,提取效率为77.35%~96.02%.RSD 为7.97%.
2.3 样品与光源的距离对氯菊酯光降解的影响
样品与光源的距离是影响光降解的一个最基本的因素,因为氯菊酯的光降解是分子吸收光能导致化学键断裂而产生的,分子得到的光能会随着距离的增加而减少,降解率也随之降低.实验研究了1.0g样品在300 W汞灯下5,10,15,20,25,30cm 这几个不同距离时降解30min的降解率.实验结果表明:沙土中的氯菊酯的降解率与距离成反比,从5cm 到20cm 随着距离变远,降解率降低的很快,在20cm 之后降解率变化趋于平缓.
2.4 沙土厚度对氯菊酯光降解的影响
农药在土壤中的光降解往往都是在表面进行,所以在表面一定的厚度会对降解产生影响.在铺开面积相同的条件下,1.0g沙土厚度可以忽略,而2.0g的沙土有一定的厚度,所以本实验使用1.0g和2.0g样品,研究这2种情况对氯菊酯最终降解率的影响.图1是样品在300 W 汞灯下距光源10cm 时降解率随时间的变化图,从图1中可知1.0g样品开始降解得很快,30min时降解率就超过50%,之后曲线慢慢变得平缓,90min时降解率能够到达最高96.75%,90min后降解率几乎没有变化.2.0g样品同样在90 min时达到最高降解率74.65%,但是降解率超过50%的时间滞后了20min.因为在条件相同的情况下1.0g样品比2.0g样品更全面地接受了光照,2.0g沙土比1.0g沙土厚,存在光线无法穿透的部分,导致最终降解率下降.
2.5 光源对氯菊酯光降解的影响
不同光源下农药的光降解率会有较大差异,实验分别以300 W 汞灯,100 W 汞灯,350 W 氙灯和500 W金卤灯做光源,比较氯菊酯在不同光源照射下120min内氯菊酯的降解率.图2是1.0g样品在不同类型的光源下,距离光源10cm 时氯菊酯降解率随时间的变化图,由图2可知,不同光源的降解率为350 W 氙灯<100W 汞灯<500W 金卤灯<300W 汞灯.产生这种现象的原因主要与光源的发射光谱能量分布有关.汞灯发射光谱主要集中在紫外区,能量在365.0~366.3nm 达到最大,菊酯分子中的化学键能一般在波长380nm以下,C=O 键与C—H 键分别在164nm 和280nm 光照射下断裂,有利于化学键的断裂.氙灯光谱集中在可见区,波长偏长且能量较低,能量在800~1 000nm 达到最大,不能使拟除虫菊酯化学键断裂,从而降低了降解率.
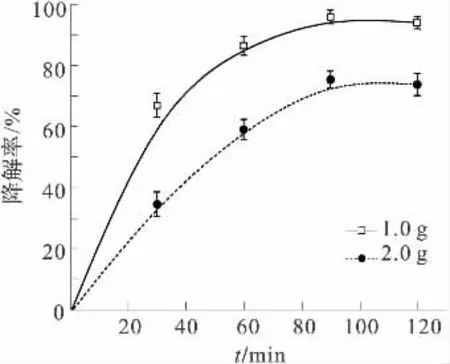
图1 氯菊酯在1.0g和2.0g沙土中的降解率随时间变化Fig.1 Permethrin degradation rate changes with time on the 1.0g and 2.0g sand surface
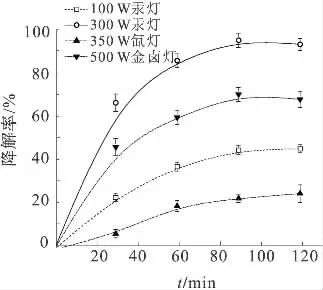
图2 不同光源照射下氯菊酯的降解率随时间的变化Fig.2 Permethrin degradation rate changes with time in different types of light sources
2.6 沙土的含水量对氯菊酯光降解的影响
自然土壤都会含有一定的水分,并且随着天气的变化,含水量也会变化,为了研究含水量对光降解的影响,实验在1.0g和2.0g样品中分别加入0.1~0.5mL超纯水并进行光降解.图3是不同加水量在300 W汞灯下距离10cm 光降解10min时的降解率变化图.由图3可以看出,无论是1.0g还是2.0g沙土,含水量对于沙土表面的光降解影响并不是很大,这与研究对硫磷在土壤中光降解时含水量的影响相符17].因为土壤表面有一定的吸附能力,环境中的水量如果不能保证持续一段时间对固体表面进行冲刷就很难对农药的迁移降解造成影响.
2.7 沙土pH 对氯菊酯光降解的影响
实际土壤的pH 分为几个等级,小于4.5的为极强酸性土壤,大于9.5的为极强碱性土壤,为了研究在不同酸碱度土壤中农药的降解,实验制备pH 为4,5,6,7,8,9的缓冲液10mL,按照环境质量标准中规定的比例土(g):液(mL)=1:2.5加入4.0g沙土中,自然阴干,再加入氯菊酯制成不同pH 的沙土样品,取出1.0g进行光降解.实验所用沙土的原pH 为6.5.图4是不同pH 值的沙土标样在300 W 汞灯距离为15cm时,降解30min时的降解率图.由图可知在干燥的沙土中pH 对氯菊酯光解的影响很小,随着pH 增大降解率略有提升.原因在于干燥的沙土环境中,酸碱并不能像在溶液中那样提供氢离子和氢氧基来发挥作用,而氯菊酯本身在酸性条件下比在碱性条件下稳定.

图3 沙土的不同加水量对氯菊酯降解率的影响Fig.3 Effect of different moisture content of the sand on permethrin degradation rate

图4 不同pH 对氯菊酯降解率的影响Fig.4 Effect of pH on permethrin degradation rate
2.8 腐殖酸对氯菊酯光降解的影响
在实验室环境下氯菊酯在直接光照下能达到较好的去除效果,但实际环境中有更为复杂的成分,影响其对太阳光的吸收能力,很多天然有机物对拟除虫菊酯的光降解起到促进作用[18-19].为了研究土壤中复杂成分的影响,实验选用了土壤中广泛存在的腐殖酸.图5是在1.0g沙土样品中加入不同量的腐殖酸,距300 W汞灯15cm 时光降解30min降解率变化图.由图5可知腐殖酸质量分数在20mg/kg以内时,降解率随着浓度的增加而提高,说明腐殖酸促进了氯菊酯光降解.但是当质量分数继续增加时,光降解效率降低,这是由于腐殖酸本身也会吸收光子,因此,超过一定浓度后会反而抑制氯菊酯的光降解.
2.9 无机离子对氯菊酯光降解的影响
环境土壤中还存在着很多种类的无机成分,为了研究其对氯菊酯降解的影响,实验将几种常见无机盐Fe3+,Cu2+,Mn2+,NO-3水溶液,分别取适量加入沙土中震荡阴干(其加入量根据自然环境中的大致含量确定),再加入氯菊酯,制成含不同无机盐的氯菊酯沙土样品,图6是在1.0g样品距300 W 汞灯15cm 降解30min时降解率变化图.可以看出随着含铁无机盐浓度的增大降解率也明显增大,说明含铁无机盐可以促进光降解反应,含铜的结果相反,说明对光解有抑制作用,可能是铜的存在减少了氯菊酯在土壤上的吸附,影响了氯菊酯对光能的吸收[20].含锰、含硝酸根无机盐对光降解率没有明显影响.
3 沙土中氯菊酯的降解过程
目前土壤中菊酯类农药的降解过程研究尚少,没有系统的研究可以说明整个过程如何,实验使用10mg/kg和50mg/kg的沙土样品,距离300 W 汞灯15cm,分别光解10min,20min,30min和60min,通过气相色谱-质谱对实验结果的分析,发现整个过程中沙土中氯菊酯的含量在不断减少,但是并没有发现二次污染物的产生,这与文献中报道的溶剂中的光降解结果有些差异.因为在沙土中氯菊酯不能像在溶剂那样均一的环境中自由移动,所以氯菊酯降解时产生的烷基自由基、氢氧自由基等氧化剂直接局部发生反应氧化中间产物导致中间产物也很快的降解,而不是像在溶剂中经过一个先由易氧化产物的开始,然后氧化难氧化物质直到都降解完全的降解过程.

图5 腐殖酸对氯菊脂降解率的影响Fig.5 Effect of humus on permethrin degradation rate

图6 不同无机离子对氯菊酯降解率的影响Fig.6 Effect of different inorganic ion on permethrin degradation rate
4 结论
由上述实验结果可知,样品与光源的距离,厚度、光源种类和添加含铁无机盐是影响土壤表面氯菊酯降解的重要因素.靠近光源、减少厚度、使用紫外灯光和添加含铁无机盐均有利于氯菊酯在土壤表面降解.实验的结果表明:沙土表面氯菊酯在紫外灯下降解地比较彻底,并没有产生新的污染.实验只是对几种常见的影响因素进行了摸索研究,虽然沙土比硅胶和氧化铝等更接近实际土壤,但是仍然不是实际土壤,氯菊酯在实际土壤中光降解以及更多的影响因素尚待研究.
随着农药的大量使用,农药在土壤中的残留日益突出,自然环境中,农药在土壤中的光降解普遍存在,研究其在不同条件下的光解具有很重要的理论意义和实用价值.通过对农药的研究,人们可以了解不同环境因素对农药光降解的影响,控制农药在环境中的负面作用,将其对生态系统的破坏降到最低.
[1] JEROME J,SCHLEIER III,ROBERT K D,et al.Toxicity and risk of permethrin and naled to non-target insects after adult mosquito management[J].Ecotoxicology,2010,19:1140-1146.
[2] MANUEL C,CINZIA N,DONATELLA F,et al.The impact of early life permethrin exposure on development of neurodegeneration in adulthood[J].Experimental Gerontology,2012,47:60-66.
[3] 刘大鹏,钱万红,姜志宽,等.氯菊酯在皮肤上的残留率与实践关系的研究[J].中国媒介生物学及控制杂志,2000,11(4):273-275.LIU Dapeng,QIAN Wanhong,JIANG Zhikuan,et al.Study on the relation between time and residual rate of per-methrim on the surface of human skin[J].Chinese Journal of Vector Biology and Control,2000,11(4):273-275.
[4] WILLIAM G R,JOHN H R,JEFFREY H D.Experimental methods for determining permethrin dermal absorption[J].Journal of Toxicology and Environmental Health,2011,74:325-335.
[5] 黄晓会,薛健,吴晓波,等.气相色谱法检测桑叶中有机氯及菊酯类农药[J].分析科学学报,2012,28(3):328-332.HUANG Xiaohui,XUE Jian,WU Xiaobo,et al.Determination of organochlorine and pyrethrpid pesticides in mulberry leaf by gas chromatography[J].Journal of Analytical Science,2012,28(3):328-332.
[6] 庄婉娥,弓振斌,叶江雷.凝胶渗透色谱净化-气相色谱-质谱法同时测定金银花中33种农药残留组分[J].分析化学,2010,38(6):811-816.ZHUANG Wan'e,GONG Zhenbin,YE Jianglei,et al.Determination of 33pesticide residues in honeysuckle by gel permeation chromatography purification and gas chromatography-mass spectrometry[J].Chinese Journal of Analytical Chemistry,2010,38(6):811-816.
[7] 邴欣,汝少国.四种拟除虫菊酯类农药的环境雌激素活性研究[J].中国环境科学,2009,29(2):152-156.BING Xin,RU Shaoguo.Determination of environmental estrogenic activity of four pyrethroid pesticides[J].China Environmental Science,2009,29(2):152-156.
[8] FERNáNDEZ-áLVAREZ M,LORES M,LLOMPART M,et al.The photochemical behaviour of five household pyrethroid insecticides and a synergist as studied by photo-solid-phase microextraction [J].Analytical and Bioanalytical Chemistry,2007,388:1235-1247
[9] LIU Pengyan,LIU Yujie,LIU Qingxue,et al.Photodegradation mechanism of deltamethrin and fenvalerate original research article[J].Journal of Environmental Sciences,2010,22(7):1123-1128.
[10] COLY A,AARON J.Cyclodextrin-enhanced fluorescence and photochemically-induced fluorescence determination of five aromatic pesticides in water[J].Analytica Chimica Acta,1994,360:129-141.
[11] FERNANDEZ-ALVAREZ M,LLOMPART M,GARCIA-JARES C,et al.Investigation of the photochemical behaviour ofpyrethroids lacking the cyclopropane ring byphoto-solid-phase microextraction and gaschromatography/mass spectrometry[J].Rapid Communications in Mass Spectrometry,2009,23:3673-3687.
[12] SOVACS M F.EPA guidelines on environment fate[J].Residue Reviews,1983,85:4-16.
[13] TURNER E.An Assessment of test methods of photolysis of chemical in the environment of brussels,belgium:ecology and toxicology center[J].European Chemical Industry,1981.
[14] 中华人民共和国农业部.农药登记资料规定[Z].2007.
[15] 李玉玲,刘艳,颜冬云,等.拟除虫菊酯类农药的降解与代谢研究进展[J].环境科学与技术,2010,33(4):65-69.LI Yuling,LIU Yan,YAN Dongyun,et al.Research progress on degradation and metabolism of pyrethroid insecticides[J].Environmental Science &Technology,2010,33(4):65-69.
[16] 毕刚,田世忠,冯子刚,等.拟除虫菊酯与有机磷农药混合溶液的光敏降解[J].环境科学学报,1996,16(3):317-324. BI Gang,TIAN Shizhong,FENG Zhigang,et al.Photolysis of pyrethroids blended with organic phosphorus pesticides[J].Acta Scientiae Circumstantiae,1996,16(3):317-324.
[17] HAUTALA R R.Surfactant effects on pesticide photochemistry water and soil[Z].Environmental Protect ion Agency,1978.
[18] PENNEYL M,YUPING C.Photoinduced degradation of carbaryl in a wetland surface water[J].Jounal of Agricultural and Food Chemistry,2002,50:6758-6765.
[19] VIALATON D,PILICHOWSKI J,BAGLIO D.Phototransformation of propiconazole in aqueous media[J].Jounal of Agricultural and Food Chemistry,2001,49:5377-5382.
[20] LIU Tingfeng,SUN Cheng,TA Na,et al.Effect of copper on the degradation of pesticides cypermethrin and cyhalothrin[J].Journal of Environmental Sciences,2007,19:1235-1238.
