4-氨基安替比林法和邻-甲联苯胺法测定游离血红蛋白结果比较
2014-06-13冀慧
冀 慧
(安阳中心血站 河南 安阳 455000)
游离血红蛋白(FHb)含量测定是血站全血及成分血质量要求和质量控制的检查项目之一,也是临床溶血性疾病和溶血性输血反应常用的辅助检查方法。2012年新版《全血及成分血质量要求 GB18469-2012》[1]中对所有含红细胞的制品均要求进行血浆或上清液FHb的含量测定。《血站技术操作规程2012版》[2]推荐方法为邻-甲联苯胺法,该方法操作步骤复杂,试剂需新鲜配制,影响因素较多,重复性和稳定性较差。目前部分血液中心和血站使用三波长法[3]、紫外分光光度法[4]等进行FHb的测定,但未发现使用4-氨基安替比林比色法测定FHb的含量,4-氨基安替比林比色法目前有市售的试剂盒,操作简单快捷。笔者比较了邻-甲联苯胺法和4-氨基安替比林法测定FHb的准确性和稳定性及测量时的注意事项,探讨采供血机构测定FHb含量最适宜的方法。
1 材料与方法
1.1 仪器 分光光度计(上海美谱达V-18D);37℃恒温培养箱(上海新苗DNP-9162BS-Ⅲ型);血球计数仪(日本KX-21)。
1.2 试剂及样品
1.2.1 一般试剂准备:邻-甲联苯胺(分析纯,批号:20130723,天津市光复精细化工研究所);30%过氧化氢溶液(分析纯,批号20130518,天津市津北精细化工有限公司);冰醋酸溶液(分析纯,批号20121113,天津市富宇精细化工有限公司)。邻-甲联苯胺溶液:称取邻-甲联苯胺200 mg,溶于冰醋酸60 ml,溶解后加蒸馏水至100 ml,保存于冰箱中,可用8~12周。1%过氧化氢溶液:由30%的过氧化氢溶液配制而成,现用现配。10%冰醋酸溶液:由冰醋酸溶液用蒸馏水稀释而成,现用现配。血浆游离血红蛋白测定试剂盒(北京瑞尔达生物科技有限公司,20131202);全血质控物(MAKER,111312G);KX-21 稀 释 液 (日 本,20130805);KX-21溶血剂(日本,20130731)。
1.2.2 血红蛋白标准品的制备:新鲜全血5 ml离心,1 500 g离心15 min后弃去上层血浆及白膜层;加3倍体积0.9%氯化钠溶液,混匀后离心,430 g离心10 min,弃去上清液,重复3次得到压积红细胞;加15 ml蒸馏水,轻摇30 min后离心,10 000 g离心30 min,弃去下层沉淀[5],用血球计数仪测其浓度;用0.9%氯化钠溶液调节浓度至100 g/L,于低温冰箱中保存,得到FHb标准品储备液[6],用时稀释成相应浓度。
1.3 方法
1.3.1 邻-甲联苯胺操作方法[7]:试剂处理后,迅速在435 nm波长下比色,光径10 mm,空白调零,结果计算:FHb/(mg/L)=A样品/A标准×100。正常人群FHb参考值 <40 mg/L[7],解冻红细胞 FHb参考值≤1 000 mg/L[1],红细胞制品中FHb的含量一般都要远远高于正常人群参考值。具体步骤见表1。

表1 邻-甲联苯胺法操作步骤
1.3.2 4-氨基安替比林操作方法:按照血浆游离血红蛋白测定试剂盒说明书进行操作(北京瑞尔达生物科技有限公司)。在505 nm波长下比色,光径10 mm,空白调零,结果计算:FHb(mg/L)=A样品/A标准×100,见表2。
1.3.3 线性范围:将FHb标准品(100 g/L)用0.9%氯化钠溶液分别稀释成 50、100、150、200、250 mg/L,用邻-甲联苯胺比色法,平行分析3次;将FHb标准品(100 g/L)用0.9%氯化钠溶液分别稀释成50、100、200、300、400 mg/L,用4-氨基安替比林比色法,平行分析3次。

表2 4-氨基安替比林法操作步骤
1.3.4 精密度:将FHb标准品(100 g/L)用0.9%氯化钠溶液分别稀释成100、500、1 000 mg/L,用两种方法分别测定其FHb含量,每份样品平行分析5次。统计分析5个平行样品之间的变异性。
1.3.5 准确性:将FHb标准品(100 g/L)用0.9%氯化钠溶液分别稀释成100、500、1 000 mg/L,用两种方法分别测定其FHb含量,每份样品平行分析3次,统计分析测定的准确性。
1.3.6 稳定性:将FHb标准品(100 g/L)用0.9%氯化钠溶液分别稀释成200、400、800 mg/L,用两种方法分别测定其 FHb含量及放置5、10、30、60 min后的FHb吸光度值。
1.4 数据分析 统计学分析采用SPSS 19.0进行处理,FHb含量与吸光度的关系采用相关性分析,率的比较采用χ2检验,P<0.05为差异具有统计学意义。
2 结果
2.1 线性范围 邻-甲联苯胺法:FHb≤250 mg/L时有良好的线性关系(r=0.996,P <0.05);4-氨基安替比林法:FHb≤400 mg/L时有良好的线性关系(r=0.999,P <0.05),见表 3。4-氨基安替比林法的线性范围大于邻-甲联苯胺法的线性范围,用线性范围宽的4-氨基安替比林法测定高浓度FHb含量时可减少对测定样品的稀释倍数。

表3 两种方法测定标准品含量与吸光度关系
2.2 精密度 邻-甲联苯胺法:低浓度样品 CV=4.01%,中浓度样品 CV=8.91%,高浓度样品 CV=7.52%;4-氨基安替比林法:低浓度样品CV=2.61%,中浓度样品CV=3.63%,高浓度样品CV=4.61%。两种方法变异系数均≤10%,但4-氨基安替比林法在测定高中低不同浓度样品时的变异系数相差不大,邻-甲联苯胺法在测定高中浓度样品时变异系数相差较大,4-氨基安替比林法的试验重复性要优于邻-甲联苯胺法,见表4。

表4 两种方法测定精密度试验结果(mg/L)
2.3 准确性 邻-甲联苯胺法(平均值为93.02%)和4-氨基安替比林法(平均值为93.32%)在测定高中低不同浓度样品时的准确度相差不大,差异均无统计学意义(P >0.05)。见表5。

表5 两种方法测定准确度试验结果
2.4 稳定性 邻-甲联苯胺法反应结束后,高中低3个浓度样品的吸光度值随时间的不断延长而不断降低,呈直线向下的趋势,见图1;4-氨基安替比林法反应结束后,高中低3个浓度样品的吸光度值没有太大变化,基本上呈直线趋势,见图2。4-氨基安替比林法因试剂中加入一定量的稳定剂,反应结束后颜色变化很稳定。4-氨基安替比林法的稳定性要大大优于邻-甲联苯胺法。

图1 邻-甲联苯胺法测定结果稳定性
3 讨论
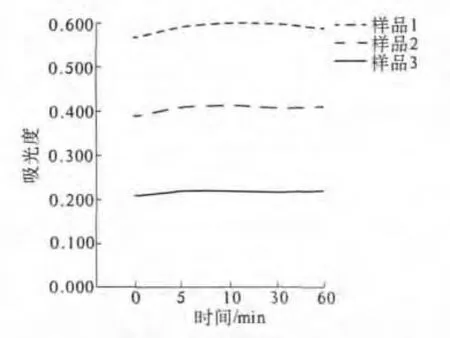
图2 4-氨基安替比林法测定结果稳定性
FHb是血浆中血红蛋白的含量,是血液保存质量测定的常规指标。在血液采集和血液成分制备过程中有时会造成红细胞破裂而释放出血红蛋白。如输入的血液中含有过量的FHb,会对机体造成伤害,主要原因在于Hb中的血红素可引起自由基产生和脂质过氧化反应,导致组织损伤,比较严重的后果是对神经系统具有毒性作用[8];另外,输入过量的Hb还可迅速结合掉循环系统中的NO,引起血管无法舒张,最终导致受血者血压升高,缺血缺氧,甚至威胁生命[9]。2012年新版《全血及成分血质量要求GB18469-2012》中对血站制备的所有含红细胞的制品均要求进行血浆或上清液FHb的含量测定。《血站技术操作规程2012版》推荐方法为邻-甲联苯胺法,该方法操作步骤复杂,试剂需新鲜配制,影响因素较多,而且所用试剂冰醋酸和过氧化氢对人体皮肤和黏膜均有刺激性和腐蚀性,且邻-甲联苯胺属于有机有毒品,对人体还有一定的致癌作用。因冰醋酸具有挥发性,过氧化氢易氧化分解,所以冰醋酸溶液和过氧化氢溶液均需要新鲜配制,否则二者含量都会随保存时间的增加而不断减少,引起样品吸光度值变小。我们在用邻-甲联苯胺法测定较多样品时,如测定时间超过3 h,则需重新配制过氧化氢溶液和冰醋酸溶液,并将过氧化氢溶液配置后盛放于棕色瓶中避光保存;邻-甲联苯胺溶液虽说可在冰箱保存8~12周,但我们发现邻-甲联苯胺溶液在保存过程中颜色会逐渐加深,如颜色明显变深,则需重新配制。4-氨基安替比林法目前有市售的整套试剂盒,无需新鲜配制试剂,大大简化了操作步骤,减少了有害试剂对人体的伤害。因试剂中含有稳定剂,结果稳定可靠,重复性好。综上所述,4-氨基安替比林法相对于邻-甲联苯胺法更适合采供血机构测定FHb含量使用。
[1] 中华人民共和国卫生部.全血及成分血质量要求[S].GB18469-2012.
[2] 中华人民共和国卫生部.血站技术操作规程(2012版)[S].卫医政发[2012]1号.
[3] 于清,王红,刘嘉馨,等.游离血红蛋白测定:三波长法和邻联甲苯胺法的比较研究[J].中国输血杂志,2012,25(2):138-141.
[4] 王莉,张淑琴,赵君,等.紫外分光光度法检测血浆游离血红蛋白[J].中国输血杂志,2006,19(6):477-479.
[5] Cripps C M.Rapid method for the estimation of plasma haemoglobin levels[J].J Clin Pathol,1968,21(1):110-112.
[6] 掌友湖,梁启忠,程玉根.全血质控物配制标准液在血浆游离血红蛋白测定中的应用[J].中国输血杂志,2009,22(10):823-824.
[7] 中华人民共和国卫生部医政司.全国临床检验操作规程[M].第3版.南京:东南大学出版社,2006:258.
[8] 吴波,方国恩.游离血红蛋白主要测定方法及输入过量对机体影响的研究进展[J].实用医药杂志,2008,25(5):612-614.
[9] Gross S S,Lane P.Physiological reactions of nitric oxide and hemoglobin:a radical rethink[J].Proc Natl Acad Sci U S A,1999,96(18):9967-9969.
