子宫肌瘤MRI特征与高强度聚焦超声消融疗效
2014-06-09姜曼赵卫易根发姚瑞红
姜曼,赵卫,易根发,姚瑞红
·非血管介入Non-vascular intervention·
子宫肌瘤MRI特征与高强度聚焦超声消融疗效
姜曼,赵卫,易根发,姚瑞红
目的通过对高强度聚焦超声消融(HIFUA)治疗子宫肌瘤前后MRI的表现进行对比观察,探讨影响子宫肌瘤HIFUA疗效的因素。方法通过回顾性分析128例(154枚)子宫肌瘤患者HIFUA治疗前、后病灶MRI表现及临床资料,观察各组肌瘤体积消融率及能效因子。结果子宫肌瘤病灶位于后壁、MRIT2WI高信号、MRIT1WI增强高信号者HIFUA治疗体积消融率相对较低,所需能效因子高。结论HIFUA治疗子宫肌瘤疗效与肌瘤位置、MRIT2WI信号强度及血供情况有关,与肌瘤的大小无关。
子宫肌瘤;核磁共振信号;超声消融;能效因子
子宫肌瘤的治疗方法主要根据患者的症状、生育要求、心理等情况综合考虑。目前治疗方法主要有外科手术治疗、微创治疗、药物治疗等。高强度聚焦超声消融(high intensity focused ultrasound ablation,HIFUA)是一种非侵袭性治疗子宫肌瘤的方法,它利用适当频率超声波的束射-会聚特性、在人体组织中的良好穿透性和组织固有的吸声特性,所吸收声能转化的热能使组织升温至蛋白变性的阈值温度(毒理温度)而发生凝固性坏死[1]。HIFUA治疗子宫肌瘤可减轻、缓解子宫肌瘤引起的临床症状和体征,具有安全,有效,并发症少等优点[2-3],已逐渐被医患接受。HIFUA治疗子宫肌瘤的疗效差异性较大[4]。本研究探讨MRI特征与HIFUA治疗子宫肌瘤疗效的关系,明确影响消融治疗效果的因素,指导临床实践,为患者选择最优化的治疗方法。
1 材料与方法
1.1 材料
1.1.1 临床资料选择2011年8月—2013年3月,我院经临床及B超、MRI确诊并行HIFUA治疗的子宫肌瘤患者128例,共154个肌瘤,其中单发肌瘤95例,多发肌瘤(2~4个)33例;年龄26~49岁平均(38±5)岁,入选本次研究,所有患者均签署了知情同意书。
1.1.2 入选标准①症状性子宫肌瘤及患者迫切要求治疗的非症状性子宫肌瘤;②绝经期前女性;③治疗系统机载超声可见的子宫肌瘤,肌瘤直径在2 cm以上;④患者能准确交流治疗过程中的感受;⑤患者均行一次性超声消融;⑥同意接受镇静镇痛下超声消融治疗。
1.1.3 排除标准①宫颈肌瘤、血管平滑肌瘤、子宫肉瘤;②宫颈细胞学检查(TCT)提示有异常细胞者;③妇科检查及影像学检查怀疑有盆腔内组织、器官粘连者;④合并妇科其他疾病者,如严重的阴道炎、急性盆腔炎、肿瘤等;⑤妊娠期及哺乳期妇女;⑥声通道不良者,如下腹部有严重的手术瘢痕或接受过大剂量放疗;或患有结缔组织疾病;⑦合并严重重要器官器质性病变,如高血压、心脏病、脑血管疾病及其他严重全身性疾病等;⑧因患者自身原因资料未完善者8例;⑨因患者肌瘤多发或自身耐受限制行2次超声消融者3例。
1.1.4 检查和治疗器材成像设备采用荷兰Philips公司Achieva 3.0T双梯度超导磁共振成像仪及GE Signa HDxt 1.5T超导磁共振成像仪,常规MR成像采集横断位、矢状位、冠状位扫描,动态增强MR使用顺磁性对比剂钆喷替酸葡甲胺(Gd-DTPA),采集矢状位、冠状位扫描,HIFUA术后1周复查磁共振,扫描序列、参数与术前一致。
JC200型聚焦超声肿瘤治疗系统采用重庆海扶(HIFU)技术有限公司生产设备。该系统主要治疗参数:治疗功率100~400 W,产生的生物学焦域为3 mm×3 mm×8 mm,治疗头频率0.8 MHz,焦距132 cm,介质水含气量<3×10-6,超声对比剂六氟化硫微泡。
1.2 方法
1.2.1 研究分组①根据子宫肌瘤的位置分为前壁、后壁及侧壁肌瘤。②以正常子宫肌层及骨骼肌信号为参照,根据MRIT2WI信号将子宫肌瘤分为4组,低信号:子宫肌瘤信号低于或等于骨骼肌;等信号:子宫肌瘤信号低于或等于子宫肌层,高于骨骼肌;高信号:子宫肌瘤信号均匀高于子宫平滑肌;高低混杂信号:子宫肌瘤信号为高于子宫肌层和等于子宫肌层信号相混杂。③根据子宫肌瘤平均径线分为直径(d)<4 cm、4~7 cm和>7 cm 3组(平均径线d=(a+b+c)/3在T2WI压脂序列上测量肌瘤三维径线:横断位平行子宫内膜方向测得最大横径a;矢状位上平行子宫内膜方向测得肌瘤的最大前后径b;垂直于前后径测得最大长径c)。④根据子宫肌瘤MRIT1WI增强信号与子宫平滑肌信号相比分为3组,T1增强高信号,指子宫肌瘤MRIT1增强信号比子宫平滑肌信号高;T1增强等信号,指子宫肌瘤MRIT1增强信号与子宫平滑肌信号相等;T1增强低信号,指子宫肌瘤MRI T1增强信号比子宫平滑肌信号低。
1.2.2 疗效指标
1.2.2.1 体积消融率(non-perfused volume ratio,NPVR):在T2WI上测量子宫肌瘤径线,T1WI增强测量术后无灌注区体积(non-perfused volume,NPV):
靶肌瘤体积(mm3)=0.523 3×a×b×c;
体积消融率=无灌注区体积/靶肌瘤体积× 100%
(a为横径;b为前后径;c为长径)
1.2.2.2 能效因子:HIFUA治疗完毕后,记录每个肌瘤的治疗剂量、治疗时间、治疗功率。计量学用能效因子(energy-efficiency factor,EEF)表示,为单位体积消融所需的超声能量。

其中,TD表示治疗剂量(therapeutical dose,TD);V表示无灌注区体积;η表示HIFU换能器聚焦系数,η=0.7;P表示HIFU源声功率(W);t表示辐照疗时间(s)。
1.3 统计学方法
通过SPSS17.0统计软件进行数据分析,数据结果以x±s表示。根据MRI表现,对子宫肌瘤的位置、MRIT2WI信号、平均径线、血供情况与肌瘤消融反应性进行单因素F检验,P<0.05为差异有统计学意义,进而进行SNK-q检验。
2 结果
2.1 不同位置的肌瘤HIFUA结果
前壁、后壁、侧壁肌瘤体积消融率分别为(85.32± 12.52)%、(68.64±18.31)%、(76.42±20.62)%;EEF分别为(7.91±2.32)J/mm3、(12.32±4.73)J/ mm3、(9.42±1.54)J/mm3。HIFUA疗效与肌瘤位置差异有统计学意义(P<0.05),后壁肌瘤超声消融效果相对较差,所需EEF较高,表1、图1。
2.2 MRIT2WI信号特征与肌瘤HIFUA结果
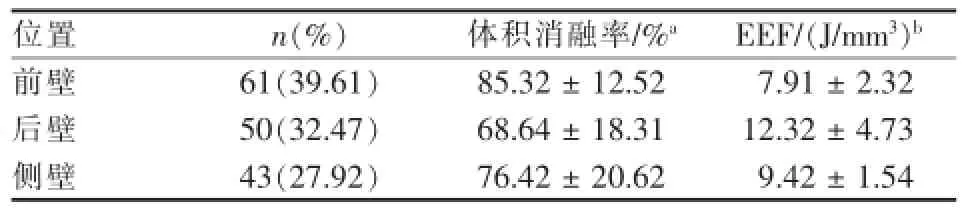
表1 不同位置子宫肌瘤体积消融率结果
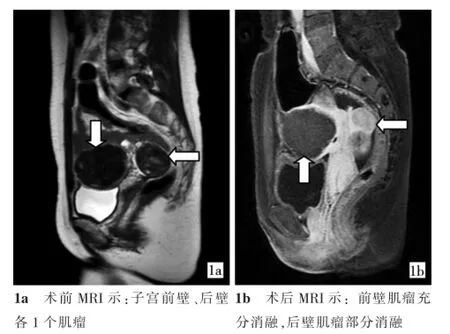
图1 不同位置子宫肌瘤HIFUA疗效反应
MRIT2WI信号为低、等、高、混杂信号的子宫肌瘤体积消融率分别为(86.03±11.44)%、(70.43± 14.54)%、(64.33±17.51)%、(71.54±19.32)%;能效因子分别为(6.30±2.53)J/mm3、(10.71±1.84)J/ mm3、(17.64±3.41)J/mm3、(8.24±2.72)J/mm3。MRI T2WI高信号的子宫肌瘤体积消融率明显低于低信号的肌瘤,高信号的肌瘤EEF明显高于低信号肌瘤。子宫肌瘤HIFUA疗效与MRIT2WI信号的差异有统计学意义(P<0.05),表2、图2。
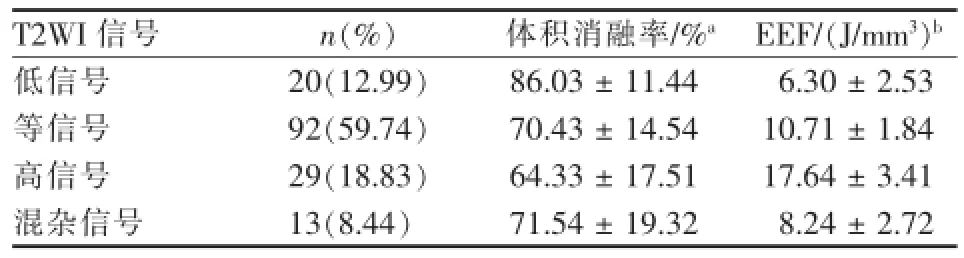
表2 子宫肌瘤MRIT2WI信号体积消融率结果
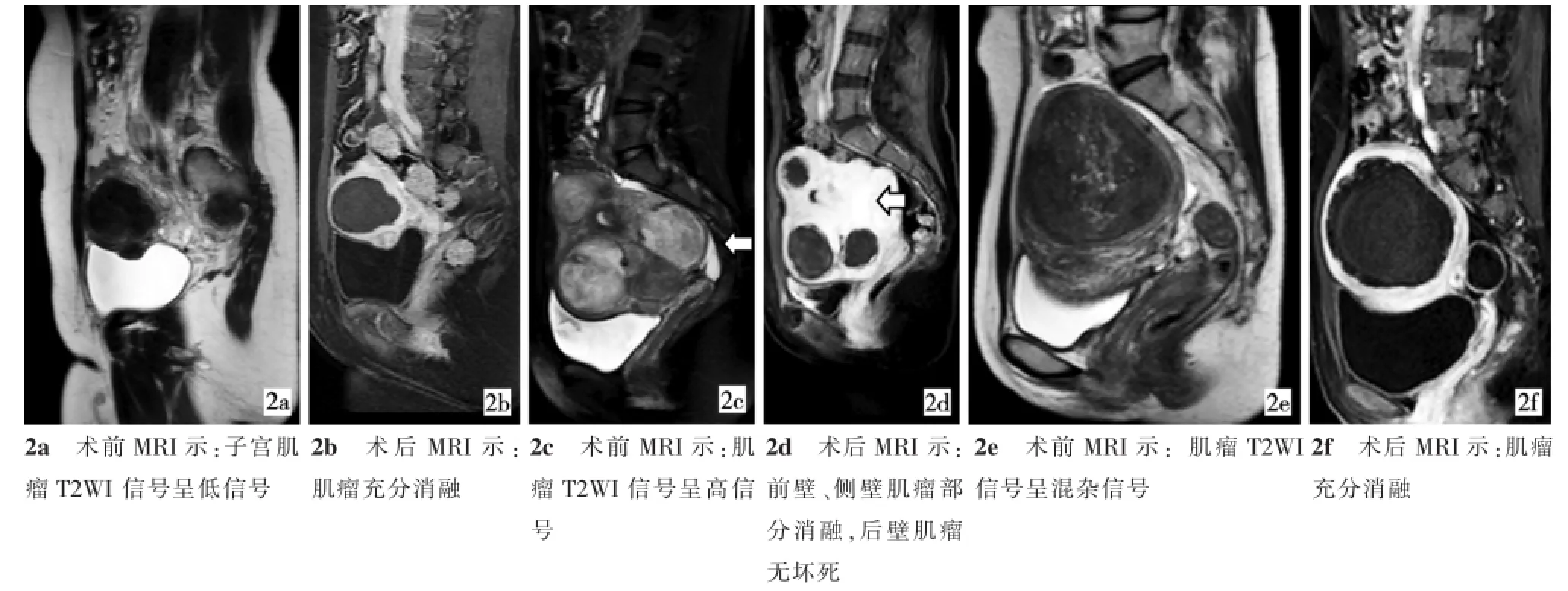
图2 子宫肌瘤MRI信号与HIFUA疗效反应性
2.3 不同大小的肌瘤HIFUA结果
平均径线d<4 cm,4~7 cm,d>7cm的肌瘤体积消融率为分别为(80.70±12.63)%、(82.54± 14.31)%、(78.30±18.74)%;能效因子分别为(8.74± 2.54)J/mm3、(11.81±3.32)J/mm3、(5.54±3.52)J/ mm3。4~7 cm的肌瘤体积消融率略高于其他两组,但不同大小肌瘤体积消融率差异无统计学意义(P>0.05);d>7 cm的肌瘤能效因子最低,不同大小肌瘤能效因子差异有统计学意义(P<0.05),表3、图3。
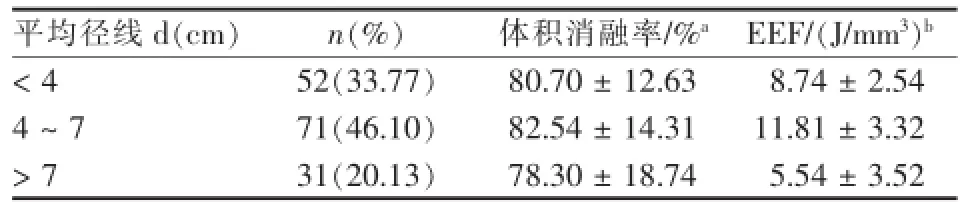
表3 不同大小子宫肌瘤体积消融率结果
2.4 不同血供的肌瘤超声消融结果
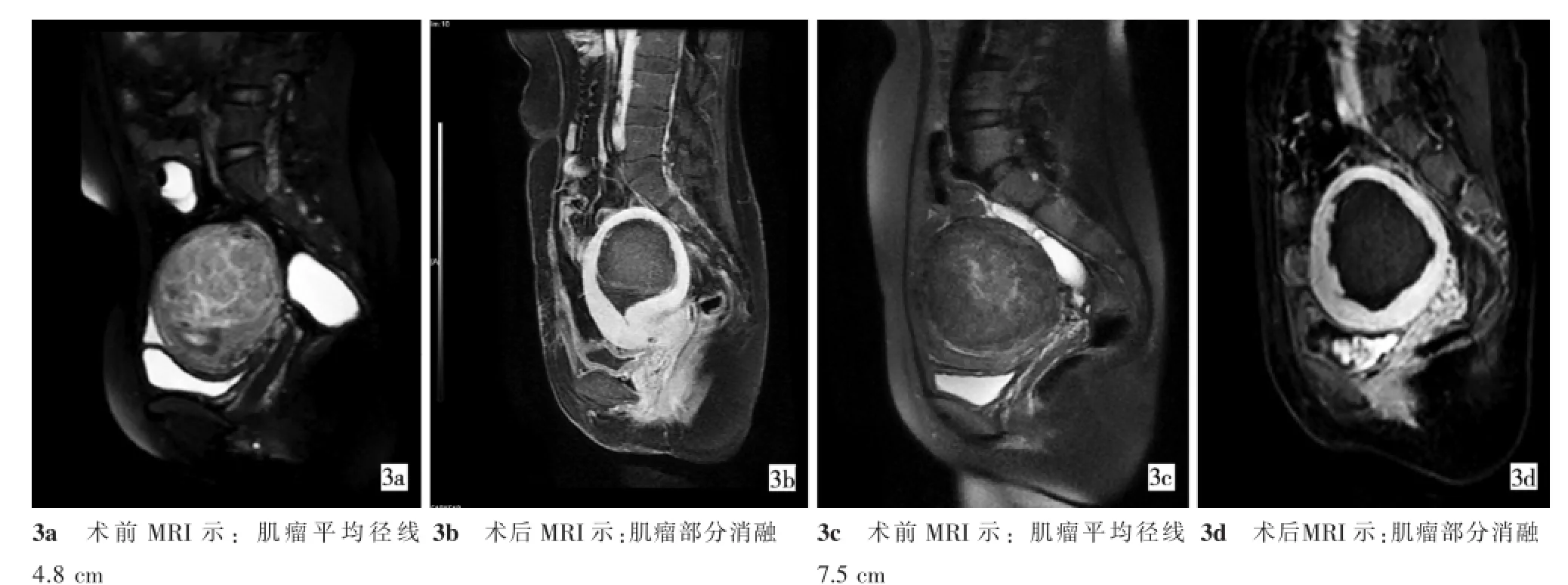
图3 不同大小的肌瘤HIFUA疗效的反应性
MRIT1WI增强信号为低信号、等信号、高信号的子宫肌瘤体积消融率分别为(83.30±16.72)%、(75.83±17.21)%、(67.32±15.63)%;EEF分别为(8.84±1.93)J/mm3、(11.72±3.21)J/mm3、(16.83± 3.62)J/mm3。MRIT1增强信号越高HIFUA体积消融率越低,EEF越高,不同血供的肌瘤消融疗效差异有统计学意义(P<0.05),表4、图4。

表4 不同血供子宫肌瘤体积消融率结果
3 讨论
MRI是目前评价HIFUA治疗子宫肌瘤疗效的可靠方法。MRI空间、软组织分辨率高,能准确地判断肿瘤的形态、大小、解剖学位置以及肌瘤的血供,从而准确判断超声消融治疗的效果。有研究表明,消融10%肌瘤体积即可以减轻子宫肌相关症状[5],消融子宫肌瘤70%体积,其2年的临床效果与子宫肌瘤剔除术相当[6-7]。
EEF为单位体积消融所需的超声能量,表示损伤单位体积组织所需的能量大小,是超声消融子宫肌瘤的量化指标。EEF越小,表示损伤组织的能量沉积效率越高,为损伤一定体积的组织需要较小的能量或以一定的能量可以致较大体积的组织损伤。
在HIFUA治疗过程中,治疗前壁肌瘤时一般只需要将膀胱充盈到一个合适的程度,将肠道推挤出去,建立一个超声通道来治疗肌瘤,因此前壁肌瘤周边的组织器官主要为膀胱、正常子宫等,肌瘤位置相对较浅,超声在传导过程中的衰减就越少,能量容易沉积,并且前壁肌瘤距离骶骨较远,相对较安全。后壁的肌瘤,其深方距离骶骨较近,周边有神经组织和肠管[8],HIFUA治疗时因骶骨反射,后场的反应(骶尾骨疼痛,臀部疼痛,肛门疼痛,双下肢疼痛等)较大[8],加之离体表较远并多需利用推挤水囊建立超声通道,超声波能量在传导过程中衰减,同时水囊增加了反射界面,降低疗效,而出现皮肤烧灼、水泡等损害的概率增加[9]。EEF与靶区深面到皮肤表面的距离有关,距离越大,所需的能量越大,所以后壁肌瘤消融时间较长,所需剂量多。治疗时避免出现并发症,需严格掌控治疗时间及治疗剂量。
根据MR成像原理,MR信号强度取决于组织的质子密度和T1、T2弛豫时间,因此不同质子密度、T1和T2弛豫时间的组织,其信号强度是不同的。子宫肌瘤MRI信号形成的病理基础:子宫肌瘤内部MRI信号的特点取决于平滑肌细胞与结缔组织含量的比例,细胞的形状、排列、分布及是否变性[10]。子宫肌瘤在平扫MRIT1WI上均呈等或低信号,无显著差异,在T2WI上病灶信号与子宫肌层及宫腔黏液信号有很大的反差,颇具特征[11]。根据MRI信号特点对子宫肌瘤进行分型:①普通未变性肌瘤,在T2WI上呈均匀低信号,一般认为与肌瘤胶原纤维的含量较多,其间缺乏足够空间储存液体和黏蛋白有关;②富含细胞性肌瘤,在T2WI上呈均匀或略不均匀高信号,可能与肿瘤大小、细胞成分有一定的关系;③肌瘤囊性变,肌瘤信号明显不均,可见局限性、片状水样低T1WI信号、高T2WI信号区;④黏液样变肌瘤,在T2WI上肌瘤内可见局灶性不均匀高信号区,边缘不规则;⑤红色变肌瘤,在T1WI上呈高信号且脂肪抑制成像后信号强度不降低,T2WI上信号多变,可呈高或低信号;⑥肌瘤恶变,在肌瘤内可见大片出血、坏死区,肌瘤形态不规则,边界不清楚。

图4 不同血供(部位)的肌瘤HIFUA疗效的反应性
依据其病理学组织的特点,子宫肌瘤在影像上有不同的表现形式。子宫肌瘤在MRIT2WI上呈高信号,表明肌瘤含水量增多,胶原纤维含量减少,所以行HIFUA治疗时,能量不易沉积,消融效果较差。当子宫肌瘤发生囊性变、黏液样变等退行性变时,肌瘤内部成分不均匀,MRIT2WI信号呈混杂信号,消融效果与肌瘤内部成分有关。所以MRI信号特点反映了子宫肌瘤的病理学组织类型,故根据子宫肌瘤术前MRIT2WI表现可预测HIFUA疗效反应性,为临床的诊治提供依据。
子宫肌瘤大小对消融疗效影响不大。子宫肌瘤瘤体较小时,其滋养血管较细,内部血流不丰富,HIFUA治疗容易使滋养血管闭塞,能量容易沉积。子宫肌瘤体积大,说明其生长时间长,肌瘤内部纤维组织含量高,结构致密,声阻较大;另外肌瘤内部回声不均质,组织声学性质不均质致声波散射及吸收增加,HIFUA时能量易沉积[12];并且肌瘤越大其内部缺血的可能就越大,消融效果也越好。虽然肌瘤的大小对消融效果影响不大,但肌瘤越大消融所需的效能因子较低,表明子宫肌瘤越大损伤组织的能量沉积效率越高。但子宫肌瘤过大,消融时间及所需能量较多,出现并发症的概率增大,所以较大的肌瘤很难一次性消融。
增强MRI中若肌瘤的图像信号高于子宫肌层的图像信号,则认定为血供丰富。血供丰富的肌瘤在行HIFUA治疗时,热量很容易经过血流流失,难以沉积,达不到使肌瘤发生凝固、坏死的治疗温度,故增强扫描高信号的肌瘤消融效果相对较差。另外,HIFUA对肿瘤血管的作用与血管管径、血流速度等有关[13],HIFUA可将2 mm以下的肿瘤滋养血管闭塞,使肌瘤发生缺血坏死,但对大血管闭塞效果较差,即使短期内血管闭塞,而子宫动脉侧支吻合支可使子宫肌瘤血运部分再通,从而影响治疗效果。HIFUA主要通过热量积累达到高温效应,使组织发生凝固性坏死,所以肌瘤内部血流情况对HIFUA治疗疗效影响显著。
本研究旨在明确影响HIFUA治疗子宫肌瘤疗效反应性的因素,通过MRI特征表现预测HIFUA治疗子宫肌瘤的疗效反应性,指导临床,选择合适的治疗方案。
[1]牛凤岐,朱承纲,程洋.国内高强度聚焦超声12年历程的评说[J].中华医学超声杂志:电子版,2012,9:385-392.
[2]陈亚民,郭慧石,杨亚莉,等.高强度聚焦超声治疗子宫肌瘤79例临床分析[J].中国现代医药杂志,2009,11:96-98.
[3]王冬,杨珂,闵加艳,等.高强度聚焦超声联合纳米微泡造影剂对兔VX2乳腺移植瘤辐照效果的影响[J].中国介入影像与治疗学,2012,9:213-216.
[4]祝宝让,杨武威,李静,等.高强度聚焦超声消融子宫肌瘤疗效相关因素分析[J].中华临床医师杂志:电子版,2012,6:374-377.
[5]Fennessy FM,Tempany CM,Mcdannold NJ,et al.Uterine leiomyomas:MR imaging-guided focused ultrasound surgery—results of different treatment protocols[J].Radiology,2007, 243:885-893.
[6]Stewart EA,Gostout B,Rabinovici J,et al.Sustained relief of leiomyoma symptoms by using focused ultrasound surgery[J]. ObstetGynecol,2007,110:279-287.
[7]Hanafi M.Predictors of leiomyoma recurrence after myomectomy[J].ObstetGynecol,2005,105:877-881.
[8]鄢利梅,何佳,黄国华,等.高强度聚焦超声消融治疗子宫后位肌瘤的临床研究[J].中国超声医学杂志,2012,28:72-74.
[9]Zhang L,Chen WZ,Liu YJ,et al.Feasibility of magnetic resonance imaging-guided high intensity focused ultrasound therapy for ablating uterine fibroids in patients with bowel lies anterior to uterus[J].Eur JRadiol,2010,73:396-403.
[10]Hynynen K,Chung AH,Colucci V,et al.Potential adverse effects of high-intensity focused ultrasound exposure on blood vessels in vivo[J].Ultrasound Med Biol,1996,22:193-201.
[11]韩慧敏,王清涛.子宫肌瘤病理特点与低场MRI表现对照分析[J].临床军医杂志,2011,39:1172-1174.
[12]祝宝让,杨武威,李静,等.高强度聚焦超声消融子宫肌瘤疗效相关因素分析[J].中华临床医师杂志:电子版,2012,6:374-377.
[13]韩慧敏,王清涛.子宫肌瘤的低场MRI表现及诊断价值(附24例分析)[J].临床军医杂志,2008,36:573-575.
MRI features of uterine fibroids and high-intensity focused ultrasound ablation treatment
JIANG
Man,ZHAOWei,YIGen-fa,YAO Rui-hong.Department of Medical Imaging,the First Affiliated Hospital of Kunming Medical University,Kunming,Yunnan Province 650032,China
ZHAOWei,E-mail:13888510359@139.com
ObjectiveTo explore the factors influencing the therapeutic results of uterine fibroids treated with high-intensity focused ultrasound ablation(HIFUA)through comparing the postoperative MRI findingswith preoperative ones.M ethods The clinical data of 128 patientswith uterine fibroids(154 lesion in total),including MRI findings and clinicalmaterials,were retrospectively analyzed.The ablated volume ratio and the energy-efficiency factor of uterine fibroids were estimated.The results were analyzed.Results The ablated volume ratio was relatively lower in the uterine fibroids thatwere located at the posterior wall of the uterine and showed high signal on T2WIand enhanced high signal on T1WI,and these lesions required higher energy factor.Conclusion The therapeutic effect of HIFUA for uterine fibroids is related to the lesion’s location,the signal intensity on T2WI and its blood supply,and the therapeutic effect lacks the relationship to the lesion’s size.(J Intervent Radiol,2014,23:314-319)
uterine fibroid;MRIsignal;ultrasound ablation;energy-efficiency factor
R737.33
A
1008-794X(2014)-04-0314-06
2013-06-08)
(本文编辑:俞瑞纲)
10.3969/j.issn.1008-794X.2014.04.011
650032昆明医科大学第一附属医院医学影像科;
赵卫E-mail:13888510359@139.com
