五子衍宗丸高效液相色谱指纹图谱研究*
2014-05-15刘伟周建良陈碧莲祝明
刘伟,周建良,陈碧莲,祝明
(1.浙江中医药大学,杭州 310053;2.浙江省食品药品检验研究院,杭州 310004)
五子衍宗丸高效液相色谱指纹图谱研究*
刘伟1,周建良2,陈碧莲2,祝明2
(1.浙江中医药大学,杭州 310053;2.浙江省食品药品检验研究院,杭州 310004)
目的 建立五子衍宗丸的高效液相色谱(HPLC)指纹图谱。方法使用Agilent Extend C18(250 mm× 4.6 mm,5 μm)色谱柱,柱温30℃,以乙腈-甲醇(10∶1)和0.4%磷酸为流动相,梯度洗脱,流速1.0 mL·min-1,检测波长254 nm,并利用液相色谱-质谱(LC-MS)对主要色谱峰进行指认。结果根据LC-MS数据、对照品比对或文献参照对10个共有峰中的9个色谱峰进行了指认。用建立的对照指纹图谱测定16批五子衍宗丸,其相似度均>0.93。结论该方法精密度、稳定性、重复性良好。该方法为五子衍宗丸的全面质量评价奠定基础。
五子衍宗丸;指纹图谱;色谱法,高效液相
指纹图谱是评价含多组分的复杂中药样品整体质量的有效手段,中药或中成药的色谱指纹图谱分析方法是药物指纹图谱分析的一个分支[1-4]。近年来,应用色谱指纹图谱分析方法对中药材及中药成药的质量评价已日益广泛[5-7]。五子衍宗丸是由枸杞子、菟丝子(炒)、覆盆子、五味子(蒸)和车前子(盐炒)加工制成的丸剂,具有补肾益精的功效[8]。《中华人民共和国药典》2010年版一部收载的五子衍宗丸的质量标准中只规定枸杞子、五味子甲素的薄层色谱(thin-layer chromatography,TLC)化学鉴别方法,但无含量测定项。目前文献报道的五子衍宗丸含量测定主要是针对五味子甲素、五味子乙素[9-10]及金丝桃苷[11]等单一成分的高效液相色谱(high performance liquid chromatography, HPLC)法,这些方法远不能满足中药现代化的质量控制要求。因此,为了更有效地控制五子衍宗丸的质量,笔者采用HPLC法建立五子衍宗丸的指纹图谱,以便实现从多药物、多成分的系统化角度控制其内在质量。
1 仪器与试药
1.1 仪器 Shimadzu LC-20ADXR高效液相色谱仪(配备在线脱气机、二元泵、自动进样器、柱温箱和PDA检测器);美国Agilent 6430液相色谱-三重四级杆质谱联用仪,配有ESI离子源和美国Agilent 1260快速液相色谱仪(RRLC)(配有在线脱气机、二元泵、自动进样器、柱温箱和可变波长检测器);KODO JAC 4020P超声波清洗器;METTLERTOLEDO AG285电子天平(十万分之一)。
1.2 试药 绿原酸(批号:110753-200413)、金丝桃苷(批号:1521-200202)、毛蕊花糖苷(批号:111530-200505)、山奈酚(批号:110861-200405)、五味子醇甲(批号:110857-200406)、五味子甲素(批号:0764-200107)和五味子乙素(批号:110765-200407)对照品均购自中国食品药品检定研究院。乙腈、甲醇均为色谱纯(Merck),水为双蒸水,磷酸为分析纯(国药集团化学试剂有限公司),甲酸(纯度>98%,Merck)。共收集到7个厂家生产的16批五子衍宗丸,见表1。
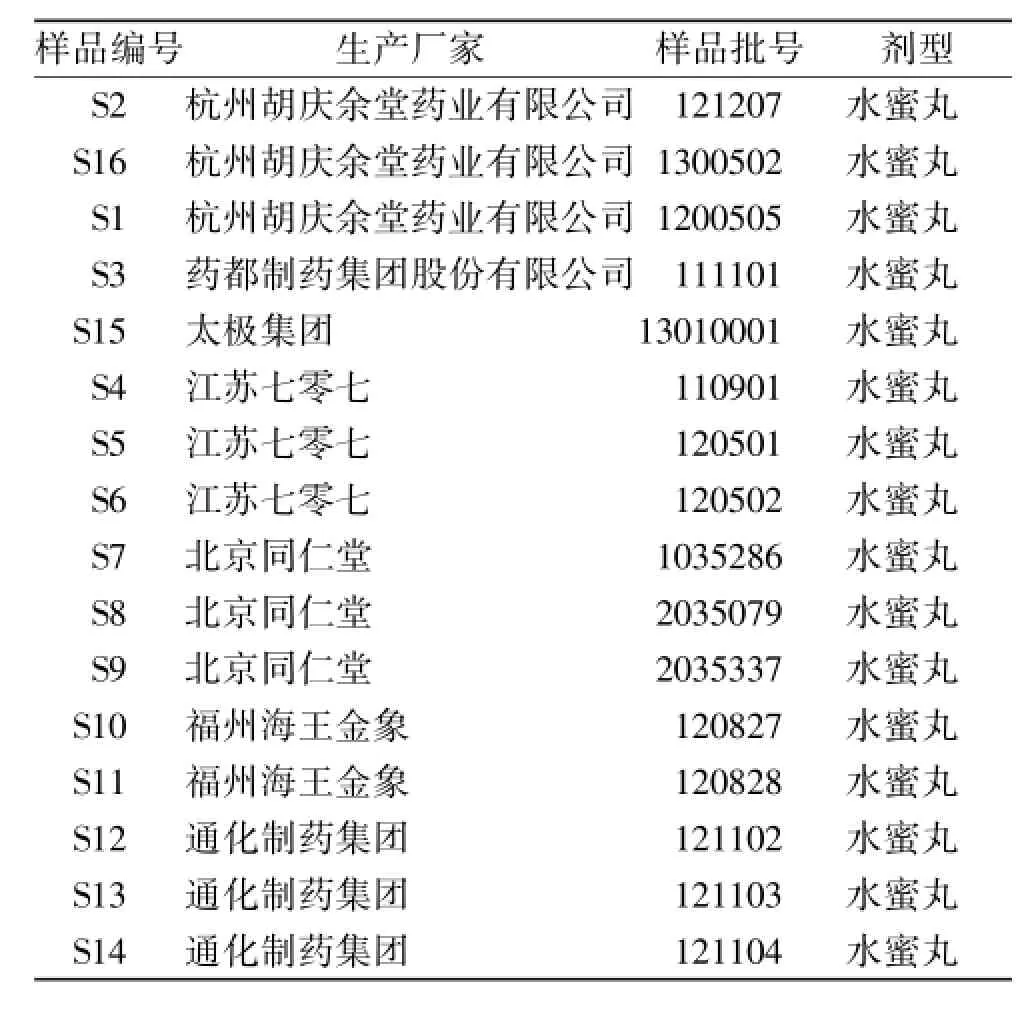
表1 五子衍宗丸样品来源Tab.1 Origin of wuzi yanzong pill sample
2 方法与结果
2.1 色谱条件 Agilent Extend C18(250 mm×4.6 mm, 5 μm);柱温30℃;流动相:A为乙腈-甲醇(10∶1);B为0.4%磷酸水溶液,梯度洗脱:0~5 min为5%~15%A;~15 min为15%~19%A;~25 min为19%~21%A;~70min为21%~90%A;流速1.0 mL·min-1;检测波长254 nm;进样量5 μL。
2.2 参照物溶液的制备 分别精密称取绿原酸12.03 mg,金丝桃苷18.09 mg,毛蕊花糖苷10.56 mg,山奈酚16.34 mg,五味子醇甲17.38 mg,五味子甲素16.83 mg,五味子乙素7.22 mg,用70%甲醇配成浓度分别为240.6,361.8,211.2,326.8,695.2,841.5, 288.8 μg·mL-1的对照品储备液,并于4℃保存。分别吸取上述对照品储备液适量,用70%甲醇分别稀释10,6,15,30,30,30,30倍得到混合对照品工作液。
2.3 供试品溶液的制备 取本品2 g,研细,精密称定,置100 mL具塞锥形瓶中,精密加入70%甲醇50 mL,称定质量,超声处理60 min,取出,放冷,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.4 各单味药材供试品溶液的制备 取各单味药材粉末各约1 g,按照“2.3”项方法处理后,制取单味药材的供试品溶液。
2.5 指纹图谱方法学考察
2.5.1 精密度实验 精密吸取同一份供试品溶液(批号:2035337),在上述色谱条件下连续进样测定6次,分别对各共有峰的相对保留时间及相对峰面积的变化情况进行考察。各共有峰相对保留时间的RSD均<0.2%,相对峰面积的RSD均<4.6%,表明方法精密度较好。
2.5.2 重复性实验 精密称取同一批次的五子衍宗丸样品(批号:2035337)6份,按“2.3”项下方法制备供试品溶液,按上述色谱条件测定,分别对各共有峰的相对保留时间及相对峰面积的变化情况进行考察。各共有峰相对保留时间的RSD均<0.1%,相对峰面积的RSD均<2.9%,表明本方法的重复性良好。
2.5.3 稳定性实验 取同一份供试品溶液(批号: 2035337),分别在制备后0,2,4,8,12,24和36 h按上述色谱条件进样测定,分别对各共有峰的相对保留时间及相对峰面积的变化情况进行考察。各共有峰相对保留时间的RSD均<0.1%,相对峰面积的RSD均<3.8%,表明供试品溶液的稳定性良好。
2.6 指纹图谱的建立与共有指纹峰的确定
2.6.1 指纹图谱的建立 取16批五子衍宗丸,按“2.3”项的方法制备各供试品溶液,吸取各供试品溶液5 μL进样,按上述色谱条件测定并记录色谱图,得到16批五子衍宗丸HPLC指纹图谱,根据色谱图中各色谱峰的相对保留时间,确定共有峰,并选取其中10个共有峰作为特征指纹峰,建立的对照指纹图谱见图1。
2.6.2 共有指纹峰的标定 五子衍宗丸HPLC指纹图谱中,共有指纹峰10个,以7号峰(山奈酚)为参照峰(S峰),计算各色谱峰保留时间和峰面积与同一图谱中S峰的保留时间和峰面积比值,得到的相对保留时间和相对峰面积见表2,3。
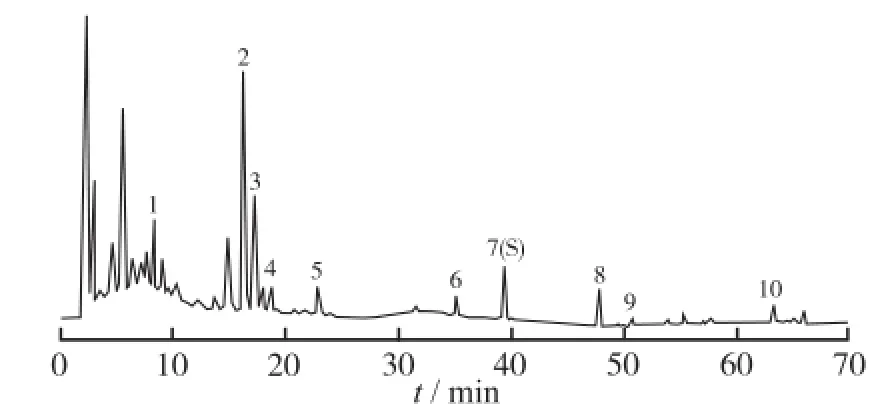
图1 五子衍宗丸HPLC图Fig.1 HPLC fingerprint of wuzi yanzong pill
2.6.3 共有指纹峰的指认 使用LC-MS技术对HPLC指纹图谱10个共有峰中的9个色谱峰进行指认。LC-MS分析条件如下:色谱条件与“2.1”项一致,仅流动相B改为0.1%甲酸;质谱电喷雾离子源(ESI),载气温度:350℃;载气流速:10 L·min-1;喷雾电压(Nebulizer):238 kPa;毛细管电压:4 000 V;正离子检测模式;碰撞电压(Fragmentor)135 V;一级全扫描质量数范围100~1 000。共有峰的鉴定结果见表4。
2.6.4 制剂与药材的相关性 取“2.3”项得到的五子衍宗丸HPLC指纹图谱与“2.5”项得到的各单味药的HPLC指纹图谱进行比较,对比各吸收峰的紫外吸收光谱和相对保留时间,确定10个共有峰主要来源于菟丝子、覆盆子、车前子、五味子等4味药材,与相关文献报道一致[12-16],结果见表4。
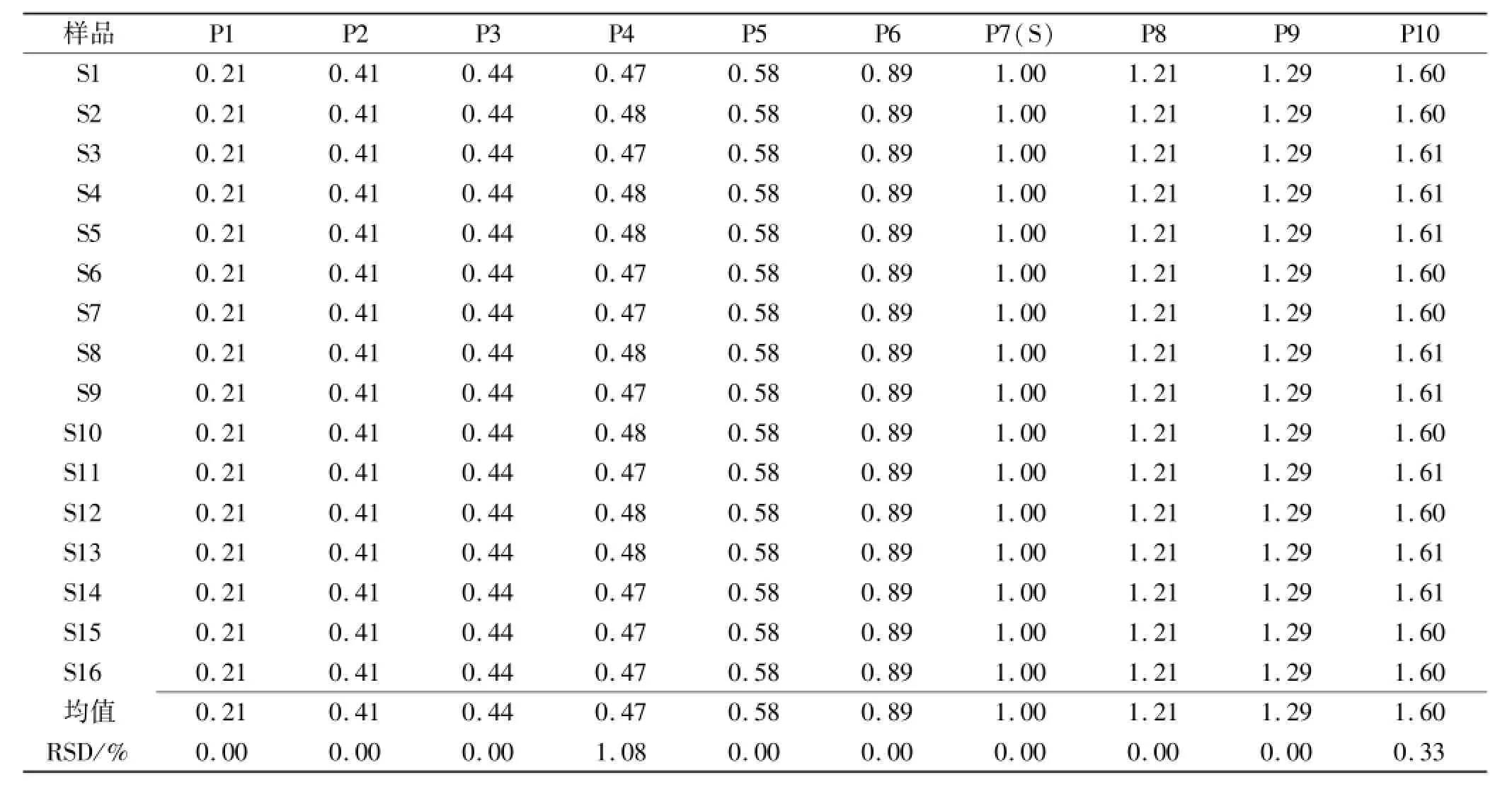
表2 16批五子衍宗丸指纹图谱共有峰相对保留时间Tab.2 Relative retention time of common peaks of sixteen batches of wuzi yanzong pill
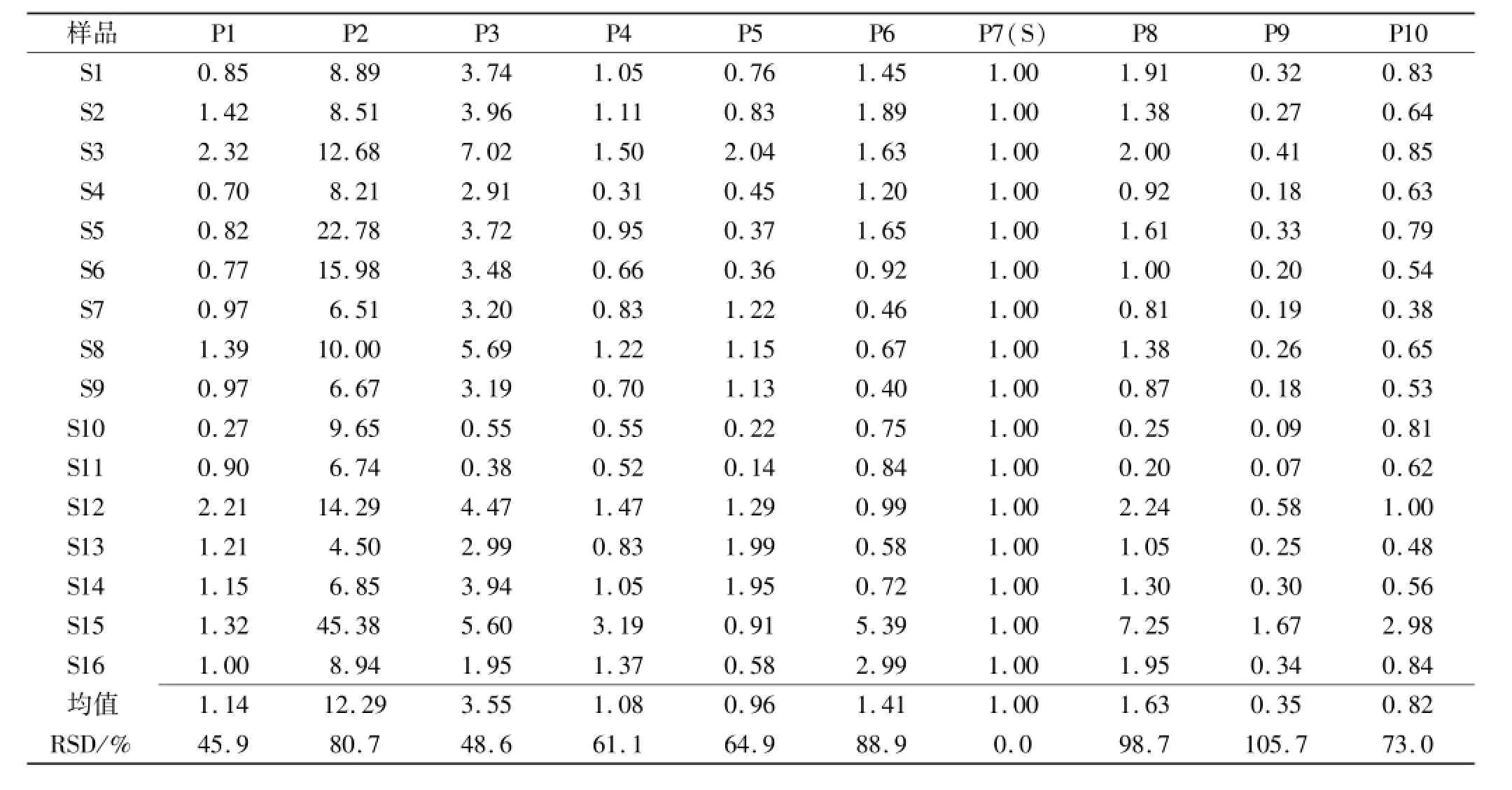
表3 16批五子衍宗丸指纹图谱共有峰相对峰面积Tab.3 Relative peak area of common peaks of sixteen batches of wuzi yanzong pill

表4 五子衍宗丸指纹图谱共有峰指认Tab.4 Analysis result of common peaks of wuzi yanzong pills
2.7 16批五子衍宗丸指纹图谱相似度评价 将16批五子衍宗丸指纹图谱导入国家药典委员会颁布的“中药色谱指纹图谱相似度评价系统”,进行色谱峰匹配,匹配结果见图2。相似度计算结果表明:16批样品与生成的对照谱之间的相似度依次为0.992,0.988, 0.974,0.990,0.969,0.986,0.984,0.976,0.982, 0.949,0.952,0.998,0.930,0.996,0.961,0.965。
3 讨论
3.1 检测波长的确定 用PAD检测器在波长200~360 nm范围对五子衍宗丸供试液进行紫外扫描检测,结果供试品在254 nm检测波长下检出峰数较多、且响应较高,包含的信息量大,故选择254 nm作为检测波长。
3.2 流动相的选择 本实验曾选用甲醇-0.4%磷酸水溶液、乙腈-0.4%磷酸水溶液进行梯度洗脱,结果表明采用这两种流动相,色谱峰达不到分离要求,选择乙腈∶甲醇(10∶1)-0.4%磷酸水溶液进行梯度洗脱时,色谱峰分离度好,出峰明显增多且峰形有较大改善,所以选择乙腈∶甲醇(10∶1)-0.4%磷酸溶液作为本实验的流动相。
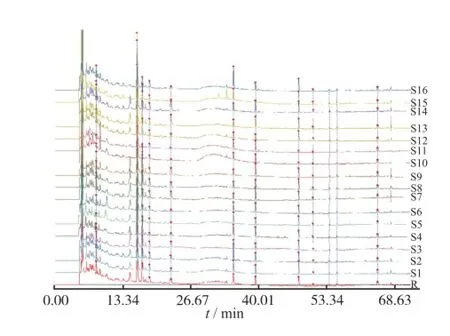
图2 16批五子衍宗丸HPLC指纹图谱共有模式图Fig.2 Common pattern of HPLC fingerprint of sisteen batches of wuzi yanzong pill
3.3 供试品溶液制备方法的选择 分别以乙醇、甲醇和70%甲醇为提取溶剂,并采用超声和加热回流两种提取方式。结果表明,当以70%甲醇提取时,色谱图出峰数和响应较理想,超声和加热回流两种提取方式得到的色谱图无明显区别。为操作简便,本实验选择70%甲醇超声60 min为最终提取方法。
3.4 耐用性考察 本实验比较0.3%,0.4%和0.5%磷酸溶液(水相)对样品测定的影响,结果在各条件下各成分均能基线分离,表明不同浓度的磷酸溶液(水相)对本方法几乎无影响。本实验选取3种不同品牌的色谱柱Angilent Extend C18(250 mm×4.6 mm, 5 μm),Kromasil-C18(250 mm×4.6 mm,5 μm),Ecosil C18(250 mm×4.6 mm,5 μm)对样品进行测定,结果均得到满意的分离度,表明本法对C18柱品牌无特殊要求。本实验还比较了25,30,35℃的柱温对样品测定的影响,结果在各条件下各成分均能得到较好的分离度,表明不同的柱温对本方法几乎无影响。
本研究建立了五子衍宗丸HPLC指纹图谱分析方法,共有峰中9个成分已经明确,可以反映4种药材的特性与质量。该方法稳定、可靠、重复性好。应用该方法研究五子衍宗丸,可以反映成药内在质量和制备工艺的整体差异性。通过对7个厂家16批五子衍宗丸的指纹图谱研究,获得特征性、专属性和整体性的综合信息,为五子衍宗丸的整体质量控制提供方法参考。
[1] 孙国祥,张静娴.系统指纹定量法鉴别龙胆泻肝丸质量[J].分析化学,2009,37(8):1183-1187.
[2] 谢培山.中药色谱指纹图谱鉴别的概念、属性、技术与应用[J].中国中药杂志,2001,26(10):653-655.
[3] 洪筱坤,王智华.色谱指纹谱在中药质量标准研究中的应用[J].中成药,2001,23(3):157-159.
[4] 屠鹏飞.高效液相色谱法制定中药材和中药注射剂特征指纹图谱的探讨[J].中成药,2000,22(7):516.
[5] 王嗣岑,朱丽华,贺浪冲.川芎药材活性部位的高效液相色谱指纹图谱定性分析方法[J].西安交通大学学报:医学版,2003,24(3):221-223.
[6] 汤树良,杨滨,黄璐琦,等.山楂高效液相指纹图谱研究[J].中国实验方剂学杂志,2004,10(4):9-13.
[7] 曾志,杨东晖,宋力飞,等.高效液相色谱指纹图谱应用于板蓝根的鉴定[J].分析化学,2002,30(7):849-852.
[8] 国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:532.
[9] 郭怡飚,胡晓炜,倪美文.RP-HPLC法测定五子衍宗丸中五味子甲素、五味子乙素含量[J].中草药,2002,33(4): 317-318.
[10] 蒋平,文永盛,吴艳辉,等.五子衍宗丸中五味子乙素的含量测定[J].中国药师,2006,9(1):9-10.
[11] 李敏芳,李慧,王学美,等.高效液相色谱法测定五子衍宗丸中金丝桃苷的含量[J].中国实验方剂学杂志, 2008,14(2):1-3.
[12] 肖岚,杨梓懿,石继连.HPLC同时测定菟丝子不同炮制品中五种主要活性成分含量[J].湖南中医药大学学报, 2012,32(7):50-53.
[13] 王隶书,王友联,李明洋,等.HPLC测定市售车前子中毛蕊花糖苷的含量[J].中国药师,2011,14(11):1581-1582.
[14] 林倩,贾凌云,孙启时.菟丝子的化学成分[J].沈阳药科大学学报,2009,26(12):968-971.
[15] 肖洪明,祖灵博,李石平,等.掌叶覆盆子化学成分的研究[J].中国药物化学杂志,2011,21(3):220-226.
[16] 夏丽文,彭丽萍,杨东华,等.超高效液相色谱-电喷雾飞行时间质谱分析五味子化学成分[J].中医药信息, 2012,29(4):27-30.
DOI 10.3870/yydb.2014.10.029
HPLC Fingerprint Analysis of Wuzi Yanzong Pills
LIU Wei1,ZHOU Jian-liang2,CHEN Bi-lian2,ZHU Ming2
(1.Zhejiang Chinese Medical University,Hangzhou 310053,China;2.Zhejiang Institute for Food and Drug Control,Hangzhou 310004,China)
ObjectiveTo establish the high performance liquid chromatography(HPLC)fingerprint ofwuzi yanzongpills.MethodsHPLC was performed on Agilent Extend C18column(250 mm×4.6 mm,5 μm)with a gradient elution system using acetonitrile:methanol(10∶1)-0.4%phosphoric acid as the mobile phase.The column temperature was set at 30℃and the flow rate was 1.0 mL·min-1.The eluate was detected at the wavelength of 254 nm.Chromatographic peaks were identified by LC-MS method.ResultsNine common peaks inwuzi yanzongpill samples were identified by comparing their LC-MS data with those of reference compounds and related reference reports.The HPLC fingerprint ofwuzi yanzongpills was finally developed based on the analysis of sixteen batches of samples and their similarities were above 0.93.ConclusionThis method has high precision,stability and repeatability.This study could be used for overall quality assessment ofwuzi yanzongpills.
Wuzi yanzongpills;Fingerprint;Chromatography,high performance liquid
R286;R927.2
B
1004-0781(2014)10-1360-05
2013-09-17
2014-01-29
*国家科技部“十二五”资助项目中药质量标准研究和信息化体系建设平台(2012ZX09304-005)
刘伟(1989-),女,山东济南人,硕士,研究方向:中药质量评价及新药开发研究。电话:(0)18042323810,E-mail:liuw1989@yeah.net。
祝明(1958-),女,浙江金华人,主任中药师,硕士生导师,学士,研究方向:中药有效成分及质量控制研究。电话:0571-86734991,E-mail:zhumingd@hotmail.com。
