利用聚灿烂绿薄膜修饰电极测定盐酸利多卡因
2014-05-13周谷珍孙元喜
周谷珍,陈 敏,孙元喜
利用聚灿烂绿薄膜修饰电极测定盐酸利多卡因
周谷珍*,陈 敏,孙元喜
(湖南文理学院 化学化工学院, 湖南 常德, 415000)
利用循环伏安法, 将灿烂绿(BG)电聚合于玻碳基体电极表面, 成功地制备出对盐酸利多卡因(LH)具有良好电催化作用的聚灿烂绿薄膜修饰电极(PBGE). 结果表明, 在0.1 mol/L KNO3+ 0.05 mol/L PBS(pH = 6.8)体系中, LH的浓度在6.9 × 10-6~1.4×10-4mol/L范围内时, 氧化峰电流与浓度呈现良好的线性关系, 线性方程和线性相关系数分别为:pa(mA) =-11.71-2.85×10-5LH(mol/L),= 0.998 8, 检测限可达3.5 × 10-6mol/L. 将该法用于盐酸利多卡因样品的测定, 8次平行测定结果的相对标准偏差不大于4.9%, 样品回收率范围为95.6%~102.9%, 符合微量分析的要求.
聚灿烂绿; 薄膜修饰电极; 盐酸利多卡因; 测定
本文在文献[1—5]的研究基础上, 利用生物染料灿烂绿作为单体, 采用循环伏安法制备成PBGE, 研究了药物利多卡因在PBGE上的电化学行为, 建立了测定利多卡因含量的定量分析方法, 并对药物样品中有效成分利多卡因的含量进行了定量测定.
1 实验部分
1.1 仪器与试剂
仪器: CHI660电化学工作站(上海辰华仪器公司); SB3200超声波清洗器(上海超声波仪器厂); 100 µL微量进样器(上海医用激光仪器厂); 实验过程采用三电极系统: 工作电极为玻碳电极(直径3 mm, 天津兰力科公司)或PBGE(自制), 铂电极为辅助电极, 饱和甘汞电极为参比电极.
试剂: 灿烂绿(天津大茂化学试剂厂), 配制成1.0 × 10-3mol/L溶液; 盐酸利多卡因注射液(天津药业集团新郑股份有限公司, 4 mg/2 mL, 国药准字H41024475); 样品林可霉素利多卡因凝胶等. 实验中所用常规试剂均采用分析纯配制而成. 实验过程全部采用超纯水, 无需通氮除氧, 且在室温条件下进行.
1.2 PBGE电极的制备
将预处理后的玻碳电极放入0.05 mol/L KH2PO4-Na2HPO4(Ph = 6.8) + 0.1 mol/L KNO3+ 2.5×10-4mol/L BG(总= 10.0 mL)聚合体系中, 控制扫描电位范围为-1.2~1.8 V, 以50 mV/s的扫描速率, 连续循环扫描电聚合30周(图1), 即可制得PBGE.
取出电极用二次蒸馏水洗净后, 放入PBS缓冲体系中保存待用. 用此法制备的电极稳定性好, 使用1周其性能变化不大.

图1 电聚合制备PBGE CV图. 聚合体系: 0.05 mol/L PBS(Ph = 6.8) + 0.1mol/L KNO3 +2.5×10-4mol/L BG; 电位范围: -1.2~1.8 V; 扫描速率: 50 mV/s; 扫描周数: 30周.
1.3 实验方法
以聚灿烂绿膜修饰电极为工作电极, 采用三电极系统, 在0.1 mol/L KNO3+ 0.05 mol/L PBS(pH = 6.8)中, 以100 mV/s扫速于-0.3~0.4 V电位范围内进行循环伏安扫描, 记录不同LH浓度下的伏安图, 根据峰电流的大小, 利用标准加入法或工作曲线法进行LH的定量分析.
每次扫描结束后, 将电极置于空白底液中循环扫描至稳定, 这样可保持修饰电极良好的稳定性和重现性.

图2 PBGE在含LH中的CV图. 空白体系: 0.05 mol/L PBS(pH =6.8)+ 0.1 mol/L KNO3; 测试体系: 0.05 mol/L PBS(pH = 6.8) + 0.1mol/L KNO3 + 6.9×10-5 mol/L LH; 1. GC在测试体系中;2.PBGE在空白体系中;3. PBGE在测试体系中.
2 结果与讨论
2.1 PBGE对LH的电催化作用
将PBGE和裸玻碳电极(GCE)分别放入空白体系和含LH的测试体系中, 控制扫描电位范围为-0.3~0.4 V, 以100 mV/s的扫描速率进行循环伏安扫描(图2). 从图2中可以看出, PBGE对利多卡因具有明显的电催化作用, 而玻碳电极上利多卡因没有响应.
2.2 测试利多卡因的条件选择
2.2.1 缓冲体系对峰电流的影响
缓冲体系对利多卡因的氧化还原具有一定的影响. 实验发现, 在PBS(pH = 6.8)体系中利多卡因的氧化峰电流最大, 峰形最好. 对LH进行定量测定选择pH = 6.8的PBS缓冲体系较为合适.
2.2.2 扫描速率对峰电流的影响
扫描速率与峰电流密切相关. 实验测定了10~300 mV/s扫速范围内, 扫速与峰电流的关系. 实验表明, 在10~100 mV/s时, 峰电流与成正比, 线性方程及相关系数分别为pa(mA) = 4.976-2.88(mV/s),=-0.999. 当扫描速率较高时(100~300 mV/s), 峰电流与1/2成正比, 其线性方程及相关系数分别为pa(mA) = 2.740-2.241/2(mV/s),=-0.998. 定量分析时, 选择扫速为100 mV/s.
2.2.3 盐酸利多卡因浓度对峰电流的影响
盐酸利多卡因的浓度不同, 其对应的峰电流大小不同. 结果表明, 在6.9 × 10-6~1.3×10-4mol/L的浓度范围内, 氧化峰电流与浓度呈较好的线性关系, 线性回归方程及相关系数分别为:pa(mA) =-11.71-2.85 × 10-5LH(mol/L),= 0.998 8.
2.3 样品分析
林可霉素利多卡因凝胶样品溶液的制备. 分别准确称取一定质量的林可霉素利多卡因片凝胶, 加水静置, 使林可霉素利多卡因溶解, 定容至100 mL. 将配置好的样品溶液编号贴签后放置于冰箱备用.
在0.05 mol/L PBS(pH = 6.8) + 0.1 mol/L KNO3体系中, 分别加入上述样品溶液, 定容至10 mL. 在-0.3~0.4 V的电位范围内, 以100 mV/s的扫描速率进行循环伏安扫描, 记录峰电流. 利用工作曲线法进行定量分析的结果见表1.
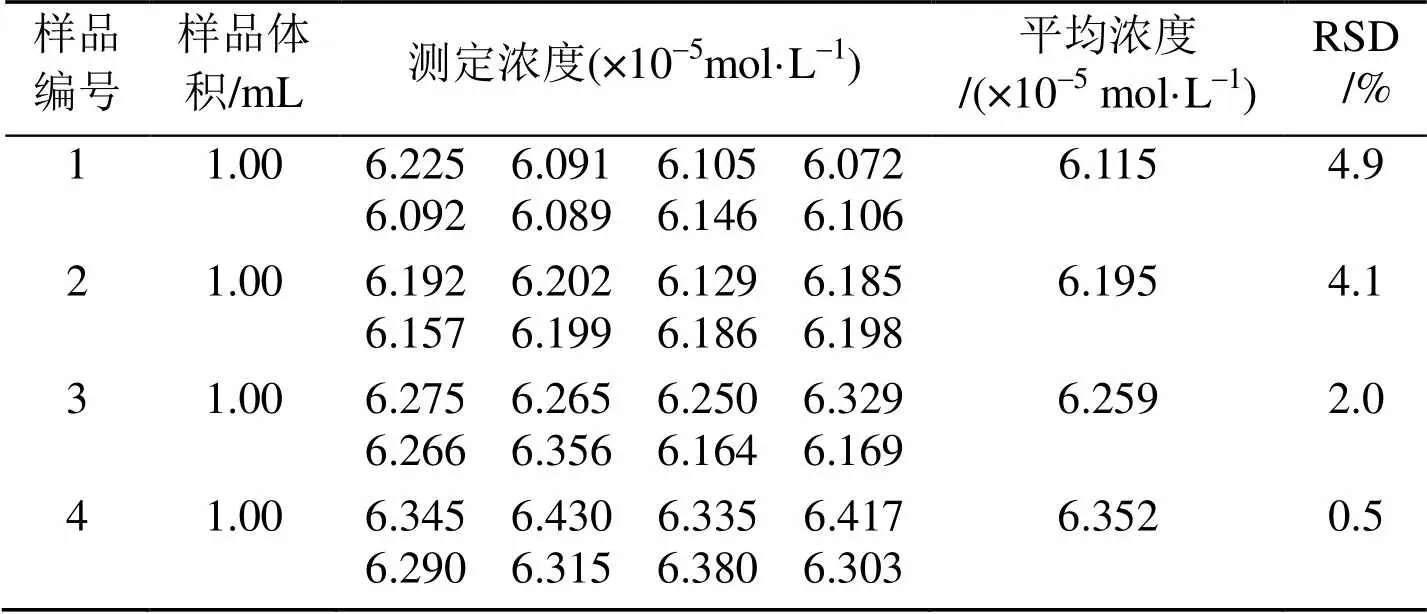
表1 样品测定结果
由表1数据分析得到: 样品1中含LH 3.985 mg/g, 样品2中含LH 3.997 mg/g, 样品3中含LH 3.999 mg/g, 样品4中含LH 4.011 mg/g, 测定结果与标示值基本吻合.
本实验用林可霉素利多卡因凝胶进行样品回收率实验. 取样品1 2.202 7 g, 样品2 3.021 6 g, 再在其中加入盐酸利多卡因标准品溶液(6.90 × 10-3mol/L) 2 mL, 用蒸馏水稀释至100 mL, 即为回收率实验测试液. 取测试液1 mL, 按照样品分析方法进行测定, 实验结果列于表2.
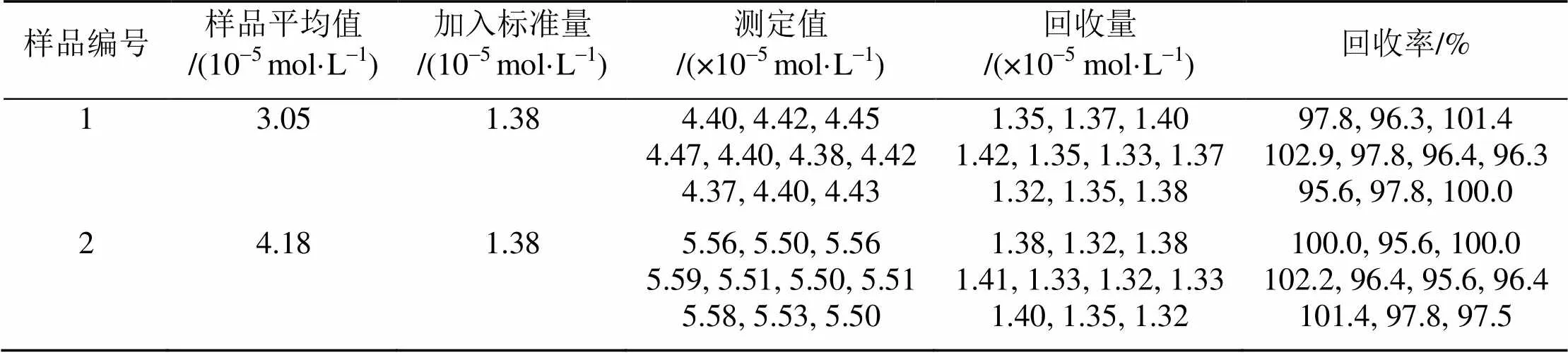
表2 样品回收率实验结果
3 结论
本实验在0.05 mol/L PBS(pH = 6.8) + 0.1 mol/L KNO3+ 2.5 × 10-4BG的聚合体系中电聚合制备出性能良好、电活性高、并对利多卡因有较好的电催化氧化作用的PBGE. 利用PBGE为工作电极, 建立了对LH含量进行定量分析的一种电分析方法. 将该法用于实际药物样品中利多卡因的测定, 取得满意结果.
[1] 周谷珍, 陈望爱, 孙元喜. 利用聚中性红薄膜修饰电极测定盐酸环丙沙星[J]. 中国抗生素杂志, 2007, 32(5): 305—307.
[2] 孙元喜. 聚茜素红薄膜修饰电极对氯霉素的电催化作用[J]. 湖南文理学院学报: 自然科学版, 2008, 20(1): 46—48.
[3] 孙元喜. 利用碳纳米管修饰石墨电极测定马来酸氯苯那敏[J]. 药物分析杂志, 2009, 29(9): 216—218.
[4] 周谷珍, 覃文化, 孙元喜. 利用聚硫堇薄膜修饰电极测定对乙酰氨基酚[J]. 湖南文理学院学报: 自然科学版, 2010, 22(2): 40—42.
[5] 周谷珍, 鲁丹, 孙元喜. 利用聚钙黄绿素薄膜修饰电极测定阿司匹林[J]. 湖南文理学院学报: 自然科学版, 2012, 24(2): 28—30.
Determination of lidocaine hydrochloride by poly (brilliant green) film modified electrodes
ZHOU GuZhen, CHEN Min, SUN YuanXi
(College of Chemistry and Chemical Engineering, Hunan University of Arts and Science, Changde 415000, China)
BG was modified on glass carbon electrode surface by the cyclic voltammetry, and the poly (BG) film modified electrode (PBGE) was successfully prepared which had good electrocatalytic reaction on lidocaine hydrochloride. The results indicated that there was an irreversible deoxidation peak of LH in the system of 0.1 mol/L KNO3+ 0.05 mol/L PBS, good linearity was found between oxidization peak current and concentration of LH when concentration was 6.9 × 10-6~1.4 × 10-4mol/L, the method detection limit is 3.5 × 10-6mol/L. The linear equation waspa(mA) =-11.71-2.85 × 10-5LH(mol/L) and linear correlation coeffcient-0.998 8 can be obtained. The relative standard deviation (RSD) of 8 times was not more than 4.9% and the recovery rate range was 95.6%~102.9%. The PBGE can be used for quantitative determination of lidocaine hydrochloride in real samples.
poly(brilliant green); film modified electrode; lidocaine hydrochloride; determination
10.3969/j.issn.1672-6146.2014.04.006
O 657.1
1672-6146(2014)04-0025-03
email: 575912837@qq.com.
2014-07-28
(责任编校:刘晓霞)
