亚硝酸盐对外碳源反硝化过程N2O还原的影响
2014-05-13王淑莹李夕耀何岳兰彭永臻北京工业大学北京市水质科学与水环境恢复工程重点实验室北京100124
委 燕,王淑莹,马 斌,李夕耀,何岳兰,彭永臻 (北京工业大学北京市水质科学与水环境恢复工程重点实验室,北京 100124)
亚硝酸盐对外碳源反硝化过程N2O还原的影响
委 燕,王淑莹*,马 斌,李夕耀,何岳兰,彭永臻 (北京工业大学北京市水质科学与水环境恢复工程重点实验室,北京 100124)
本试验通过批次试验考察了亚硝酸盐对外碳源反硝化过程N2O还原的影响.结果表明NO2--N初始浓度为5.92~35.23mg/L时,随着NO2--N浓度的增加,反硝化过程中N2O的积累量逐渐增加;当NO2--N浓度为35.23mg/L时,NO2--N还原量的46.26%被转化为N2O.通过对比试验得出,N2O还原酶与亚硝酸盐还原酶对电子的竞争和游离亚硝酸(FNA)对N2O还原酶的抑制会导致N2O比还原速率下降,造成反硝化过程N2O积累.基于上述试验结果提出,污水处理厂可通过调控运行条件控制NO2--N浓度,降低反硝化过程的N2O的产生与释放;也可以通过短程硝化提高NO2--N浓度,促进反硝化过程N2O的积累,再通过N2O氧化甲烷减少N2O排放,同时提高产能37%.
污水处理;生物脱氮;反硝化;温室气体氧化亚氮(N2O);抑制;亚硝酸盐
全球变暖引发极端天气的频繁出现,使得人们更加关注温室气体减排.N2O作为一种温室气体,其全球增温潜势是 CO2的 190~270倍.2003~2009年间我国生活污水处理过程中排放的N2O占主要污水处理部门温室气体总排放的 50%以上,是主要温室气体排放源[1-2].因此研究污水处理过程中N2O的释放控制具有重要的意义.
N2O是生物反硝化过程中间产物之一,N2O的还原速率小于 N2O的生成速率时就会造成反硝化过程N2O的积累与释放.反硝化过程中N2O的还原是由N2O还原酶作用在接受电子的条件下将N2O还原为N2,因此N2O的还原速率与N2O还原酶活性和有机物氧化提供电子的速率有关.现有研究表明,高亚硝酸盐浓度(或 FNA)会抑制N2O还原酶活性,导致反硝化过程N2O积累[3-7].至于电子供应方面,内碳源(PHAs)作为反硝化碳源时会因内碳源氧化速率慢导致电子供应不足,从而造成N2O的积累[8-9].溶解性COD的降解速率是内碳源(PHB)的6~20倍[6],一般认为外碳源反硝化过程中不会出现电子供应不足的情况[8],但是事实却很少研究过.污水处理厂脱氮为了降低曝气量与减少有机碳源消耗量,而实现短程硝化反硝化[10],这就造成反硝化过程中可能存在较高浓度的亚硝酸盐,因此研究亚硝酸盐对 N2O积累的影响将有助于控制污水处理厂N2O释放.本文通过设置不同浓度的亚硝酸盐,考察亚硝酸盐对外碳源反硝化过程中N2O还原的影响,并从 N2O还原酶抑制和电子竞争的角度分析亚硝酸盐浓度对 N2O还原的影响机理,从而为控制反硝化过程中N2O的产生与释放提供理论支持.
1 材料与方法
1.1 污泥来源
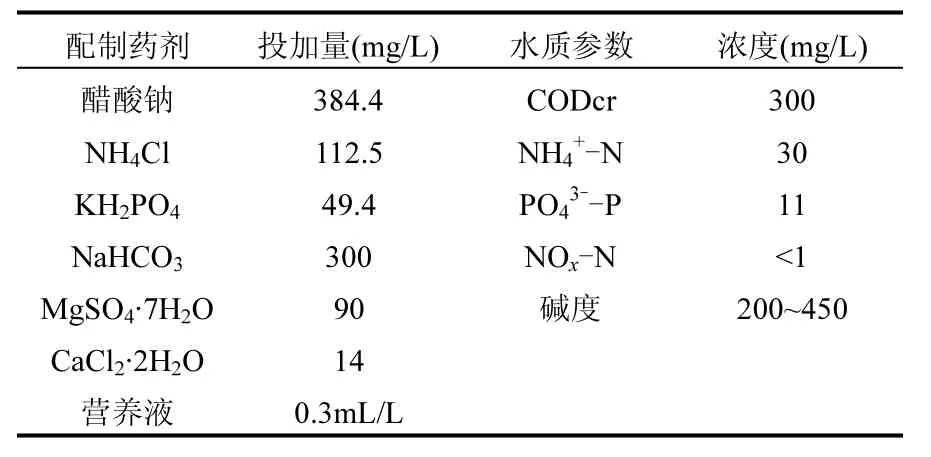
表1 模拟生活污水成分及水质指标Table 1 Composition and quality of synthetic wastewater
试验污泥取自于实验室稳定运行的亚硝酸盐型反硝化除磷系统,该系统采用 SBR作为反应器,有效容积10L,排水比为50%.进水为人工配制的模拟生活污水,其水质指标如表1和表2所示,使用恒温装置控制系统温度为(28±1)℃.反应器以厌氧-缺氧-好氧(AAO)方式运行时,每周期运行时间为8h,包括进水10min,厌氧110min,缺氧180min,好氧60min,沉淀60min,排水5min,闲置55min.厌氧末用蠕动泵加入50mL亚硝酸盐贮备溶液,使得反应器中NO2--N初始浓度为40mg/L.系统水力停留时间(HRT)=12h,污泥龄(SRT)为12d,混合液悬浮固体浓度(MLSS)保持在2000mg/L左右,挥发性悬浮固体浓度(MLVSS)与MLSS之比为0.60~0.75,亚硝酸盐去除率大于99%.
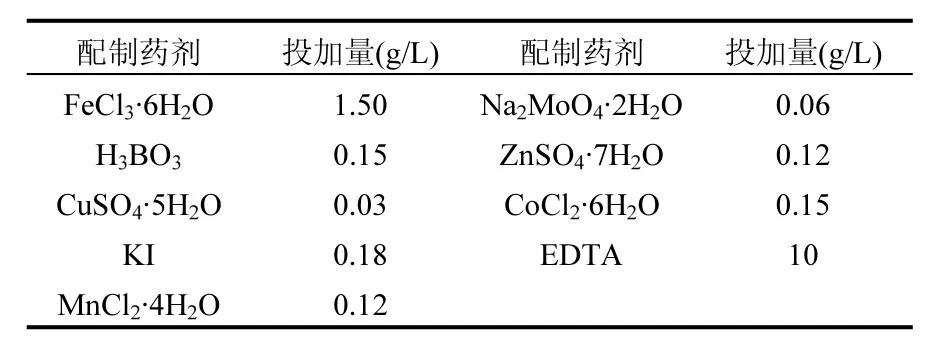
表2 营养液成分与组成[11]Table 2 Composition of nutrient solution
1.2 间歇试验
采用密封性有机玻璃反应器,有效容积为1L,见图1.顶部连接1L的气袋便于平衡反应器内外压力,UnisenseN2O微电极由密封盖顶部圆孔插入反应器,在线监测液相 N2O浓度.试验开始前,首先取反硝化除磷系统好氧结束的污泥混合液1L,静沉后倒去上清液,并离心洗泥 3次.然后将污泥加入间歇试验反应器,再加入上述人工配水定容至1L,并曝氮气 10min,充气速率为 250mL/ min,确保反硝化在缺氧环境下进行,反应器温度为25~27℃.
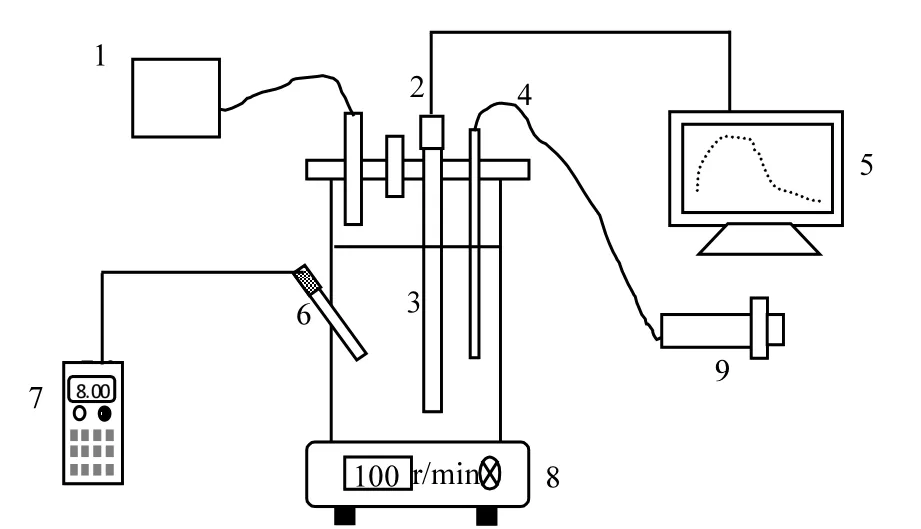
图1 间歇试验装置Fig.1 Schematic diagram of batch reactor
为了考察亚硝酸盐对N2O还原的影响,设计如下:称取62.1gNaNO2加入500mL的Milli-Q水配置1.8mol/L的NaNO2贮备液.准备N2O饱和液,在100mL的Milli-Q水中曝N2O标准气体气5min,N2O-N饱和液浓度为500~670mg/L.做5组不同NO2
--N浓度(5、15、25、30和35mg/L)试验,分别对应于a、b、c、d和e,N2O初始浓度都固定在11~15mg/L.每组试验首先做只有NO2-N还原的空白试验,然后做同时投加N2O和亚硝酸盐的对比试验.试验过程中,使用 0.5mol/L的HCL和 NaOH的调节反硝化过程 pH=8.0± 0.05[12].通过在线传感器监测反应器中N2O浓度,当N2O-N浓度接近0mg/L时停止试验.每组试验开始前 30min内,间隔 5min取混合液 20mL; 30min至试验结束期间,间隔 10min取混合液20mL.
为了探讨电子竞争对N2O还原的影响,还研究了投加N2O对亚硝酸盐还原的影响.本试验采用的NO2
--N浓度为5、15、25、30和35mg/L,首先做只有亚硝酸盐还原的空白试验,然后同时投加亚硝酸盐和N2O(N2O-N浓度为11~15mg/L)的对比试验,每组试验均持续30min,间隔5min取水样20mL.
1.3 NO2
--N和N2O-N比还原速率的计算本试验通过NO2--N和N2O-N浓度变化曲线进行线性拟合(R2>0.95),计算亚硝酸盐和 N2O的最大消耗速率,每组试验的计算时间是反硝化前30min.亚硝酸盐和N2O的表观比消耗速率就是单位生物量(以MLVSS计)的最大消耗速率,记为rNO2,c和rN2O,c,单位为mg N/(gVSS⋅min)(当亚硝酸盐还原过程中发生N2O积累时, N2O积累速率看作是负消耗速率,即 rN2O,c是负值).亚硝酸盐和N2O真正的比还原速率(分别为rNO2和rN2O)通过以下公式计算:
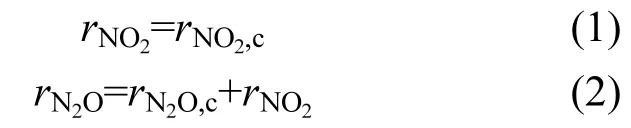
1.4 分析项目与方法
SCOD:D快速测定仪;水样经过0.45μm滤纸过 滤 后 ,采 用 美 国 LACHAT 公 司QuikChem8500Series2流动注射分析仪测定NO2--N;pH值采用德国WTW pH/oxi340i仪在线监测.MLSS采用滤纸称重法;MLVSS采用马弗炉灼烧重量法测定[13].
2 结果与讨论
2.1 不同 NO2--N浓度条件下反硝化过程中N2O的积累
不同 NO2--N 浓度条件下反硝化过程中N2O-N浓度与NO2--N浓度变化如图2所示.可以看出投加不同浓度亚硝酸盐的反硝化过程中都出现了不同程度的N2O积累.在NO2--N初始浓度为 15mg/L时,反应前 5min内反应器内N2O-N浓度不断增加,随后5~20min内开始缓慢下降,当亚硝酸盐被完全还原结束时(20min时刻)N2O开始迅速下降(图2b).在NO2--N初始浓度为35mg/L时,60min时亚硝酸盐基本被消耗完,还原量为31.79mg/L,此时反应器中N2O-N浓度达到最大,N2O-N 浓度增加了 14.71mg/L,占NO2--N还原量的46.26%(图2e).Miao等[14]在恒定pH为8.0时仅以亚硝酸盐作为电子受体进行反硝化,也发现亚硝酸盐还原基本完成时,N2O积累达到最大浓度.目前污水处理厂污泥发酵产生的甲烷,而后通过燃烧发电实现污水处理厂能量的回收.上述燃烧过程中是利用空气中的氧气氧化甲烷产生能量,若燃烧过程能用N2O代替氧气氧化甲烷则可使产能提高 37%[式(3),式(4)][15],因此,通过实现污水处理过程中N2O的积累,而后将其收集用于氧化甲烷,则有望提高污水处理厂能量回收率;同时由于N2O氧化甲烷后变为 N2,可实现温室气体N2O的减排.
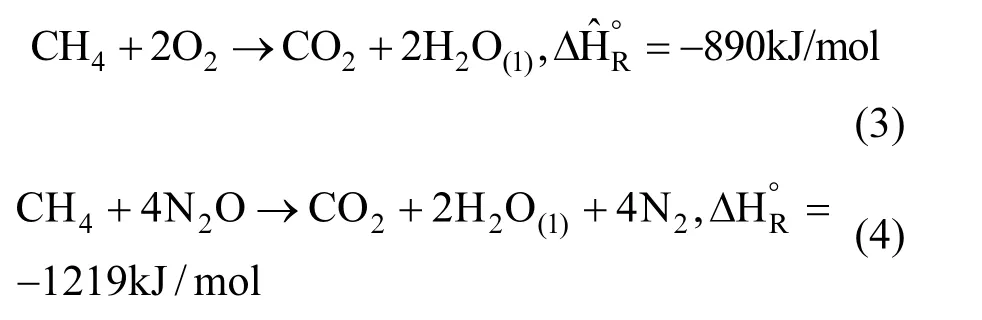
2.2 亚硝酸盐对反硝化过程中N2O还原的影响机理分析
反硝化过程中N2O积累的原因是N2O的还原速率小于N2O的生成速率.N2O还原活性(即存在亚硝酸盐时,N2O-比还原速率占仅含N2O时的N2O比还原速率的百分比)如图3所示.可以看出在 NO2--N由 5.92mg/L增加至26.86mg/L时,N2O的还原活性随着NO2--N浓度的增加而降低;NO2--N由26.86mg/L增加至35.23mg/L的过程中,N2O还原活性降低的幅度更大.

图2 不同 NO2--N浓度条件下反硝化过程中N2O-N和NO2--N的变化情况Fig.2 Variations of N2O-N and NO2--N under different NO2--N concentration conditions during denitrification
Zhou等[3]研究表明FNA可抑制N2O还原酶活性,当FNA浓度为0.0007~0.001mg NHO2-N /L时,N2O还原酶活性降低50%.本研究中NO2--N浓度为 26.85mg/L,pH=8.0±0.05时,FNA浓度为0.0006mg NHO2-N /L,N2O还原活性为67.5%,与Zhou等[3]研究结果相一致.但当NO2--N浓度增加至 35.23mg/L时,FNA 浓度为 0.0008mg NHO2-N/L,N2O还原活性却只有11.25%,远低于Zhou等[3]报道的50%(图4).在Zhou等[3]试验中FNA为 0.0007mg NHO2-N/L时,pH值为 7.5, NO2--N浓度为10mg/L,低于本实验中35.23mg/L,这就说明本试验中N2O还原过程中添加亚硝酸盐会增加反硝化过程的电子需求速率.则本试验中的N2O还原酶活性低可能除了来自于FNA的抑制,同时还来自于亚硝酸盐还原酶和N2O还原酶之间的电子竞争.为了进一步验证上述分析,考察了单独投加N2O和同时投加N2O与亚硝酸盐时,N2O 比还原速率的变化情况.结果表明在N2O--N初始浓度一致的条件下,投加不同浓度的亚硝酸盐后,N2O比还原速率都明显下降(图4a),但这仍不能将N2O比还原速率的下降归因于投加亚硝酸盐与N2O竞争电子,因为投加的电子受体亚硝酸盐会对N2O还原酶产生抑制.为此又考察了单独投加亚硝酸盐和同时投加亚硝酸盐与 N2O时,亚硝酸盐比还原速率的变化情况(图4b).虽然 N2O并不会对亚硝酸盐的还原产生抑制,但N2O的投加同样也导致了亚硝酸盐比还原速率下降.上述试验结果说明单独以N2O或亚硝酸盐作为电子受体的反硝化系统,若引入另外一种电子受体,则会造成N2O还原酶和亚硝酸盐还原酶竞争电子,从而导致N2O或亚硝酸盐比还原速率的下降;同时也说明在引入第二种电子受体导致电子需求速率增大,反硝化菌并不能通过调整有机物氧化速率满足各种还原酶对电子的需求,才导致亚硝酸盐还原酶和N2O还原酶竞争电子.本研究说明除了FNA抑制N2O还原酶活性外,亚硝酸盐还原酶和N2O还原酶对电子的竞争也是导致N2O还原不完全的重要因素.
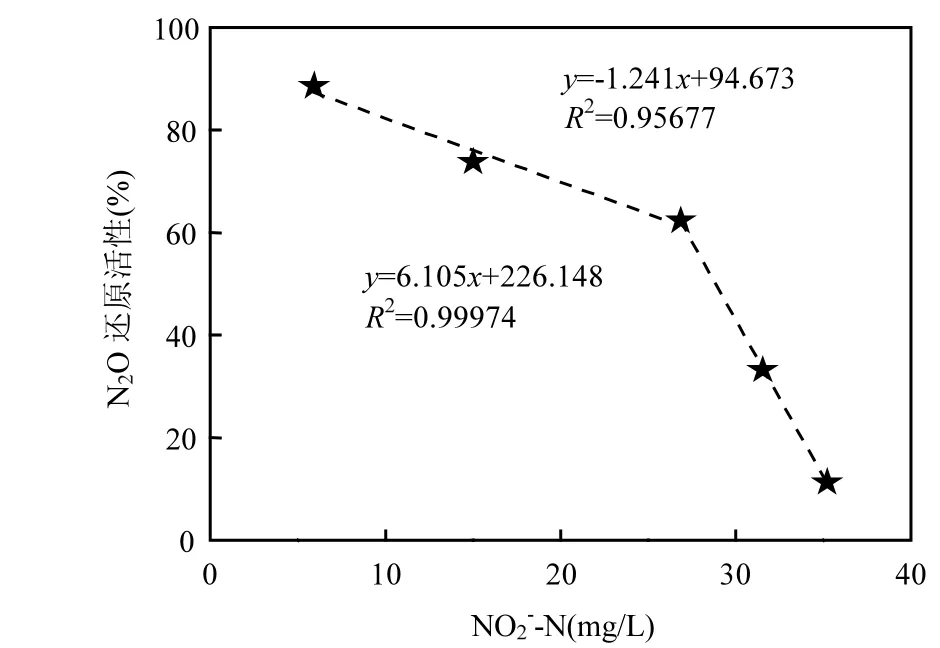
图3 不同NO2--N浓度下的N2O还原活性Fig.3 The N2O reduction activity under different NO2--N concentrations
2.3 亚硝酸盐对N2O还原的影响在污水处理厂中应用
本研究表明高NO2--N浓度会导致反硝化过程N2O的积累,但N2O是一种重要的温室气体,因此要严格控制N2O的释放.可从两个方面来控制污水处理厂反硝化过程中N2O的释放:第一个方面就是通过全程硝化反硝化脱氮,控制好氧区NO2
--N浓度,从而降低缺氧反硝化区的NO2--N浓度,从而控制反硝化阶段 N2O的产生与释放.低 DO或高氨氮容易造成亚硝酸盐的积累,可通过确保曝气量充足、增大反应器的容积和均衡进水流量等措施缓解氨氮或者有机物负荷变化,也可通过提高内回流比降低系统中氨氮和NO2--N浓度[16],来降低好氧区出水NO2--N浓度.此外,分段进水也可以降低反应器中的氨氮浓度和NO2
--N浓度,使得N2O的产生量降低50%[10].第二个方面是通过调控运行条件实现短程硝化
[17-19],提高缺氧段NO2--N浓度,促进反硝化阶段N2O积累,而后通过曝气吹脱收集N2O,用作甲烷燃烧过程的氧化剂,提高甲烷燃烧过程中的能量产量,同时将N2O转化为N2达到温室气体减排的目的[15].
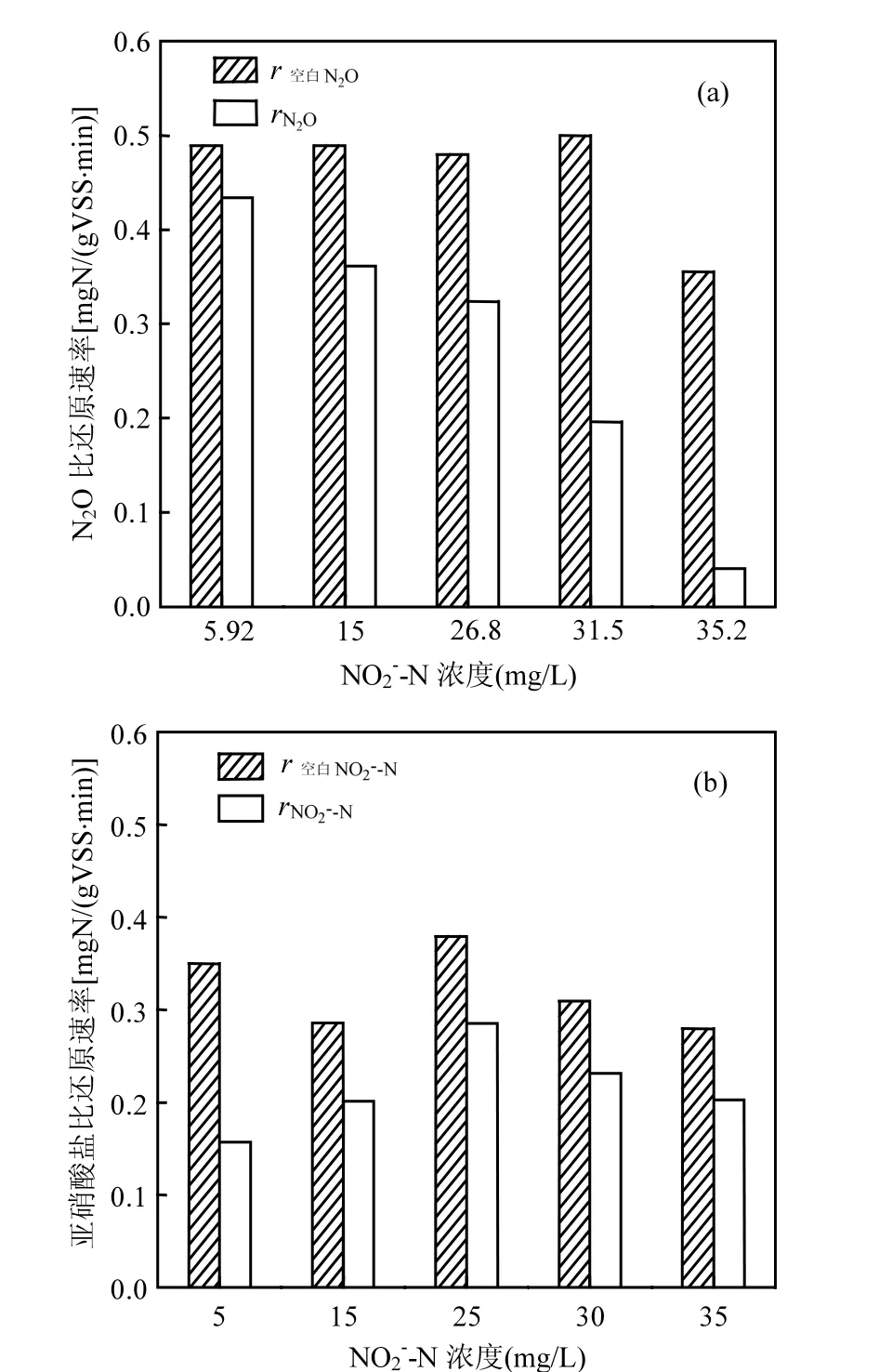
图4 亚硝酸盐对N2O比还原速率的影响以及N2O对亚硝酸盐比还原速率的影响Fig.4 The effect of nitrite on the N2O specific reduction rate and the effect of N2O on the nitrite specific reduction rate
3 结论
3.1 随着 NO2--N浓度的增加,反硝化过程中N2O的积累量不断增加,当 NO2--N初始浓度为35.23mg/L时,NO2--N还原量的46.26%被转化为N2O.
3.2 高NO2--N浓度导致反硝化过程N2O产生与积累的原因,一方面来自于FNA对N2O还原酶活性的抑制,另一方面来自于N2O还原酶与亚硝酸盐还原酶对电子的竞争.
3.3 对于城市污水处理厂可通过调控运行条件控制NO2--N浓度来控制反硝化过程N2O的产生与释放,也可以通过提高反硝化区的 NO2--N浓度,提高N2O的积累量,而后通过收集N2O氧化甲烷提高产能和控制N2O释放.
[1] 周 兴,郑有飞,吴荣军,等.2003-2009年中国污水处理部门温室气体排放研究 [J]. 气候变化研究进展, 2012,8(02):131-136.
[2] 刘秀红,彭永臻,马 涛,等.硝化类型对污水脱氮过程中N2O产生量的影响 [J]. 中国环境科学, 2007,27(5):633-637.
[3] Itokawa H, Hanaki K,Matsuo T. Nitrous oxide production in high-loading biological nitrogen removal process under low cod/n ratio condition [J]. Water Research, 2001,35(3):657-664.
[4] Zhou Y, Pijuan M, Zeng R J, et al. Free Nitrous acid inhibition on nitrous oxide reduction by a denitrifying-enhanced biological phosphorus removal sludge [J]. Environmental Science and Technology, 2008,42(22):8260-8265.
[5] Ye L, Pijuan M,Yuan Z G. The effect of free nitrous acid on key anaerobic processes in enhanced biological phosphorus removal systems [J]. Bioresource Technology, 2013,130(0):382-389.
[6] 张静蓉,王淑莹,尚会来,等.硝化过程亚硝态氮氧化阶段的 N2O产生情况 [J]. 中国给水排水, 2010,26(03):25-29.
[7] Kampschreur M J, Temmink H, Kleerebezem R, et al. Nitrous oxide emission during wastewater treatment [J]. Water Research, 2009,43(17):4093-4103.
[8] Li C, Zhang J, Liang S, et al. Nitrous oxide generation in denitrifying phosphorus removal process: main causes and control measures [J]. Environmental Science and Pollution Research International, 2013,20(8):5353-60.
[9] Wang Y Y, Geng J J, Ren Z J, et al. Effect of anaerobic reaction time on denitrifying phosphorus removal and N2O production [J]. Bioresource Technology, 2011,102(10):5674-5684.
[10] Yang Q, Peng Y., Liu X, et al. Nitrogen removal via nitrite from municipal wastewater at low temperatures using real-time control to optimize nitrifying communities [J]. Environmental Science & Technology, 2007,41(23):8159-8164.
[11] Rodriguez-Caballero A,Pijuan M. N2O and NO emissions from a partial nitrification sequencing batch reactor: Exploring dynamics, sources and minimization mechanisms [J]. Water Research, 2013,47(9):3131-3140.
[12] Wunderlin P, Lehmann M F, Siegrist H, et al. Isotope Signatures of N2O in a Mixed Microbial Population System: Constraints on N2O Producing Pathways in Wastewater Treatment [J]. Environmental Science and Technology, 2013,47(3):1339-1348.
[13] 国家环境保护总局.水和废水监测分析方法 [M]. 北京:中国环境科学出版社, 2002:252-354.
[14] Miao Z J, Peng Y Z, Wang S Y, et al. Effect of pH on denitrifying phosphorus removal and N2O metabolism by Polyphosphate Accumulating Organisms [J]. Journal of Chemical Technology and Biotechnology, 2013, Submitted.
[15] Scherson Y D, Wells G F, Woo S G, et al. Nitrogen removal with energy recovery through N2O decomposition [J]. Energy and Environmental Science, 2013,6(1):241-248.
[16] Kampschreur M J, Temmink H, Kleerebezem R, et al. Nitrous oxide emission during wastewater treatment [J]. Water Research, 2009,43(17):4093-103.
[17] 高大文,彭永臻,王淑莹.不同方式实现短程硝化反硝化生物脱氮工艺的比较 [J]. 中国环境科学, 2004,24(5):618-622.
[18] 董怡君,王淑莹,汪传新,等.亚硝酸盐氧化菌(NOB)的富集培养与其污泥特性分析 [J]. 中国环境科学, 2013,33(11):1978-1983.
[19] 马 娟,彭永臻,王 丽,等.温度对反硝化过程的影响以及pH值变化规律 [J]. 中国环境科学, 2008,28(11):1004-1008.
The effect of nitrite on N2O reduction during denitrification process using external carbon source.
WEI Yan, WANG
Shu-ying*, MA Bin, LI Xi-yao, HE Yue-lan, PENG Yong-zhen (Beijing Key Laboratory of Water Quality Science and Water Environment Recovery, Beijing University of Technology, Beijing 100124, China). China Environmental Science, 2014,34(7):1722~1727
In this study, the effect of nitrite on N2O reduction during denitrification using external carbon sources was investigated in batch tests. The results showed that N2O accumulation grew with increase of the initial nitrite concentration at levels of 5.92~35.23mg/L. Specially, when NO2--N was 35.23mg/L, the N2O produced accounted for 46.26% of the total reduced nitrite. By contrast, the N2O accumulation during denitrification was attributed to the decrease of specific reduction rate due to the synergistic reactionof the free nitrous acid (FNA) inhibition and the electron competition between N2O reductase and nitrite reductase. These findings suggest that the N2O emission control could be achieved by decreasing nitrite concentration through the operation optimization. Moreover, N2O could be used to oxidize methane for increasing energy production by 37% and reducing N2O emission, which could be achieved by increasing nitrite concentration via nitritation.
wastewater treatment;biological nitrogen removal;denitrification;greenhouse gas nitrous oxide (N2O);inhibition;nitrite
X703.1
A
1000-6923(2014)07-1722-06
委 燕(1989-),女,甘肃民勤人,北京工业大学硕士研究生,主要从事污水生物脱氮除磷 N2O的释放与控制研究.发表论文1篇.
2013-10-26
国家“863”项目(2012AA063406)
* 责任作者, 教授, wsy@bjut.edu.cn
