氟化石墨工艺技术研究
2014-05-04李霞温丰源
李霞,温丰源
(多氟多化工股份有限公司,河南 焦作 454006)
氟化石墨工艺技术研究
李霞,温丰源
(多氟多化工股份有限公司,河南 焦作 454006)
气相法制备氟化石墨由于工艺简单、产品纯度高而成为合成氟化石墨最常用的方法。氟化石墨的合成过程涉及高温与活性单质氟气两方面的因素,安全控制十分重要。从原料、反应时间、反应温度、反应设备和纯化方法等方面对合成氟化石墨的工艺技术进行对比,旨在避免生产过程中出现潜在的危险,寻求提高氟化石墨产品质量的新方法,提升氟化石墨整体制备工艺的安全性。
氟化石墨;氟气;石墨原料
氟化石墨是当今国际上高性能、高效益、高科技的石墨材料重点研究对象,因其具有低的表面自由能、好的热稳定性和化学稳定性、在功能材料中不可或缺,因而广泛应用于军事、航空航天、冶金、机电、化工等领域。
高温合成法(气相法)制备氟化石墨由于具有工艺简单、产品纯度高等特点而成为合成氟化石墨最常用的方法。该方法是将粉末状石墨装入反应器中,通入干燥氮气除去反应物中的挥发性杂质,然后通入氟气或氟氮混合气进行反应,反应温度为300~600℃,反应时间为1~200 h。制得氟化石墨的成分和性能受石墨原料、反应时间、反应温度、反应设备和纯化方法等因素的影响。
笔者通过查阅国内外相关专利文献,对合成氟化石墨的工艺技术进行对比,旨在避免生产过程中出现潜在的危险,寻求提高氟化石墨产品质量的新方法,提升氟化石墨整体制备工艺的安全性,对氟化石墨合成工艺的研究者或者生产厂家起到警示和推动作用。
1 原料的影响
1.1 存在的问题
在工业规模生产氟化石墨的过程中,从反应速率的角度考虑,通常采用无定形炭材料或者粒径小于100μm的石墨材料作原料。但是,采用粒径小于100μm的炭材料作原料时,不论是生成(CF)n还是(C2F)n,即使反应过程中对炭材料不进行搅拌,氟化反应也会不可避免地引起目标产物的分解。此外,当粒度小于100μm的石墨材料与氟气在静止状态下反应时,反应器中放置的石墨材料的厚度仅限于1 cm,如果石墨材料的厚度大于1 cm,期望得到的氟化石墨就不会在石墨材料床层的深层区域生成,导致床层最下方的石墨材料不反应。为了使石墨材料床层最下方的反应可以继续进行,常常采用搅拌或震动反应体系,但是搅拌或震动都会导致产物的分解加剧。因此,采用粒度小于100μm的炭材料作原料不利于氟化石墨的生产。
1.2 解决措施及效果
YasushiKita等[1]研究发现,当采用粒度为100~10 000μm的炭材料作原料时,氟化反应可以在炭材料床层的整个深度进行,即使要氟化的炭材料在反应器中以静止的状态放置,厚度为几厘米到几十厘米。但是也有人指出,即使采用粒度为100~10 000μm的炭材料作原料,当炭材料被剧烈搅拌或震动时,炭材料的氟化反应偶尔也会出现因爆炸引起的产物分解。为了完全避免因爆炸引起的产物分解,且氟化反应可以稳定进行,该发明的研究者采用的方法是,使用粒度为100~10 000μm的炭材料作原料进行氟化反应,在反应完成之前就结束氟化反应,把生成的产物用筛子筛选,将未反应的炭从氟化石墨中除去。
筛子的材质可以是不锈钢、黄铜、青铜或者镍,筛孔孔径取决于炭材料的粒度,一般选择38~106μm。如果筛孔孔径太小分离效率就会下降,筛孔孔径太大则不利于产物的回收。研究发现,形成的氟化石墨非常易碎,从氟化石墨中将未反应的炭材料有效地分离有一定的困难。研究者通过在筛网中放置由橡胶或者类似物制成的长方形块或者软球来改善分离效率和回收问题。分离出来的未反应的炭材料可以再次使用。
研究者使用平均粒度为400μm(粒度分布为150~990μm)的人造石墨制备氟化石墨,用电磁振动筛对获得的氟化石墨进行筛分,时间为1 h。振动筛先后提供孔径为250、106、63、38μm的筛子,20个直径为10mm的橡胶球置于机器中以改善分离效率。筛分好的产品进行X射线衍射分析,结果如表1所示。从表1可知,粒径大于106μm产品的衍射峰强度很高,这归因于未反应的石墨;粒径小于106μm产品的衍射峰强度非常弱。因此,使用孔径小于106μm的筛子来获得含有少量未反应石墨的氟化石墨是可行的。
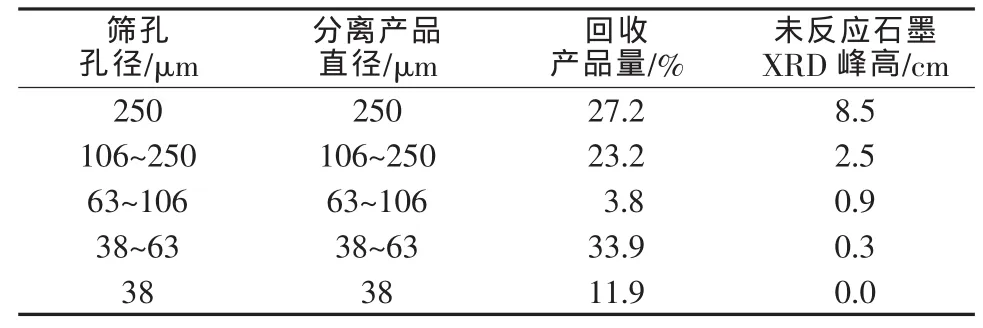
表1 氟化石墨筛分结果分析
2 反应温度和反应时间的影响
2.1 存在的问题
在400~600℃的温度范围内,可以制备出氟碳比(氟碳原子比)为0.6~1.0、产物为(CF)n和(C2F)n混合物的氟化石墨。一般情况下,单纯的石墨和氟气反应制备氟化石墨的反应时间较长,需要几十到几百个小时,既浪费人力、物力,也降低了实验的安全性。
2.2 解决措施及效果
NobuatsuWatanabe等[2]研究发现,将石墨与金属氟化物掺杂,然后再与氟气反应制备氟化石墨,所得产品质量高,而且能够使氟化反应的时间大大缩短。金属元素包括元素周期表中IB、ⅡB和Ⅲ族的碱金属和碱土金属以及第一周期的过渡金属。
实验在蒙乃尔合金环的反应器中进行。将天然片状石墨和金属氟化物混合装入反应器中,将氟气在室温下引入反应器,达到压力为101.32 kPa。反应系统以一定的升温速率升温到指定温度,并在此温度下持续一定的时间。得到的氟化石墨为灰色,氟碳比为0.5~0.8,产品收率为100%。表2为不同条件下制得氟化石墨的氟碳比。
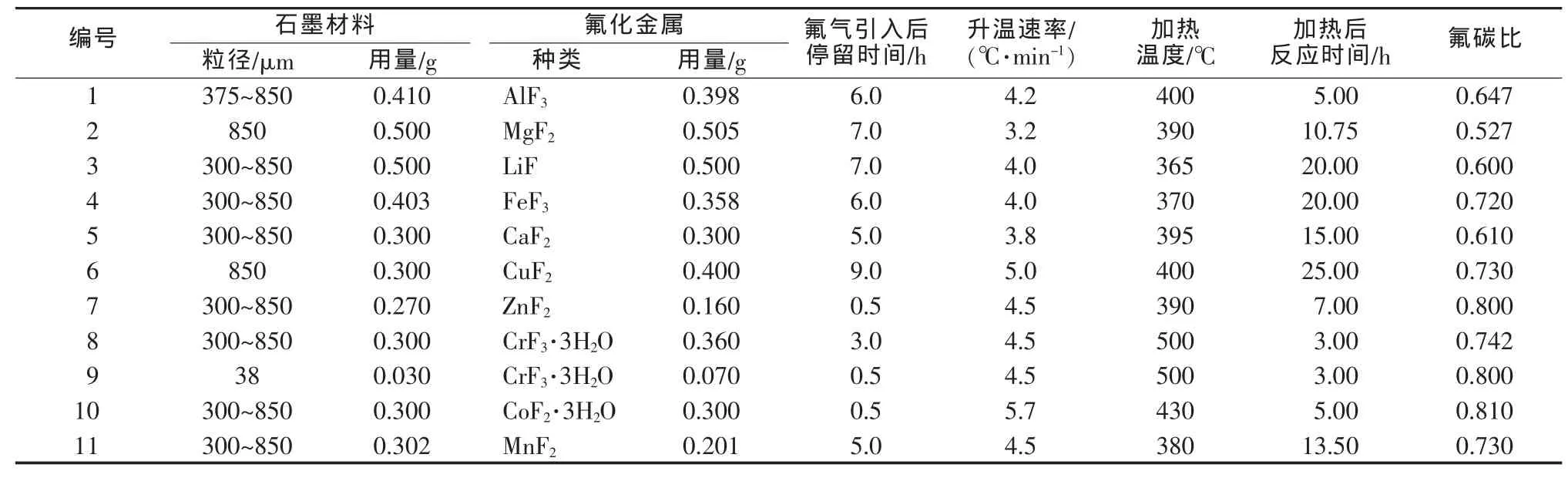
表2 不同条件下制得氟化石墨的氟碳比
从表2可以看出,石墨中掺杂金属氟化物,可以使氟化反应时间大大缩短,且产品的氟碳比均能达到理想值。
以AlF3和MgF2为例,选用粒度为46μm的石墨原料,其他条件不变,对比掺杂与不掺杂金属氟化物制备氟化石墨的效果,结果见表3。

表3 掺杂与不掺杂金属氟化物制得氟化石墨的氟碳比
从表3可以看出,同等条件下在石墨原料中掺杂金属氟化物制得氟化石墨的氟碳比比不掺杂金属氟化物时高,且反应时间缩短1/2。
3 反应设备的影响
3.1 存在的问题
图1为氟化反应常用的管式反应炉。炭材料放在陶瓷方舟或托盘中,静置于反应炉内,然后通入氟气进行反应。

图1 管式反应炉
炭材料与氟气反应形成氟化石墨(CFχ)n,其中0<χ<1.25:

式(3)表示生成的氟化石墨分解。由于式(1)和(2)都是放热反应,会引起反应(3)的发生。在大多数情况下,分解反应(3)在短时间内大量发生,产生大量的热量和大量的气体氟碳化合物,结果使反应体系的氟化石墨迅速且剧烈地分解。在这种情况下,无法获得理想的产物——氟化石墨。另外,由于氟化石墨分解爆炸可能会导致反应容器的损坏。
3.2 解决措施及效果
Yasushi Kita等[3]使用具有水平延长圆柱形外壳的反应器,内部有托盘和隔间。反应器内径为300mm,高为1 000mm。反应器的内部与外壁隔开。限定在反应器内的反应室垂直截面是矩形,内部反应器的侧壁上设置有支架支撑托盘。反应器具有气体循环线路(包含管道和风扇),这样循环的氟气可以通过圆柱形的外墙和内部反应器之间的空间,用甲醇和干冰作为捕获剂供给气体循环管路的外部管道中,以除去氟气中的高碳氟化合物(即碳原子大于4的碳氟化合物,如:C5F10,C5F12,C6F12,C7F14,C8F16,C9F20,C10F20,C12F26等)。
研究者发现,从初始反应到72 h以内,反应器内的气压会急剧上升,安全反应装置会发生破裂。引起压力上升的原因是通过氟化反应生成的氟化石墨的瞬间分解。在发生瞬间分解之前,高碳氟化合物在反应腔内占气体总体积的3.1%。因此,YasushiKita等[3]提出,每隔一定的时间(如20 h),测量气相中大于4个碳原子的高碳氟化合物的总浓度,逐步卸去一部分上述反应区域内的气体,控制高碳氟化合物在气相中的总浓度,保持小于或等于3%的体积分数,以防止氟化石墨的分解。
4 纯化方法的影响
4.1 存在的问题
通常制备的氟化石墨的纯度不能满足电池级氟化石墨的要求,必须对产物进行纯化。对于氟化石墨使用浮选法很难除去浸染在石墨中的极细的杂质,氯化焙烧法使用的氯气对环境污染较大,而强酸强碱以及使用高温的方法,容易使C—F键的结构改变,从而影响电池的储电容量。
4.2 解决措施及效果
杨先金等[4]将适量的氢氟酸溶液加入纯度为99%~99.9%的氟化石墨中,在超声波辅助下清洗,然后抽滤,将滤饼在150~200℃的热解炉中烘干水分及将多余的HF变为气体挥发,即得到电池级氟化石墨。产品呈灰白色,氟质量分数为55%~61%,杂质离子质量分数:w(Fe)<100×10-6,w(Cu)<50×10-6,w(Ni)<50×10-6,达到电池材料的要求。
使用超声波辅助清洗,利用超声波的空化效应,加大清洗液对氟化石墨的冲击,能有效地将深包埋的金属离子溶解。使用稀HF溶液作为清洗液,能有效地溶解各种金属离子,同时清洗液中含有大量F离子,能够有效地保持C—F结构,不影响氟化石墨的性质。
5 结语
氟化石墨合成过程涉及高温与活性单质氟气两方面的因素,安全监控十分重要。除了合成环境需要通风,所用设备也都需要经过耐氟处理,阀门、管接头、调压阀、测量装置、过滤器的材质选择应以镍合金为主。同时,需要做好废水的收集及处理工作,有害液体交由专业废水处理厂处理。多层废气吸收系统用固体氧化钙(CaO)回收气体,并在排空环节前安置气体检测装置,慎防氟气尾气外漏。
[1]Yasushi Kita,Hishaji Nakano,Shiro Moroi,et al.Process for producingagraphite fluoride:US,4593132[P].1986-06-03.
[2]Nobuatsu Watanabe,Tsuyoshi Nakajima,Masayuki Kawaguchi. Process for producing a graphite fluoride comprising mainly polydicarbonmonofluoride represented by the formula(C2F)n:US,4423261[P].1983-12-27.
[3]Yasushi Kita,Hishaji Nakano,Shiro Moroi,et al.Method of safely preparinggraphite fluoride:US,4590316[P].1986-05-20.
[4]杨先金,张艳.一种电池级氟化石墨的纯化方法:中国,102602908[P].2012-07-25.
联系方式:lixiawfy123@163.com
Research on graphite fluoride technology
LiXia,Wen Fengyuan
(Do-Fluoride Chemicals Co.,Ltd.,Jiaozuo 454006,China)
Gaseousmethod has become themost commonmethod to produce graphite fluoride because of its simply process and high purity product.The synthesis process involves two factorsofhigh temperature and activity of fluorine,therefore,security control is very important.For the purpose of avoiding the latent danger in the production process,seeking the new method to improve the graphite fluoride′s quality,and promoting the whole preparation technology′s security,the research contrastabout synthesis technologies of graphite fluoride from aspects of raw materials,reaction time,reaction temperature,equipment,and purificationmethodsetc.wasmade.
graphite fluoride;fluorine;graphitematerial
TQ124.3;127.1
A
1006-4990(2014)09-0052-04
2014-03-20
李霞(1983—),女,硕士研究生,助理工程师,长期从事氟化工研究,发表论文3篇,申请专利2项。
