色谱法测定人血浆中万古霉素的浓度
2014-04-30姜慧婷陈冰杨婉花
姜慧婷,陈冰,杨婉花
上海交通大学医学院附属瑞金医院药剂科,上海 200025
色谱法测定人血浆中万古霉素的浓度
姜慧婷,陈冰,杨婉花*
上海交通大学医学院附属瑞金医院药剂科,上海 200025
目的:建立HPLC法和液相色谱-串联质谱(LC-MS/MS)法检测人血浆中万古霉素的浓度,并分别与FPIA法进行比较。方法:HPLC法:100 μL血浆样品加入等体积10%的高氯酸沉淀,振荡离心后取上清液进样。采用Agilent Eclipse XDB-C18(250 mm×4.6 mm,5 μm),柱温为35℃,流动相为0.05 mol·L-1KH2PO4(pH=3.2)-甲醇(74∶26,v/v),流速为1 mL·min-1,检测波长为230 nm。LC-MS/MS法:100 μL血浆样品用300 μL乙腈沉淀,振荡离心后取上清液进样。色谱柱为Agilent Eclipse XDB-C18(100 mm×2.1 mm,3.5 μm),柱温为40℃,流动相为水(含0.1%甲酸)-乙腈(90∶10,v/v),流速为0.20 mL·min-1。采用电喷雾化离子源(ESI),多离子反应模式(MRM)检测,万古霉素和内标去甲万古霉素的监测离子对分别为m/z 725.0→144.0和718.5→144.0。采用建立的HPLC法和LC-MS/MS法测定95份临床样本,并与FPIA法进行相关性和测定方法的偏倚分析。结果:HPLC法和LC-MS/MS法测定万古霉素的线性范围分别为1.2~96 μg·mL-1和0.4~96 μg·mL-1,低、中、高三种浓度质控品日内和日间相对标准差(RSD)均<15%。两种方法与FPIA法有很强的相关性(r=0.9621,P<0.0001和r=0.9466,P<0.0001),无明显偏倚。结论:建立的HPLC和LC-MS/MS法快速、灵敏、准确,样本测定结果与FPIA法无显著差异,适用于万古霉素的常规血药浓度监测及人体药物代谢动力学研究。
万古霉素;高效液相;液相色谱-串联质谱;荧光偏振免疫法
万古霉素(vancomycin)是一种糖肽类抗生素,对革兰阳性菌有较强的杀菌作用,尤其适用于耐甲氧西林金黄色葡萄球菌和表皮葡萄球菌的感染[1]。以往的研究发现,老年人、长疗程和万古霉素谷浓度过高(30~65 μg·mL-1)是万古霉素引起肾毒性的危险因素,并且合用氨基糖苷类抗生素后肾毒性的发生率大大提高,因此建议长疗程、高浓度药物维持的患者,合并其他耳肾毒性药物和肾功能不全患者,老年、新生儿等特殊群体患者须进行常规血药浓度监测。实施个体化用药,以保证用药的安全性和有效性,同时减少耐药菌产生的几率[2]。
目前国内外对万古霉素的血药浓度监测方法有微生物法、荧光偏振免疫(FPIA)法、高效液相色谱(HPLC)法、液相色谱-串联质谱(LC-MS/MS)法等[3]。临床多采用基于免疫原理的FPIA法,但是需要专门仪器,且专用试剂盒需从国外进口,若供应中断的情况下,临床万古霉素血药浓度监测无法正常进行。国内已有较多采用HPLC法测定万古霉素血药浓度的文献报道。而LC-MS/MS法则有检测食品中万古霉素的残留量的报道,样品处理需经过萃取和净化过程,时间过长且步骤繁琐,不适用于临床样本的测定[4-5]。本文参考了相关文献[6-9],建立了HPLC法和LC-MS/MS法快速准确测定血浆中万古霉素的浓度。
1 材料
1.1 仪器
Aglient 1100系列高效液相色谱仪(美国Aglient公司);API4000型三重四级杆质谱仪(美国Applied Biosystems公司),配备电喷雾离子化源(ESI)以及Analyte 1.5.1数据处理软件;Prominence 20A液相色谱仪(日本Shimadzu公司);TDL-5型低速大容量离心机(上海安亭科学仪器厂);BS224S型精密天平(德国赛多利斯公司);XW-80A型漩涡混合器(上海医大仪器厂);Milli-Q超纯水系统(美国Millipore公司)。
1.2 药品和试剂
万古霉素对照品(纯度>90%,大连美伦生物技术有限公司,批号:20120601);内标去甲万古霉素(纯度>95%,华北制药股份有限公司,批号:12070202);磷酸二氢钾(上海振欣试剂厂,批号:20120305);乙腈和甲醇(色谱纯,美国Tedia公司);其余试剂均为分析纯;试验用水为纯水。
2 方法与结果
2.1 HPLC法
2.1.1 色谱条件色谱柱:Agilent Eclipse XDBC18(250 mm×4.6 mm,5 μm);流动相:0.05 mol·L-1KH2PO4(pH=3.2)-甲醇(74∶26);流速:1 mL·min-1;柱温:35℃;检测波长:230 nm。
2.1.2 对照品血浆和内标溶液的配制精密称取万古霉素对照品4.8 mg,加入1 mL纯水溶解,依次用纯水稀释成以下浓度:960、480、240、120、60、30、12、4.0 μg·mL-1作为工作液。再分别取对照品工作液各10 μL,加入空白血浆90 μL,稀释成浓度分别为96、48、24、12、6.0、3.0、1.2、0.4 μg·mL-1的对照品血浆。
精密量取内标去甲万古霉素8.0 mg,加1 mL纯水溶解使浓度为8.0 mg·mL-1去甲万古霉素标准储备液,将储备液用纯水稀释至150.0 μg·mL-1。
以上储备液及内标溶液均保存在4℃冰箱内备用。
2.1.3 血浆样品处理精密吸取血浆样品100 μL,加入20 μL内标溶液(150.0 μg·mL-1去甲万古霉素),混匀后加入10%高氯酸100 μL进行沉淀,涡旋振荡30 s,13000 r·min-1离心10 min,取上层20 μL进样。
2.1.4 方法专属性考察分别取空白血浆、标准品血浆(加入内标)以及患者用药后血浆(加入内标),按“2.1.3”项处理,进样分析得色谱图(见图1)。万古霉素和内标去甲万古霉素保留时间分别为14.2 min和18.9 min,峰形良好,万古霉素和内标能完全分离,血浆中内源性物质和患者使用的其它药物均不干扰万古霉素和内标的测定。
2.1.5 标准曲线和定量下限按照“2.1.2”项下方法配制不同浓度的系列对照品血浆。按“2.1.3”项方法处理标准品血浆,以血浆中待测物浓度与内标物浓度的比值为横坐标X,以待测物与内标物的峰面积比值为纵坐标Y,用加权最小二乘法进行回归运算,求得的直线回归方程:Y=4.526X+13.52(r=0.998,n=7)

图1 万古霉素和去甲万古霉素(内标)的典型色谱图
结果表明,万古霉素血药浓度在1.2~96 μg·mL-1范围内线性关系良好。万古霉素的定量下限为1.2 μg·mL-1(n=5,相对标准差RSD=7.35%,准确度RE= 98.67%)。
2.1.6 精密度与准确度试验按照“2.1.2”项下方法配制低、中、高(5.75、23.0、92.0 μg·mL-1)3种浓度的万古霉素标准品血浆,每种浓度5份,再按“2.1.3”项方法处理后同日内测定,依据当日各自的标准曲线计算万古霉素的血浆浓度,考察日内精密度;连续3天同法操作,考察日间精密度,结果见表1。
表1 HPLC法的准确度与精密度(±s,n=5)
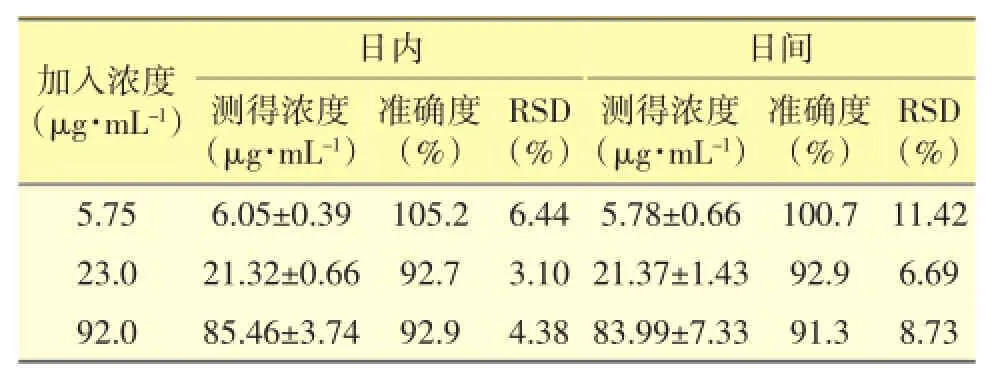
表1 HPLC法的准确度与精密度(±s,n=5)
?
2.1.7 提取回收率试验按照“2.1.2”项下方法配制低、中、高(5.75、23.0、92.0 μg·mL-1)3种浓度的万古霉素标准品血浆,每种浓度5份,再按“2.1.3”项方法处理后进样分析。另用等量纯水代替空白血浆配置对照品溶液,每种浓度5份,按“2.1.3”项方法处理后进样分析。以每一浓度前者峰面积与后者峰面积之比计算提取回收率,结果低、中、高三种浓度的血浆样品的提取回收率分别为68.68%、54.52%、58.34%。
2.1.8 样品稳定性考察
冻融稳定性:血浆样品经历3次冰冻-解冻循环后测定,万古霉素低、中、高3种浓度的RSD分别为7.69%、3.57%、5.89%。
冷冻样品的稳定性:血浆样品在-40℃放置20 d后处理测定,万古霉素低、中、高3种浓度的RSD分别为10.25%、4.78%、4.94%。
室温放置6 h稳定性:在室温放置6 h后处理测定,万古霉素低、中、高3种浓度的RSD分别为8.64%、5.83%、7.38%。
血浆样品进样器稳定性:血浆样品处理后置于进样器24 h后,用当日处理的标准曲线计算,万古霉素低、中、高3种浓度的RSD分别为13.25%、11.49%、6.30%。
结果表明,在上述稳定性考察条件下,万古霉素均保持稳定,未出现明显变化。符合生物样品分析要求。
2.2 LC-MS/MS法
2.2.1 色谱条件色谱柱:Agilent Eclipse XDB-C18(100 mm×2.1 mm,3.5 μm);流动相:水(含0.1%甲酸)-乙腈(90∶10,v/v);流速:0.20 mL·min-1;柱温:40℃。
2.2.2 质谱条件采用电喷雾离子化电离源(ESI),多离子反应模式(MRM)检测:源电压:5.5 kV,源温度:500℃,GS1气体流速:25 psi,GS2气体流速:25 psi,帘气流速:10 psi。测定万古霉素和去甲万古霉素的离子对分别为m/z 725.0→144.0,m/z 718.5→144.0;两者的解簇电压(DP)和碰撞能量(CE)分别为:53.6 eV和58.5 eV;27.3 eV和29.4 eV。
2.2.3 对照品血浆和内标溶液的配制对照品血浆的配制同“2.1.2”。将8.0 mg·mL-1去甲万古霉素标准储备液用乙腈稀释至4.0 μg·mL-1,以此作为含内标的沉淀剂。以上储备液及内标溶液均保存在4℃冰箱内备用。
2.2.4 血浆样品处理精密吸取血浆样品100 μL,加入300 μL内标溶液(4.0 μg·mL-1去甲万古霉素)进行沉淀,涡旋振荡1 min,置于高速离心机中13000 r·min-1离心10 min,取50 μL上清液,加入50 μL纯水混匀,取5 μL进样分析。
2.2.5 质谱分析和特异性分别取空白血浆、对照品血浆(加入内标溶液)和患者用药后血浆(加入内标溶液)样本,按“2.2.3”项方法处理,其典型色谱见图2。万古霉素和内标去甲万古霉素的保留时间均为1.6 min,峰形良好,血浆中内源性物质和患者使用的其他药物均不干扰万古霉素和内标的测定。
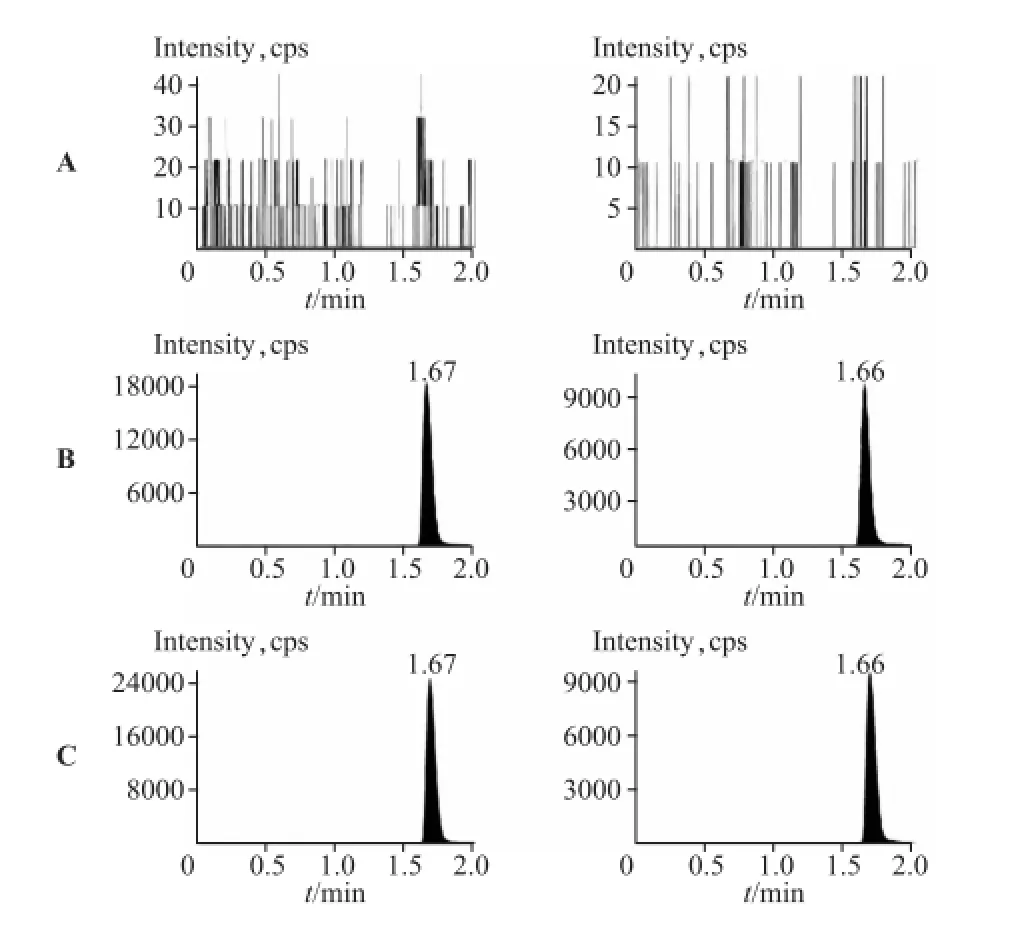
图2 万古霉素和去甲万古霉素的典型色谱图
2.2.6 标准曲线及定量下限按照“2.2.3”项下方法配制不同浓度的系列对照品血浆。按“2.2.4”项方法处理后进行分析,记录万古霉素和内标去甲万古霉素色谱峰面积。以待测物浓度为横坐标X(μg· mL-1),以待测物与内标物的峰面积比值为纵坐标Y,用加权(W=1/X)最小二乘法进行回归运算,求得的直线回归方程Y=0.103X+0.0222(r=0.9997,n=8)。结果显示,万古霉素在0.4~96 μg·mL-1的范围线性关系良好。最低定量限0.4 μg·mL-1浓度水平上,连续测定5份最低定量限样本,准确度为104.9%,精密度为4.9%。
2.2.7 精密度和准确度按照“2.2.3”项下方法,分别配制含万古霉素低、中、高(0.958、5.75、92.0 μg·L-1)3种浓度的质控血浆样本。按照“2.2.4”项下方法处理样本,每一浓度均为5份进样分析,连续测定3天。根据当日标准曲线计算质控样本的测定浓度,计算日内、日间精密度和准确度,结果见表2。
表2 LC-MS/MS法的精密度、准确度、提取回收率与基质效应(±s,n=5)
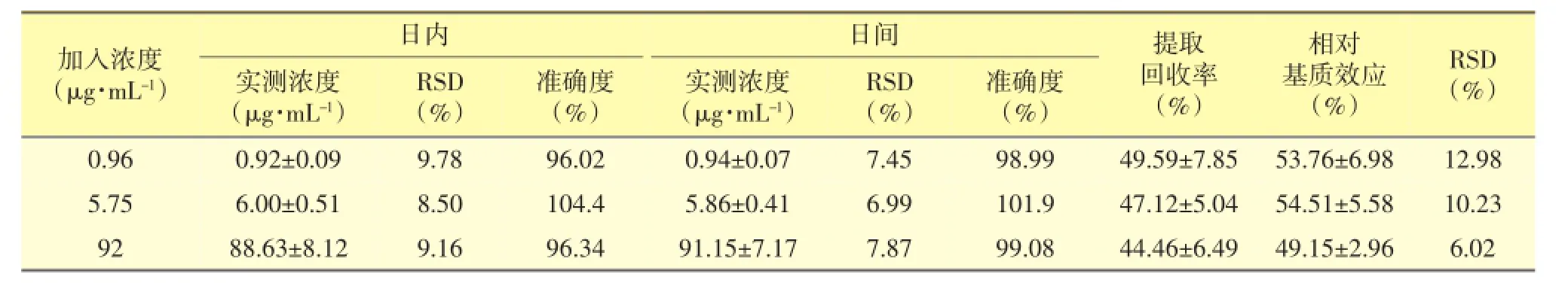
表2 LC-MS/MS法的精密度、准确度、提取回收率与基质效应(±s,n=5)
?
2.2.8 提取回收率和基质效应按照“2.2.4”项下方法处理低、中、高(0.958、5.75、92.0 μg·L-1)3种浓度的质控血浆样本,每一浓度均为5份,进样分析后获得峰面积A;取空白血浆若干,加入3倍体积乙腈沉淀处理后获得上清液,另取10 μL低、中、高3种浓度的工作液各5份,分别加入390 μL的此上清液,涡旋振荡1 min,置于高速离心机中以13000 r·min-1离心10 min,取50 μL上清液,加入50 μL纯水混匀,取5 μL进样分析后获得相应的峰面积B;取10 μL低、中、高3种浓度的工作液各5份,分别加入90 μL的纯水配置成对照品溶液,并按照“2.2.4”项下方法处理,进样分析后获得相应的峰面积C。提取回收率为峰面积A与峰面积B之比,基质效应为峰面积B与峰面积C之比:血浆样本的提取回收率为(47.06±6.34)%,基质效应为(52.47± 5.51)%,其他结果见表2。
2.2.9 稳定性考察按照“2.2.4”项下方法处理质控样本,每一浓度5份进样分析,考察了血浆样本经历3次冷冻-解冻循环稳定性、-40℃冷冻放置20 d稳定性、室温放置6 h稳定性以及处理后室温放置24 h稳定性,其中血浆样品经历3次冰冻-解冻循环后万古霉素低、中、高3种浓度的RSD分别为9.03%、4.17%、1.52%;血浆样品在-40℃放置20 d后处理测定万古霉素低、中、高3种浓度的RSD分别为11.38%、5.40%、4.54%;血浆样品室温放置6 h后处理测定万古霉素血浆样品低、中、高3种浓度的RSD分别为8.64%、5.83%、7.39%;处理后置于进样器24 h后,用当日处理的标准曲线计算万古霉素低、中、高3种浓度的RSD分别为13.32%、5.51%、2.41%。结果表明,在上述稳定性考察条件下,万古霉素均保持稳定,未出现明显变化。符合生物样品分析要求。
3 样本检测结果与比较
分别采用HPLC法、LC-MS/MS法和FPIA法检测95份临床使用万古霉素进行血药浓度监测的样本,并采用SPSS 11.5软件对测定结果进行相关性分析和偏倚分析,发现HPLC法和LC-MS/MS法分别与FPIA法测定结果具有显著相关性,r=0.9621,P<0.0001和r=0.9466,P<0.0001(见图3),Bland-Altman偏倚分析发现只有95%的样本都在Mean± 1.96SD范围内,所以认为HPLC法和LC-MS/MS法与FPIA法的偏倚不显著。
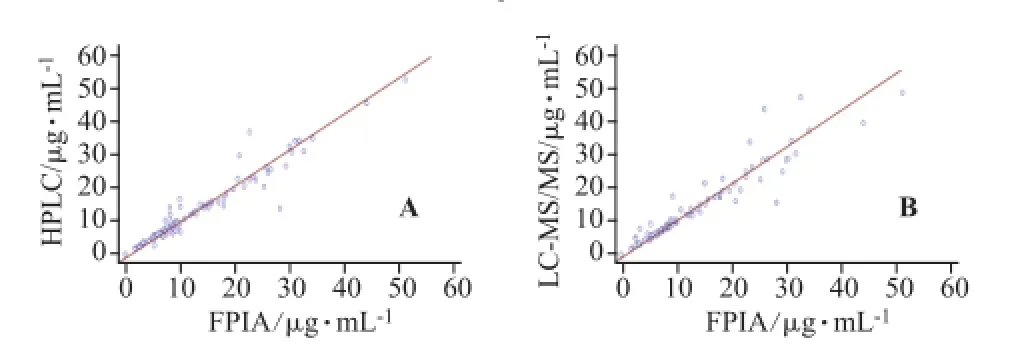
图3 HPLC法、LC-MS/MS法与FPIA法测定万古霉素血药浓度的相关性(n=95)
4 讨论
目前对万古霉素进行常规血药浓度监测,应用最多的方法是FPIA法,具有较为快速、经济、结果准确的特点;但是基于免疫学原理的众多监测方法其共同缺点是易受到其它药物或代谢物的干扰,若商品化的试剂盒的供应不及时可能影响临床的监测,同时专用的检测设备及每个监测品种的专用试剂盒也不够灵活。基于色谱的方法具有特异性好、使用灵活的特点:其中HPLC法使用尤其广泛,但也有操作繁琐、分析时间长、灵敏度达不到要求的缺点;LC-MS/MS法具有灵敏、快速、简便、准确的优势,已有很多实验室用于基础研究和临床研究,但仪器昂贵,基质效应大。3种方法各有优劣,我们分别采用3种方法检测了95例万古霉素血药浓度,两种方法与FPIA法较为一致,经Passing-Bablok分析,分别仅有5个标本偏差>1.96 SD,不存在显著偏倚。
万古霉素和去甲万古霉素均为双电荷母离子[M+2H]2+,因此选择m/z 725.0→144.0和718.5→144.0作为定量离子对。万古霉素属于水溶性分子,所以本文建立的HPLC和LC-MS/MS测定法均采用耗时较短的蛋白沉淀法处理血浆样品。目前,酸、盐、有机溶剂等都可用作沉淀剂,其中强酸高氯酸,可在较少用量时较为完全地沉淀血浆,从而较少地稀释样本,适用于灵敏度较低的HPLC法。而乙腈的沉淀效率高,能够完全沉淀蛋白并对残余杂质起稀释作用,所以适用于灵敏度较高的LC-MS/MS法,整个处理过程中8倍稀释工作液后的最低检测限仍然达到0.4 μg·mL-1,可以满足人体药物代谢动力学研究的要求。但两种方法的提取回收率均不高,且LC-MS/MS法存在较强的基质效应,在其他文献[4]中也存在此现象。推测原因可能是万古霉素在沉淀剂中的低溶解度导致沉淀过程中产生较大损耗,特别是有机溶剂(乙腈)能更大程度地降低万古霉素的溶解度,进而降低其回收率[10]。徐冰等用HPLC法测定血浆中万古霉素浓度时的提取回收率为68%~72%[6],焦志铁等用HPLC法测定血浆中去甲万古霉素浓度时的提取回收率为53%~57%[11],冼燕萍等建立的UPLC-MS/MS法测定猪肉中万古霉素与去甲万古霉素时认为其方法存在较大的基质效应[4]。虽然采用液液萃取和固相萃取[12]等多种手段联合的方法可将提取回收率提高至70%以上,并一定程度上降低基质效应[5],但却大大延长了样品处理时间。因此考虑多次测定同一批样本结果未出现较大波动,及与FPIA法测定结果具有较强的相关性和较小偏倚,本研究仍然采用沉淀法处理血浆样品,确保测定方法准确而快速。
本文建立了HPLC法和LC-MS/MS法用于监测血浆中万古霉素血药浓度,方法与FPIA法结果一致,均可替代FPIA法进行万古霉素的血药浓度监测及人体药物代谢动力学的研究。
[1] 四川美康医药软件研究开发有限公司.药物临床信息参考[M].重庆:重庆出版社,2008:192-3.
[2] 陈佰义,管向东,何礼贤.万古霉素临床应用中国专家共识[J].中国新药与临床杂志,2011,30(8):561-73.
[3] 王维忠,钱南萍,陈斌,等.高效液相色谱法和化学发光酶免疫法测定万古霉素的血药浓度[J].中国药业,2012,21(20):27-9.
[4] 冼燕萍,陈立伟,罗海英,等.UPLC-MS/MS法测定猪肉中万古霉素与去甲万古霉素[J].分析测试学报,2013,32(2):162-7.
[5] 郭启雷,史海良,杨红梅,等.液相色谱-串联质谱法测定牛奶中万古霉素和去甲万古霉素残留[J].食品工业科技,2013,34(008):86-7.
[6] 徐兵,李昕,张莉.反相高效液相色谱法测定患者血浆中万古霉素的浓度[J].中南药学,2009,7(2):100-2.
[7] Cass RT,Villa JS,Karr DE,et al.Rapid bioanalysis of vancomycin in serum and urine by high-performance liquid chromatography tandem mass spectrometry using on-linesampleextractionandparallelanalytical columns[J].RapidCommunicationsinMass Spectrometry,2001,15(6):406-12.
[8] Shibata N,Ishida M,Venkata Rama Prasad Y,et al.Highly sensitive quantification of vancomycin in plasma samplesusingliquidchromatography-tandemmass spectrometry and oral bioavailability in rats[J].Journal of Chromatography B,2003,789(2):211-8.
[9] Zhang T,Watson DG,Azike C,et al.Determination of vancomycin in serum by liquid chromatography-high resolution full scan mass spectrometry[J].J Chromatogr B,2007,857(2):352-6.
[10] 唐云彪,张萌萌,隋因,等.LC-MS/MS法测定人血浆中万古霉素的血药浓度[J].药物分析杂志,2013,33(9):1501-6.
[11] 焦志铁,张树倩.血浆去甲万古霉素的浓度测定[J].医药导报,2008,27(12):1523-5.
[12] 向平,沈敏,卓先义.液相色谱-质谱分析中的基质效应[J].分析测试学报,2009,28(6):753-6.
Establishment of Chromatographic Methods for the Determination of Vancomycin in Human Serum
JIANG Hui-ting,CHEN Bing,YANG Wan-hua*
Department of Pharmacy,Ruijin Hospital,Shanghai JiaoTong University School of Medicine,Shanghai 200025,China
Objective:To establish an HPLC and LC-MS/MS method for determining vancomycin in humanserumandtocomparewithFPIA.Methods:SerumsamplesforHPLCwereextractedby sedimentation with 10%perchloric acid.The chromatographic column of NovaPak C18was used and the column temperature was kept at 35℃.The mobile phase was composed of KH2PO4buffer solution-methanol (85∶15,v/v,pH=3.2),the flow rate was 1 mL·min-1and the UV detection was performed at 230 nm.Serum samples for LC-MS/MS were precipitated by acetonitrile and the supernatants were used.The separations were performed on an Agilent Eclipse XDB-C18analytical column(100 mm×2.1 mm,3.5 μm)at 40℃with the mobile phase composed of water(0.1%formic acid)-acetonitrile(90∶10,v/v)at a flow rate of 0.2 mL· min-1.ESI was used which was performed in the multiple reaction monitoring mode(MRM)using target ionsm/z725.0→144.0(vancomycin)andm/z718.5→144.0(IS).Then the HPLC and LC-MS/MS methods were used to determine 95 clinical samples comparing with FPIA.Results:The linear range of the two methods were 0.4~96 and 1.2~96 μg·mL-1,respectively,with LLOQ at 0.4 and 1.2 μg·mL-1.The intra-and inter-day RSD were within 15%.The HPLC and LC-MS/MS methods strongly correlated with FPIA without significantdifferences.Conclusion:TheHPLCandLC-MS/MSmethodsweestablishedwererapid, sensitive,precise and reliable for the determination of vancomycin in human serum,which can be applied in the study of human vancomycin pharmacokinetics and the practice of therapeutic drug monitoring.
Vancomycin;HPLC;LC-MS/MS;FPIA
R969.1
A
1673-7806(2014)06-509-05
姜慧婷,女,硕士研究生 E-mail:jianghuiting0227@163.com
*通讯作者 杨婉花,女,主任药师,硕士生导师 E-mail:yangwanhuaxy@163.com
2014-04-10
2014-06-16