不同来源莪术中姜黄素类成分的含量差异研究
2014-04-30蔡颖宋珅徐杰陈建伟崔小兵
蔡颖,宋珅,徐杰,陈建伟,崔小兵
1南京市白下区建中中医院,南京 210004;2南京中医药大学,南京 210023;3温州市天禾生物科技有限公司,浙江温州 325608
不同来源莪术中姜黄素类成分的含量差异研究
蔡颖1,宋珅2*,徐杰3,陈建伟2,崔小兵2
1南京市白下区建中中医院,南京 210004;2南京中医药大学,南京 210023;3温州市天禾生物科技有限公司,浙江温州 325608
目的:用高效液相色谱法测定不同来源的莪术中3种姜黄素成分,比较姜黄素(curcumin,Ⅰ)、去甲氧基姜黄素(demethoxycurcumin,Ⅱ)和双去甲氧基姜黄素(bisdemethoxycurcumin,Ⅲ)的含量差异。方法:采用Kromasil色谱柱,流动相为乙腈-水(0.5%冰乙酸),流速为1 mL· min-1,检测波长为425 nm。结果:姜黄素、去甲氧基姜黄素、双去甲氧基姜黄素的线性范围分别为0.04~0.16 μg(r=0.9991)、0.037~0.150 μg(r=0.9990)、0.00015~0.00062 μg(r=0.9996);平均回收率(n=9)分别为103.32%、100.32%、100.06%。结论:不同来源的莪术中姜黄素类成分的含量存在着明显的差异。
姜黄素;去甲氧基姜黄素;双去甲氧基姜黄素;莪术;高效液相色谱法
莪术是姜科姜黄属植物的根茎,是一种常用的传统中药。《中国药典》2010年版一部莪术项下[1]共收载了3种植物来源,即蓬莪术(Curcuma phaeocaulisValeton)、广西莪术(Curcuma kwangsiensisS. G.Lee et C.F.Liang)和温莪术(温郁金,Curcuma wenyujinY.H.Chen et C.Ling),原植物标本见图1。莪术中含有两大类成分,即挥发油(1%~2.5%)和姜黄素类成分[2](结构式见图2)。其中,姜黄素具有抗肿瘤、护肝、调节免疫功能、抗炎和降血脂等多重药理作用,临床上可应用于肿瘤、脑梗死和高血脂等多种疾病的治疗,对肝炎和眼科系统也有一定疗效[3]。现在分析姜黄素类化合物方法有高效液相色谱-串联质谱法[4]、分光光度法[5]、RP-HPLC法[6]。由于高效液相色谱法具有分析速度快、分离效率高、灵敏度高、检测自动化、适用范围广、组分易回收、样品处理简单等优点,因此,本文使用HPLC法对莪术中的姜黄素类成分进行了研究。对3种不同来源、14个不同产地的莪术药材中姜黄素类成分:姜黄素(curcuminⅠ)、去甲氧基姜黄素(demethoxycurcuminⅡ)和双去甲氧基姜黄素(bisdemethoxycurcuminⅢ)进行了含量测定,为制定莪术饮片的质量标准及临床评价莪术质量提供参考。

图1 3种莪术原植物标本

图2 3种姜黄素成分化学结构
1 实验材料
1.1 仪器
Waters 2690高效液相色谱仪(美国Waters公司)。
1.2 药品与试剂
姜黄素对照品(批号:110823-201004,中国药品生物制品检定所);去甲氧基姜黄素、双去甲氧基姜黄素对照品(纯度>99.0%,上海源叶生物技术有限公司)。
甲醇(色谱纯);乙醇(分析纯);超纯水系统(美国Merck Millipore公司)。
药材:温莪术又称温郁金Curcuma wenyujin,从浙江省温州市12个不同地区收集的药材;蓬莪术Curcuma phaeocaulis5个批次购自成都荷花池药材市场(四川产);广西莪术Curcuma kwangsiensis2个批次购自广西省玉林市。经本文作者之一陈建伟鉴定均符合《中国药典》规定的药材。
2 实验方法
2.1 样品的挥发油含量测定
准确称取各产地鲜品温莪术、加工品温莪术放入1000 mL圆底烧瓶中,加入水,参照2010年版《中国药典》一部(附录ⅩD)挥发油测定甲法进行总挥发油提取,无水硫酸钠脱水干燥,得挥发油,计算挥发油得率,结果见表1。
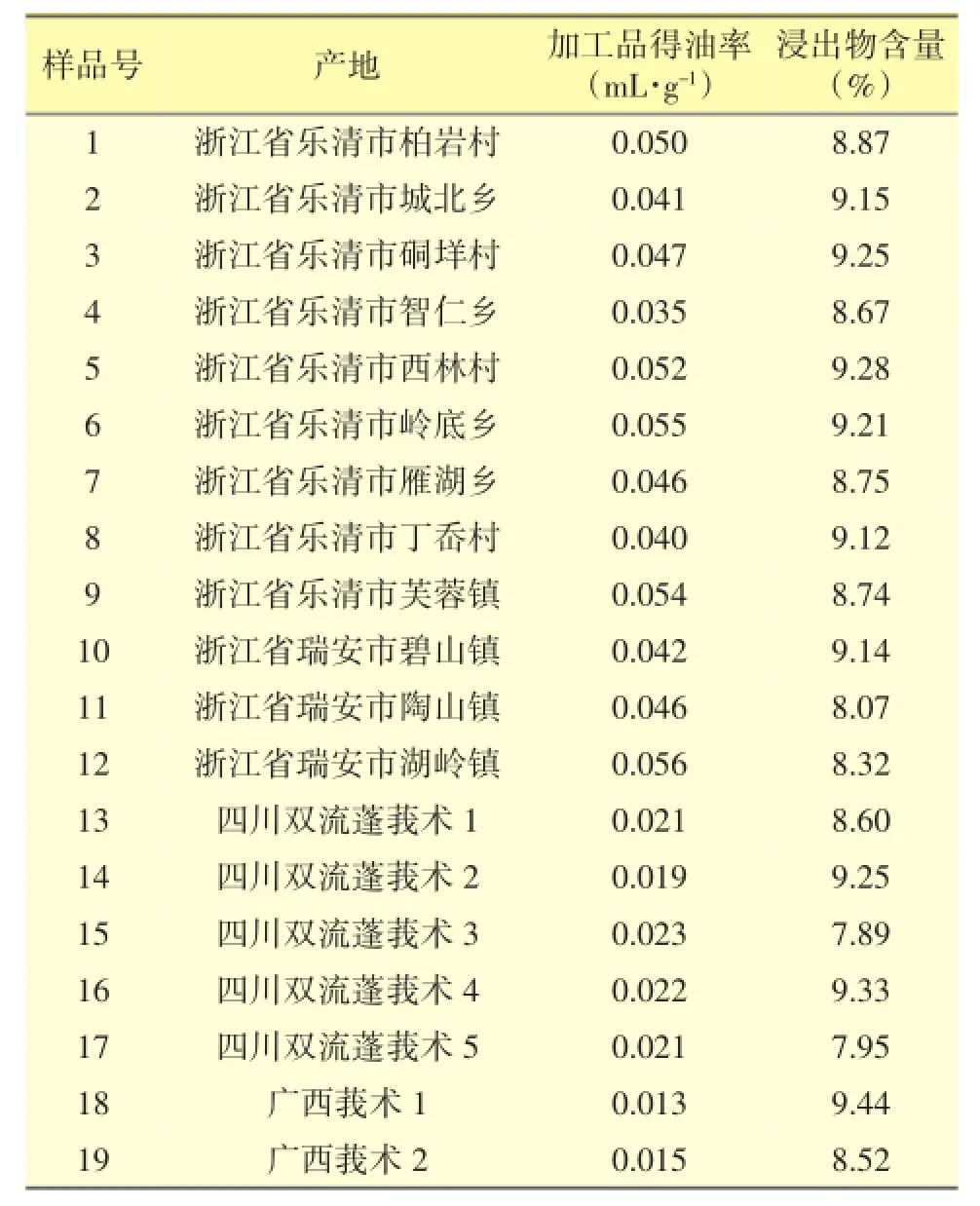
表1 药材挥发油及浸出物测定结果
2.2 浸出物测定
照《中华人民共和国药典》附录ⅩA项下的热浸法测定,用稀乙醇做溶剂,结果见表1。
2.2.1 色谱条件的选择色谱柱:Kromasil C18(250 mm×4.6 mm,5 μm);流动相:A相为0.5%冰醋酸水溶液,B相为甲醇,梯度洗脱(0 min:56%A,44%B;9 min:48%A,52%B;15 min:38%A,62%B);检测波长:425 nm;柱温:35℃;流速:1 mL·min-1;进样量:10 μL。理论塔板数按姜黄素、去甲氧基姜黄素和双去甲氧基姜黄素峰计算均不少于3000。HPLC图谱见图3。

图3 对照品(A)和样品(B)的HPLC图
2.2.2 供试品溶液提取制备条件的考察为确定供试品溶液最佳提取制备条件,对提取溶媒、提取方式及提取时间进行考察。
取温莪术粉末约0.5 g 3份,精密称定,分别加入溶媒(75%乙醇、无水乙醇、甲醇)10 mL,超声提取器提取,挥干溶剂,残渣加甲醇使溶解,转移至1 mL量瓶中,用甲醇定容至刻度,摇匀,精密吸取10 μL,注入液相色谱仪,测定,计算含量。结果表明,采用75%乙醇超声提取效果较好,且色谱峰峰形较好;而采用无水乙醇或甲醇提取的样品,三种姜黄素的提取效率均较75%乙醇提取的样品低,故确定采用75%乙醇超声提取。取干燥至恒重的上述温莪术粉末0.5 g,3份,精密称定。(1)置于250 mL圆底烧瓶,加75%乙醇150 mL,加热回流2 h;(2)置于100 mL具塞三角瓶中,加入75%乙醇100 mL,密塞,一次冷浸12 h;(3)置于100 mL具塞三角瓶中,加75%乙醇30 mL,超声提取30 min。3种提取液分别过滤、浓缩,最后用甲醇定容至1 mL量瓶中。进样10 μL,记录HPLC色谱图,结果表明,(2)和(3)测定结果基本一致,而(1)提取效果较差。故选用超声提取法。为保证超声提取的效率,提取用的溶媒体积为30 mL,样品提取至无色后对成分含量的影响较小,提取次数为2次。归纳表明,样品使用75%乙醇作溶剂;以超声提取2次,每次75%乙醇用量为30 mL,时间为20 min为宜。
确定供试品溶液的最佳提取条件为:药材过60目筛,精密称定药材粉末0.5 g,置50 mL离心管中,每次加入75%乙醇30 mL,超声振荡20 min,共计2次,提取液离心(转速4920 r·min-1,15 min)、过滤,用少量75%乙醇洗涤残渣及滤器,合并滤液,挥干溶剂,残渣加甲醇溶解并定容至1 mL量瓶,过微孔滤膜(0.45 μm),作为供试品。
2.3 方法学考察
2.3.1 标准曲线与线性范围考察对照品溶液的制备:精密称取各对照品适量,加入甲醇制成每1 mL分别含双去甲氧基姜黄素0.00007745 mg、去甲氧基姜黄素0.0187 mg、姜黄素0.0408 mg的溶液,作为对照品储备液。分别精密吸取上述对照品溶液,用甲醇配制成混合对照品溶液。其中,双去甲氧基姜黄素浓度为0.01548、0.03098、0.03872、0.04646、0.06196 μg·mL-1,去甲氧基姜黄素浓度为3.74、7.48、9.35、11.22、14.96 μg·mL-1,姜黄素浓度为8.16、10.20、12.24、16.32、32.64 μg·mL-1;分别吸取不同浓度对照品溶液10 μL进行分析测定。以对照品峰面积为纵坐标,对照品浓度为横坐标,绘制标准曲线。双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的回归方程和相关系数及线性范围分别为:Y= 26044X-3073.8,r2=0.9992,0.01548~0.06196 μg·mL-1;Y=153619X-286066,r2=0.9981,3.728~14.96 μg· mL-1;Y=128598X-222001,r2=0.9982,8.16~32.64 μg·mL-1。
2.3.2 精密度试验精密吸取双去甲氧基姜黄素0.06196 μg·mL-1、去甲氧基姜黄素14.96 μg·mL-1、姜黄素16.32 μg·mL-1的混合对照品溶液10 μL,按上述色谱条件,连续进样6次,结果双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的RSD分别为0.5%、0.2%、0.5%,表明仪器精密度良好。
2.3.3 重现性试验取同一产地温莪术药材(产地雁湖乡),粉碎过60目筛,精密称量0.5 g,共5份,按确定的供试品溶液制备条件制备并按上述色谱条件测定,结果双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的含量的RSD分别为0.4%、0.64%、0.43%,表明本方法重现性良好。
2.3.4 稳定性试验取重现性试验的1号样品依次于不同时间段进样测定峰面积值,双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的峰面积的RSD分别为0.41%、0.24%、0.58%,表明供试品溶液在12 h内稳定。
2.3.5 加样回收率试验分别精密称取已知含量的温莪术干燥药材(产地:雁湖乡),粉碎,过60目筛,取约0.25 g,共6份,精密称定,置50 mL离心管中,分别加入等同于样品中的双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素含量80%、100%、120%的对照品,每次加入75%乙醇30 mL,超声提取20 min,共2次,提取液离心(转速4920 r·min-1,15 min),过滤,浓缩定容至1 mL量瓶,作为供试品。过微孔滤膜(0.45 μm),取续滤液10 μL注入液相色谱仪,测定含量,结果见表2。

表2 双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素加样回收率试验结果
结果表明,双去甲氧基姜黄素的平均回收率为100.74%,RSD为2.33%;去甲氧基姜黄素的平均回收率为101.03%,RSD为2.80%;姜黄素的平均回收率为100.40%,RSD为2.02%。样品的加样回收率试验结果符合含量测定方法学的要求。
2.3.6 姜黄素类成分的含量测定取14个不同产地的莪术药材,每个产地平行3份,按照“2.2.2”项下制备成待测溶液(由于产自四川省双流镇的蓬莪术1号及2号样品中姜黄素的含量较高,在检测前将样品稀释了1倍),精密吸取10μL注入色谱仪,记录色谱图。外标法计算供试品溶液中双去甲氧基姜黄素、去甲氧基姜黄素、姜黄素的含量。结果见表3。
3 讨论与小结
3.1 从检测结果可知:温莪术中双去甲氧基姜黄素的平均含量在0.063 μg·g-1~0.113 μg·g-1,去甲氧基姜黄素的平均含量在6.035 μg·g-1~14.097 μg·g-1,姜黄素的平均含量在12.838 μg·g-1~31.423 μg·g-1。蓬莪术中双去甲氧基姜黄素的平均含量在0.270 μg·g-1~1.365 μg·g-1,去甲氧基姜黄素的平均含量在10.707 μg·g-1~16.923 μg·g-1,姜黄素的平均含量在22.722 μg·g-1~37.449 μg·g-1。而广西莪术中的所有姜黄素类成分均未检出。
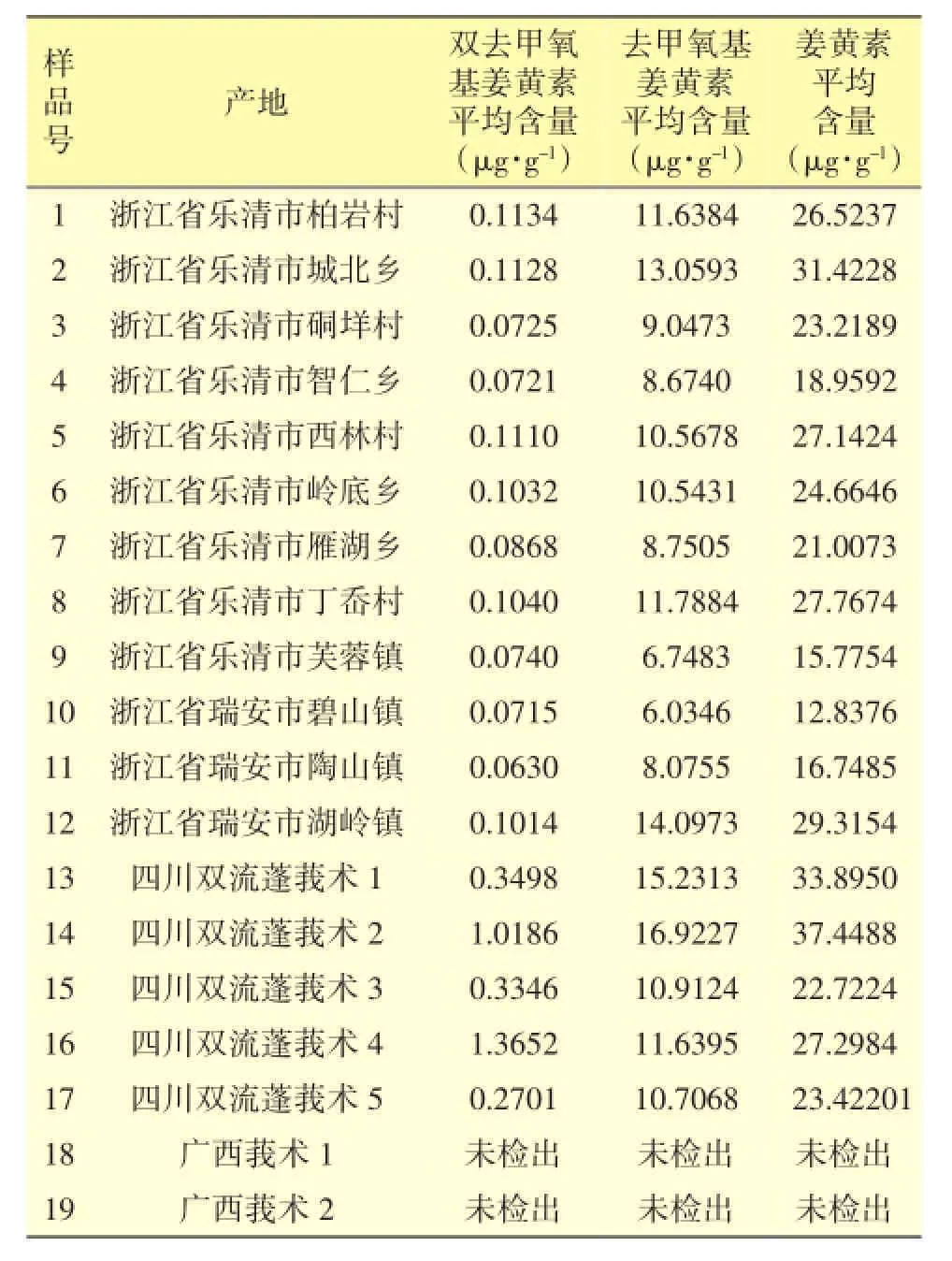
表3 不同来源的莪术药材中姜黄素类成分的含量测定结果(n=3)
3.2 本文同时进行了挥发油及醇浸出物含量的测定,与姜黄素类成分含量测定结果相对照发现:3个品种的莪术在姜黄素类成分含量及挥发油含量上相差较大:川产蓬莪术姜黄素类成分含量较高,浙江省产的温莪术挥发油含量较高。这可能是由于产地及品种不同所致。试验中曾测定2批广西莪术,发现均不含姜黄素类成分,且药材的其它成分含量也较为低下。本次实验中未检测出广西莪术的姜黄素类成分的原因有可能是这一药材品种本身姜黄素类成分含量很低,药材的质量不佳,也有可能是药材在采收加工中使用的方法不当导致的。因此,在药材采收及加工过程中,选择合理的采收时间及使用规范的加工方法对保证药材的质量相当重要。提示有必要对3种不同品种的莪术药材在采收及加工过程中的变化进行研究,并对这3个不同品种的莪术药材中姜黄素类成分、挥发油进行分别规定。同时检测结果也表明,同一品种如温莪术中姜黄素类成分含量与挥发油含量之间没有相关性。
[1] 国家药典委员会.中华人民共和国药典第一部[S].北京:化学工业出版社,2005:194.
[2] 成晓静,刘华钢,赖茂祥.莪术的化学成分及药理作用研究概况[J].广西中医学院学报,2007,10(1):79-82.
[3] 李琦,金剑,许颖.姜黄素的药理作用及其临床应用进展[J].现代中西医结合杂志,2012,21(12):1366-8.
[4] 李伟,肖红斌,王龙星,等.高效液相色谱-串联质谱法分析姜黄中微量的姜黄素类化合物[J].色谱,2009,27(3):264-9.
[5] 何媛媛,于得才,孔令辉,等.姜黄超临界CO2流体萃取物姜黄素含量测定[J].中成药,2007,29(1):122-4.
[6] 李明,周欣,赵超,等.HPLC同时测定姜黄中3种姜黄素的含量[J].药物分析杂志,2008,28(11):1810-4.
Research on Contents of Curcuminoids in Different Curcuma Samples
CAI Ying1,SONG Shen2*,XU Jie3,CHEN Jian-wei2,CUI Xiao-bing21Baixia District Jianzhong Hospital of Nanjing,Nanjing 210004,China;2Nanjing University of Traditional Chinese Medicine,Nanjing 210023,China;3Wenzhou TianHe Biological Technology Co.LTD,Wenzhou 325608,China
Objective:To research on the content differences of curcuminoids including curcumin, demethoxycurcumin and bisdemethoxycurcumin in Rhizoma Curcumae from different sources.Methods:A reversed-phase HPLC system consisting of an ODS column and a mixture of acetonitrle-water(with 0.5% acetic acid)as the mobile phase was used.The flow rate was 1.0 mL·min-1and the detection was effected at 425 nm.Results:The calibration curves of curcumin,demethoxycurcumin and bisdemethoxycurcumin were linear in the range of 0.04~0.16 μg(r=0.9991),0.037~0.150 μg(r=0.9990),0.00015~0.00062 μg(r= 0.9996),respectively;The average recoveries(n=9)were 103.32%,100.32%and 100.06%,respectively.Conclusion:The results showed that the contents of curcuminoids vary with sample source.
Curcumin;Demethoxycurcumin;Bisdemethoxycurcumin;Curcuma wenyujin;HPLC
R927.2
A
1673-7806(2014)06-502-04
蔡颖,女,副主任药师 E-mail:njcyworld@sina.com
*通讯作者 宋珅,男,副教授 E-mail:songseng@yeah.net
2014-05-30
2014-07-09