抗坏血酸在纳米金/石墨烯复合物 修饰电极上的电化学行为研究
2014-03-27刘彦培张艳丽杨应彩庞鹏飞
刘彦培,张艳丽,杨应彩,庞鹏飞
(云南民族大学 民族药资源化学国家民委-教育部重点实验室,云南 昆明650500)
石墨烯(单原子层石墨晶体薄膜)是一种新型的由碳原子构成的二维蜂窝状物质.石墨烯比表面积大(高达2600 m2/g),具有良好的热力学性能及优异的电子传递性能[1-2].因此将其作为电极修饰材料可提高反应的电子转移速率,提高灵敏度,目前人们已将石墨烯广泛应用于电化学与生物传感领域[3-5].纳米金粒子有着特异的表面效应,良好的电子学特性和生物兼容性而被广泛应用于电化学与生物传感器中[6-8].
抗坏血酸(ascorbic acid)又称维生素C(vitamin C),在蔬菜和水果中含量较高.抗坏血酸具有抗氧化性,常用做食品添加剂.抗坏血酸参与体内氨基酸的代谢,能增加肌体的抗病能力,可用于预防坏血病.因此抗坏血酸含量的测定在食品和医学等领域具有重要意义.目前,测定方法主要有高效液相色谱法[9]、氧化还原滴定法[10]、荧光法[11]、光度法[12]、电化学分析法[13-14]等.其中电化学方法是一种简便、快速、可靠且适合现场检测的方法.
本文利用本实验室合成的石墨烯,通过直接滴涂法制备石墨烯修饰玻碳电极[15],然后通过电沉积法在石墨烯表面电沉积纳米金粒子制得复合材料.结合石墨烯、纳米金粒子独特的化学性质,利用其对AA的直接催化氧化作用,制备了纳米金/石墨烯复合物修饰电极(AuNPs/GR/GCE),实现对抗坏血酸快速、灵敏的检测,与直接利用玻碳电极测定AA相比[16],AuNPs/GR/GCE具有更高的灵敏度.该修饰电极制作工艺简单、成本较低,对AA的测定具有良好的重现性和稳定性.
1 实验部分
1.1 仪器和试剂
CHI660D型电化学工作站(上海辰华仪器有限公司);pH计(梅特勒-托多利FE20型);三电极体系:以AuNPs/GR/GCE为工作电极,饱和甘汞电极(SCE)为参比电极,铂电极为辅助电极;KQ-250DA型数控超声波清洗器(昆山市超声仪器有限公司); 抗坏血酸(北京芳草医药化工研制公司);氯金酸(上海国药集团化学试剂有限公司);0.1 mol/L磷酸氢二钠-柠檬酸缓冲溶液;石墨烯分散液:称取10 mg石墨烯加入10 mL水中,用超声分散约8 h形成黑色均匀的分散液.所用试剂均为分析纯,实验用水为去离子水.
1.2 石墨烯的制备
氧化石墨的制备采用Hummers方法[17-19],将2.5 g 1 000目天然鳞片石墨粉加入到冰浴冷却的60 mL浓硫酸中,然后将1.25 g亚硝酸钠和7.5 g高锰酸钾研细并均匀混合后在搅拌下缓慢加入到上述溶液中,控制温度在5 ℃以下搅拌反应2 h后, 在35 ℃的恒温水浴中维持1 h,缓慢加入120 mL水在95 ℃维持0.5 h, 用温水稀释至350 mL,倒入适量 6%的过氧化氢,趁热过滤,用1 mol/L盐酸充分洗涤滤饼至溶液中无SO42-(用氯化钡溶液检测),在50 ℃下真空干燥15 h,密封保存.
石墨烯的制备采用水合肼还原法[18-20],将150 mg氧化石墨放入装有150 mL水的三颈烧瓶中,超声震荡至无黑色颗粒状物质存在,加入3 mL水合肼溶液呈黑色悬浮液,缓慢将温度升至95 ℃,回流24 h.用适量的水和甲醇分别洗涤滤饼,于50 ℃下干燥,密封保存.
1.3 纳米金/石墨烯复合物修饰电极的制备
将玻碳电极分别在粒径为0.3 μm和0.05 μm的Al203悬浊液上抛光成镜面,然后依次在水、无水乙醇、水中分别超声清洗3 min,在室温下晾干.取6 μL、1.0 mg / mL均匀的石墨烯分散液滴涂在玻碳电极表面,在红外灯下静置烘干后得到石墨烯修饰电极.将此修饰电极用水冲洗,晾干,置于15 mL、0.1 mg/mL氯金酸溶液中,于-0.6~1.2 V下电沉积6圈,取出后用水反复冲洗,即制得AuNPs/GR/GCE.
1.4 实验方法
移取适量的磷酸氢二钠-柠檬酸缓冲溶液(pH = 4.0)于电解池中,加入一定量的抗坏血酸标准溶液,以AuNPs/GR/GCE为工作电极,以饱和甘汞电极为参比电极,铂丝为辅助电极,用循环伏安法研究抗坏血酸的电化学行为.
2 结果与讨论
2.1 测试底液的选择
本实验考察了硝酸钾、醋酸-醋酸钠、盐酸、磷酸氢二钠-柠檬酸等作为支持电解质时AA的循环伏安行为,结果发现,在0.1 mol/L磷酸氢二钠-柠檬酸缓冲溶液中,AA的氧化峰电流最大,并且峰形较好.
2.2 石墨烯和纳米金修饰量的选择
纳米金/石墨烯复合膜的厚度会影响AA氧化峰电流的大小.实验研究了石墨烯的修饰量和纳米金的电沉积圈数对抗坏血酸氧化峰电流的影响,结果表明当石墨烯的修饰量为6 μL(1.0 mg/mL),电沉积纳米金6圈时氧化峰电流最大,故本实验采用6 μL石墨烯(1.0 mg /mL)并且电沉积纳米金6圈修饰的玻碳电极作为工作电极.
2.3 纳米金/石墨烯复合物的表征
纳米金/石墨烯复合物在玻碳电极表面的SEM图见图1,从图中可以看出,纳米金粒子均匀地分散到石墨烯的表面.

2.4 AA在不同修饰电极上的电化学行为
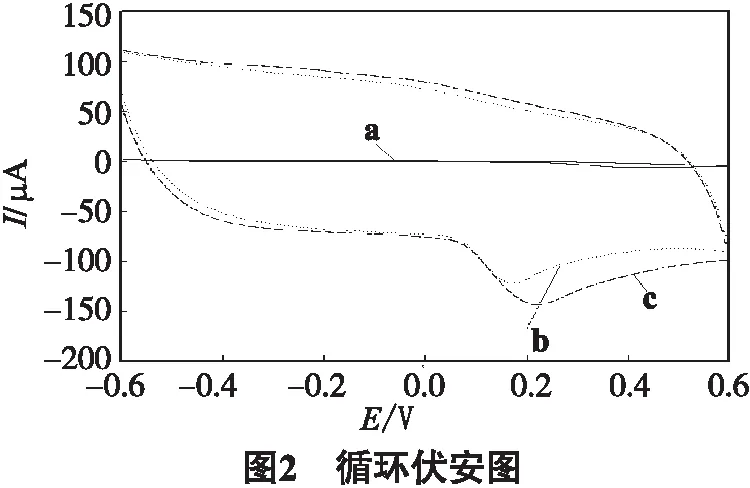
1 mmol/L AA 在裸电极GCE(a)、石墨烯修电极GR/GCE(b)和纳米金/石墨烯复合物修饰电极AuNPs/GR/GCE(c)以0.1 mol/L的磷酸氢二钠-柠檬酸缓冲溶液(pH = 4.0)作为支持电解质,扫描电位范围为-0.6~0.6 V,扫速为0.1 V/s的循环伏安曲线见图2. 从图中可以看出,AA 在不同的修饰电极上均发生不可逆的氧化反应,AA 在裸玻碳电极上只出现一个微弱的氧化峰(曲线a),而在GR/GCE上,AA的氧化峰电流显著增大(曲线b),说明石墨烯对AA的氧化有明显的电催化作用,这是因为石墨烯的比表面积大而且具有良好的电子传递能力.与前两者比较,AuNPs/GR/GCE则具有更明显的氧化峰(曲线c),这是因为纳米金作为良好的导电性物质,改善了电极的性能,对AA的电催化作用增强.
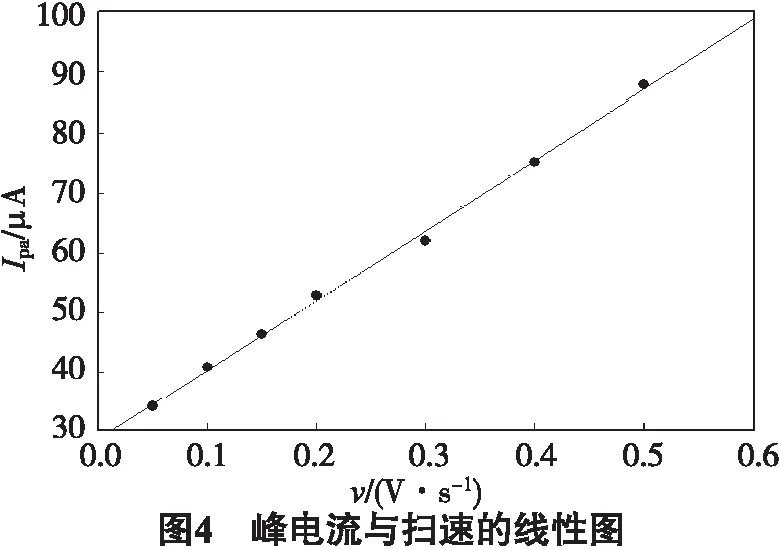
实验考察了在不同的扫描速率下AuNPs/GRGCE对AA响应电流的影响,扫描速率分别为0.05、0.10、0.15、0.20、0.30 、0.40、0.50 V/s,电极在含1×10-3mol/ L AA 的磷酸氢二钠-柠檬酸缓冲溶液 (pH = 4.0) 中的循环伏安曲线见图3,从图中可以看出,在0.05 ~ 0.5 V范围内AA的氧化峰电流随扫描速率的增大而增加.并且峰电流(Ipa)与扫速 (v) 呈良好的线性关系,见图4,线性方程为:Ipa=116.921v+28.623,相关系数R=0.999 0,说明电极过程受吸附控制.

2.5 底液pH值对AA催化作用的影响
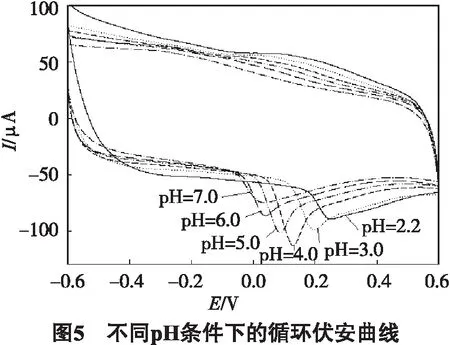
支持电解质溶液的pH会影响AuNPs/GR/GCE对AA的催化作用,在pH值为2.2~7.0范围内,用循环伏安法考察了磷酸氢二钠-柠檬酸缓冲溶液的pH值对修饰电极的影响见图5,结果表明在pH = 4.0时氧化峰电流最大,故本实验在pH = 4.0的磷酸氢二钠-柠檬酸缓冲溶液中进行.同时随着底液pH值的增大,AA的氧化峰电位发生了明显的负移,且在pH为2.2~7.0范围内与 AA 的氧化峰电位呈良好的线性关系,线性方程为Epa=0.365-0.055 pH,R=0.993 1,其斜率为-0.055 V/pH,这说明参与电极反应的质子数与电子数相同.
2.6 线性范围和检出限
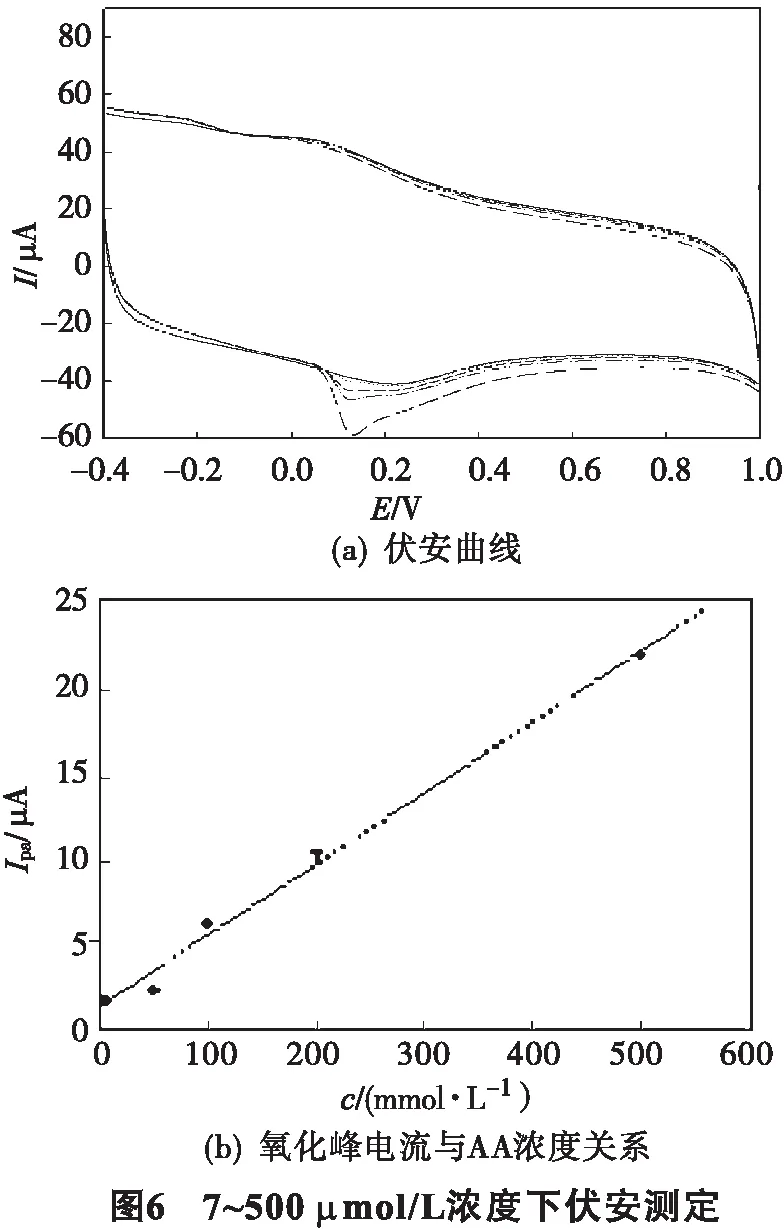
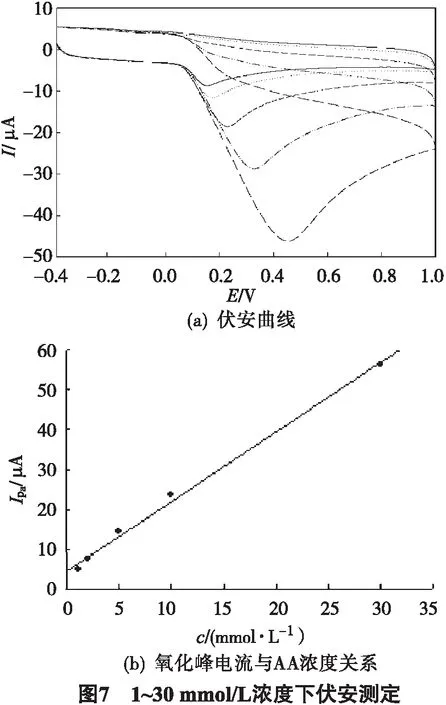
在优化的实验条件下,对不同浓度的AA进行循环伏安法测定,氧化峰电流与AA 的浓度在7 ~ 500 μmol/L(图6)和1 ~ 30 mmol/L(图7)范围内呈良好的线性,其线性方回归方程分别为:Ipa= 1.525 +0.042 0c(μmol/L),R=0.996 1;Ipa= 47.831 +17.299c(mmol/L),R=0.997 8;检出限为5 μmol/L(信噪比=3).
2.7 干扰实验
在最佳实验条件下,以AuNPs/GR/GCE工作电极,在含1 mmol/L AA的磷酸氢二钠-柠檬酸缓冲液中,考察了以下物质对AA测定的影响,结果表明10倍的葡萄糖,草酸,Cl-, NO3-, K+, Na+等对AA的测定没有明显干扰,说明此方法对AA的测定具有良好的选择性.
2.8 重现性和稳定性
连续对1 mmol/L的AA连续测定10次,其RSD值为3.2 %;用相同的方法制备5支AuNPs/GR/GCE并对1 mmol/L的AA进行检测,其RSD值为4.6%,说明此修饰电极具有良好的重现性.将电极在室温下放置15 d后再对1 mmol/L的AA进行测定,氧化峰电流为原来响应值的 95.6%,表明电极的稳定性较好.
2.9 实际样品的测定
取5片市售的维生素C药片( 0.1 g/片)研细,准确称取0.024 g用水溶解,过滤, 定容在 100 mL 容量瓶中,采用循环伏安法测定其中AA含量,加标回收实验结果(见表1),回收率在97.69 % ~ 103.5 % 之间,可用于实际样品的中AA的测定.
3 结语
本文制备了纳米金/石墨烯复合物修饰玻碳电极,研究了AA在此复合物修饰电极上的电化学行为,表明其对AA有较强的电催化作用,响应性能优于普通的玻碳电极和石墨烯修饰玻碳电极,并且具有较好的选择性、重现性、稳定性,可用于AA的检测.
参考文献:
[1] ZHANG Y B, TAN Y W, KIM P, et al. Experimental observation of the quantum Hall effect and Berry′s phase in graphene[J]. Nature, 2005, 438(7065):201-204.
[2] NOVOSELOV K S, GEIM A K, MOROZOV S V, et al. Electric field effect in atomically thin carbon films[J]. Science, 2004, 306(5696):666-669.
[3] ZHOU M, ZHAI Y M, DONG S J. Electrochemical sensing and biosensing platform based on chemically reduced graphene oxide[J]. Analytical Chemistry, 2009, 81(14):5603-5613.
[4] PUMERA M, AMBROSI A, BONANNI A, et al. Graphene for electrochemical sensing and biosensing[J]. Trends in Analytical Chemistry, 2010, 29(9):954-965.
[5] KUILA T, BOSE S, KHANRA P, et al. Recent advances in graphene-based biosensors. Biosensors and Bioelectronics, 2011, 26(12):4637-4648.
[6] 初凤红, 蔡海文, 瞿荣辉, 等. 纳米金在光学和电化学传感器中的应用[J]. 激光与光电子学进展, 2009, 46(11):58-64.
[7] LIM S H, WEI J,LIN J Y. Electrochemical genosensing properties of gold nanoparticle- carbon nanotube hybrid[J]. Chemical Physics Letters, 2004,400(4/5/6):578-582.
[8] 汪海燕, 王晔, 宋琼, 等. 葡萄糖在纳米金修饰金电极上电化学行为研究[J]. 分析科学学报, 2007, 23(2):185-188.
[9] 贾书静,冯三令, 储瑞武, 等. 高效液相色谱法测定饲料中总抗坏血酸含量[J]. 农技服务,2012,29(3):318-320.
[10] 曾盔, 周军, 王锦,等. 铁(Ⅲ)置换氧化还原滴定法测定维生素C片剂及针剂中抗坏血酸[J]. 理化检验-化学分册, 2007, 43(7):549-551.
[11] 章丽, 余世科, 高峰,等. 一种新型环糊精衍生物的制备及荧光法测定抗坏血酸[J]. 分析化学, 2005, 33(11):1583-1586.
[12] 黄光荣. 甲苯胺蓝分光光度法测定果蔬中的抗坏血酸[J]. 分析检测, 2005, 26(5):169-170.
[13] ZHENG X Y, ZHOU X, JI X, et al. Simultaneous determination of ascorbic acid, dopamine and uric acid using poly(4-aminobutyric acid) modified glassy carbon electrode[J]. Sensors and Actuators. B:Chemical, 2013, 178:359-365.
[14] ZHANG R, LIU S J, WANG L, et al. Electroanalysis of ascorbic acid using poly(bromocresol purple)film modified glassy carbon electrode[J]. Measurement, 2013, 46(3):1089 - 1093.
[15] ZHANG Y L, LIU Y P, HE J M, et al. Electrochemical behavior of caffeic acid assayed with gold nanoparticles/graphene nanosheets modified glass carbon electrode[J]. Electroanalysis, 2013, 25(5):1230-1236.
[16] 韩俊凤, 蔡雪, 贾林艳,等. 活化玻碳电极伏安法测定抗坏血酸[J]. 食品研究与开发, 2013, 34(2):70-72.
[17] HUMMERS W S, OFFEMAN R E. Preparation of graphitic oxide[J]. Journal of the Amer- ican Chemical Society, 1958, 80(6):1339.
[18] STANKOVICH S, DIKIN D A, PINER R D, et al. Synthesis of graphene-based nanosheets via chemical reduction of exfoliated graphite oxide[J]. Carbon, 2007, 45(7):1558-1565.
[19] PARK S, AN J, PINER R D, et al. Aqueous suspension and characterization of chemically modified graphene sheets[J]. Chemistry Of Materials, 2008, 20(21):6592-6594.
[20] STANKOVICH S, DIKIN D A, KOHLHAAS K M, et al. Graphene-based composite materials[J]. Nature, 2006, 442(7100):282-286.
