介孔Ag3PO4光催化剂的制备及其光电性能研究
2014-03-18段吴燕姜慧敏姜文静罗克梦
段吴燕 姜慧敏 姜文静 罗克梦
(南昌航空大学环境与化学工程学院,江西省持久性污染物控制与资源循环利用重点实验室,江西 南昌 330063 )
1 引言

本篇论文采用不同的方法,制备了一种具有介孔结构的、对可见光有吸收的Ag3PO4催化剂。在可见光下,对其光催化降解2,4-DCP有机污染物进行研究,证明介孔Ag3PO4光催化剂比普通Ag3PO4粒子的光催化活性大。
2 实验部分
2.1 实验药品
实验所用药品主要有:硝酸银、磷酸氢二钠,乙二醇、P123、丙酮、2,4-二氯苯酚,其中实验中所有药品和试剂均为分析纯,实验用水均为去离子水。
2.2 催化剂的制备
运用水热法和化学合成法制备介孔Ag3PO4光催化剂。具体如下:
①水热合成法:将适量P123溶解于混有乙二醇的去离子水中,搅拌溶解后,加入0.8 g的AgNO3混合均匀。同时,称取2.1596 g的Na2HPO4于10 mL的去离子水中,待溶解完全后倒入之前混合液中,并移入100mL的反应釜中,110℃下水热反应24 h。利用丙酮、无水乙醇、去离子水对所得黄色粉末抽滤、冲洗、去模板后,放入80℃鼓风干燥箱内烘干。
②化学合成法:AgNO3与P123的混合步骤同上,但在Na2HPO4加入混合液参与反应时,采用缓慢逐滴加入的方法进行试验。待Na2HPO4加入完毕后,搅拌并暗反应5 h,利用丙酮、无水乙醇、去离子水对所得明黄色粉末进行抽滤、冲洗、去模板后,放入80℃鼓风干燥箱内烘干。
为了对比,普通Ag3PO4粒子依据参考文献8中方法制备。
2.3 介孔Ag3PO4催化剂的表征
样品的X射线粉末衍射(XRD)采用德国Bruker D8型X射线衍射仪进行分析。利用日本JSM-7401F扫描电子显微镜表征样品的形貌结构,并利用附带的能量散射X-射线能谱(EDS)测定样品组成。运用美国麦克公司Tristar Ⅱ 3020 型全自动比表面分析仪对样品进行N2吸附脱附测试,估算样品的比表面积等参数。紫外可见漫反射光谱由紫外可见分光光度计(日立U-3900H)测得,扫描范围为350-700 nm 。利用所得漫反射数据,运用能带隙公式估算样品吸收边,确定带隙能。
(ahv)2=hv-Eg
2.4 催化剂的光催化性能研究
在光催化活性的测试中,利用所制备的样品在可见光下光降解水溶液中的2,4-二氯苯酚。将所得介孔和颗粒的Ag3PO4催化剂加入到40 mg/L的2,4-二氯苯酚水溶液中,充分搅拌分散均匀。光照前,混合液先在进行遮光暗处理30 min,以确保光催化剂和溶液之间达到一个吸脱附平衡。室温光降解中,每隔6min取样离心,取上清液用紫外-可见分光光度计测量所得2,4-DCP水溶液的吸光度。
2.5 催化剂的光电性能测试
通过浸涂法制备介孔和颗粒Ag3PO4两种粉末的薄膜电极,具体如下:将10mg 粉末样超声分散在100μL丙酮中,而后将其涂在1 cm2的导电玻璃(FTO)上,最后在室温下使其自然晾干。
光电性能测试在上海辰华CHI660D电化学工作站上完成。采用标准的三电极体系,制备的薄膜电极作为工作电极,饱和甘汞电极作为参比电极,碳棒为对电极,采用电流-时间法,用0.5 mol/L的Na2SO4溶液作为支持电解液,在0 V偏压下,对样品进行光电化学信号检测,绘制光生电流密度-时间曲线。
3 结果与讨论
3.1 样品形貌结构表征
XRD测试用于表征Ag3PO4的相结构,其中,水热法和化学法合成的未去除模板Ag3PO4的结构如图1中a和b曲线所示。由图中可知,两种方法合成的材料的XRD中均有Ag3PO4在20.884°,29.656°,33.292°,36.587°,42.485°,47.791°处立方晶相的特征峰,这与之前的报道相似[13],说明立方相Ag3PO4的存在。但水热法制备的Ag3PO4的XRD图谱中AgPO3衍射峰的出现,说明该种法制备的样品不是纯的Ag3PO4结构,不如化学法得到的样品纯净,证明了采用化学法制备介孔Ag3PO4是可行的实验方法。

图1 不同方法合成的Ag3PO4的XRD谱图:(a)水热合成法;(b)化学合成法
利用N2吸附-脱附等温曲线的测定对所获得样品的结构进一步深入分析。图2中a和b分别表示化学合成法制备的介孔Ag3PO4和普通Ag3PO4粒子的N2吸附脱附曲线。参考五类BDDT(Brunauer-Deming-Deming)吸附等温线的分类[14-15]可知,曲线a中的吸附曲线为IV型吸附等温线,但吸脱附曲线在相对中低压分段处,即P/P0在0-0.8内未能闭合,这说明此材料与氮之间有较强的作用力,可能存在强吸附势,未能实现良好的脱附。而曲线b的吸脱附过程很微弱,根据所得数据,可估算介孔Ag3PO4和普通Ag3PO4粒子的比表面积分别为5.85 m2/g和1.06 m2/g 。

图2 Ag3PO4的N2吸附-脱附曲线:(1)介孔Ag3PO4; (2)普通Ag3PO4
为观察比较普通Ag3PO4和介孔Ag3PO4的形貌结构,特对样品进行SEM表征,如图3中(a)和(b)所示。由图可知,普通Ag3PO4粒子的表面光滑,而介孔Ag3PO4的表面则凹凸不平,存在许许多多的细小的突起。这表明此类化学合成法在Ag3PO4表面形貌的改性上有一定的效果。

图3 不同结构Ag3PO4的SEM图:(a) 普通Ag3PO4; (b) 介孔Ag3PO4
进一步对样品的组分进行了测试分析,具体如图4所示。在EDS谱图中显示出了Ag,P,O,Si四种元素的特征峰,其中Si出自于硅片的基底,这进一步的证明了样品是Ag3PO4材料,与XRD所得结果相同。其中,各种元素的所占详细比例如表1所列。

图4 介孔Ag3PO4样品的EDS谱图
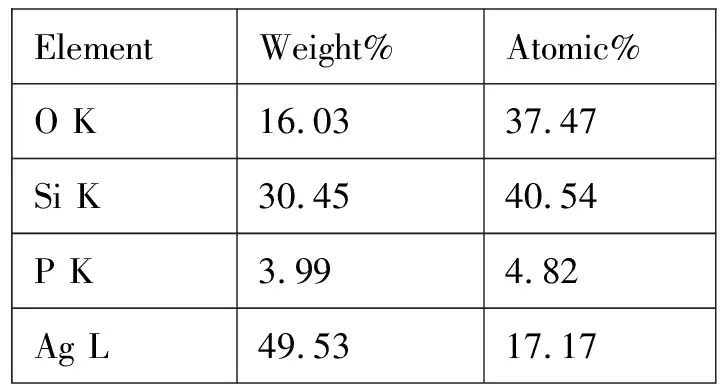
表1 EDS谱图中Ag3PO4样品详细元素比例
光催化剂的光吸收范围和带隙能的大小是决定其光催化活性的重要因素。普通结构和介孔结构的Ag3PO4光催化剂的紫外-可见漫反射吸收光谱分别如图5中曲线a和b所示。从图中可以看出,这两种结构的Ag3PO4对波长低于550 nm处的可见光均有吸收,但介孔Ag3PO4的光吸收值高于普通Ag3PO4,这尤其表现在550-700 nm之间。依据带隙能公式,将所得数据带入计算后,可绘出样品的带隙能图,具体如图5中内插图所示。由图可得,普通Ag3PO4带隙能为2.36 eV,与文献中提到相符[6],介孔Ag3PO4带隙能则为2.08 eV,小于普通粒子。实验表明,介孔Ag3PO4光催化剂的吸收边发生红移,其对可见光的响应范围和吸收值都得到了相应的增加,材料的光催化能力提升。
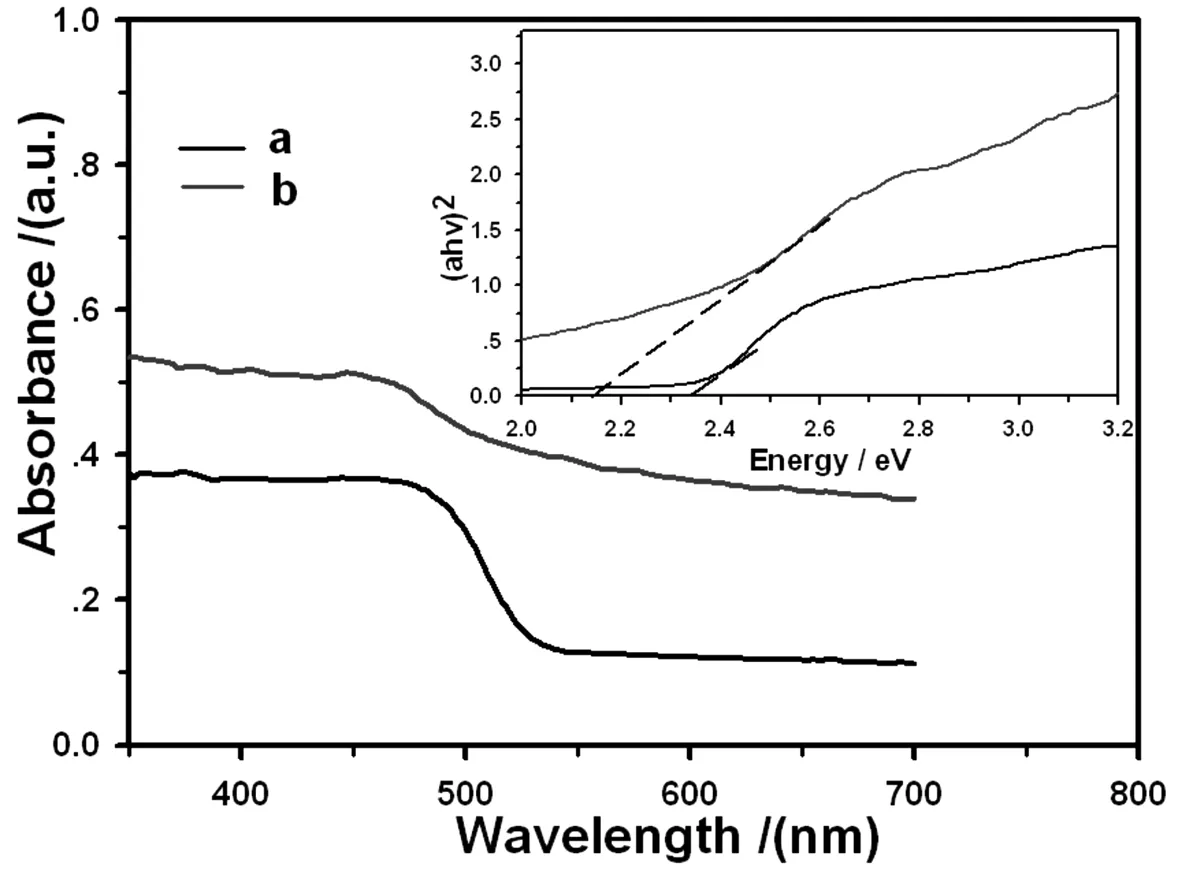
图5 Ag3PO4紫外-可见漫反射吸收光谱图: (a)普通结构;(b)介孔结构(内插图为样品的带隙能图)
3.2 催化剂的光电性质测试
光催化剂的光生电流的大小是评定材料光催化能力的重要参数,光电流值越大,说明光催化剂受光激发产生的电子和空穴复合小,能参与光催化反应的数目多,材料的光催化性能好。在0V下,以0.5 mol/L的Na2SO4溶液为电解质时,对介孔和普通Ag3PO4颗粒进行了光生电流测试,具体如图6所示。在可见光照射下,两个样品的电极均能有光生电流,但介孔Ag3PO4的光生电流密度为43μA/cm2高于普通Ag3PO4的37.5μA/cm2(分别如曲线a,b)。这可归咎于介孔Ag3PO4高的光的吸收和利用以及较低的带隙能。

图6 在可见光下催化剂的光生电流密度-时间曲线: (a)介孔Ag3PO4; (b)普通Ag3PO4
3.3 催化剂的光催化性能研究
图7为可见光下介孔Ag3PO4对40 mg/L的2,4二氯苯酚(2,4-DCP)水溶液的光催化降解的实时在线测量图。如图所示,随着降解时间的推移,2,4-DCP在283 nm处的特征峰在5 min内就已经消失,并产生特征峰为256 nm的中间产物。在光降解60 min后,目标降解物和中间产物均被降解完全,说明存在的有机官能团均已被分解。

图7 介孔Ag3PO4对40 mg/L 的2,4-DCP的实时在线紫外可见吸收光谱图
图8显示的是0.1g的介孔Ag3PO4和普通Ag3PO4在可见光照射下对100mL, 40 mg/L的2,4-DCP光降解效率-时间图。光照前,光催化剂均匀分散在2,4-二氯苯酚水溶液中,遮光暗处理30 min,介孔结构和普通结构的Ag3PO4光催化剂对溶液中2,4-DCP的吸附量分别为:17 %和10 % 。这表明介孔结构的Ag3PO4催化剂的吸附容量比普通结构的要高,有利于催化剂表面与污染物分子接触。从图中可看出,在光的照射下,两种光催化剂对2,4-DCP均表现出了较好的光催化降解能力,但介孔Ag3PO4在60 min内的光催化降解效率为90%,普通Ag3PO4才75%。这是因为介孔Ag3PO4表面多的突起能提供更多的活性位点,增加光生空穴与2,4-DCP分子之间的接触,加快光催化反应中的传质过程,进而提高其光催化降解效率。

图8 不同结构的Ag3PO4在可见光下对40 mg/L的2,4-DCP的光催化降解效率
4 结论
通过水热法和化学合成法制备了新型介孔Ag3PO4光催化剂,并对所得样品进行一系列的表征分析优化材料的合成方法。通过化学合成法制备的介孔Ag3PO4有着区别于普通Ag3PO4的表面形貌,能为光催化反应提供更多的接触位置和活性位点,提高材料的光催化活性。在可见光下,对2,4-二氯苯酚光催化降解实验中,介孔Ag3PO4表现出了明显高于普通Ag3PO4粒子的光催化降解能力。这个研究工作可为材料形貌改性和光降解有机污染物方面提供一些新的可能的思路。
[1]A. Fujishima and K. Honda. Electrochemical Photolysis of Water at a Semiconductor Electrode[J]. Nature,1972,238(7):37-38.
[2]H. Zhang, G. Chen, D. W. Bahnemann. Photoelectrocatalytic materials for environmental applications[J]. J. Mater. Chem,2009,19:5089-5121.
[3]H. Y. Luo, Structural Characterization and Photocatalytic Activity of Hydrothermally Synthesized Mesoporous TiO2for 2,4,6-Tribromophenol Degradation in Water[J]. ScienceDirect,2011,8(32):1349-1356.
[4]康华,李桂春,徐德永.Zn、Si共掺杂纳米TiO2的制备及其光催化性能[J].金属功能材料,2009,6(16):25-29.
[5]Q. Zhao, X. Li, N. Wang, et al. Facile fabrication, characterization, and enhanced photoelectrocatalytic degradation performance of highly oriented TiO2nanotube arrays[J]. Nanopart Res.2009,11:2153-2162.
[6]Z. Yi, J. Ye, N. Kikugawa, et al. An orthophosphate semiconductor with photooxidation properties under visible-light irradiation[J].Nat. Mater.2010,9:559-564.
[7]Y. Bi, H. Hu, S. Ouyang, et al. Selective growth of Ag3PO4submicro-cubes on Ag nanowires to fabricate necklace-like heterostructures for photocatalytic applications[J]. J. Mater. Chem.2012,22:14847-14850.
[8]M.Ge, N. Zhu, Y. P. hao, et al. Sunlight-Assisted Degradation of Dye Pollutants in Ag3PO4Suspension[J]. Ind. Eng. Chem. Res.2012,51:5167-5173.
[9]X. Yan, Q. Gao, J. Qin, et al. Morphology-controlled synthesis of Ag3PO4 microcubes with enhanced visible-light-driven photocatalytic activity[J]. Ceramics International,2013,39:9715-9720.
[10]Y. Bi, S. Ouyang, N. Umezawa, et al. Facet Effect of Single-Crystalline Ag3PO4 Sub-microcrystals on Photocatalytic Properties[J]. J. Am. Chem. Soc,2011,133,6490-6492.
[11]Y. Bi, H. Hu, Z. Jiao, et al. Two-dimensional dendritic Ag3PO4 nanostructures and their photocatalytic properties[J]. Physical Chemistry Chemical Physics,2012,14:14486-14488.
[12]Z. B. Jiao, Y. Zhang, H. C. Yu, et al. Concave trisoctahedral Ag3PO4 microcrystals with high-index facets and enhanced photocatalytic properties[J].Chemical Communications,2013,49:636-638.
[13]Y. Bi, S. Ouyang, N. Umezawa, et al. Facet Effect of Single-Crystalline Ag3PO4 Sub-microcrystals on Photocatalytic Properties[J]. J. Am. Chem. Soc,2011,133,6490-6492.
[14]S. J. Greqq, J. Jacobs. An examination of the adsorption theory of Brunauer, Emmett, and Teller, and Brunauer, Deming, Deming and Teller[J]. Trans. Faraday Soc.,1948,44:574-588.
[15]M. P. Tsyurupa, V. A. Dacankov, Porous structure of hypercrosslinked polystyrene: State-of-the-art mini-review[J]. React. Funct. Polymers,2006,7:768-779.
