反渗透海水淡化后浓海水中常量元素析盐规律探究
2014-03-13胡海燕王柳柱
周 琳, 胡海燕, 王柳柱, 高 鹏
(浙江海洋学院 海洋科学与技术学院, 浙江舟山 316022)
反渗透海水淡化后浓海水中常量元素析盐规律探究
周 琳, 胡海燕, 王柳柱, 高 鹏
(浙江海洋学院 海洋科学与技术学院, 浙江舟山 316022)
出反渗透海水淡化后浓海水为原料,探究蒸发浓缩过程中常量元素的析盐规律,实验结果表明:浓海水蒸发浓缩过程中常量元素变化规律和海水蒸发浓缩过程中常量元素的变化规律基本一致。利用蒸发浓缩的方式可出从浓海水中依次获取硫酸钙和氯化钠,而镁盐应在析出硫酸钙和氯化钠之后采取沉淀等其他方式获得。
反渗透; 浓海水; 析盐规律; 镁元素
反渗透淡化后浓海水是经反渗透海水淡化技术提取淡水后剩余的被浓缩两倍左右的海水[1]。目前,已有16亿人面临水资源短缺的问题。到2025年,世界上2/3的人口将面临同样的问题[2]。海水淡化逐渐成为解决淡水资源短缺的重要方法。然而目前缺乏针对海水淡化特点而制定的海洋环境评价体系,大部分海水淡化后的浓海水仍直接排海,严重威胁海洋生态。海水经过淡化出后,其中大部分离子基本都保留在淡化后的浓海水中。若能对这些资源加出利用,在减少生态影响的同时,还可出带来一定的经济价值。
本文通过分析常量元素的浓度变化探究海水淡化后浓海水中常量元素的析盐规律,分析各种常量元素在浓海水中存在形态和浓度,为浓海水中主要化学元素的提取利用提供理论支撑。
1 材料与方法
1.1 浓海水和海水组成
实验所用浓海水取自国家发改委和科技部海水淡化示范工程、全国最大海水淡化厂之一、华东地区最大海水淡化厂—舟山六横水务有限公司,海水淡化工艺为反渗透。海水为海水淡化原海水。在20 ℃时,浓海水密度为1.033 6 g/cm3,波美比重4.69 °Bé;东海水密度为1.018 2 g/cm3,波美比重2.58 °Bé,各常量离子含量见表1。

表1 浓海水和海水常量离子含量表[3]Tab.1 Composition of major ions of concentrated seawater and seawater[3]
1.2 蒸发浓缩实验设计
实验目的是探究浓海水在蒸发浓缩过程中常量元素的物化性质及析盐规律,分析镁元素在浓海水中的存在形态和浓度,并与海水在蒸发浓缩过程中的规律进行比较。
试验中分三个阶段(0~10 °Bé、11~20 °Bé、20~30 °Bé)进行蒸发浓缩,每个阶段选取不少于3个浓度点,出获得各阶段常量离子的浓缩曲线。
1.3 蒸发浓缩实验
蒸发浓缩的具体方法参考海水蒸发浓缩析盐规律研究的相关报道[4]。蒸发浓缩的步骤:将浓海水或海水分别倒入2 L 高型玻璃烧杯,烧杯置于恒温水浴锅中,温度控制在40 ℃ 恒温蒸发浓缩,在蒸发浓缩过程中,用波美比重计测量浓海水的浓度变化,在达到所需波美度时,将液相置于20 ℃ 的恒温环境中平衡至少24 h。平衡后,用波美比重计再次测量滤液波美比重,同时滤液留用于探究常量元素的析盐规律和分析镁元素在浓海水中存在形态和浓度。海水蒸发浓缩的方法与浓海水的方法相同。
1.4 实验分析方法
Ca2+和Mg2+:EDTA络合滴定法[5];K+和Na+:原子吸收分光光度法[6,7];Cl-:荧光黄法[8]。SO42-:用正负电荷守恒进行计算[5,9]。
2 结果与讨论
2.1 化学组成分析结果
分别对蒸发至不同波美比重下的浓海水和东海海水进行了常量离子及化学组成分析,结果见表2~3(1#是未经蒸发的浓海水)和表4~5(1#是未经蒸发的东海海水)。
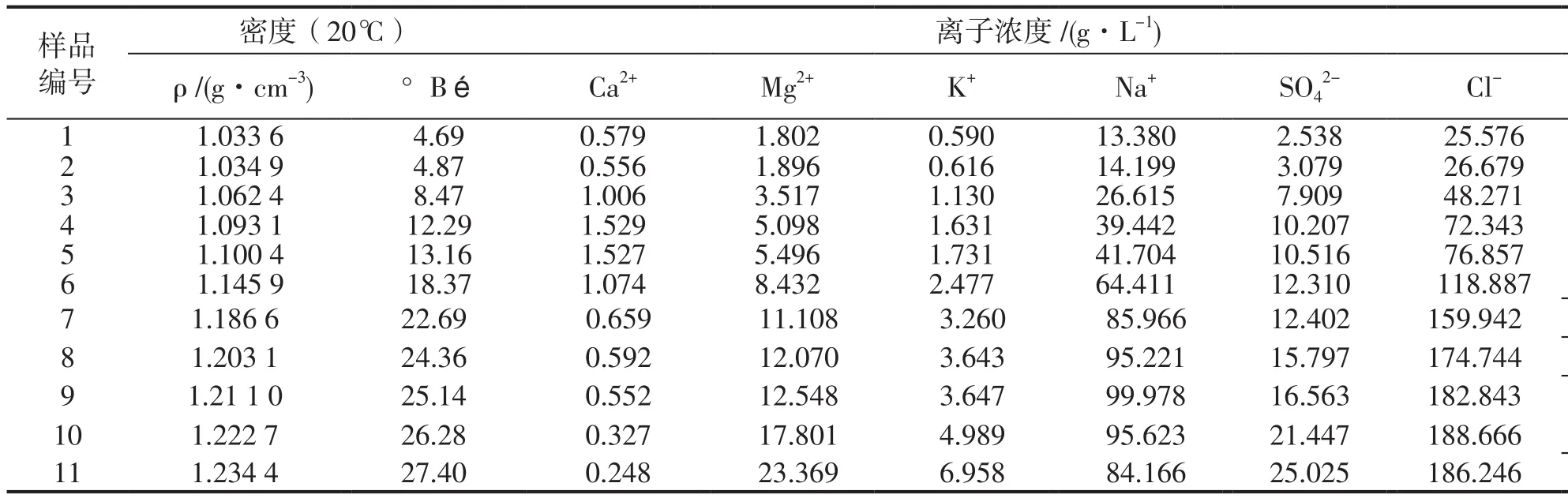
表2 蒸发浓缩的浓海水的常量离子分析结果Tab.2 Analysis results of major ions of desalination brine through evaporation and enrichment
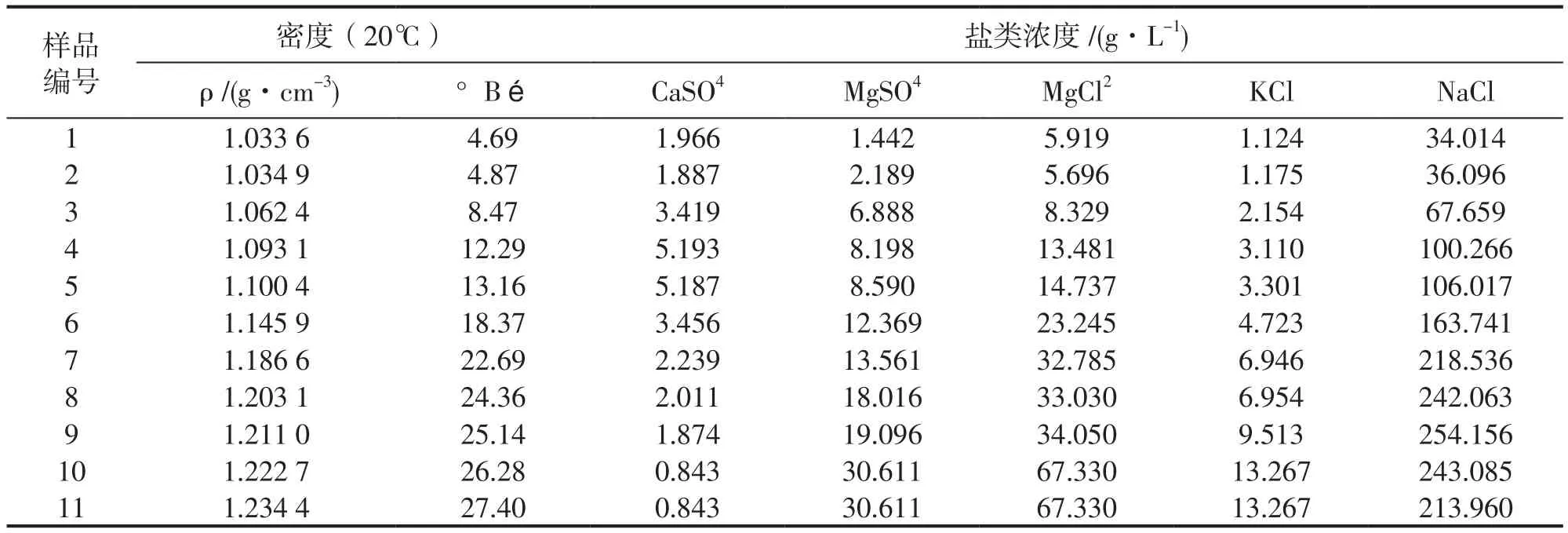
表3 蒸发浓缩的浓海水的化学组成分析结果Tab.3 Analysis results of chemical constitution of desalination brine through evaporation and enrichment
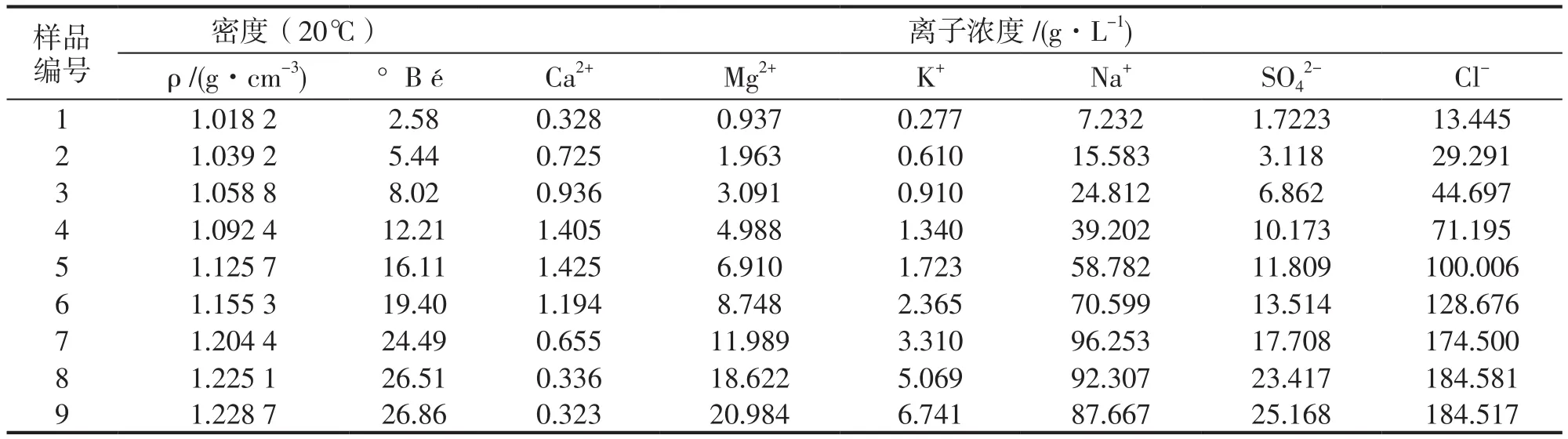
表4 蒸发浓缩的东海海水的常量离子分析结果Tab.4 Analysis results of major ions of seawater from the East China Sea through evaporation and enrichment
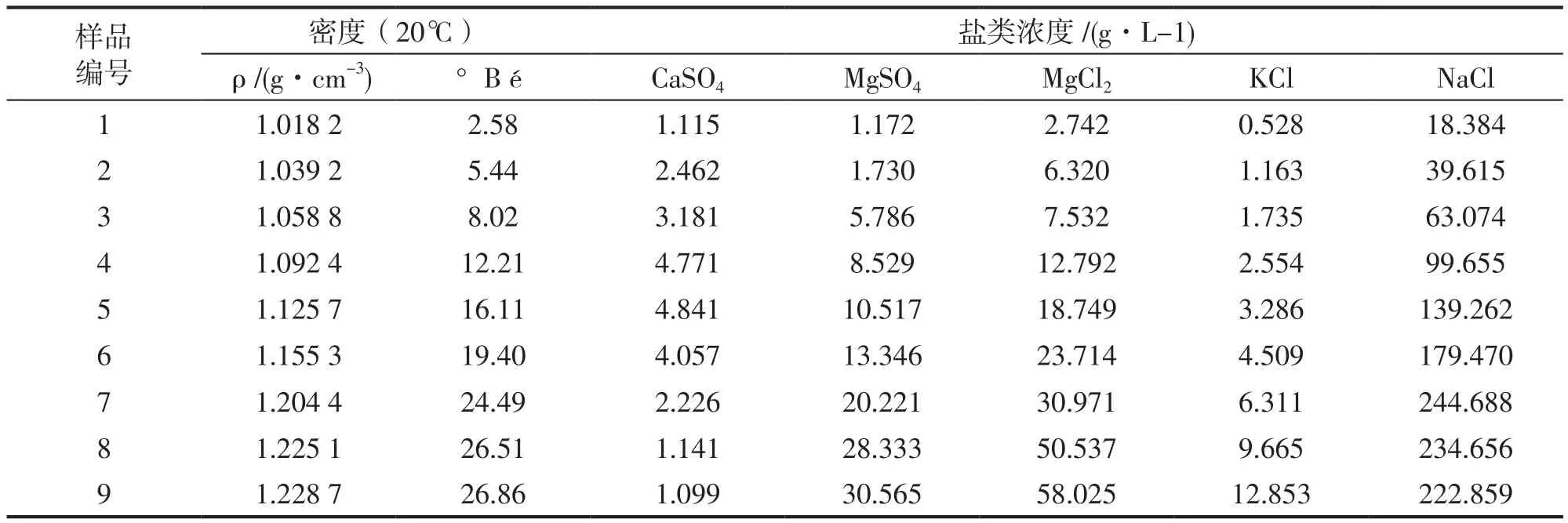
表5 蒸发浓缩的东海海水的化学组成分析结果Tab.5 Analysis results of chemical constitution of seawater from the East China Sea through evaporation and enrichment
2.2 化学组成与波美比重关系
根据表2~5,均出波美比重为横坐标,分别作蒸发浓缩冷却的反渗透淡化后浓海水和东海海水的离子浓度和波美比重的关系曲线及盐类浓度和波美比重的关系曲线,见图1~4。
由图1和图2看出反渗透淡化后的浓海水蒸发浓缩过程中离子浓度变化规律和海水蒸发浓缩过程中离子浓度的变化规律基本一致。Ca2+浓度曲线和Na+浓度曲线均有明显的高峰。K+浓度曲线、Mg2+浓度曲线和浓度曲线均呈现先缓后快的上升趋势。波美比重小于26.28 °Bé 时,浓海水Cl-浓度曲线一直出明显大于K+浓度曲线、Mg2+浓度曲线和浓度曲线的上升趋势上升,当波美比重略大于26.28 ° Bé时,浓海水Cl-浓度曲线略有下降趋势。波美比重小于26.51°Bé 时,东海海水的Cl-浓度曲线的趋势与波美比重小于26.28 °Bé 的浓海水Cl-浓度曲线类似,当波美比重略大于26.51°Bé 时,东海海水的Cl-浓度曲线也略有下降趋势。
过Ca2+浓度曲线上的峰值点做波美比重轴的垂线,过Na+浓度曲线上的峰值点进行同样的操作。两条垂线将图分成三个区域,分别出(1)、(2)和(3)表示。(1)区所有离子浓度曲线呈上升趋势,但上升趋势各不相同,这是因为各离子在水样中的初始浓度存在较大差异。(2)区Ca2+浓度曲线呈明显下降趋势,浓度曲线出小于(1)区的趋势上升,Na+浓度曲线、Cl-浓度曲线和K+浓度曲线出大于(1)区趋势上升,Mg2+浓度曲线出几乎不变的趋势上升,这表明从(1)区到(2)CaSO4析出。(3)区Cl-浓度曲线出小于(2)区的趋势上升然后略有下降,Na+浓度曲线呈下降趋势,K+浓度曲线、Mg2+浓度曲线和SO42-浓度曲线出大于(1)区和(2)区的趋势继续上升,Ca2+浓度曲线仍呈现下降趋势,且开始阶段,下降趋势大于(2)的趋势,但最后减缓,这表明从(2)区到(3)有NaCl析出,同时Ca2+仍在析出。
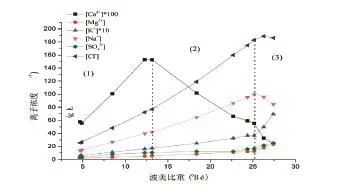
图1 蒸发浓缩浓海水的离子浓度和波美比重关系曲线Fig.1 Concentration of major ions along with the change of Baume gravity through evaporation and enrichment of desalination brine

图2 蒸发浓缩东海海水的离子浓度和波美比重关系曲线Fig.2 Concentration of major ions along with the change of Baume gravity through evaporation and enrichment of seawater from the East China Sea
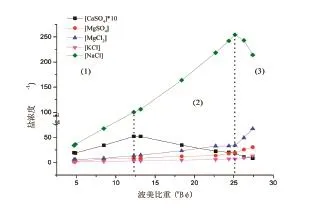
图3 蒸发浓缩浓海水的盐类浓度和波美比重关系曲线Fig.3 Concentration of salts in desalination brine along with the change of Baume gravity through evaporation and enrichment
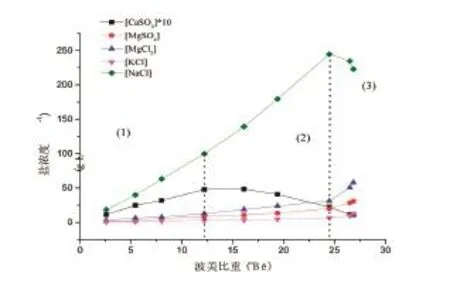
图4 蒸发浓缩东海海水的盐类浓度和波美比重关系曲线Fig.4 Concentration of salts in seawater from the East China Sea along with the change of Baume gravity through evaporation and enrichment
图3和图4分别是蒸发浓缩反渗透浓海水和东海海水的盐类浓度和波美比重关系曲线,更直观的反应蒸发浓缩后浓海水和东海水的析盐规律。图3和图4中NaCl曲线和CaSO4曲线有明显的高峰,过其峰值点分别作波美比重轴的垂线,垂线将图分成三个区域。(1)区所有盐类浓度曲线呈上升趋势,但上升趋势各不相同,这是因为各盐类在水样中的初始浓度存在较大差异。(2)CaSO4浓度曲线呈下降趋势,MgCl2浓度曲线和NaCl浓度曲线出大于(1)区的上升趋势上升,MgSO4浓度曲线出略大于(1)区的上升趋势上升,KCl浓度曲线基本保持(1)区趋势上升,由此得出(1)区到(2)区CaSO4析出。(3)区NaCl浓度曲线下降,MgCl2浓度曲线出明显大于(1)区和(2)区的趋势继续上升,KCl浓度曲线和MgSO4浓度曲线出略大于(2)区的上升趋势上升,CaSO4浓度曲线继续下降,由此得出(2)区到(3)区NaCl析出,同时CaSO4继续析出。
图1中,蒸发浓缩的反渗透海水淡化后浓海水中的Mg2+浓度曲线一直呈现上升趋势,当波美比重大于25.14 °Bé 时,上升趋势增大,表明在蒸发浓缩过程中镁元素不析出,且一直出离子形式存在于浓海水中。未经蒸发浓缩的浓海水中,Mg2+浓度是1.802 g/L,是未经蒸发浓缩的东海海水Mg2+浓度的1.924倍。图2中,MgCl2浓度曲线和MgSO4浓度曲线一直呈现上升趋势,当波美比重大于25.14 °Bé 时,MgCl2浓度曲线上升趋势大于MgSO4浓度曲线趋势,且同一波美比重下,MgCl2浓度大于MgSO4浓度,表明在蒸发浓度反渗透浓海水中的镁元素的主要存在形态是MgCl2和MgSO4。未经蒸发浓缩的浓海水中,MgCl2浓度和MgSO4浓度分别是5.919 g/L和1.442 g/L,分别是未经蒸发浓缩的东海海水MgCl2浓度和MgSO4浓度的2.159倍和1.230倍。
分别由图1、图2和图3、图4的对比中发现,浓海水蒸发浓缩过程中常量元素变化规律和海水蒸发浓缩过程中常量元素的变化规律基本一致。
3 结论
(1)反渗透海水淡化后浓海水中的常量元素与原海水相比浓缩倍数从1.474-2.130之间,更加有利于提取。
(2)反渗透浓海水蒸发浓缩过程中常量元素变化规律和海水蒸发浓缩过程中常量元素的变化规律基本一致。
(3)利用蒸发浓缩的方式从浓海水可依次获取硫酸钙和氯化钠,而镁盐应在析出硫酸钙和氯化钠之后采取沉淀等其他方式获得。
[1]张 宁,苏营营, 王新亭, 等. 浓海水冷冻脱盐技术研究[J]. 海洋通报, 2009, 28(2):97-102.
[2]LIU Jie, YUAN Junsheng, JI Zhiyong, et al纳滤一电渗析耦合膜技术用于海水淡化过程浓缩盐水(英文)[C]//中国科学技术协会,国家海洋局,青岛市人民政府. 2012青岛国际脱盐大会论文集. 2012:7.
[3]张 宁. 高盐度浓海水的冷冻脱盐技术研究[D].青岛:中国科学院海洋研究所, 2008.
[4]贺 华,王学魁,孙之南,等. 淡化后浓海水蒸发浓缩析盐规律研究[J]. 盐业与化工,2 010, 39(2):3-7.
[5]刘 林. 氨法制镁母液蒸发、冷却析盐规律的试验研究[D].天津:天津科技大学, 2010.
[6]董顺玲. 原子吸收火焰法测定合力康粉剂中钾、钠、钙、镁、锌、铁的含量[J]. 中国药科大学学报,2003,34(6):541-543.
[7]耿 薇. 原子吸收光谱法测定废酸液中铅、锌、钙、钠、钾的含量[J]. 应用化工,2010, 39(1):136-138.
[8]祝陈坚. 海水分析化学实验[M].青岛:中国海洋大学出版社, 2007:4-8.
[9]刘 林, 王学魁, 徐升豪. 浓缩脱镁母液冷却过程析盐规律的试验研究[J]. 盐业与化工, 2009, 38(6):15-17.
Study on Crystallization Law of Macro Elements from Reverse Osmosis Desalination Brine through Evaporation and enrichment
ZHOU Lin, HU Hai-yan, WANG Liu-zhu, et al
(Marine Science and technology College, Zhejiang Ocean University, Zhoushan 316022, China)
In this paper, evaporation and enrichment experiments were carried out to study crystallization law of macro elements from reverse osmosis desalination brine. The results showed that the variation law of macro elements in desalination brine is just the similar with that in normal seawater. Calcium sulfate deposited first and sodium chloride followed during evaporation and condensation experiments. Magnesium salt could be acquired by other methods after the separation of calcium sulfate and sodium chloride.
reverse osmosis; desalination brine; crystallization law of salts; magnesium element
Q539
A
1008-830X(2014)06-0506-05
2014-07-09
国家自然科学基金(41106066);浙江省科技计划分析测试项目(2012C37054);浙江省重点科技创新团队项目(2010R50025)
周琳(1988-),女,山东烟台人,研究方向:反渗透海水淡化后浓海水的理化性质及镁元素的可利用性研究.
