工业废水中微量碘离子的分析方法研究
2014-03-10郑丽娟王高升宋志杨许丹红金晓云
郑丽娟,王高升,宋志杨,许丹红,金晓云,任 斌
(浙江省化工研究院有限公司,浙江 杭州310023 )
碘是人体不可缺少的生命元素之一,也是化工行业制造各种无机及有机碘化物以及合成中常用的重要原料,因此工业废水中常含有一定的碘离子,既是碘资源的浪费,也会影响水体质量,进而影响生命健康。所以,对废水中碘离子进行分析检测,具有十分重要的研究意义,也为工业废水碘的回收打好基础[1]。
1 碘离子的测定方法
1.1 碘离子选择电极法
离子选择性电极是近年来获得广泛应用的电化学传感器,离子选择性电极是基于各种膜对离子有选择性的电位响应来测定离子含量的。Ⅰ-选择电极主要是混晶膜(AgI-Ag2S),加入Ag2S 的作用是增加膜的机械强度、降低内阻和减小光敏作用。离子选择电极都遵循Nerst 定律Φ=φ+RTInaA/ZAF。离子选择电极法操作简单快速、灵敏度高、具有良好的重现性,利于自动化批量连续测定[2]。
1.2 火焰原子吸收法
基于被测元素基态原子在蒸汽状态对其原子共振辐射吸收进行元素定量分析的方法。原子吸收光谱法有许多优点:检出限低,准确度高,选择性好,大多数情况下共存元素对被测元素不产生干扰;分析速度快;应用范围广,价格较低廉。刘英杰等通过I-和Hg(NO3)2生成较难热解离的HgI2的方法,石墨炉原子吸收法间接测定水中I-,检出限达到了1 μg/L[3]。
1.3 气相色谱法
气相色谱法测定I-是通过衍生化反应来进行的。一种是在酸性条件下,用氧化剂把I-氧化为单质I2,然后用酮和I2反应生成碘代酮,用有机溶剂萃取,采用一定的色谱条件测定,根据积分面积进行定量测定。庞敏好等用该原理衍生气相色谱法测定奶粉中的微量碘,平均回收率在93.3%~106.0%之间,变异系数小于10.7%,最小检出浓度为0.0162 mg/kg[4-5]。另一种是采用碘与硫酸二甲酷能发生甲基化反应生成碘甲烷,采用HS-GCECD 测定。符展明等则是采用该方法测定食盐、植物油、啤酒中的碘[6]。
1.4 分光光度法(碘一淀粉显色光度法)
该方法是基于单质碘与淀粉作用生成蓝色吸附络合物,该蓝色络合物在580 nm 处有吸收,根据吸光度与碘浓度之间的关系进行定量测定,各种研究方法的区别主要在于所采用的氧化剂的不同,碘-淀粉显色光度法测定碘选择性好,灵敏度较高,操作简单快速,但显色反应不够稳定,淀粉要新鲜配制的,采用甘油一淀粉溶液则能显著改变淀粉溶液的稳定性[7]。
1.5 容量法(次氯酸盐法)
在酸性溶液中,加入定量的氧化剂把I-氧化为IO3ˉ,再用适当的还原剂除去过量的氧化剂,然后加入KI 结晶和IO3ˉ反应生成I2,用标准Na2S2O3溶液滴定至淡黄色,加入淀粉指示剂,接着用Na2S2O3溶液滴定溶液至蓝色消失为止,通过消耗的Na2S2O3溶液的体积计算碘含量[8]。
针对工业废水中碘离子的检测,采用了碘离子选择性电极测定碘离子含量,为工业生产中工业废水碘的回收提供参考。
2 实验部分
2.1 主要试剂
标准碘溶液:准确称取于105 ℃干燥2 h 的碘化钾1.3081 g,称准至0.0001 g,溶于水稀释至1000 mL。此溶液每毫升含碘1 mg。工作液稀释20 倍。每毫升含碘50 μg。
溴甲酚绿—甲基红混合指示剂:0.1%溴酚绿乙醇液与0.2%甲基红乙醇液按3:1 比例混合。
2.2 主要仪器
PHS-3C 精密pH 计(上海雷磁仪器厂);
PI-1 型碘离子选择电极(上海雷磁仪器厂);
217 型饱和甘汞参比电极(用饱和硝酸钾溶液作为盐桥,上海雷磁仪器厂)。
2.3 实验方法
2.3.1 标准曲线
用微量移液管分别吸取含碘50 μg/mL 标准溶液:0.00、1.00、2.00、4.00、6.00、8.00、10.00 mL 于50 mL 容量瓶中,滴加2 滴溴甲酚绿—甲基红混合指示剂,用10%氢氧化钠和5%硫酸调至溶液刚变绿,水稀释至刻度摇匀。于50 mL 烧杯中,用PI-1 型碘离子选择电极和217 型饱和甘汞参比电极测定其电位E。绘制logC—E 曲线。
2.3.2 测定方法
准确吸取2.00 mL 待测废水于50 mL 容量瓶中,滴加2 滴溴甲酚绿—甲基红混合指示剂,用10%氢氧化钠和5%硫酸调至溶液刚变绿,水稀释至刻度摇匀。于50 mL 烧杯中,用PI-1 型碘离子选择电极和217 型饱和甘汞参比电极测定其电位E。若碘含量超出线性范围,则稀释至碘的线性范围。
3 结果和讨论
3.1 线性范围的测定
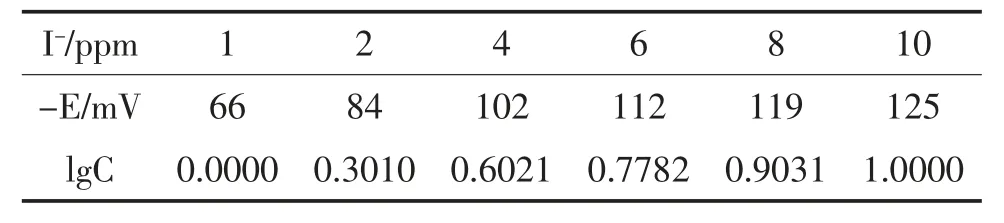
表1 I-浓度与E 的关系
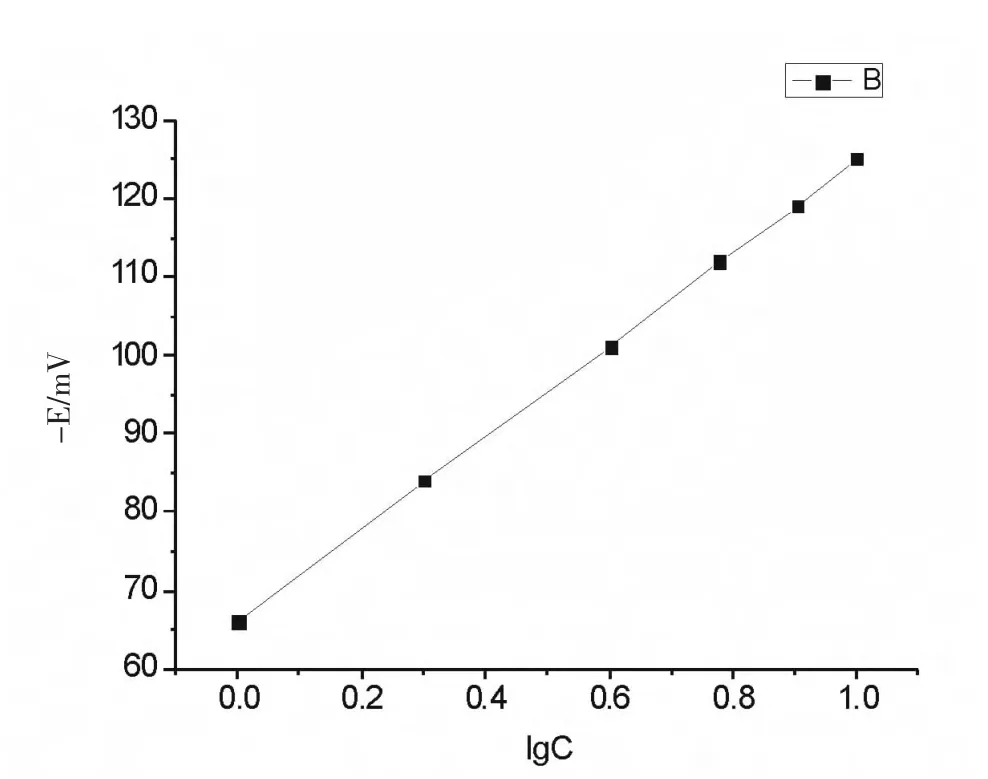
图1 I-浓度与E 的关系图
由表1 及图1 可以看出,碘离子浓度在2~10 ppm 范围时,显直线关系,符合Nerst 定律。
3.2 干扰离子对碘离子选择电极法测定的影响
主要对废水如生产七氟碘丙烷的副产物KI回收I2所产生的废水进行试验,在碘回收的废水中含有大量的KCl、K2SO4、KNO3。下面就这些物质对测定碘离子的影响分别模拟测定。
3.2.1 KCl 对测定碘离子的影响
吸取100 ppm 碘标准溶液2.00 mL 于50 mL容量瓶中,加5 mL 1 mol/L KNO3溶液,分别加入25% KCl 溶液0、2、10、20、30、40 mL,水稀释到刻度。配成含KCl 为0%,1%,5%,10%,15%,20%的4 ppm 碘溶液,分别测定其电位,看氯化钾浓度对测定的影响。结果如表2,从电位E1可以看出,当KCl 为5%时,电位开始增大,即是用标准加入法测定碘可以减少干扰,但当氯化钾的浓度大于5%时,还是产生严重干扰。
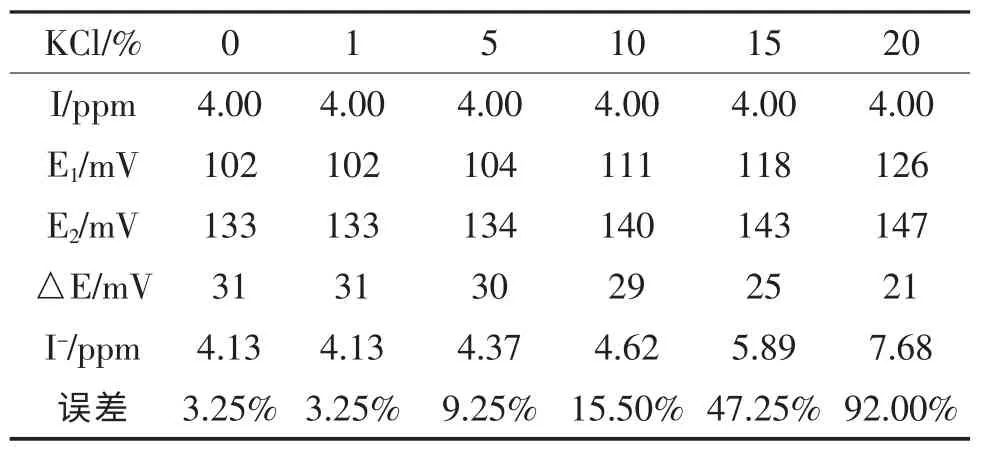
表2 氯化钾浓度对测定的影响
3.2.2 K2SO4对测定碘离子的影响
根据废水中硫酸钾的浓度约3.5%,所以分别配成含K2SO4为0%,3.4%和4.0%的碘测定溶液,其中碘离子为4.00 ppm,然后分别测定其电位,结果如表3。
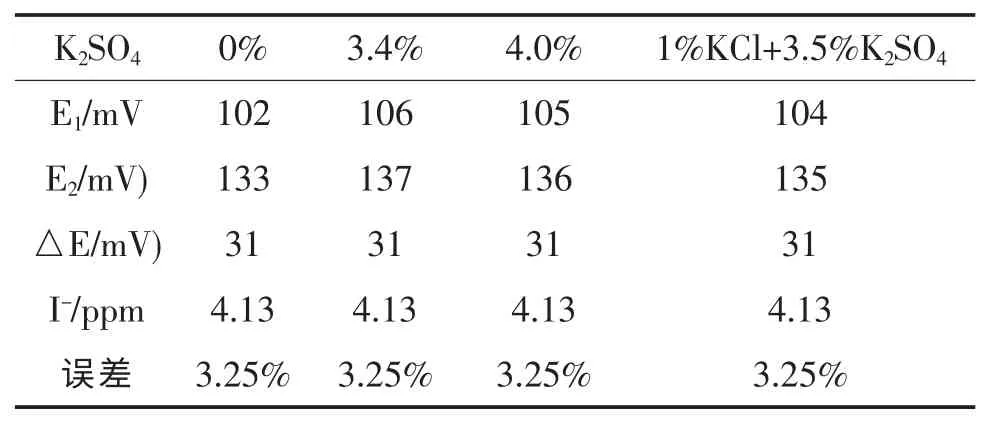
表3 K2SO4对测定碘离子的影响
从电位E1结果可知硫酸钾对测定干扰比较大,但采用标准加入法就可以消除影响。1%KCl加3.5%K2SO4对碘测定没有影响。
4 结语
碘是稀缺资源,因此针对工业废水中碘的回收具有十分重要的意义。采用碘离子选择性电极测定碘离子含量,结果准确度可信、简单易行,方便碘回收时监控,是一种方便有效的碘离子检测方法。
[1]金文斌,黄鹃.褪色光度法测定微量碘的研究[J].干旱环境检测,2002,16(3):129-130.
[2]刘伟利,吴庆生,丁亚平.壳聚糖修饰铂电极半微分伏安法测定微量碘[J].理化检验一化学分册,2004,40(3):145-147.
[3]刘英杰,周庆鹃.石墨炉原子吸收法间接测定水中碘[J].理化检验一化学分册,1998,34(6):273-275.
[4]焦海一,戴一鸣.气相色谱法(混酸消解尿样)测定尿碘[J].色谱,1991,9(6):387-388.
[5]陈书生,王建新.无机碘的气相色谱分析[J].色谱,1986,2(2):66-67.
[6]符展明,任建华.顶空气相色谱法测定血清中微量碘[J].现代仪器,1997,1:39-41.
[7]张银根.过氧化氢分光光度法测定碘盐中碘化钾的含量[J].中国卫生检验杂志,1995,5(1):53-54.
[8]李玉莲,史永红.碘量法连续测定盐卤水中的嗅碘[J].内蒙古科技与经济,2005,9:130-131.
