乌司他丁对黑火药烟雾所致吸入性肺损伤大鼠的保护作用以及对IL-1β、TNF-α基因表达的抑制作用
2014-03-02刘一凡王正冠唐红卫吴小利谢尹晶张洪瑞李登清王成彬
刘一凡,王正冠,唐红卫,吴小利,谢尹晶,张洪瑞,李登清,王成彬
吸入性肺损伤是指因吸入热力或化学性刺激物而引起的呼吸道以至肺实质的损害,往往也是导致严重全身性病变的重要原因。黑火药被广泛应用于军事和民用方面,如战争、演习或烟花爆竹的燃放等,在爆炸、燃烧过程中所释放的有毒气体及粉尘颗粒会引发急性吸入性肺损伤,造成肺组织充血、水肿及炎性细胞浸润等[1-2]。体外研究表明,黑火药烟雾会导致支气管上皮细胞炎性细胞因子IL-6、IL-8表达增加,活性氧相对含量增高[3],而其体内损伤机制尚未明确。乌司他丁(ulinastatin,UTI)作为一种蛋白酶抑制剂,目前在临床上主要用于胰腺炎的治疗。研究发现,除对多种蛋白酶、脂水解酶等有抑制作用外,UTI还具有清除氧自由基、抑制炎症介质的过度释放等功能[4-6]。动物实验表明UTI对脂多糖、烧伤及缺血再灌注导致的肺损伤具有保护作用[7-9],但是否能减轻烟雾吸入所致的肺损伤尚未见报道。本研究通过建立黑火药烟雾所致肺损伤大鼠模型,探讨UTI对烟雾吸入性肺损伤的保护作用及其可能机制。
1 材料与方法
1.1 实验动物 健康成年雄性Wistar大鼠30只,体重210~230g,由解放军总医院实验动物中心提供,合格证号SCXK(京)2012-0001。大鼠于清洁房中饲养,温度21~24℃,湿度50%~60%,昼夜12h节律,自由进食、饮水。
1.2 主要药物及试剂 乌司他丁(规格:10万单位;批号:031301103;广东天普生化医药公司);硝酸钾、碳粉、硫黄粉(纯度99.9%,200目,北京西四化工原料公司);丙二醛(malondialdehyde,MDA)及髓过氧化物酶(myeloperoxidase,MPO)试剂盒(南京建成生物工程研究所);TransScript All-in-One First-Strand cDNA Synthesis SuperMix试剂盒(北京TransGen公司)。实验所用引物由上海生物工程技术服务有限公司合成。
1.3 实验分组及动物模型制备 30只Wistar大鼠随机分为正常对照组(C组)、吸入性肺损伤组(I组)、乌司他丁高剂量组(UH组)、乌司他丁中剂量组(UM组)、乌司他丁低剂量组(UL组),每组6只。C组大鼠暴露于动物烟熏箱的空气中8min,I组、UH组、UM组、UL组置于动物烟熏箱,在10g火药产生的烟雾中暴露8min,制作黑火药烟雾吸入性肺损伤模型[1]。UH组、UM组、UL组分别按100000、50000、20000U/(kg.d)计算出UTI用量,稀释至3ml,于烟雾吸入后10min经腹腔注射,C组、I组注入3ml 0.9% NaCl注射液。所有大鼠均于烟雾暴露后40h经腹腔注射4%水合氯醛(1ml/kg)麻醉,暴露分离腹主动脉,取动脉血1ml,处死并取材。
1.4 观察指标
1.4.1 动脉血气分析 麻醉大鼠并取腹主动脉血1ml,于30min内采用罗氏Cobasb血气分析仪进行动脉血气分析。
1.4.2 肺湿/干重比(W/D) 处死大鼠后取右肺前叶及中叶,拭干表面血液后称湿重并记录,然后放入60℃烘箱烘烤48h至恒重并记录干重,计算W/D值。
1.4.3 支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)细胞计数及蛋白含量测定 处死大鼠后,打开胸腔,分离主支气管,夹闭右主支气管,在主支气管切开处置入自制灌洗针并结扎固定,用4℃生理盐水2.5ml行左肺灌洗,重复3次,记录回收量。BALF经1500r/min离心10min,收集上清液,BCA法测定总蛋白含量,取沉淀重悬于1ml生理盐水并进行细胞计数。
1.4.4 血清、肺组织MPO活性及肺组织MDA含量测定 取肺组织100mg,置于液氮中研磨后以1:9比例加入生理盐水,制成10%的肺组织匀浆,采用MPO及MDA试剂盒测定肺组织MPO活性及MDA含量,具体操作严格按照试剂盒说明书进行。大鼠麻醉后取腹主动脉血5ml,3000r/min离心5min,测血清MPO活性,具体操作按照MPO试剂盒说明书进行。
1.4.5肺组织Toll样受体4(toll-like receptor 4,TLR-4)、白细胞介素-1β(interleukin-1β,IL-1β)、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)mRNA表达水平检测 采用Trizol试剂盒提取肺组织总RNA。取2μl RNA样本,加入不含RNA酶的双蒸水198μl,置于核酸分析仪中测定纯度和浓度,取A260/A280值在1.8~2.0的RNA,采用TransScript All-in-One First-Strand cDNA Synthesis SuperMix试剂盒进行反转录,合成cDNA,实验所用引物序列见表1。PCR采用20μl反应体系,包括上游引物(10μmol/L)0.5μl,下游引物(10μmol/L)0.5μl,2×TransStart Green qPCRSuperMix 10μl,模板2μl,双蒸水7μl。扩增条件:94℃ 180s;94℃ 30s,58℃ 30s,72℃60s,共45个循环;95℃ 30s,58℃ 30s,72℃ 30s。扩增完成后从50℃升温绘制熔解曲线验证扩增产物的特异性。
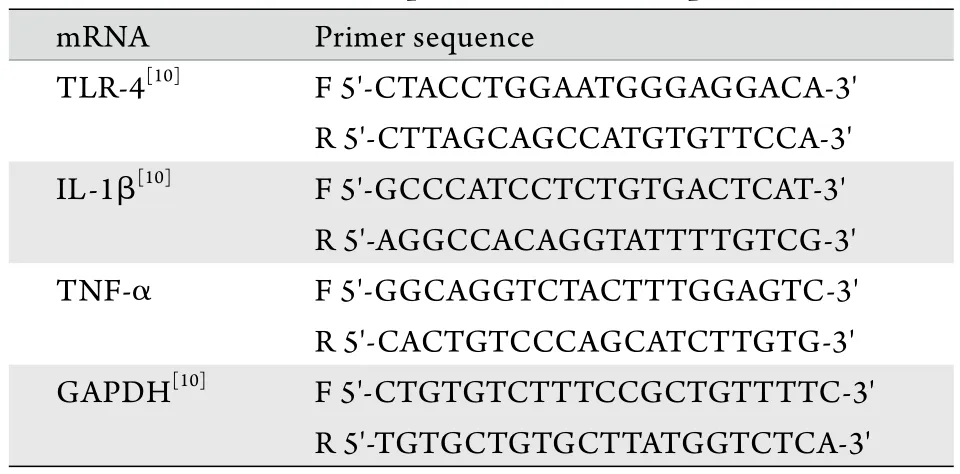
表1 PCR引物序列Tab. 1Primer sequence for PCR amplification
1.4.6 肺组织病理学检查 观察肺组织大体病理改变,取右肺后叶浸入4%中性缓冲甲醛溶液中固定24h,石蜡包埋,4μm连续切片,常规HE染色后光镜下观察。
1.5 统计学处理 采用SPSS 17.0软件进行统计分析。符合正态分布及方差齐性的计量资料以±sx表示,多组间比较采用单因素方差分析(One-way ANOVA),进一步两两比较采用LSD-t检验。P<0.05为差异有统计学意义。
2 结 果
2.1 动脉血气分析结果 与C组比较,在暴露于黑火药烟雾40h后,I组PaO2明显降低,PaCO2明显升高(P<0.05)。给予不同剂量UTI处理后,UH、UM、UL组PaO2均高于I组(P<0.05),UM与UL组PaCO2水平低于I组(P<0.05),3组PaO2、PaCO2与C组比较差异均无统计学意义(P>0.05,表2)。
2.2 肺W/D及BALF白细胞计数、蛋白含量测定结果 I组肺W/D显著高于C组和使用UTI治疗的三组(P<0.05),而C组与使用UTI治疗的3组相比差异无统计学意义(P>0.05)。I组大鼠BALF白细胞计数显著高于其余4组(P<0.05),BALF蛋白含量明显高于C组及UM组、UL组(P<0.05),与UH组比较差异无统计学意义(P>0.05,表2)。
2.3 MPO活性及MDA含量测定结果 UH组血清、肺组织MPO活性及肺组织MDA含量均低于I组(P<0.05),且与C组比较差异无统计学意义(P>0.05)。UM、UL组血清MPO活性显著低于I组(P<0.05,表3)。
表2 烟雾吸入后40h各组PaCO2、PaO2、W/D及BALF中白细胞计数和蛋白含量比较(±sx,n=6)Tab. 2Arterial blood gas analysis, WBC count and protein contents in BALF of 5groups at 40h post smog inhalation (±sx, n=6)
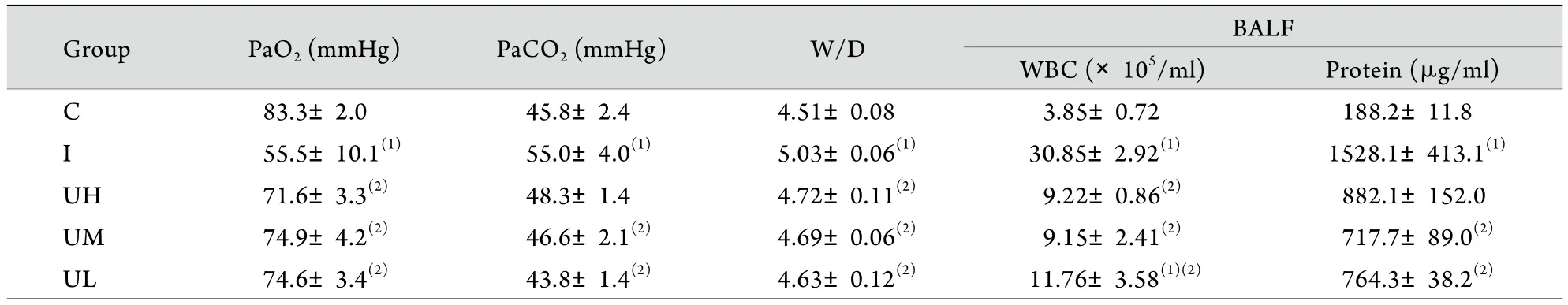
表2 烟雾吸入后40h各组PaCO2、PaO2、W/D及BALF中白细胞计数和蛋白含量比较(±sx,n=6)Tab. 2Arterial blood gas analysis, WBC count and protein contents in BALF of 5groups at 40h post smog inhalation (±sx, n=6)
(1)P<0.05compared with group C; (2)P<0.05compared with group I
Group PaO2 (mmHg) PaCO2 (mmHg) W/D BALF WBC (×105/ml) Protein (μg/ml)C 83.3±2.0 45.8±2.4 4.51±0.08 3.85±0.72 188.2±11.8I 55.5±10.1(1) 55.0±4.0(1) 5.03±0.06(1) 30.85±2.92(1) 1528.1±413.1(1)UH 71.6±3.3(2) 48.3±1.4 4.72±0.11(2) 9.22±0.86(2) 882.1±152.0UM 74.9±4.2(2) 46.6±2.1(2) 4.69±0.06(2) 9.15±2.41(2) 717.7±89.0(2)UL 74.6±3.4(2) 43.8±1.4(2) 4.63±0.12(2) 11.76±3.58(1)(2) 764.3±38.2(2)
2.4 肺组织TLR-4、IL-1β、TNF-α mRNA表达水平
各组之间TLR-4mRNA表达差异均无统计学意义(P>0.05,图1)。UH组IL-1β、TNF-α mRNA表达均低于I组(P<0.05),且与C组比较差异无统计学意义(P>0.05);UM、UL组IL-1βmRNA表达显著低于I组(P<0.05),而TNF-α mRNA表达与I组比较差异无统计学意义(P>0.05,图1)。
2.5 病理学检查结果 大体观察见C组大鼠肺组织呈肉粉色,质地柔软、弹性好。I组大鼠肺表面可见片状出血坏死灶,弹性较差。UH、UM、UL组肺表面观无明显差异,整体呈肉红色,弹性尚可,UL组偶见点状出血梗死灶。光镜下可见C组大鼠肺泡结构完整、清晰,肺泡腔干净,肺泡间隔均匀一致,间质无炎细胞浸润;烟雾吸入后40h的I组大鼠肺泡腔增大,肺泡间隔增厚,腔内可见渗出,肺泡间质可见炎细胞浸润;UH组、UM组肺泡间质炎性浸润均较I组明显减轻,肺泡腔内未见渗出,UL组肺泡腔内渗出情况及炎细胞浸润现象也较I组减轻(图2)。
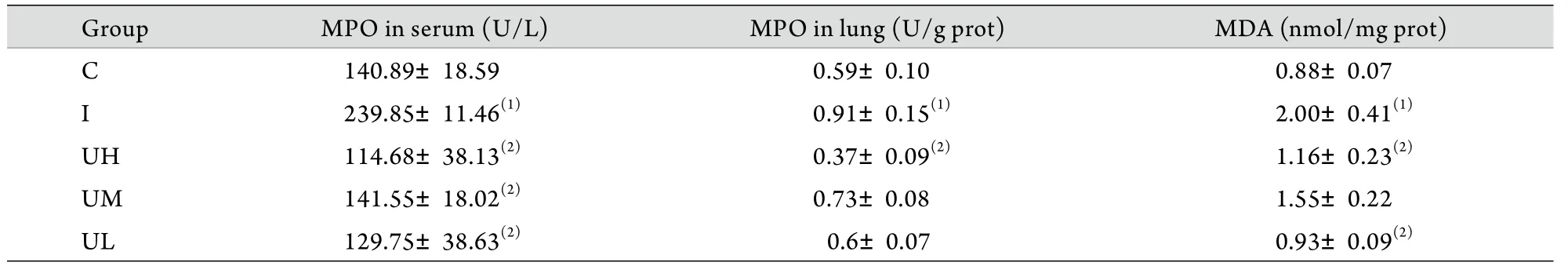
表3 烟雾吸入后40h各组血清、肺组织MPO活性及肺组织MDA含量比较(x±sx,n=6)Tab. 3MPO activity in serum and lung tissue and MDA concentration in lung tissue at 40h post smog inhalation (x±sx, n=6)
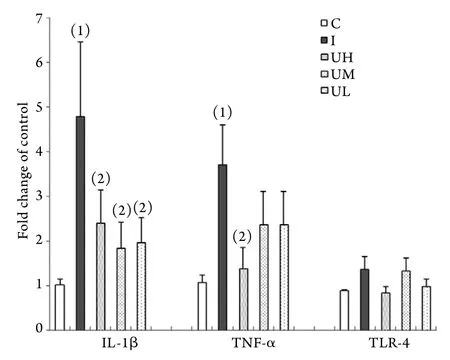
图1 烟雾吸入后40h各组TLR-4、IL-1β、TNF-α mRNA表达水平比较(n=6)Fig. 1Expression levels of TLR-4, IL-1β and TNF-α mRNA in 5groups at 40h post smog inhalation (n=6)
3 讨 论
研究认为,吸入性肺损伤发生的主要原因为当机体吸入热力物质、有毒气体或刺激性粉尘后,导致单核巨噬细胞及中性粒细胞等的活化和积聚,释放MPO、氧自由基及多种炎性细胞因子等,同时,因中性粒细胞与肺组织内的血管内皮细胞发生黏附而阻塞肺组织内微血管,加重局部组织缺血缺氧,使血管内皮通透性增加,进一步加速肺组织水肿的发生,最终加重肺部炎症反应[11-12]。
目前,以地塞米松为代表的糖皮质激素类药物在抗炎治疗中应用较为广泛,该类药物具有较强的免疫抑制作用,能广泛调节机体内多种炎性介质的表达,但因其会产生药物依赖、激素抵抗等一系列不良反应,故一直不能作为临床治疗的最佳选择。UTI是一种由肝脏分泌的具有广谱蛋白酶抑制作用的糖蛋白,属于内源性抑炎介质。在由细菌内毒素所致的急性肺损伤大鼠模型中,UTI能有效抑制TNF-α水平和MPO活性的升高,减轻肺泡间隔炎性细胞的浸润、水肿、出血等,也可通过降低IL-18等炎性因子及NF-κB的表达,减轻肺部炎性反应[13-14]。
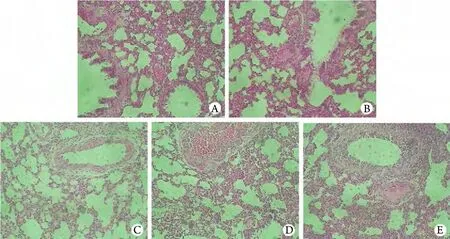
图2 肺组织病理学观察(HE ×100)Fig. 2Histopathological observation of the lung tissues (HE ×100)
本研究使用自制的发烟装置建立了黑火药烟雾所致大鼠吸入性肺损伤模型,使用高、中、低3个剂量的UTI进行干预。血气分析结果表明UTI可显著改善吸入性肺损伤大鼠的PaO2,使之恢复正常水平,同时有效降低了UM组、UL组的PaCO2水平(P<0.05)。UH组PaCO2水平略低于I组,但差异无统计学意义(P>0.05),考虑与大鼠数量有限或血气测定时点差异有关。肺组织W/D以及BALF中蛋白含量是衡量肺内微血管通透性的主要指标,本研究结果显示,与I组相比,UTI能有效降低W/D值,同时减少蛋白渗出(P<0.05),与Qiu等[11]的研究结果一致。UH组BALF中蛋白含量虽与I组相比差异无统计学意义,但数值仍低于后者,考虑可能是在收集BALF时因操作不当使标本混入了溶血后的血液,从而导致所测定的蛋白水平假性增高。
MPO活性是组织中性粒细胞浸润的主要标志。本研究结果显示高剂量UTI能显著降低血清及肺组织MPO的活性(P<0.05),且与BALF中白细胞计数的变化趋势一致,提示UTI能有效抑制中性粒细胞的渗出以及MPO的释放,减轻肺组织损伤,从而起到保护作用。与UH组相比,UM、UL组肺组织MPO活性下降不明显(P>0.05),考虑与UTI剂量有关。MDA是脂质过氧化反应的最终产物,其含量可反映组织中自由基的多少及脂质过氧化程度。I组MDA含量增加表明黑火药烟雾吸入可破坏肺组织的细胞膜结构,而UH组肺组织MDA含量与I组相比显著下降(P<0.05),表明高剂量UTI具有抗氧化作用。
TLR-4是目前研究较为广泛的病原微生物模式识别受体,本研究结果显示TLR-4mRNA表达在各组之间差异无统计学意义(P>0.05),提示在黑火药烟雾吸入引起的无菌性炎症中,TLR-4相关炎性通路可能未被激活。TNF-α是感染、烧伤等炎症反应中最主要的促炎性细胞因子,主要由巨噬细胞产生,可通过诱导IL-1β等其他细胞因子和炎症介质进一步启动炎症反应的发生。本研究结果显示,高剂量UTI可显著抑制TNF-α及IL-1β mRNA的表达(P<0.05),而中、低剂量UTI则仅可减少IL-1β mRNA的表达(P<0.05),提示高剂量UTL对烟雾吸入引起的肺损伤可发挥有效的保护作用。上述结果与病理观察变化趋势一致。
综述所述,本研究结果显示UTI可通过抗炎、抗氧化对黑火药烟雾所致大鼠肺损伤发挥保护作用,且高剂量UTI可通过有效抑制IL-1β、TNF-α mRNA的表达起到更为显著的保护效果。
[1]Liu YF, Tang HW, Wu XL, et al. Establishment and evaluation of a rat model of inhalation lung injury caused by black gunpowder smog[J]. Med J Chin PLA, 2013, 38(8): 60-65. [刘一凡, 唐红卫, 吴小利, 等. 黑火药烟雾致吸入性肺损伤大鼠模型的建立与评价[J]. 解放军医学杂志, 2013, 38(8): 60-65.]
[2]Zhou Y, Lan XM, Wang CB. Study on the secretion of IL-8and IL-6by bronchial epithelial cells (BEAS-2B) injured by black powder smoke and the curative effect of puerarin[J]. Med J Chin PLA, 2012, 37(3): 260-262.[周莹, 兰晓梅, 王成彬. 葛根素对火药烟雾致支气管上皮细胞损伤的防护效应[J]. 解放军医学杂志, 2012, 37(3): 260-262.]
[3]Zhou Y, Wang CB, Lan XM. Puerarin inhibits gene expression of IL-8and IL-6in BEAS-2B cells injured by black powder smoke[J]. Pharm J Chin PLA, 2012, 28(1): 10-14. [周莹, 王成彬, 兰晓梅. 葛根素对黑火药烟雾诱导支气管上皮细胞IL-8和IL-6基因表达的抑制作用[J]. 解放军药学学报, 2012,28(1): 10-14.]
[4]Sato Y, Ishikawa S, Otaki A, et al. Induction of acute-phase reactive substances during open-heard surgery and efficacy of ulinastatin in inhibiting cytokines and postoperative organ injury[J]. Jpn J Thorac Cardiovasc Surg, 2000, 48(7): 428-434.
[5]Li N, You SY, Wang CL, et al. The effects of ulinastatin on sp-a in lung injury induced by severe acute pancreatitis in rats[J].Tianjin Med J, 2013, 41(3): 241-243.[李楠, 尤胜义, 王春立,等. 乌司他丁对大鼠重症急性胰腺炎肺损伤中SP-A的影响[J]. 天津医药, 2013, 41(3): 241-243.]
[6]Wang XH, Hu JH, Shen YZ. Protective effects of Xingnaojing combined with ulinastatin on brain injury in severe acute pancreatitis of rats[J]. Tianjin Med J, 2013, 41(4):349-352.[王小红, 胡江鸿, 沈云志. 醒脑静联合乌司他丁对重症急性胰腺炎大鼠脑损伤的保护作用[J]. 天津医药, 2013, 41(4):349-352.]
[7]Inoue K, Takano H, Shimada A, et al. Urinary trypsin inhibitor protects against systemic inflammation induced by lipopolysaccharide[J]. Mol Pharmacol, 2005, 67(3): 673-680.
[8]Gao C, Liu Y, Ma L, et al. Protective effects of ulinastatin on pulmonary damage in rats following scald injury[J]. Burns, 2012,38(7): 1027-1034.
[9]Xu M, Wen XH, Chen SP, et al. Addition of ulinastatin to preservation solution promotes protection against ischemiareperfusion injury in rabbit lung[J]. Chin Med J (Engl), 2011,124(14): 2179-2183.
[10]Yao L, Kan EM, Lu J, et al. Toll-like receptor 4mediates microglial activation and production of inflammatory mediators in neonatal rat brain following hypoxia: role of TLR4in hypoxic microglia[J]. J Neuroinflammation, 2013, 10: 23.
[11]Qiu X, Wang J, Li H, et al. The therapeutic efficacy of ulinastatin for rats with smoking inhalation injury[J].Intimmunopharmacol, 2012, 14(3): 289-295.
[12]Hu Q, Chai JK, Yang HM. Research progression of lung injury after burn-blast combined injury[J]. Med J Chin PLA, 2013,38(5): 428-432.[胡泉, 柴家科, 杨红明. 烧冲复合伤肺损伤的研究进展[J]. 解放军医学杂志, 2013, 38(5): 428-432.]
[13]Ito K, Mizutani A, Kira S, et al. Effect of ulinastatin, a human urinary trypsin inhibitor, on the oleic acid-induced acute lung injury in rats via the inhibition of activated leukocytes[J]. Injury,2005, 36(3): 387-394.
[14]Xu P, Fang Y, Yu WR, et al. Protective effects of ulinastatin on lung injury from severe burns in rats[J]. J Shanghai Jiaotong Univ (Med Sci), 2009, 29(1): 51-53.[徐鹏, 方勇, 俞为荣, 等.乌司他丁对Ⅲ度烫伤大鼠肺组织的保护作用[J]. 上海交通大学学报(医学版), 2009, 29(1): 51-53.]
