抗坏血酸对蔬菜中亚硝酸盐含量的影响
2014-02-28詹秀环王子云郭鹏飞
詹秀环,王子云,郭鹏飞
(周口师范学院化学化工学院,河南周口 466001)
抗坏血酸对蔬菜中亚硝酸盐含量的影响
詹秀环,王子云,郭鹏飞
(周口师范学院化学化工学院,河南周口 466001)
采用盐酸萘乙二胺法测定几种不同蔬菜中亚硝酸盐含量,并研究抗坏血酸对亚硝酸盐清除作用的最佳条件。结果表明,络合物在550 nm波长处有最大吸光度,线性方程为Y=0.002 8+0.027 97X,R2=0.999 18。油菜、西葫芦亚硝酸盐含量较高,胡萝卜较低;抗坏血酸在酸性、40℃环境下,与亚硝酸盐反应10 min,清除作用最明显,抗坏血酸浓度越高越好。
亚硝酸盐;蔬菜;抗坏血酸
亚硝酸盐是一种有毒物质,对人体有极大危害。当人体摄入过量亚硝酸盐时,使血液中2价铁离子变为3价铁离子,使正常血红蛋白变为高铁血红蛋白,从而失去携带氧的能力,引起组织缺氧,发生亚硝酸盐中毒。人体摄入亚硝酸盐后,可与次级胺(仲胺、叔胺、酰胺和氨基酸)结合,形成强致癌物亚硝胺化合物[1],从而诱发消化系统癌变[2]。亚硝酸盐还能通过胎盘进入胎儿体内,可能诱发胎儿畸形[3]。亚硝酸盐广泛存在于土壤、水体、蔬菜中,而蔬菜作为人体维生素、矿物质等营养元素的重要来源,是人类必不可少的。人体因摄入了蔬菜中大量的亚硝酸盐发生中毒或死亡的案例时有报道[4]。目前亚硝酸盐的检测主要有光度法[5-7]、化学发光法、电化学法[8]、色谱法[9-11]和毛细管电泳法[12]等。
作者在不同的条件下,向亚硝酸钠溶液中加入抗坏血酸溶液,采用国家标准方法中推荐的盐酸萘乙二胺比色法[13]测定亚硝酸盐含量,找出清除亚硝酸钠的最佳条件,旨在找出降低亚硝酸盐含量的方法,这对保障人们身体健康具有重要的实践意义。现将有关结果报道如下。
1 材料与方法
1.1 材料
研究用的蔬菜油菜、胡萝卜、黄瓜、番茄、西葫芦、马铃薯均为市场购入。
试剂有5µg·m L-1亚硝酸钠溶液,0.4%对氨基苯磺酸溶液,0.2%盐酸萘乙二胺溶液,饱和硼砂溶液,106g·L-1亚铁氰化钾溶液,150g·L-1硫酸锌溶液,200µg·m L-1抗坏血酸溶液,冰乙酸,盐酸,蒸馏水,V c片(药店购入)。
主要仪器有SP-22型可见分光光度计(上海棱光技术有限公司),电子天平(北京赛多利斯天平有限公司),H H-S4型恒温水浴锅(巩义市予华
仪器有限责任公司),九阳果蔬料理机,玻璃仪器口气流烘干器(巩义市英峪高科仪器厂),P H S-3C型酸度计(上海精密科学仪器有限公司)。
1.2 方法
1.2.1 样品处理
将油菜洗净晾干,用果蔬料理机打碎,取79.942 3g于烧杯中,加蒸馏水后过滤,多冲洗几次。向滤液中加入6 m L硼砂饱和溶液,2 m L亚铁氰化钾溶液,2 m L硫酸锌溶液,以沉淀蛋白质,加入活性炭脱色,过滤,得到滤液200 m L,备用。胡萝卜、黄瓜、番茄、马铃薯、西葫芦用同样的方法处理。
1.2.2 最大吸收波长的确定
向25 m L比色管中加入2 m L亚硝酸钠标准使用液,2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,在波长530~560 nm处测量吸光度,测得最大吸收波长为550 nm。
1.2.3 标准曲线的绘制
采用盐酸萘乙二胺比色法测定亚硝酸盐含量,在酸性环境下,亚硝酸盐与对氨基苯磺酸重氮化,再与盐酸萘乙二胺偶联生成紫红色偶氮染料,利用分光光度计测量吸光度,根据不同浓度亚硝酸钠标准溶液测得的吸光度,做出标准曲线。取5支25 m L比色管,依次向其中加入0.20,0.40,0.80, 1.20,2.00 m L亚硝酸钠标准使用液,再依次加入2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。各比色管中亚硝酸钠含量分别为1.00,2.00,4.00,6.00,10.00µg。以试剂空白作参比,测量吸光度。线性方程为Y=0.002 8+ 0.027 97X,决定系数R2=0.999 18。
1.2.4 亚硝酸盐含量的测定
取6支25 m L比色管,分别加入油菜、胡萝卜、黄瓜、番茄、马铃薯、西葫芦处理液各5 m L,再分别加入2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度。对于样品测得的吸光度在标准曲线上对照,得出样品亚硝酸盐含量。
2 结果与分析
2.1 抗坏血酸清除亚硝酸钠最佳条件的确定
2.1.1 反应时间
取7支25 m L比色管,各加入2 m L亚硝酸钠标准使用液,再分别加入0.00,2.00,2.00, 2.00,2.00,2.00 m L200µg·m L-1的抗坏血酸溶液。管2~7分别按5,10,15,20,25,30 min进行反应。反应后,加入2 m L对氨基苯磺酸溶液, 1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度。结果反应时间5,10,15, 20,25,30 min处理的清除率分别为56.8%, 66.8%,62.9%,58.2%,57.1%和56.4%。可见,随着抗坏血酸溶液对亚硝酸盐作用时间的延长,亚硝酸盐的清除率上升,10 min即可达到最佳清除效果,清除率为66.8%,进一步延长时间清除效果反而减弱。
2.1.2 抗坏血酸浓度
取8支25 m L比色管,各加入2 m L亚硝酸钠标准使用液,再分别加入0.00,0.50,1.00, 1.50,2.00,2.50,3.00,3.50 m L200µg·m L-1的抗坏血酸溶液,放置10 min,分别加入2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度。结果抗坏血酸0,4,8,12,16,20,24,28µg·m L-1处理的清除率分别为0,15.6%,24.7%,42.2%, 50.9%,50.5%,50.9%和51.2%。可见,随着抗坏血酸浓度的增大,对亚硝酸盐的清除率也增大。
2.1.3 反应温度
取6支25 m L比色管,各加入2 m L亚硝酸钠标准使用液,再分别加入0.00,2.00,2.00, 2.00,2.00,2.00 m L200µg·m L-1的抗坏血酸溶液,将管2~6分别至于20,40,60,80,100℃的恒温水浴中进行反应。放置10 min,向6支比色管中分别加入2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度。结果反应温度20,40,60,80,100℃处理的清除率分别为37.0%,64.4%,49.5%, 35.6%和27.8%。抗坏血酸对亚硝酸钠的清除率在40℃时最大。继续提高温度,清除率呈下降趋势。
2.1.4 pH值
取6支25 m L比色管,各加入2 m L亚硝酸钠标准使用液,管2~6各加入2 m L200µg·m L-1的抗坏血酸溶液。使用乙酸与氢氧化钠调节管2~6的pH值分别为3.00,4.00,5.00,6.00,7.00。放置10 min,向各管加入2 m L对氨基苯磺酸溶液, 1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度。结果pH值3.00,4.00,
5.00,6.00,7.00处理的清除率分别为66.8%, 49.5%,37.8%,20.1%和11.8%。反应时的pH值对抗坏血酸清除亚硝酸盐有很大的影响,中性条件下清除效果最差,酸性条件下较好,而且随着pH值的下降其清除率有所增加,抗坏血酸对亚硝酸钠的清除率在pH值3.00时最大。
2.2 蔬菜样品中亚硝酸盐含量
将蔬菜处理液分别于即时和放置2 d测定亚硝酸盐含量。表1表明,在6种蔬菜中,西葫芦与油菜亚硝酸盐含量最高,分别为4.290,4.240 mg· kg-1;放置2 d后,6种蔬菜中的亚硝酸盐含量均有不同程度的升高。
2.3 抗坏血酸对蔬菜中亚硝酸盐的清除作用
取6支25 m L比色管,分别加入油菜、胡萝卜、黄瓜、番茄、马铃薯、西葫芦处理液各5 m L,再分别加入2 m L200µg·m L-1的抗坏血酸溶液,调节pH值为3.00,于40℃环境中放置10 min,向各管分别加入2 m L对氨基苯磺酸溶液,1 m L盐酸萘乙二胺溶液,定容混匀。以试剂空白作参比,测量吸光度,计算清除率,结果如表1。
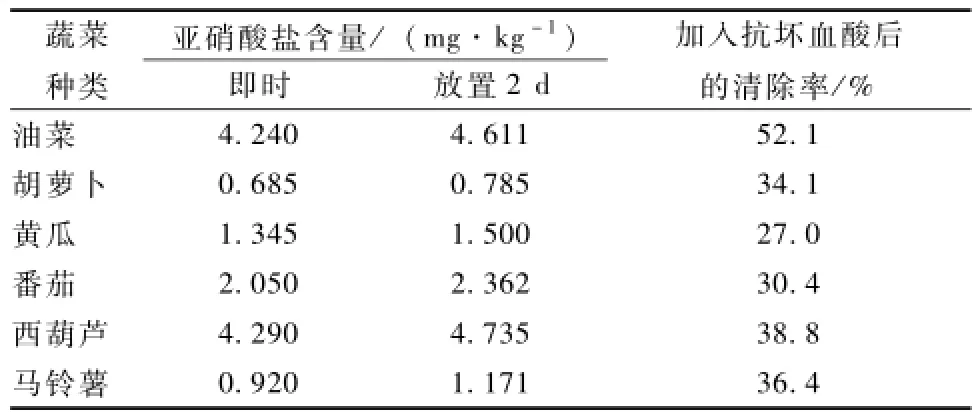
表1 6种蔬菜亚硝酸盐含量及抗坏血酸对其的清除率
抗坏血酸对西葫芦与油菜这2种亚硝酸盐含量高的蔬菜中的清除作用也强,分别达到38.8%和52.1%,对其他4种蔬菜中亚硝酸盐也具有一定的清除作用。
3 小结与讨论
试验结果表明,络合物在λ=550 nm时有最大吸光度,亚硝酸盐含量与吸光度之间具有良好的线性关系,线性方程为Y=0.002 8+0.027 97X,决定系数R2=0.999 18。抗坏血酸在pH为3.00左右、40℃环境中,与亚硝酸盐反应10 min,表现出很强的清除能力,随着抗坏血酸浓度的增高,清除能力也不断提高。测定的几种蔬菜样品中,油菜和西葫芦亚硝酸盐含量较高,胡萝卜最低。无公害蔬菜亚硝酸盐含量不得超过4 mg·kg-1,油菜与西葫芦超标,其余均合格。蔬菜经放置后,亚硝酸盐含量有不同程度的升高。该试验为解决蔬菜中亚硝酸盐的清除问题提供了依据。因此应尽量购买新鲜蔬菜,不可放置过久。日常生活中可口服维生素C或多食用新鲜水果,降低体内亚硝酸盐含量,保障人们身体健康。
[1] 李桂星,胡晓丹,孙红男,等.模拟胃液条件下苹果多酚对亚硝酸盐的清除作用[J].食品科学,2011,32(11):1-4.
[2] 潘静娴,张艳,毛洪斌.不同处理方式对几种根茎类蔬菜[J].食品科学,2011,32(9):118-121.
[3] 曹会兰.亚硝酸盐对人体的危害和预防[J].微量元素与健康研究,2003,20(2):57-58.
[4] 林周孟,吴叶仙,李建勇,等.存放时间及存放温度对蔬菜亚硝酸盐含量的影响[J].职业与健康,2008,24(24):2676-2678.
[5] 李宁,王凤霞,李建兰,等.食品中亚硝酸盐含量分析方法[J].重庆工商大学学报,2010,26(1):57-60.
[6] 崔英,谢国红.催化动力学光度法测定水中痕量亚硝酸根[J].化工环保2010,30(3):270-273.
[7] 范志影,朱超,田园,等.流动注射光度法测定蔬菜中的亚硝酸盐和硝酸盐[J].现代科学仪器,2010(1):65-67.
[8] 柏林洋,宋金海,冯刚.亚硝酸盐检测方法的研究进展[J].广州化工,2011,39(13):31-33.
[9] 徐霞,应兴华,陈能,等.离子色谱法同时测定蔬菜中的亚硝酸盐与硝酸盐[J].环境化学,2005,24(6):733-734.
[10] 徐霞,应兴华,段彬伍,等.膜渗透与离子色谱联用技术测定蔬菜中亚硝酸盐和硝酸盐[J].分析化学,2007,30(11):1586-1590.
[11] 陈文生,张明时,杨琼,等.液相色谱法测定蔬菜中的硝酸盐、亚硝酸盐[J].食品科学,2008,29(7):352-355.
[12] 姚魏,徐淑坤.流动注射-毛细管电脉直接紫外测定环境中水的硝酸根和亚硝酸根[J].分析化学,2002,30(7):836-838.
[13] 邓全民.贮藏条件和时间对蔬菜中亚硝酸盐含量的影响[J].聊城大学学报,2011,24(3):101-102.
(责任编辑:张才德)
S 63;T S 201.6文献标志码:A文章编号:0528-9017(2014)05-0678-03
2014-03-01
詹秀环(1964-)女,河南商水人,教授,硕士,主要从事食品污染物分析检验工作。E-mail:z ha nx i uhua n@126.com。
王子云。E-mail:z ks y w z y@163.com。
文献著录格式:詹秀环,王子云,郭鹏飞.抗坏血酸对蔬菜中亚硝酸盐含量的影响[J].浙江农业科学,2014(5):678-680.
