Glisson蒂横断式原位肝切除在肝细胞癌治疗中的应用
2014-02-27韩福洲蒋洪朋宋建伟王毓利马立新乔海泉
韩福洲 蒋洪朋 宋建伟 王毓利 马立新 乔海泉
肝细胞癌是我国常见恶性肿瘤之一,在肿瘤死亡率中排第二位[1-2]。以手术为主的外科治疗是目前治疗肝细胞癌的首要手段[3]。本文通过回顾性分析由我科同一医疗组行肝切除术的71例肝细胞癌病人的临床资料,探讨Glisson蒂横断式原位肝切除术在肝细胞癌外科治疗中的应用价值。
资料与方法
一、临床资料
2011年1月至2014年3月因肝细胞癌于我科行肝切除术71例,其中行Glisson蒂横断式原位肝切除(Glisson组)37例,应用第一肝门阻断法肝切除术(常规组)34例。术前所有病人心肺功能等均良好,肝功能均调整为Child-Pugh分级A级,既往均无介入、射频消融、放化疗等治疗史。两组病人均由同一医疗组进行手术,随机采用一种术式。两组术前详细资料见表1、2,各组结果差异均无统计学意义,P>0.05。
二、手术方法
1.Glisson组 取右侧肋缘下反L形或倒T形切口进腹,多数情况下需切除胆囊,解剖肝门板,游离并整束阻断相应肝段的Glisson蒂(无需打开Glisson鞘分离门静脉、肝动脉及胆道系统),可见相应肝段缺血变色,解剖第二肝门,阻断回流相应肝段的肝静脉(根据需要决定是否结扎切断),沿着缺血区域的标记线断肝。Glisson蒂三级分支的走行在个体间存在无规律性的差异,但相应三级分支往往容易在其二级分支周围1~2 cm范围内找到,因此对于较小的肿瘤,只需要解剖部分肝实质以分离阻断Glisson蒂三级分支,而不必阻断Glisson蒂二级分支。若断肝时创面渗血较多,可间歇阻断相邻肝段的Glisson蒂以减少肝脏断面血供,控制术中出血。当 Glisson 蒂于肝脏表面难以分离阻断或深埋于肝实质内时,可先用超吸刀打开部分肝脏实质,即可分离阻断相应Glisson蒂。本术式要求进腹后不搬动肝脏,在原位解剖离断相应Glisson蒂并断肝。(图1~6)
常规组:取右侧肋缘下反L形或倒T形切口进腹,切断肝圆韧带及镰状韧带,充分游离肝脏,分离肝十二指肠韧带,于第一肝门处预置阻断带,有时需要在肝外结扎切断相应肝动脉、门静脉分支。采用Pringle法阻断第一肝门,第一次阻断15 min,以后每次阻断时间控制在20 min内,多次阻断者间隔3至5 min内,距离肿瘤边缘1~2 cm处拟定肝脏预切线,沿此线以钳榨法或使用超吸刀断肝。
三、观察指标
两组的手术时间,术中出血量,术后第3天(D3)和第7天(D7)的丙氨酸转氨酶(ALT)、白蛋白(ALB)、总胆红素(TBIL)及肿瘤切缘阳性、术后顽固性腹水、胆汁漏、腹腔出血(术后24 h内新鲜出血大于300 ml)、肝性脑病发生的例数及术后平均住院时间。
四、统计学方法

表1 病人术前一般资料

图1 切除胆囊,沿肝门板分离肝蒂诸支(第一肝门处预置阻断带) 图2 S7段切除后所见 图3 S6、S7段切除断面所见 图4 S5、S6、S7段切除后所见 图5 右半肝切除所见 图6 S4、S5、S8段切除后所见
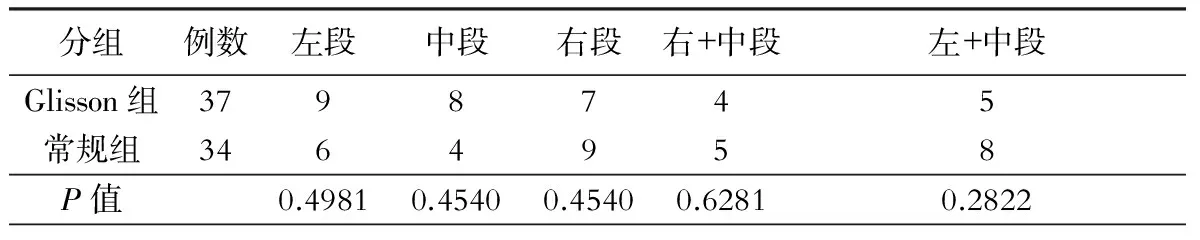
表2 肿瘤所在肝段(例)
注:Takasaki按照肝内门静脉走行以锥单元为基础将肝脏分为左段、中段、右段及尾状叶,右段约相当于右后叶,中段约相当于右前叶,左段相当于肝左叶
结 果
所有病人均成功进行肝切除术,无围手术期死亡病例。两组病人术后均无肝性脑出现;两组手术时间、术后出血例数及术后1年死亡人数差异无统计学意义(P>0.05);Glisson组术中出血量、术后第3天及第7天的ALT、ALB、TBIL以及术后平均住院日数结果均优于常规组(P<0.05)。Glisson组术后出现顽固性腹水2例,胆汁漏1例,病理回报肿瘤切缘阳性1例,均少于常规组,差异有统计学意义(P<0.05)。具体结果见表3。
讨 论
肝细胞癌是最常见的恶性肿瘤之一,死亡率高,发病机制尚不完全明确[4]。手术切除及肝脏移植对于是肝癌的根治性治疗手段,因供肝严重短缺,肝切除目前仍是肝癌治疗的首选[3,5-7]。有研究表明[8-9],手术还可提高肝癌合并门静脉癌栓的病人疗效,改善病人的生活质量,延长其生存期。肝切除术经历了经验性肝切除术,规则性肝叶切除术,局部肝切除术,解剖性肝段切除术,目前已经达到了解剖性段、亚段或联合段的肝切除阶段,进入了精确肝切除术时代,要求在完整切除肿瘤的同时,最大限度地保留正常肝组织,用“最小创伤侵袭,最大脏器保护和最佳康复效果”来评价手术质量[10-11];结合术前影像学发现(如肝脏三维重建),仔细阅片即可在术前确定手术方案。
减少术中对残肝血供的影响,减少断肝断面的出血,减少荷瘤肝脏的过分游离,行肿瘤所在肝段的解剖性原位切除对病人术后近期的肝功能恢复和提高远期生存率有重要意义。常规肝切除术中非选择性的阻断了肝脏的入肝血流,势必会造成残肝的缺血缺氧,引起缺血再灌注损伤,导致术后肝功能恢复缓慢,甚至肝衰竭,病人死亡,操作过程中未能阻断经由肝静脉回流入肝的血流,造成术中肝脏断面渗血较多[12-13];肝细胞癌主要经由门静脉系统行肝内转移,常规肝切除在操作过程中对于肿瘤的挤压会促进肿瘤细胞在肝内的播散,促进其转移及术后复发;由于我国肝癌病人均合并不同程度的肝硬化,对于肿瘤较大因占位效应导致解剖结构发生改变时在肝外游离结扎肝动脉、门静脉及胆管分支往往比较困难;术中纤细胆管的损伤常常难以发现,造成术后胆汁漏;经验性切除容易导致肿瘤细胞残存等。此外,常规肝切除术易造成局部肝组织缺血、缺氧,上调缺氧诱导因子等的表达,该因子已被证实能促进肿瘤的生长、转移[14]。
为此日本学者Takasaki于1998年提出Glisson蒂横断式肝切除术,其将肝脏按门静脉系统走形分为肝左段、中段、右段及尾状叶,分别对应Couinaud分段的Ⅱ、Ⅲ、Ⅳ段,Ⅴ、Ⅷ段,Ⅵ、Ⅶ段及Ⅰ段[15],既简化了Couinaud分段又有自己的特点。结扎肿瘤所在肝段的相应Glisson蒂,按缺血平面来确定肝脏切除范围,未影响残肝的血供,避免操作过程中缺血再灌注损伤,有利于术后肝功能的恢复[16-17];肝段间只有肝静脉及其属支而没有较大的肝动脉、门静脉和胆道系统[18],阻断相应肝静脉后可明显减少经静脉系统回肝血流,减少术中出血及术后胆汁漏和腹腔出血等并发症,对于合并较重肝硬化而无法耐受较大范围肝切除术的小肝癌病人,在术中超声引导下选择性阻断相应Glisson蒂三级或更小分支切除肿瘤所在的锥单元从而达到解剖性肝切除也是可行的,应用此法完整切除包含病灶及其门静脉属支的肝段、肝叶,切缘距离肿瘤有足够的距离,保证了切缘无瘤;切肝之前已经结扎了荷瘤的门静脉属支,减少了对肿瘤随门静脉系统肝内播散的风险,加之行原位肝切除,操作过程中未搬动肝脏,较常规肝切除减轻了对肿瘤的挤压进而减少了癌细胞的脱落;是实现解剖性肝切除并防止肿瘤肝内转移的理想方法[19-20]。本实验Glisson组与常规组术后1年于我院复查的病人分别为19例与15例;Glisson组中2例发现肝内转移灶,常规组中5例发现肝内转移灶;P<0.05。Takasaki[21]应用Glisson蒂横断式肝切除术治疗了3 000余例肝细胞癌的病人,其5年和10年生存率高出其他肝外科中心约20%。本实验Glisson组术后腹腔出血1例(2.7%),常规组4例(11.7%),但差异无统计学意义(P>0.05),考虑因样本量较小所致;因随访时间较短,未统计两组病人远期生存率的差别。
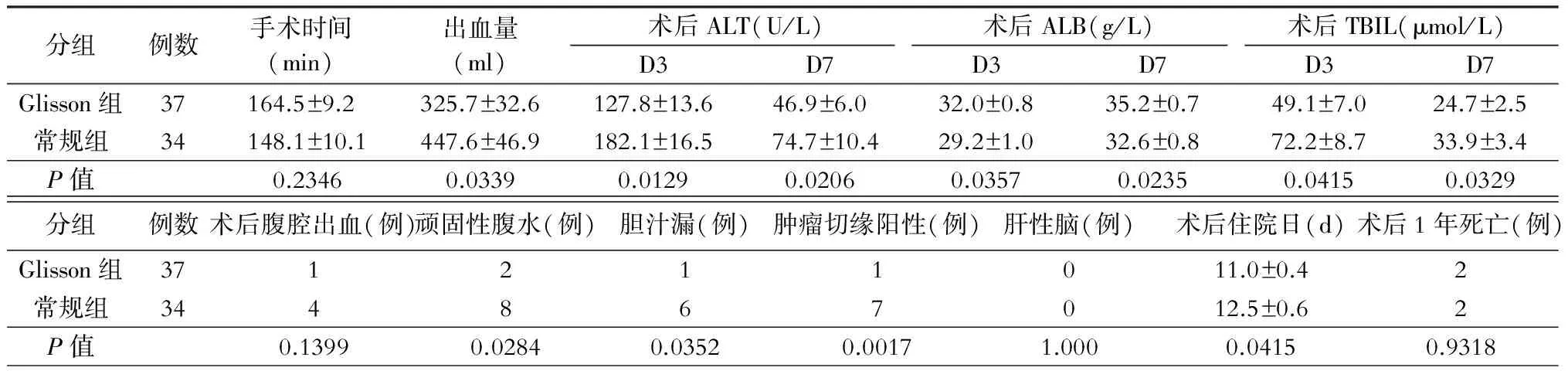
表3 两组术中及术后结果对比
Glisson蒂横断式原位肝切除的成功实施需要术者熟练掌握肝门板的结构及常见变异,熟悉Glisson系统的肝内走行,解剖肝门时及分离相应Glisson蒂时,有的Glisson蒂的二级分支在入肝时即分为多个三级分支,引起其二级分支主干相对较短,分离悬吊二级分支时可能会损伤其三级分支,造成难以控制的出血或胆管损伤,因此需从不同方向、角度小心尝试,避免暴力操作损伤周围组织;解剖肝门板及相应Glisson蒂时的中少量出血一般为肝实质的撕裂伤,干纱条压迫或电凝止血即可收到较好成效;断肝过程中对于断面中发现的细小管道均应仔细认真结扎。若术中遇到难以控制的大出血则需应用Pringe法阻断全部入肝血流以控制出血,安全起见,在完成肝门部的解剖后可预防性的在Glisson蒂主干处放置一阻断带。并不是所有部位的肝切除都必须行胆囊切除术,但切除胆囊后可以更好的解剖肝门板,肝切除完成后可通过胆囊管注入美蓝或脂肪乳等显影液体以检查创面有无胆汁漏。对于肝硬化程度较重的肝癌病人,其肝实质的改变可能导致Glisson鞘的走行发生改变,行此法肝切除有一定风险;当肝癌侵犯肝门部时,分离解剖Glisson鞘风险较大,不宜采用此法。
Glisson蒂横断式原位肝切除术不需解剖肝门部门管三联(门静脉、肝动脉及胆道)结构,操作相对简单、安全,避免了不必要的肝门部胆管及血管损伤,结合肝右、肝中静脉可更好的确定肝切除界面。总之,Glisson蒂横断式原位肝切除术更易确定肝切除界面,减少术中出血,有效地避免了肿瘤的术中肝内转移,保留了足够的健康肝脏,在肝细胞癌的外科治疗中具有重要价值。
1 郝捷,陈万青.中国肿瘤登记年报(2012).北京:军事医学科学出版社,2012.
2 Jemal A,Bray F,Center MM,et al.Global cancer statistics.CA Cancer J Clin,2011,61:69-90.
3 Llovet JM,Bruix J.Novel advancements in the management of hepatocellular carcinoma in 2008.J Hepatol,2008,48Suppl 1:S20-S37.
4 Jin-Yong Zhou,Le Zhang,Lei Li,et al.High hepatitis B virus loadis associated with hepatocellular carcinomas development in Chinese chronic hepatitis B patients:a case control study.Virology Journal,2012,9:1-5.
5 Lau WY.Management of hepatocellular carcinoma.JR Coll Surg Edinb,2002,47:389-399.
6 Lai EC,Lau WY.The continuing challenge of hepatic cancer in Asia.Surgeon,2005,3:210-215.
7 Lau WY,Lai EC.Hepatocellular carcinoma:current management and recent advances.Hepatobiliary Pancreat Dis Int,2008,7:237-257.
8 陈孝平,张志伟,张必翔,等.肝细胞癌伴门静脉癌栓的基础与临床研究.腹部外科,2003,16:343-346.
9 高丹,涂振霄,张贯启,等.肝癌合并门静脉癌栓的手术治疗.腹部外科,2014,2:124-126.
10陆昌友,郭伟昌,黄君,等.Glisson 蒂横断式肝切除术在临床中的应用研究.胃肠病学和肝病学杂志,2010,19:529-532.
11董家鸿,黄志强.精准肝切除-21世纪肝脏外科新理念.中华外科杂志,2009,47:1601-1609.
12Muller MK,Petrowsky H,Clavien PA.Techniques of vascular control and protective strategies for parenchymal transaction.Hepatocellular Carcinoma.Singapore:World Scientific Publishing,2008.507-528.
13刘允怡,赖俊雄,刘晓欣.肝血流阻断技术在肝切除中的应用.中国实用外科杂志,2010,30:625-626.
14姜洪池,姜宪,孙学英.针对肿瘤缺氧微环境探寻新的治疗方法.世界华人消化杂志,2010,18:1741-1746.
15Takasaki K.Glissonean pedicle transection method for hepatic resection:a new concept of liver segmentation.J Hepatobiliary Pancreat Surg,1998,5:286-291.
16Shirabe K,Motomura T,Takeishi K,etal.Human early liver regeneration after hepatectomy in patients with hepatocellular carcinoma:special reference to age.Scand J Surg,2013,102:101-105.
17Xie KL,Zeng Y,Wu H.Hepatic Trisectionectomy for Hepatocellular Carcinoma Using the Glisson Pedicle Method Combined with Anterior Approach.World J Surg,2014,38:2358-2362.
18Smyrniotis V,Kostopanagiotou G,Theodoraki K,et al.The role of central venous pressure and type of vascular control in blood loss during major liver resections.Am J Surg,2004,187:398- 402.
19Wong IH,Yeo W,Leung T,et al.Circulating tumor cell mRNAs in peripheral blood from hepatocellular carcinoma patients under radiotherapy,surgical resection or chemotherapy:a quantitative evaluation.Cancer Lett,2001,167:183-191.
20Yamamoto M,Katagiri S,Ariizumi S,et al.Glissonean pedicle transection method for liver surgery.Hepatobiliary Pancreat Sci,2012,19:3-8.
21Takasaki K.Glissonean pedicle transection method for hepatic Resection.Tokyo:Springer,2007.1-162.
