我院药品不良反应130例分析
2014-02-14李冬,王萍
李 冬 ,王 萍
药品不良反应(ADR)监测是提高临床用药质量、确保用药安全的重要举措。临床药师通过参与临床治疗工作,能够及时发现ADR,协助医师及时调整治疗方案,对减轻患者损害、减少ADR发生具有积极意义。本研究对解放军474医院2011年9月—2012年2月上报的有效ADR 130例进行分类统计、分析,旨在总结该院ADR发生的规律、特点及相关因素,为临床安全、合理用药提供参考依据。
1 资料与方法
由临床药师对130例ADR按患者性别与年龄分布、给药途径、引起ADR的药品种类、ADR累及系统或器官、ADR发生时间、ADR程度分级、ADR因果关系评价及转归等项目进行统计分析。药品分类方法参照《中国国家处方集》[1]的分类目录,ADR累及系统或器官根据《WHO药品不良反应术语集》定义,ADR程度分级参照《药品不良反应报告和监测管理办法》的相关规定。
2 结果
2.1 性别及年龄分布 130例ADR中男74例,女56例。各年龄段均有发生,其中年龄最小者7个月,最大者93岁。≥60岁的老年人ADR发生率最高(43.08%,56/130)。本组ADR性别与年龄分布见表1。
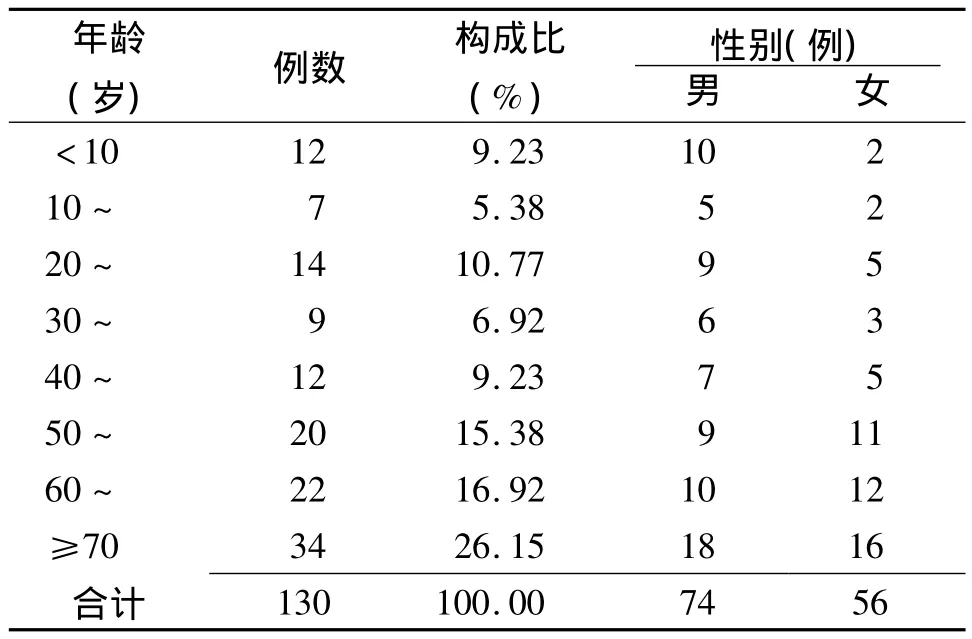
表1 130例药物不良反应性别及年龄分布
2.2 给药途径 130例ADR中静脉用药92例(70.77%),口服 28 例(21.54%),局部外用 5 例(3.85%),皮下注射 4 例(3.08%),肌内注射 1 例(0.77%)。
2.3 引起ADR的药品种类 本组按引起ADR的药品种类计算,共引发ADR 144例次,涉及13种药物,排在前3位的分别是抗感染药物70例次(48.61%),中药注射剂17 例次(11.81%),心脑血管药物14例次(9.72%),其他依次为神经系统药物7例次(4.86%),呼吸系统药物 6例次(4.17%),血液系统药物、激素及免疫调节剂、眼科用药、电解质及营养制剂各5例次(3.47%),生物制剂 4例次(2.78%),消化系统药物 3例次(2.08%),内分泌系统药物2例次(1.39%),麻醉药1 例次(0.69%)。
2.4 ADR累及系统或器官 本组按累及系统或器官计算,共发生ADR 195例次,涉及最多的是皮肤及附件损害64例次(32.82%),其他依次为全身性损害35例次(17.95%),神经系统损害28例次(14.36%),消化系统损害 25 例次(12.82%),心血管系统损害13例次(6.67%),呼吸系统损害10例次(5.13%),血液系统损害 5 例次(2.56%),泌尿系统损害2例次(1.03%),其他13例次(6.67%)。2.5 ADR发生时间 ADR发生的最短时间为用药后2 min,最长时间为用药后22 d。其中用药后2~30 min发生 46例(35.38%),0.5~2 h 32例(24.62%),3 h ~1 d 18 例(13.85%),2 ~7 d 19 例(14.62%),8 ~22 d 15 例(11.54%)。
2.6 ADR程度分级 130例ADR中程度为一般109 例(83.85%),新的一般5 例(3.85%),严重13例(10.00%),新的严重 3 例(2.31%)。新的和严重的ADR占报告总数的16.15%(21/130),其中由抗感染药物引起12例(57.14%),其次是中药制剂3 例(14.29%),其余分别是调脂药 2 例(9.52%),抗凝药、麻醉药、质子泵抑制剂、抗癫痫药各1例(4.76%)。严重的ADR主要表现为药物性肝肾功能损害、过敏性休克、血细胞减少等。
2.7 ADR因果关系评价及转归 在报告的130例ADR中,与药物“肯定相关”15例,“很可能有关”103例,“可能有关”8例,“待评价”2例,“可能无关”2例。130例 ADR中自愈71例(54.62%),治愈48例(36.92%),好转 6例(4.62%),持续 5例(3.85%)。大多数ADR在停用可疑药品或予对症治疗后均会治愈或好转,仅极少数因治疗需要未停药而症状持续存在。
3 讨论
3.1 与年龄的关系 本组ADR各年龄段人群均有发生,≥60岁人群发生率最高,占43.08%。原因为:老年患者生理功能下降,对药物的代谢能力下降,加之原患疾病的影响,更易发生ADR。本调查发现,老年患者用药剂量多为正常剂量,而根据生理特点,老年患者用药剂量应为正常剂量的1/2~2/3[2],因此应合理调整老年患者用药剂量,加强用药监护。另外,儿童脏器功能发育不完善,因此也要注意调整患儿的用药剂量,密切关注病情变化。
3.2 与给药途径的关系 本调查由静脉滴注引起ADR所占比例远高于其他给药途径。静脉给药可引起ADR的因素较多[3],因此应根据患者病情选择合适的给药方法,需静脉给药者应加强观察,及时发现和处理紧急事件,避免造成严重后果。
3.3 与药品种类的关系 本调查药品种类上报数量位居第一的是抗感染药物,其中头孢菌素引起的ADR最常见,其次是喹诺酮类药物。有研究表明,头孢菌素类药物化学结构中的β内酰胺酶核进入机体后易降解成为过敏原[4]。氟喹诺酮类药物可与脑内γ-氨基丁酸A型(GABAA)受体结合,从而阻滞抑制性神经递质,引发头昏、抽搐等中枢神经系统不良反应;其结构中含有的氟原子可透过血脑屏障,共同导致中枢神经系统兴奋性增高[5]。
本调查中中药注射剂引起的ADR居第2位。其引发ADR的原因很多,如中药成分复杂,含有多种植物蛋白、多肽、鞣质、多糖等致敏原,一旦入血刺激机体产生抗体或致敏淋巴细胞,当再次接触该抗原时即可发生ADR[6]。ADR的发生除与患者个体差异有关外,也与临床超剂量使用、多药联用及溶媒选择不当有关。提示临床医师在使用中药注射剂时应严格掌握适应证和应用原则,尽量减少联合用药,并注意滴注速度及溶媒选择,必要时避光保存,以降低中药注射剂ADR的发生率[7]。
3.4 临床表现 本调查ADR累及多个系统和(或)器官,最常见的是皮肤及附件损害,以皮疹为主,多数伴有瘙痒;其次是全身性损害,其中以寒战、高热为主,最严重的为过敏性休克。对于肝、肾功能受损及血生化改变等需要行生化检测或多方面考虑的ADR,医务人员需高度警惕,加强用药监护,才能及时发现隐匿的ADR,减少误诊和漏报现象。
3.5 ADR发生时间 有研究显示,单次用药引起的ADR多为速发型变态反应,是由IgE介导的免疫反应,多在30 min内发生[8-9]。这可能与药物本身含有的热原、微粒等有关,也可能与药物代谢产物有关。本调查中有96例ADR均在用药后1 d内出现,其中46例为用药后30 min内发生。因此在用药后的前30 min内,护士应加强巡视和观察,及时发现患者的不适反应,及时处理。
3.6 ADR程度分级 本调查中新的ADR多为药品说明书中未载明或提示少见的情况,涉及药品主要包括抗感染药物、心血管系统药物等,如头孢哌酮钠/他唑巴坦引起癫痫大发作,雷公藤多苷引起白细胞减少,参芎注射液引起腮腺增大,利福平+异烟肼引起粒细胞缺乏症,低分子肝素钙引起白细胞、红细胞、血小板同时减少。严重的ADR以肝、肾功能损害为主,其他为全身剥脱性皮炎、过敏性休克、血细胞减少等。本调查新的和严重的ADR占16.15%,远高于我国7.1%的平均水平,但低于WHO规定该类报告30.0%的标准[2]。
3.7 ADR因果关系评价 在因果关系评价时,评价为“肯定”必须满足“再次使用可疑药品,再次出现同样反应”的条件,而临床一旦出现可疑药品的ADR,一般会立即停药或改用其他药物,因此,本研究“肯定相关”的评价结果不多,评价为“很可能有关”和“可能有关”的ADR报告居多。
3.8 预防措施 对ADR的预防应注意以下几点:①对老弱妇幼等特殊人群尽可能根据其生理特点选择药品,同时注意调整药物剂量;②用药前详细询问患者有无ADR既往史,对过敏和特异体质患者用药应尤为慎重;③联合用药可一定程度增加ADR发生率,因此应尽量避免;④用药时应严格掌握静脉用药适应证,在用药过程中尤其是前30 min内应密切观察,一旦发现ADR发生应及时停药并予对症处理;⑤使用对脏器有损害的药品期间应注意监测相应脏器的功能性指标。
笔者所在医院ADR上报以临床住院科室为主渠道,患者在院易监测和诊断,而门诊患者多以院外用药为主,可能造成口服用药引起的ADR漏报。因此临床药师要对医护人员和患者进行ADR宣传教育,同时对门诊患者应加强用药指导,普及ADR报告常识,发生ADR时及时处理上报[10]。本组ADR发生例数较2010年全年报告总数(10例)明显增加,但ADR报告填写质量仍存在以下问题:①信息缺项,对一些关键项目的叙述不详尽;②一些专业术语、药品通用名不准确;③报告级别划分有误;④重复报告。因此,应进一步强调ADR报告的规范化,针对性地开展ADR监测工作的督促管理和宣传培训,同时利用医院信息系统平台在线监测和提取ADR报告信息,更加科学合理地开展ADR监测工作,为临床安全、合理用药提供可靠的参考依据和有效的保障[11]。
[1] 《中国国家处方集》编委会.中国国家处方集[M].北京:人民军医出版社,2010:12-16.
[2] 刘毅萍.2007—2008年杭州市2694例新的和严重的药品不良反应报告分析[J].中国医院药学杂志,2010,30(3):268-270.
[3] 金桂兰,唐文,赵美菊.528例药品不良反应报告分析[J].药物流行病学杂志,2004,13(5):247-249.
[4] 龙丽萍,蒋冬贵,臧萍.湖南省2008年987例严重药品不良反应病例情况分析[J].中南药学,2009,7(6):472-474.
[5] Stahlmann R.Clinical toxicological aspects of fluoroquinolones[J].Toxicol Lett,2002,127(1-3):269-277.
[6] 朱发伟,王金明.浙江台州市椒江区726例药品不良反应报告分析[J].中国药房,2011,22(2):171-173.
[7] 张丽,赵怡婷,陈冰.623例中药不良反应报告分析[J].中国医院用药评价与分析,2009,9(2):151-153.
[8] 林洁娜,刘金英.125例β内酰胺酶类抗菌药物所致不良反应分析[J].中国实用医药,2009,4(21):17-19.
[9] Herrero T,Tornero P,Infante S,et al.Diagnosis and management of hypersensitivity reactions caused by oxaliplatin[J].J Investig Allergol Clin Immunol,2006,16(5):327-330.
[10]许峰,张全英.全国690家样本医院2005—2006年用药分析[J].中国药房,2008,19(17):1293-1296.
[11]吴桂芝,王春婷,张力.药品不良反应自发报告系统信息采集内容和方式的分析[J].中国药物警戒,2011,8(10):596-599
