远端肢体转移瘤的临床特点及外科治疗策略
2014-02-13杨荣利汤小东燕太强
黄 林 郭 卫 杨荣利 汤小东 燕太强
. 骨肿瘤 Bone neoplasms .
远端肢体转移瘤的临床特点及外科治疗策略
黄 林 郭 卫 杨荣利 汤小东 燕太强
目的 分析膝、肘关节以远肢体转移瘤临床发病特点及相关预后因素,并探讨此类罕见转移疾病的外科治疗方案。方法 2000 年1 月至 2013 年6 月,北京大学人民医院骨与软组织肿瘤中心诊治远端肢体转移瘤患者 30 例 ( 41 处肢体远端转移病变 ),通过回顾其住院病历、影像学检查及病理学结果,总结其临床特征及诊断要点。41 处病变中,位于胫骨者21 处,尺骨8 处,腓骨6 处,桡骨3 处,足3 处。所有患者以VAS 评分评价疼痛程度。4 例发生病理性骨折,未发生病理性骨折的长骨病变以 Mirels 评分评价骨折风险。28 例接受手术治疗,手术患者以 MSTS 评分评价患者术后功能情况。统计学采用 Kaplan-Meier 法测算生存率,单因素分析采用 t 检验。结果28 例手术患者中位生存期9 个月,平均生存期13 个月,半年生存率 80.8%,1 年生存率24.4%,2 年生存率12.2%。未发生病理性骨折的长骨转移瘤 Mirels 评分平均为9.56 分。入院平均 VAS 评分6.86 分,接受手术治疗患者术后平均 VAS 评分2.63 分。术后平均 MSTS 功能评分为22.85 分。结论 详细的病史采集、合理的影像学检查及肿瘤学筛查是明确诊断、避免误诊的必要条件,对于难以确诊的病例,需进行进一步活检。外科手术治疗结合术后放疗及全身治疗,可明显提高患者的生活质量。
转移瘤切除术;骨肿瘤;膝关节;肘关节;远端肢体
骨骼系统是继肺及肝脏之后最容易发生肿瘤 转移的器官。骨转移瘤的发病率远高于骨原发肿瘤[1],脊柱、骨盆、肋骨、股骨及颅骨是其发生的最常见部位[2-3]。而位于膝关节和肘关节以远的骨转移瘤发病率很低,目前对此类转移疾病的发病特点及治疗策略的描述仅限于部分小样本研究及个案报道[1-2,4-6]。因其临床上的罕见性,远端肢体转移瘤诊断往往较为困难,特别是对于没有原发肿瘤病史的患者,容易出现误诊并延误治疗。
为此,我们回顾性分析了 30 例远端肢体转移瘤患者的住院病历、影像学检查、病理学结果、治疗方案及术后随访资料,对此类转移疾病的转移部位、发病表现、诊断过程、治疗策略及疾病转归等进行了总结。
资料与方法
2000 年1 月至 2013 年6 月,北京大学人民医院骨与软组织肿瘤中心共诊治 1014 例骨转移瘤患者。纳入标准:(1) 存在远端肢体骨破坏,即尺骨、桡骨、胫骨、腓骨或手足部骨破坏病灶;(2)穿刺活检或术后病理证实病变为肿瘤转移 ( 因淋巴瘤、骨髓瘤生物学行为与转移癌有很大相似性,本研究将其纳入转移癌讨论 );(3) 病历资料完整,影像学资料及病理结果可供复核。经筛选后共发现30 例远端肢体骨转移患者,通过回顾其住院病历、影像学检查及病理学结果,总结其临床特征及诊断要点,并通过统计其术后生存时间、术后功能评分,分析远端肢体转移瘤的外科治疗策略。
30 例 ( 41 处肢体远端转移病变 ) 中,男24 例,女6 例,平均年龄为 56.1 (13~73 ) 岁。12 例表现为单发骨破坏,18 例表现为多发骨破坏,8 例存在多处远端肢体病变 ( 表1)。41 处转移病变位于胫骨者21 处,尺骨8 处,腓骨6 处,桡骨3 处,足3 处。无手部转移病例。原发肿瘤包括肺癌8 例,肝癌5 例,乳腺癌3 例,肾癌3 例,膀胱癌2 例,淋巴瘤2 例、结肠癌2 例、骨髓瘤1 例、黑色素瘤1 例、骨肉瘤1 例,2 例原发肿瘤不详。入院前有明确肿瘤史者18 例,平均肿瘤时长 45.28 (4~180 ) 个月。9 例接受穿刺活检,其中6 例入院诊断为骨原发恶性肿瘤,经活检病理证实为转移瘤。
29 例以疼痛为首要发病症状,其疼痛症状变化情况通过 VAS 评分进行评估。10 例伴有软组织包块形成,其中1 例以发现局部包块为首发症状。回顾病例的影像学资料发现,除1 例乳腺癌骨胫骨转移及1 例骨肉瘤尺骨转移患者 X 线表现为成骨改变外,其余患者 X 线表现均呈溶骨性改变。5 例入院时存在病理性骨折,2 例发生于胫骨,2 例发生于尺骨,1 例发生于足跖骨,其余未发生病理性骨折的长骨病变均以 Mirels 评分评价病理性骨折的发生风险。全身检查发现9 例存在多器官转移。
1 例肺癌胫骨转移患者拒绝接受手术治疗并失访。1 例肝癌胫腓骨转移患者因全身情况较差,未接受手术治疗。其余28 例共计 38 处病变均予手术治疗。接受手术的19 例胫骨病变中,2 例行肿瘤刮除+骨水泥填充术,10 例行肿瘤刮除+骨水泥填充+髓内针 / 钢板内固定术 ( 髓内钉8 例,钢板2 例 ),6 例胫骨上段病变行瘤段截除+人工膝关节置换术,1 例因病变广泛且软组织严重受累行小腿中下1 /3 截肢术;8 例尺骨病变中,3 例尺骨干病变行肿瘤刮除+骨水泥填充+钢板 / 髓内针内固定术 ( 髓内针1 例,钢板2 例 ),4 例尺骨近端病变累及肘关节者行尺骨瘤段截除+人工肘关节置换术,1 例尺骨远端病变行单纯瘤段截除;5 例腓骨病变行瘤段截除术;3 例桡骨病变行肿瘤刮除+骨水泥填充+髓内针内固定术;3 例足部病变均行肿瘤刮除术 ( 表2,3)。多发转移灶与单发转移灶处理原则相同 ( 表1)。除1 例骨肉瘤尺骨转移患者外,其余患者均接受二磷酸盐治疗。部分患者根据不同原发肿瘤特点接受化学治疗及激素治疗。对于接受囊内刮除手术的患者术后常规接受放射治疗。
所有手术患者依据肌肉骨骼肿瘤学会 ( musculo-skeletal tumor society,MSTS ) 评分评价术后功能。采用 SPSS19.0 统计学软件测算 Kaplan-Meier 生存曲线,自确诊转移疾病开始计算生存期,患者死亡或随访结束时终止。单因素分析应用 t 检验。

表1 多发远端肢体转移患者原发病变、转移部位及手术方式Tab.1 The primary lesions, metastatic sites and surgical options of multiple metastatic lesions distal to the elbow and knee
结 果
本组 30 例中,远端肢体转移瘤发病率为全部骨转移瘤的2.96% ( 30 / 1014 ),胫骨 ( 51.2% ) 和尺骨(19.5% ) 是其最常见的发生部位 ( 图1)。60% 的患者有明确肿瘤病史,原发肿瘤中肺癌 (26.7% ) 和肝癌 (16.7% ) 分别居第一、二位 ( 表1)。
疼痛是远端肢体转移瘤最常见症状 ( 96.7% ),33.3% 的患者伴有软组织包块形成。93.3% 的病灶X 线表现为溶骨性改变。60% 的患者为多发骨转移。30% 的患者合并肺转移。
26 例手术患者获1~72 个月随访。2 例于本研究随访终止时带瘤存活。术后中位生存期9 个月,平均生存期13 个月。Kaplan-Meier 生存曲线 ( 图2)显示半年生存率 80.8%,1 年生存率24.4%,2 年生存率12.2%。单因素分析显示病理性骨折是影响预后的重要因素 ( χ2=7.072,P=0.008 ) ( 图3),多发骨转移 ( χ2=0.429,P=0.513 )、术前肿瘤史 ( χ2=0.243,P=0.622 ) 及内脏转移 ( χ2=1.090,P=0.296 )对生存率没有显著影响。
除2 例足部病灶位于骰骨及楔骨外,其它远端肢体病灶均位于长骨 ( n=39 ),病变位于骨干的21 例 ( 处 ),位于干骺端的18 例 ( 处 )。其中12.8%的病灶发生病理性骨折 ( n=5)。对未发生骨折的长骨病灶以 Mirels 评分进行骨折风险评估。平均 Mirels评分为9.53 (8~11 ) 分。
所有手术患者疼痛症状均得到显著缓解,28 例手术患者入院平均 VAS 评分6.82 分,其中中度疼痛10 例 (3<VAS ≤6),重度疼痛18 例 (6<VAS ≤10 )。出院平均 VAS 评分2 分,中度疼痛2 例,轻度疼痛26 例 ( VAS ≤3),2 例疼痛完全缓解 ( VAS=0 )。
术后8~12 周以 MSTS 评分评价患肢功能。37 处病灶术后平均 MSTS 评分22.57 分,其中上肢平均 MSTS 评分21.36 分,下肢平均 MSTS 评分23.08 分。钢板、髓内针内固定组 MSTS 评分22.81分,关节置换组 MSTS 评分20.40 分,内固定组术后功能显著优于关节置换组 ( P=0.004 )。

表2 胫骨转移癌的手术方案Tab.2 The treatment algorithm for tibial metastases

表3 尺桡骨转移瘤的手术方案Tab.3 The treatment algorithm for radial and ulnar metastases

表4 远端肢体转移癌的原发肿瘤类型Tab.4 Primary metastatic lesions distal to the elbow and knee

图1 远端肢体转移瘤的发病部位 ( *部分病例存在多处病变 )图2 肢体远端转移瘤的 Kaplan-Meier 生存曲线图3 病理性骨折对生存率的影响Fig.1 The pathogenic sites of metastatic lesions distal to the elbow and knee ( including some patients with multiple metastases )Fig.2 The Kaplan-Meier survival curve of metastatic lesions in the distal extremitiesFig.3 The effects of pathological fractures on the survival rate
本组术后3 例发生并发症,占10.71% (3 /28 )。均发生于胫骨病变膝关节置换患者,术后伤口愈合不良和术后膝关节腔积液各1 例,予对症处理后均明显好转。1 例肝癌骨转移患者术后发生严重肺部感染,术后4 周死亡。没有出现内植物失败等情况 ( 表4,5)。
讨 论
一、远端肢体骨转移瘤病因及诊断流程
位于膝关节和肘关节以远的转移瘤非常少见[1,5-6],据 Leeson 等[5]报道,远端肢体转移瘤发生率为7%,而本中心发生远端肢体转移瘤患者仅占全部转移患者的2.96%,远低于中轴骨及近端长骨转移瘤的发生率。由于 Baston[4]静脉系统的存在,发生于肺脏、乳腺、肾脏及前列腺的肿瘤可直接随血流进入椎体、骨盆、肋骨及近端肢带骨,从而增加了相应部位骨转移瘤的发生风险。
文献报道肺癌、乳腺癌和肾癌为发生远端肢体转移的最常见的原发肿瘤[2,5]。发生远端肢体转移是肺癌的一个特征,近半数发生于手部的骨转移瘤及约15% 的足部转移瘤来自肺[6]。与国外文献报道不同,本组结果提示肝癌为继肺癌后最常见的原发肿瘤灶,此现象可能与我国肝癌显著高发有关。
疼痛是远端肢体转移瘤最常见的首发症状,多数表现为典型的持续发作性疼痛,有明显的静息痛和夜间痛。局部软组织包块在转移瘤患者中并不常见,但它的出现往往对诊断造成一定的困难,特别是对于既往没有肿瘤病史的患者,可能误诊为骨的原发肿瘤或其它骨病变。本组中10 例就诊时有软组织包块形成,其中4 例诊断为骨原发肿瘤或软组织肉瘤,后经穿刺活检病理证实为转移瘤。骨转移瘤与原发性骨肿瘤有着截然不同的治疗原则,如果对骨原发恶性肿瘤采取如囊内刮除、经皮髓内针固定等治疗将导致肿瘤细胞髓内播散,增加肿瘤转移、复发风险,增加保肢难度并影响患者的预期生存,因此远端肢体转移瘤的诊断过程更应谨慎[7]( 图4)。

图4 远端肢体转移瘤的诊断流程Fig.4 A diagnostic flow chart for metastatic lesions in the distal limbs
骨转移瘤患者中,约10% 可能发生病理性骨折[8]。病理性骨折是四肢长骨转移瘤最常见及最严重的并发症,一旦发生将影响患者的预后并增加手术治疗难度[9]。在远端肢体转移瘤中,胫骨、尺桡骨及足部转移病灶是病理性骨折的高发部位。本研究5 例出现病理性骨折的患者中,有2 例位于胫骨,2 例位于尺骨,1 例位于足跖骨。胫骨作为负重骨,承担躯体重力5 /6 的轴向负荷[10],当病变范围较大时,容易在身体的重力作用下发生骨折。前臂旋前旋后范围大,尺桡骨的双骨结构在旋前和旋后的动作中始终承担扭转应力的负荷,较轻微的病变即可导致骨折。而足骨骨骼在承担重力产生的轴向负荷的同时,还需要承受足部运动产生的弯曲负荷,也是属于骨折高发部位之一。而腓骨和手部骨骼因受力负荷较小,发生病理性骨折的风向相对较低。

表5 常用病理性骨折风险评分标准及手术指征Tab.5 Frequently-used scoring systems for evaluating the risks of pathological fractures and criteria for surgical intervention
目前已有多种评分系统用于评价病理性骨折风险,其中以 Harrington 系统和 Mirels 评分系统应用最为广泛,并可根据不同标准的评分指导骨转移灶的治疗方案 ( 表3)。但需要指出的是,现存评分系统最初研究的对象均为股骨、肱骨等较为常见的骨转移病例[11-13],将其应用于临床上较为罕见的远端肢体转移病灶时可能有一定偏差。例如尺骨转移瘤病例,因病变位于上肢,其 Mirels 评分最高仅为10 分,由于前臂双骨受力结构的特殊性,即便Mirels 评分较低也存在较高的骨折风险,可能需要早期手术干预。笔者认为对于远端肢体转移病变的骨折风险的评估体系有待进一步研究修正。
二、远端肢体骨转移瘤外科治疗
病理性骨折是手术治疗的绝对适应证,手术的目的是减轻疼痛和恢复患者生活自理能力。对于未发生病理性骨折的远端肢体转移瘤患者,应充分考虑病理性骨折风险和患者预期生存时间,选择最优化的治疗措施,预防病理性骨折的发生。
胫骨转移瘤在远端肢体转移瘤中最为常见。作为下肢主要负重骨之一,胫骨转移瘤发生病理性骨折风险较高。一旦发生骨折,将对患者的活动能力产生严重影响,并降低患者生活质量。目前对胫骨转移瘤的研究报道较少,对其外科治疗原则尚有争议,Kelly 等[2]认为对于已发生病理性骨折或存在病理性骨折高风险的患者应予积极的外科治疗。本中心对手术指征的把握与其基本相同,即对已发生或即将生的病理性骨折,或者疼痛症状剧烈经保守治疗无明显改善的患者进行手术治疗。依据肿瘤所在位置不同,所采取的手术策略也各有不同。胫骨近端的转移灶,若病变范围较局限且不侵犯膝关节的病例,多采用肿瘤刮除+骨水泥填充+髓内钉 /钢板内固定。对于广泛胫骨近端病变伴有严重组织侵犯或累及膝关节的病例,可采用瘤段截除+人工膝关节置换术。胫骨中段的转移灶可采用交锁髓内钉+骨水泥填充的方式对患肢进行固定,一方面可对范围较广泛的病灶进行必要的固定,一方面可以达到充分的应力分散,避免内固定物折断等相关术后并发生的发生率。对于病变破坏相对较轻的中段病灶,可采用闭合髓内钉进行固定,以尽量减少手术创伤,达到早期下地。位于胫骨远端的病灶刮除后行骨水泥填充,可通过经跟骨距骨入路倒打髓内钉实现固定,或使用钢板进行内固定。
腓骨转移瘤非常少见,因腓骨仅承担小腿压力负荷的1 /6,且腓骨头与胫骨相连接,并不参与膝关节的构成,在胫骨保持完整的情况下腓骨一般不会发生病理性骨折[10]。因此,腓骨转移病变一般采取化疗及局部放疗等保守治疗。仅对于部分疼痛症状明显的患者,可进行单纯病灶刮除或瘤段截除。
本组尺骨是远端肢体转移瘤中仅次于胫骨的转移部位,其发生率占远端肢体转移瘤的19.5%,桡骨转移相对少见,为7.3% ( 表1)。此结果与文献报道不尽相同,Leeson 等[5]经过回顾 827 例骨转移瘤患者,发现桡骨转移7 例,尺骨转移4 例;而Kelly 等[2]回顾的 592 例中,未发现肘关节以远转移病例。因尺桡骨特殊的双骨结构,尺桡骨始终处于扭转应力的负荷之下,一旦发生转移病变很容易发生病理性骨折。本组5 例病理性骨折即有2 例发生于尺骨,因此,本中心认为对于尺骨及桡骨的转移瘤应进行积极的手术干预,对于乳癌、甲状腺癌等预期生存期较长的转移瘤患者或接受过局部放疗但仍有疼痛症状的患者可适度放宽手术指征。因尺桡骨不是负重骨,所承担轴向负荷较小,多数可采取病灶刮除+骨水泥填充+钢板内固定治疗。对于累及肘关节面的尺骨病变可行全肘关节置换,对于累及腕关节的桡骨病变可通过腓骨代桡骨术进行重建。而对于尺骨远端侵犯腕关节及桡骨近端侵犯肘关节病变,因其对关节功能影响相对较小且重建较为困难,可行截骨并旷置。
位于手足部位的转移瘤鲜有报道,一般仅见于肺癌骨转移患者[14]。本组无手部转移病例,3 例足转移瘤患者原发肿瘤分别为肺癌、肝癌及膀胱癌。文献报道,对于症状不严重的手部转移瘤可单纯采用放疗,疼痛症状严重或发生病理性骨折的病例可采用刮除+骨水泥填充+接骨板内固定,对于病变较为广泛的可行截骨旷置[15]。与手部病变相比,足部转移瘤承担更大的压力负荷和弯曲负荷,更容易发生病理性骨折,应早期采取手术治疗,手术方式多采用单纯病灶刮除或截骨旷置。
本组病例于术后6~8 周接受肢体功能评估,评价指标为 MSTS 评分。因转移病变部位、范围各有不同,本研究的统计学分析仅针对手术方式为内固定或关节置换进行单因素分析,未涉及病变部位、病理性骨折、内固定方式等。数据显示接受内固定组 MSTS 评分显著高于关节置换组。术中内固定组软组织剥离明显小于关节置换组是影响术后功能的主要原因。近年在治疗骨的原发肿瘤中,关节置换术中使用人工韧带进行软组织重建日趋增多,一定程度上提高了术后功能情况。因转移瘤患者生存期较短,且术后多需接受放疗增加并发症风险,目前此技术尚未在转移病例中广泛开展,对于其应用需要进一步临床研究。
转移瘤的主要术后并发症包括局部感染、内固定失败、术区出血、肿瘤复发、静脉栓塞等[2],发生率因原发肿瘤类型、病变位置、手术方式、内固定物、是否接受放化疗等各有不同。一般情况下,下肢变肺栓塞发生率远高于上肢患者,而使用髓内钉内固定者更容易发生脂肪栓塞;内固定失败主要与手术经验不足、内固定物选择不恰当、肿瘤控制不满意等有关;术前局部放疗患者术区出血及局部感染率高于未放疗患者。本组26 例接受随访的手术患者中,除1 例严重肺部感染患者于术后1 个月死于多脏器功能衰竭外,仅2 例出现伤口并发症,没有患者出现内植物失败等并发症。在骨肿瘤科专科医师的指导下进行多学科联合治疗是降低转移瘤术后并发生的风险的重要途径。
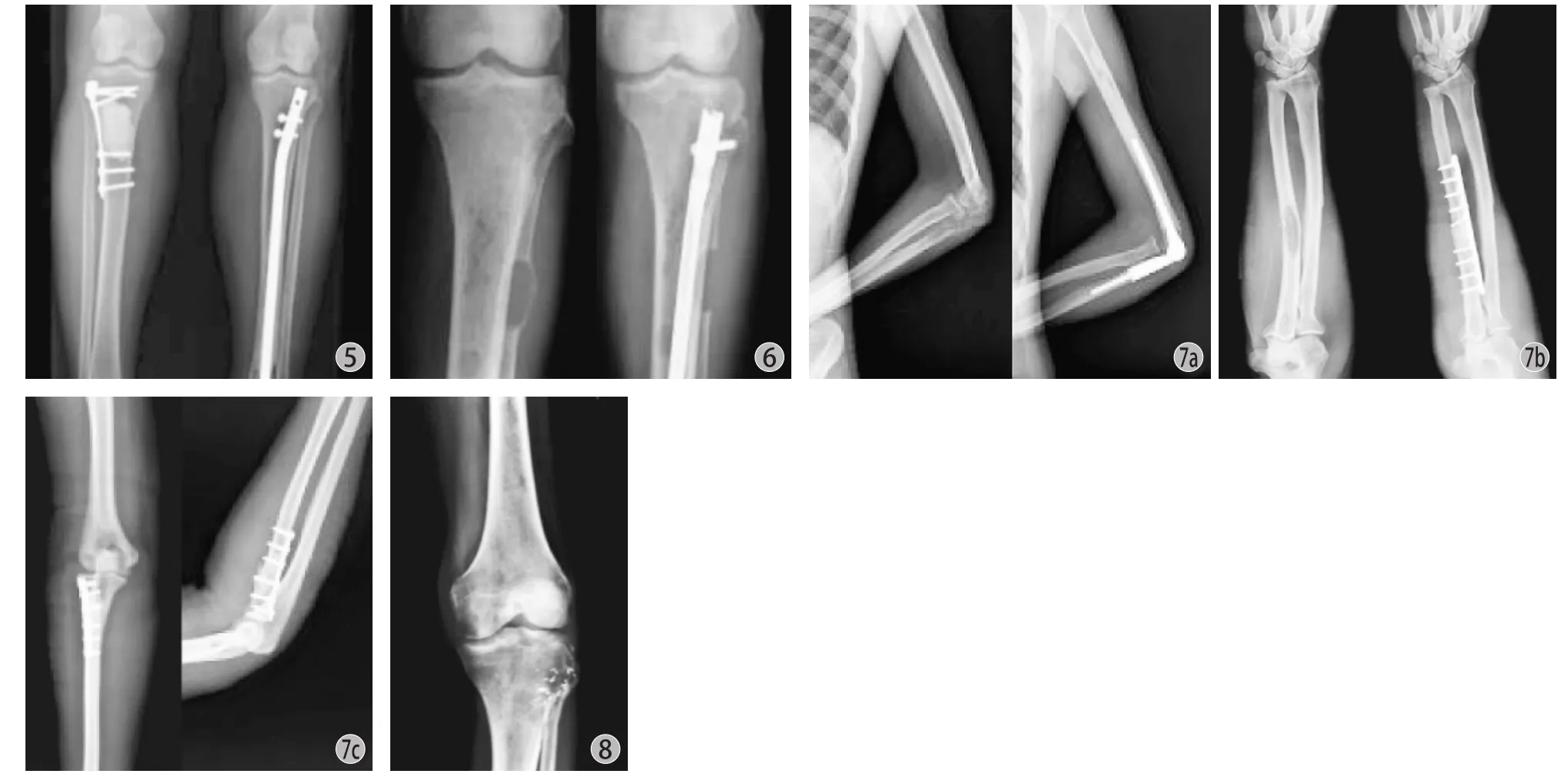
图5 1例双侧胫骨转移患者,一侧中段病变以髓内钉进行内固定,另一侧上端病变采用钢板内固定图6 1例胫腓骨多发转移瘤患者,胫骨病变予髓内钉固定,腓骨病变单纯刮除图7 a:近端尺骨病灶累及肘关节,行人工肘关节置换;b~c:尺桡骨骨干病变,合并病理性骨折,未累及关节面,予病灶刮除 + 骨水泥填充 + 钢板内固定图 81 例腓骨转移瘤接受粒子内照射治疗Fig.5 A patient with metastatic lesions in the tibia on both sides. Internal fixation by the intramedullary nail was performed for the middle lesions on one side and plate internal fixation for the proximal lesions on the other sideFig.6 A patient with multiple metastatic lesions in the tibia and fibula ipsilaterally. 7c 8As to tibial lesions, interlocking intramedullary nail fixation was carried out, and only curettage for fibular lesionsFig.7 a: A patient had proximal ulnar lesions with the elbow involved, and received artificial elbow joint replacement; b-c: The patient had metastatic lesions in the radius and ulnar combined with pathological fractures without the articular surface involved, and underwent curettage, cementation and plate internal fixationFig.8 A patient with fibular metastases was treated with local internal radiation
三、远端肢体骨转移瘤的综合治疗
针对原发肿瘤的化疗、免疫治疗及激素治疗,以及转移灶局部放疗和二磷酸盐治疗等综合治疗,对于缓解患者疼痛、预防病理性骨折发生、提高患者生存质量均有重要效果 ( 图5~8 )[16-18]。对于诸如骨髓瘤、淋巴瘤等血液来源肿瘤及某些化疗敏感的肿瘤,手术治疗并不应作为首要治疗手段。本组所有转移瘤病例均接受二磷酸盐治疗,所有接受囊内刮除手术的患者术后常规接受放射治疗,针对原发肿瘤的不同,部分患者接受化疗、激素治疗及靶向治疗。外科手术可以为患肢提供坚强固定并重建关节功能,这是保守治疗所不具备的优势。
本研究的统计学分析针对多发骨转移、术前肿瘤史、内脏转移及病理性骨折等进行单因素分析,未发现明确以上因素与患者生存有直接相关性。不同肿瘤生物学行为不同,患者生存期也存在差异,因本研究所回顾远端肢体转移瘤病例原发肿瘤类型多样,单一肿瘤病例较少,未涉及患者原发肿瘤类型等因素,故本研究结论有一定局限性。
随着肿瘤学的发展及治疗水平的进步,恶性肿瘤患者的生存期相应延长,发生骨转移的患者日益增多,发生于远端肢体的转移瘤的发病率有相应增加[19]。在充分了解此类转移疾病发病特点的基础上,通过标准流程进行诊治,将有效改善患者的不适症状、恢复肢体功能并改善生活质量,甚至可以延长部分患者的预期寿命。
[1]Du ZY, Zang J, Tang XD, et al. Experts’ agreement on therapy for bone metastases. Orthop Surg, 2010,2(4):241-253.
[2]Kelly CM, Wilkins RM, Eckardt JJ, et al. Treatment of metastatic disease of the tibia. Clin Orthop Relat Res, 2003, (415 Suppl):S219-229.
[3]Stephen D. Management of metastatic osseous lesions of the lower extremity. Techniques Orthopaedics, 2004,19(1):15-24.
[4]Batson OV. The function of the vertebral veins and their role in the spread of metastases. Ann Surg, 1940, 112(1):138-149.
[5]Leeson MC, Makley JT, Carter JR. Metastatic skeletal disease distal to the elbow and knee. Clin Orthop Relat Res, 1986, (206):94-99.
[6]Ashford RU, Pendlebury S, Stalley PD. Management of metastatic disease of the appendicular skeleton. Current Orthopaedics, 2006,20(4):299-315.
[7]汤小东, 郭卫, 杨荣利, 等. 未知来源骨转移癌患者的诊断. 中国矫形外科杂志, 2009,17(1):7-10.
[8]Coleman RE. Skeletal complications of malignancy. Cancer, 1997, 80(8 Suppl):1588-1594.
[9]Bauer HC. Controversies in the surgical management of skeletal metastases. J Bone Joint Surg Br, 2005, 87(5):608-617.
[10]Standring S, Johnson D, Ellis H, et al. Grey’s anatomy. USA: Churchill Livingstone, 2005: 298-299.
[11]Harrington KD. New trends in the management of lower extremity metastases. Clin Orthop Relat Res, 1982, (169): 53-61.
[12]Harrington KD. Impending pathologic fractures from metastatic malignancy: evaluation and management. Instr Course Lect, 1986, 35:357-381.
[13]Mirels H. Metastatic disease in long bones: A proposed scoring system for diagnosing impending pathologic fractures. 1989. Clin Orthop Relat Res, 2003, (415 Suppl):S4-13.
[14]Sugiura H, Yamada K, Sugiura T, et al. Predictors of survival in patients with bone metastasis of lung cancer. Clin Orthop Relat Res, 2008, 466(3):729-736.
[15]Aaron AD. Treatment of metastatic adenocarcinoma of the pelvis and the extremities. J Bone Joint Surg Am, 1997, 79(6): 917-932.
[16]Frassica DA. General principles of external beam radiation therapy for skeletal metastases. Clin Orthop Relat Res, 2003, (415 Suppl):S158-164.
[17]Damerla V, Packianathan S, Boerner PS. Recent developments in nuclear medicine in the management of bone metastases: a review and perspective. Am J Clin Oncol, 2005,28(5):513-520.
[18]Morris CD, Einhorn TA. Bisphosphonates in orthopaedic surgery. J Bone Joint Surg Am, 2005, 87(7):1609-1618.
[19]Damron TA, Sim FH. Surgical treatment for metastatic disease of the pelvis and the proximal end of the femur. Instr Course Lect, 2000, 49:461-470.
( 本文编辑:王永刚 )
Clinical features and surgical management of metastatic skeletal diseases distal to the elbow and knee
HUANG Lin, GUO Wei, YANG Rong-li, TANG Xiao-dong, YAN Tai-qiang. Musculoskeletal Tumor Center, Peking University People’s Hospital, Beijing, 100044, PRC
ObjectiveThe morbidity of metastatic lesions distal to the elbow and knee is quite low. To analyze the clinical characteristics and prognostic factors of metastatic diseases distal to the elbow and knee and to investigate the therapeutic strategies for such lesions.MethodsA total of 30 patients ( 41 lesions ) with metastatic lesions in the distal extremities were treated from January 2000 to June 2013. The hospital records, radiographic reports and pathological results of each patient were reviewed, so as to summarize the clinical features and diagnostic points. 41 lesions included the tibia ( n=21 ), the ulnar ( n=8 ), the fbula ( n=6), the radius ( n=3) and the foot ( n=3). The Visual Analogue Scale ( VAS ) scoring system was used to evaluate the pain in the patients. Pathological fractures were detected in4 patients, and the risk of impending pathological fractures in the other patients was evaluated by the Mirels scoring system. The surgical treatment was performed on28 patients, whose postoperative functions were evaluated by the Musculoskeletal Tumor Society ( MSTS ) scoring system. The survival rate was described with the Kaplan-Meier survival curve, and the prognostic factors were analyzed by t-test.ResultsThe median postoperative survival time and the mean postoperative survival time were9 months and13 months respectively. The half-year,1-year and2-year survival rates were 80.8%,24.4% and12.2%. The average Mirels score was9.56 points in the patients with long bone metastases but without pathological fractures. The mean VAS score of the patients was6.86 points at admission, which turned out to be2.63 points after the operation. The mean postoperative MSTS score was22.85 points. Conclusions The morbidity of metastatic diseases distal to the knee and elbow is very low. Detailed history-taking, appropriate radiographic examinations and oncology tests are essential for accurate diagnosis and avoidance of misdiagnosis. Biopsy is required when a defnite diagnosis cannot be made. The quality of life of the patients can be signifcantly improved with the surgical treatment combined with the postoperative radiotherapy and systemic therapy.
Metastasectomy; Bone neoplasms; Knee joint; Elbow joint; Distal limb
10.3969/j.issn.2095-252X.2014.07.003
R738.1
100044 北京大学人民医院骨与软组织肿瘤治疗中心
郭卫,Email: bonetumor@163.com
2013-09-03 )
