Fe3+离子荧光探针的研究进展
2014-01-29王作辉王淑敏
王作辉,王淑敏
(鹤壁职业技术学院,河南 鹤壁 458030)
金属离子荧光探针因其在环境及生物化学领域的广泛应用而受到关注[1]。铁离子是生命体必需的离子之一,很多细胞水平的生物及化学过程需要铁离子的参与[2-3]。因此,研究对铁离子的检测在环境及生命科学中都具有重要意义。目前,原子吸收光谱(AAS)、电感耦合等离子体-原子发射法(ICP-AES)、电感耦合等离子体-质谱法(ICP-MS)、电化学方法等已用来检测铁离子,尽管这些方法具有较高的灵敏度,但常需要昂贵的仪器、复杂的样品前处理和专业的操作人员等。荧光法由于具有选择性高、灵敏度好、仪器简单、操作简便等优点而备受分析工作者的关注。基于以上原因,各种结构新颖的铁离子荧光探针不断涌现。本文综述了近年来铁离子荧光探针的研究进展。
1 罗丹明类铁离子荧光探针
罗丹明类染料具有荧光量子产率高、刚性平面结构较大、水溶性好、毒性小、最大发射波长位于红色光-可见光区等优点。另外,罗丹明类染料又存在螺环与开环之间的平衡,当罗丹明染料处在螺环形式时没有荧光,而其开环状态却有强的荧光。这就使得利用金属离子调节这两种状态的平衡进而应用于其检测成为研究的热点[4-6]。
张玲菲等[7]结合硫杂杯芳烃和罗丹明衍生物各自的优势,合成了离子诱导型单取代罗丹明B荧光基团修饰的硫杂杯[4]芳烃衍生物1。在乙醇-水(1/1,V/V)Tris-HCl(pH=6.0)缓冲溶液中,1对Fe3+呈现荧光“关-开”响应,使荧光显著增强。更为重要的是还伴有颜色变红现象。据推测,这是因为1与铁离子结合时,Fe3+的络合作用诱导了1中酰胺羰基双键断裂,导致罗丹明内酰胺信号基团的开环。富电子的咕吨环重排为醌式结构,产生荧光及颜色的巨大转变,从而实现了对Fe3+的选择性识别。
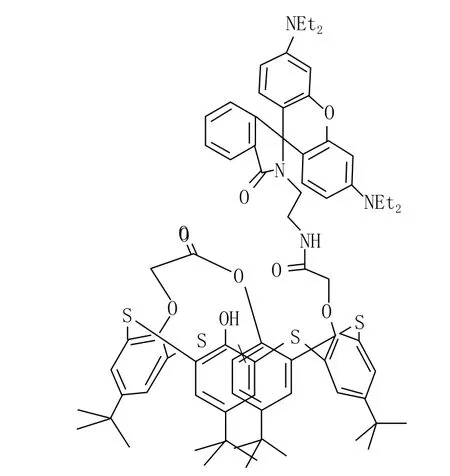
化合物1
黎俊波等[8]设计合成的罗丹明衍生物2,6-二罗丹明B酰肼西夫碱2在乙腈溶液中遇Fe3+离子后,溶液变为粉红色,且荧光增强715倍,而其它金属离子加入后无强的荧光,对Fe3+表现出高选择性。向2与Fe3+的乙腈溶液中加入EDTA(2×10-4mol·L-1)后荧光消失,2又回到“关环”状态。笔者推测,这是由于2与Fe3+络合后,螺环碳打开,形成了氧杂蒽环结构,这个共轭大π键的形成使其紫外-可见吸收及荧光大幅增加。Zhang L Z等[9]合成的Fe3+荧光探针3可以在pH值为5~9的范围内使用。据此,Zhang L Z课题组在研究中成功获得了细胞内Fe3+分布的荧光图像。
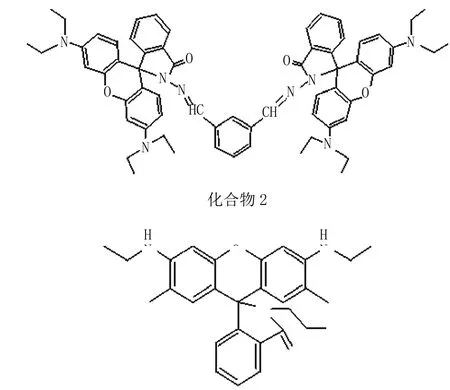
化合物3
2 吡啶类铁离子荧光探针
吡啶是含有一个氮杂原子的六元杂环化合物,吡啶环中氮原子易于同金属离子配位使其常被用于荧光探针的设计。
易卫国等[10]设计合成了以2-苯基苯并噻唑为荧光团、N-(2-吡啶甲基)胺为识别基团的荧光探针4。4在乙醇/水(1∶1,V/V)溶液中,能从常见的金属离子中以95%的荧光淬灭率选择性地识别Fe3+。探针分子荧光猝灭的机理是4取代氨基氮原子上的孤对电子容易转移,且2-芳基苯并噻唑为非对称的刚性平面结构,内含大的共轭体系,具有强吸电子能力,可使结构中电子给体与电子受体之间的相互作用大大增强。当铁离子和探针分子的识别基团配位时,引发2-芳基苯并噻唑基与双2-吡啶甲胺基的C-N键发生扭转,导致原有的共轭体系被破坏,从而引起荧光淬灭。Zhou Q Y等[11]合成了2-吡啶甲醛-对-苯基二腙5。Fe3+可以选择性淬灭5的荧光,而其它金属离子无此效果。而且,Fe3+淬灭5的荧光的行为是可逆的,当向溶液中加入还原剂如NH2OH,使 Fe3+还原为 Fe2+,5的荧光得以恢复,或者是向溶液中加入EDTA也可恢复5的荧光,这对于荧光“开-关”的设计具有一定的启发意义。
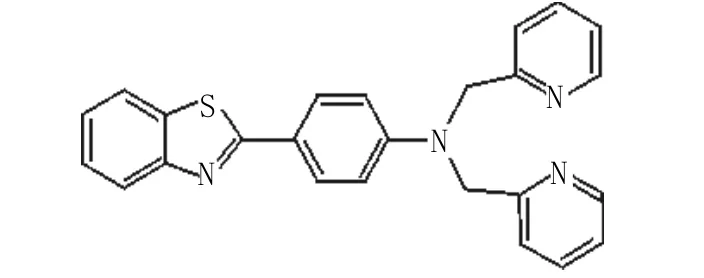
化合物4
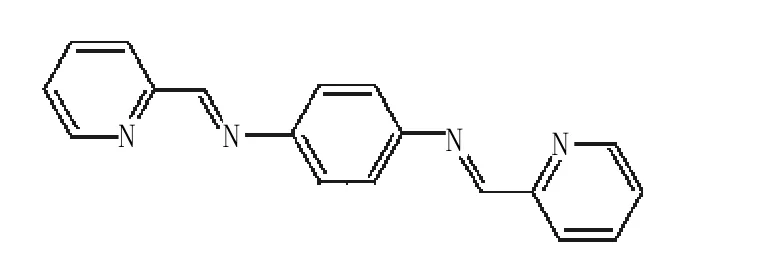
化合物5
Wei T B等[12]设计合成了一个联接萘酚O-H和亚胺基团的简单的荧光探针6。Fe3+可以使该探针溶液的颜色由黄色变为无色,而其它离子的加入则没有这种颜色变化,因此6具有比色识别Fe3+的功能。而发生这种颜色显著变化的原因是:Fe3+与探针以1∶1的比例络合时,6的结构发生了异构化,萘酚O-H基团转化为萘酚醌,同时亚胺键也被打破,从而使键长缩短,导致6遇Fe3+时颜色发生变化。另外,6还具有荧光检测Zn2+的功能。该探针能用于同时识别两种离子,为我们今后设计荧光探针提供了一种新颖的方法。Li Z X等[13]设计的荧蒽基荧光探针7可用于环境和生物样品中Fe3+的检测。当向7的乙醇溶液中加入Fe3+后,会极大地降低探针7的荧光强度。其荧光变化的机制为:Fe3+离子的顺磁性和未填充的d轨道促使荧光基团打开一个非辐射性失活通道使电子和能量发生了转移,从而使7的发光强度降低。
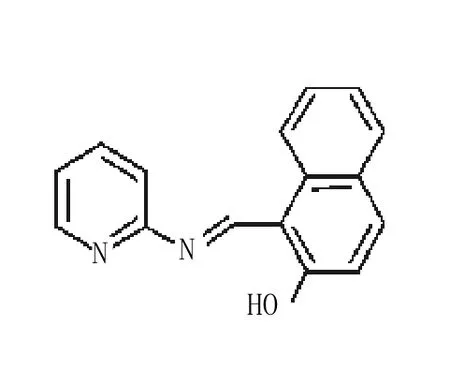
化合物6
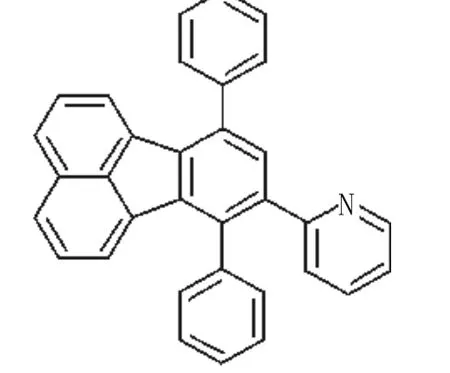
化合物7
3 萘酰亚胺类铁离子荧光探针
1,8-萘酰亚胺荧光材料的分子中包含一个平面性很强的萘环结构单元,分子的一端有强的给电子基团,另一端有强的吸电子基团,因此,其分子结构中存在着一个很大的“吸-供电子共轭体系”。处于该体系中的电子很容易受到光的照射发生跃迁,从而产生荧光。因此,1,8-萘酰亚胺是常用的合成荧光探针的优秀前体。Xu J H等[14]设计制造的荧光探针8与2-甲基丙烯酸羟乙酯在紫外光照射下发生共聚并被固定在改性石英玻璃板的表面上制成光极膜。8和Fe3+形成基态复合物导致荧光淬灭,从而实现对Fe3+的识别。在水溶液中,8对Fe3+离子的检测显示出响应快速、恢复时间短、重现性好、可逆性强和选择性高的优点。此外,由于共价固定化使得8不会从光极膜浸出。该光极膜有足够长的寿命和光谱响应特性,能保证正常使用至少2个月而不发生变化。
Yang L等[15]由1,8-萘二甲酸酐和三(2-氨基乙基)胺一步合成了Fe3+荧光探针9。9对金属离子的响应在很大程度上受溶剂的影响。在DMF中,9是一个具有高度选择性的“关断”型Fe3+荧光探针,使荧光淬灭;而在 DMF/H2O(4∶1 或 2∶3,V / V)中,9是一种具有高选择性和灵敏度的“接通”型Fe3+离子荧光探针,使荧光增强。这也给我们一个重要启示:1,8-萘二甲酰亚胺基荧光探针结构上微小的变化,就可能导致行为上的巨大差异。
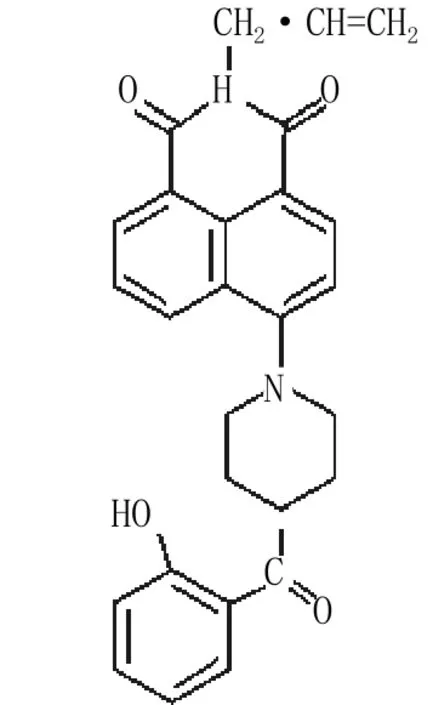
化合物8
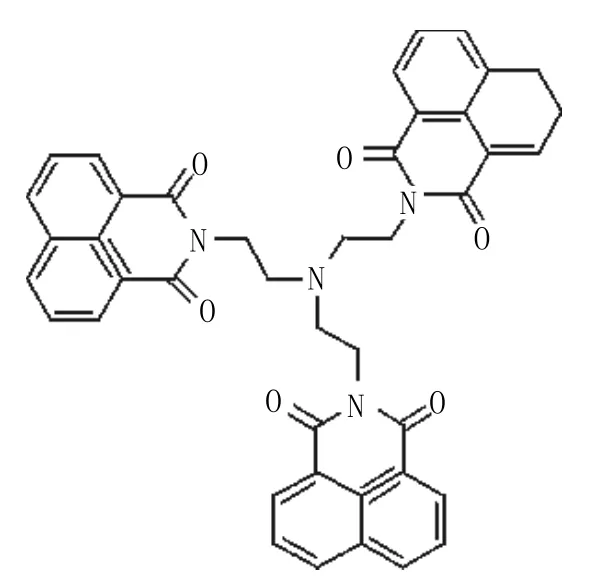
化合物9
4 其它铁离子荧光探针
Doo Y L等[16]合成的苯并咪唑类蒽偶联荧光探针10能够通过荧光比率识别Fe3+。10的分子中包含苯并咪唑和蒽两个荧光团,通过对10的溶致变色行为进行精准微调,使其对Fe3+具有很高的选择性。这两个荧光团被选择的原因是:两个荧光团可以在相同的波长被激发,但荧光输出必须是不同的;蒽基部分通常具有“开-关”行为,而苯并咪唑部分可发生“开-关”行为和电荷转移(CT)引起的波长移动。这种设计对于通过测量两种波长荧光强度的比值实现比率荧光识别是很有帮助的。比率法的优点是可以消除来自受体浓度、空白和环境的影响,这对荧光探针的设计尤为重要。
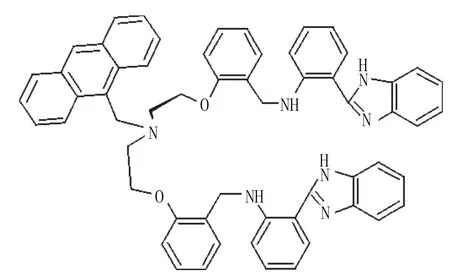
化合物10
Feng L H等[17]设计合成的Fe3+荧光探针由水溶性的β-环糊精和2,6-二(苯并恶唑基)吡啶11组成。在该荧光探针中,11作为金属离子受体,采用一个半刚性的V形构型,这样不但能够选择性地与金属离子结合,其氮原子同时还可以作为离子受体和光诱导电子转移淬灭剂。此外,11能够进入β-环糊精空腔,并形成亲水性包合物,使其能在水溶液环境下检测Fe3+。Fe3+在中性水溶液中对荧光探针有着显著的荧光淬灭,显示出对Fe3+高度的选择性和灵敏度。此外,荧光探针对Fe3+的响应信号稳定,具体表现为pH值大于3.6时,pH值几乎没有影响。
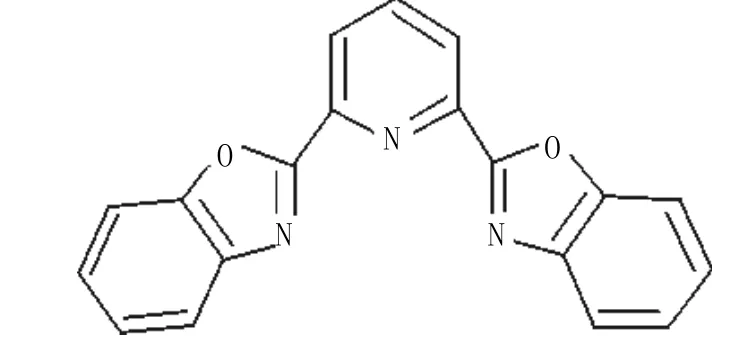
化合物11
Sr ung S等[18]设计合成的Fe3+荧光探针2-羟基苄基丹磺酰尸胺12随着Fe3+浓度的增加,表现出显著的荧光淬灭行为,对Fe3+具有很高的选择性。笔者推测,12荧光淬灭的机制是Fe3+与它的结合引起配体金属的电荷转移,12的电子电荷转移到Fe3+的d轨道,使电荷在激发态分布,最终导致12的荧光淬灭。
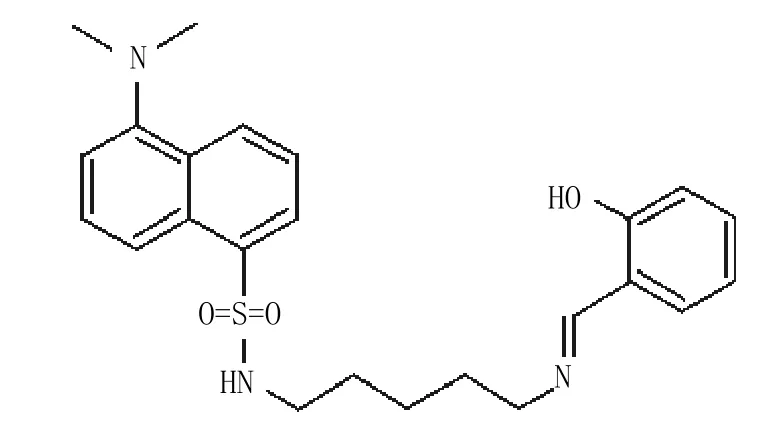
化合物12
5 展望
综上所述,近年来基于罗丹明B、吡啶、1,8-萘酰亚胺合成的Fe3+荧光探针因表现出了良好的离子选择性和灵敏性而发展比较迅速。它们在细胞内Fe3+的定量分析检测以及环境中Fe3+的快速监测方面表现出了良好的应用潜力和前景。如何将这些荧光探针应用到具体的实际中,如何设计更高灵敏度和更好选择性的Fe3+荧光探针,实现荧光探针分子的器件化、商业化进而使之更好地服务于生产、生活将是大家更为关注的课题。
[1] De Silva A P, Gunaratne H Q N, Gunn1augsson T, et al.The stability of cyclodextrin complexes in solution[J].Chem Rev.,1997(97): 1515-1566.
[2] Aisen P, Wessling-Resnick M, Leibold E A. Iron metabolism [J].Curt Opin.Chem Biol, 1999(3): 200-206.
[3] Touati D, Iron and oxidative stress in bacteria [J].Arch Bioehem Biophys, 2000(373): 1-6.
[4] Yuan M J, Zhou W D, Liu X F, et al. A multianalyte chemosensor on a single molecule:Promising structure for an integrated logic gate[J].J Org Chem.,2008(73): 5008-5014.
[5] Zheng H, Qian Z H, Xu L, et al. Switching the recognition preference of rhodamine B spirolactam by replacing one atom:design of rhodamine B thiohydrazide for recognition of Hg(Ⅱ)in aqueous solution [J]. Org Lett.,2006(8): 859-861.
[6] Huang K W, Yang H, Zhou Z G, et al. Multisigna1 chemosensor for Cr3+and its application in bioimaging[J].Org Lett.,2008(10): 2557-2560.
[7] 张玲菲,郑相勇,曾唏,等.单取代罗丹明-硫杂杯[4]芳烃衍生物的合成及对Fe3+离子的荧光探针性质研究[J].无机化学学报,2010,26(7):1183-1188.
[8] 黎俊波,李楠楠,余响林,等.高选择性铁离子荧光探针的合成及性质研究[J].武汉工程大学学报,2010,32(5):11-14.
[9] Zhang L Z, Wang J Y, Fan J L, et al. A highly selective,fluorescent chemosensor for bioimaging of Fe3+[J]. Bioorganic &Medicinal Chemistry Letters,2011(21): 5413-5416.
[10] 易卫国,曹忠,鄢东,等.芳基吡啶类Fe3+荧光探针的合成与分析应用[J].分析化学研究报告,2012,40(8):1241-1246.
[11] Zhou Q Y, Liu W Z, Chang L, et al. Spectral study of the interaction between 2-pyridinecarbal dehyde-pphenyldihydrazone and ferric iron and its analytical application[J]. Spectrochimica Acta Part A, 2012(92): 78-83.
[12] Wei T B, Zhang P, Shi B B, et al. A highly sel ective chemosensor for col orimetric detection of Fe3+and fluorescence turn-on response of Zn2+[J]. Dyes and Pigments,2013(97): 297-302.
[13] Li Z X, Zhang L F, Zhao W Y, et al.Fluoranthene-based pyridine as fluorescent chemosensor for Fe3+[J].Inorganic Chemistry Communications,2011,14: 1656-1658.
[14] Xu J H, Hou Y M, Ma Q J, et al. A highly selective fluorescent sensor for Fe3+based on covalently immobilized derivative of naphthalimide[J]. Spectrochimica Acta Part A: Molecular and Biomol ecul ar Spectroscopy, 2013(112): 116-124.
[15] Yang L, Yang W, Xu D M, et al. A highly selective and sensitive Fe3+f luorescent sensor by assembl ing three 1,8-naphthalimide fluorophores with a tris(aminoethylamine)l igand[J]. Dyes and Pigments, 2013(97): 168-174.
[16] Doo Y L, Narinder S, Doo O J. Fine tuning of a solvatochromic fluorophore for selective determination of Fe3+: a new type of benzimidazole-based anthracene-coupled receptor [J].Tetrahedron Letters, 2011(52): 1368-1371.
[17] Feng L H, Chen Z B, Wang D S.Selective sensing of Fe3+based on fluorescence quenching by 2,6-bis(benzoxazolyl)pyridine with β-cyclodextrin in neutral aqueous solution[J].Spectrochimica Acta Part A, 2007(66): 599-603.
[18] Srung S, Weerachai N, Pramuan T. Highly selective fluorescent chemosensor for Fe3+imaging in living cells[J]. Inorganic Chemistry Communications, 2011(14):351-354.
