广金钱草总黄酮-PVP-K30 固体分散体的制备和体外特征
2014-01-13赵俊霞尹蓉莉孙彩霞朱应怀苏建春于泉毅
赵俊霞, 尹蓉莉* , 孙彩霞, 朱应怀, 苏建春, 于泉毅
(1. 成都中医药大学,四川 成都611130;2. 甘肃中医学院,甘肃 兰州730000)
广金钱草总黄酮为广金钱草提取物的主要活性组分[1],具有预防草酸钙结石形成及复发、促进输尿管蠕动和增加尿量、保护肾功能、消炎、镇痛及增加冠脉血流量的作用[2-3]。但广金钱草总黄酮水溶性较差、口服生物利用度较低,限制了其临床应用。本实验以广金钱草总黄酮为模型药物,选择PVPK30 作为载体材料,利用溶剂法制备广金钱草总黄酮-PVP-K30 固体分散体,运用SEM、XRD、IR 等分析手段对其物相进行表征,并考查其体外溶出特性,为广金钱草总黄酮新制剂的开发提供依据。
1 材料与仪器
1.1 仪器 UV-1102 型紫外-可见分光光度计(上海天美科学仪器有限公司);ZRS-8G 智能溶出试验仪(天津天大天发科技有限公司);79HW-1 型恒温磁力搅拌器(江苏金坛市金城国胜实验仪器厂);DGG-9240 电热恒温鼓风干燥箱(上海森信实验仪器有限公司);BUG25-12 型超声波清洗器(必能信超声上海有限公司);6390LV 扫描电镜(日本电子公司);X’Pert Pro MPD 粉末XRD 衍射仪(Philips Company,the Netherlands);FT IR-900型红外分光光度计(美国珀金埃尔默公司)。
1.2 药品与试剂 芦丁对照品(中国药品生物制品检定所,批号100080-200707),广金钱草总黄酮提取物(以芦丁计,UV 法测得纯度≥90%,南京泽朗医药科技有限公司);聚维酮K30 (PVPK30 购于成都科龙化工试剂厂);水为蒸馏水(脱气);其他试剂均为分析纯。
2 方法
2.1 固体分散体的制备[4]
2.1.1 固体分散体的制备 采用溶剂法制备,精密称取广金钱草总黄酮1.0 g (4 份),分别用无水乙醇250 mL 溶解,再分别称取1.0、2.0、3.0、4.0 g PVP-K30 粉末,分别用无水乙醇100 mL 进行溶解,将广金钱草总黄酮溶液与PVP-K30 溶液进行混合,并超声5 min 使混合均匀,于旋转蒸发仪中60 ℃恒温挥去乙醇,将所得产物置60 ℃干燥箱干燥12 h,置装有变色硅胶的玻璃干燥器中平衡48 h,粉碎,过80 目筛备用。
2.1.2 物理混合物的制备 按同样比例称取载体和药物,分别过80 目筛后混合均匀,即为物理混合物。
2.2 广金钱草总黄酮测定
2.2.1 标准曲线的绘制[5]精密称取干燥至恒定质量的芦丁对照品10.21 mg,置50 mL 量瓶中,加50%乙醇适量,超声使溶解,定容至刻度,摇匀即得对照品贮备液。精密量取对照品贮备液1.0、2.0、3.0、4.0、5.0 mL 于50 mL 量瓶中,加入AlCl3溶液(0.1 mol/L)1.0 mL,醋酸-醋酸钠缓冲液(pH =5.5)1.0 mL,以50%的乙醇稀释至刻度,摇匀。以溶剂按同法显色作为空白,照分光光度法在272 nm 处测定吸光度,以质量浓度为横坐标,吸光度为纵坐标,进行线性回归,得回归方程为y=35.921x+0.008 9,r=0.999 9。表明芦丁在4.08 ×10-3~20.42 ×10-3mg/mL 范围内线性关系良好。
2.2.2 回收率试验 精密称取已测定的广金钱草总黄酮12.65 mg,置于50 mL 量瓶中,加50%乙醇适量,超声使溶解,定容,以0.45 μm 微孔滤膜过滤,精密量取续滤液9 份各1.0 mL,分别与3.0、4.0、5.0 mL 的0.050 6 mg/mL芦丁对照品溶液混合,定容至25 mL,按“2.2.1”项下方法测定吸光度值,计算回收率,结果平均回收率为101.6%,RSD 为2.0%。
2.3 体外溶出度试验 按照《中国药典》2010 版二部附录XC 溶出度测定第二法(桨法)[6],以900 mL 蒸馏水(脱气)为溶出介质,温度(37 ±0.5)℃,转速为(50 ±1)r/min 进行测定。分别取约90 mg 广金钱草总黄酮原料药及含等量总黄酮的固体分散体分别置于溶出杯中,并开始计时,分别于5、10、15、30、45、60、90 min 时 取 样5 mL,并及时补加5 mL 等温蒸馏水,经0.45 μm微孔滤膜过滤,吸取续滤液置25 mL 量瓶中,按“2.2.1”项下方法进行测定,计算药物累积释放百分率,绘制溶出曲线。
2.4 固体分散体物相表征
2.4.1 扫描电镜法分析[7](SEM)测试条件 真空镀金70 s,用扫描电镜观察广金钱草总黄酮原料药和固体分散体(药物与PVP-K30 比例为1 ∶2)的表面和晶体结构。
2.4.2 X-射线粉末衍射法分析(XRD)工作条件CuKɑ 靶,电压35 kV,电流30 mA,扫描速度0.15°/s,扫描范围为5 ~50°。对广金钱草总黄酮、PVP-K30、广金钱草总黄酮-PVP-K30 物理混合物(1 ∶2)及广金钱草总黄酮-PVP-K30 固体分散体进行X-射线衍射实验。
2.4.3 红外光谱法分析(IR) 波数范围4 000 ~400 cm-1,精度4 cm-1,样品采集次数10 次,KBr压片。对广金钱草总黄酮、PVP-K30、广金钱草总黄酮-PVP-K30 物理混合物(1 ∶2)及广金钱草总黄酮-PVP-K30 固体分散体进行红外光谱扫描。
3 结果
3.1 体外溶出度及溶出曲线 广金钱草总黄酮与广金钱草总黄酮-PVP-K30 物理混合物(1 ∶2)及不同比例固体分散体在90 min 的溶出度和溶出曲线分别见图1。
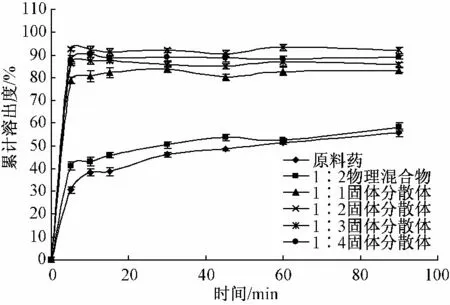
图1 广金钱草总黄酮原料药、物理混合物及固体分散体的溶出曲线(n=4)Fig.1 Dissolution curves for TFDS,TFDS with physical mixture,and TFDS with solid dispersions (at different carrier proportions)(n=4)
3.2 威布尔模型拟合[8]将广金钱草总黄酮提取物、含等量总黄酮的物理混合物和不同比例的固体分散体的溶出度分别用Weibull 公式进行拟合,回归计算溶出参数r 及Td[9],结果见表1,并采用单因素方差分析评价Td间的统计学差异。

表1 广金钱草总黄酮原料药、物理混合物及固体分散体溶出参数(n=4)Tab.1 Dissolution parameters of TFDS,TFDS physical mixture and TFDS solid dispersions (n=4)
对Td值进行方差分析,结果表明,物理混合物与原料药相比,溶出差异有统计学意义(P <0.05),4 种不同比例的固体分散体与原料药相比,溶出差异均有高度统计学意义(P <0.01),4 种不同比例的固体分散体与物理混合物相比,差异均有高度统计学意义(P <0.01),1 ∶2 固体分散体与1 ∶1 固体分散体相比,差异有统计学意义(P <0.05),与1 ∶3 及1 ∶4 固体分散体之间差异无统计学意义(P >0.05),可见将广金钱草总黄酮制成固体分散体能够显著提高其溶出速率及程度,但当载体比例增加到一定程度后,载体比例对药物溶出的影响不具有统计学意义。
3.3 固体分散体的鉴别
3.3.1 扫描电镜法分析 原料药与固体分散体的表面结构完全不同。广金钱草总黄酮原料药以大小不一的结晶体存在,而固体分散体中没有明显晶体存在,表明药物以非晶形态均匀分散在载体中,形成固体分散体,结果见图2。

图2 广金钱草总黄酮(A)与固体分散体(B)的电镜图Fig.2 SEM images of TFDS (A)and TFDS solid dispersion (B)
3.3.2 X-射线粉末衍射法分析[10]广金钱草总黄酮原料药在5 ~50°有多个强结晶特征衍射峰;PVP-K30 为无定形物,故在5 ~50°未检测到特征衍射峰;物理混合物谱图中药物仍有结晶衍射峰存在;而在固体分散体中,药物的结晶衍射峰消失,说明在形成固体分散体后,PVP-K30 对药物有抑晶作用,使药物以无定型状态或分子状态高度分散在载体材料中。结果见图3。
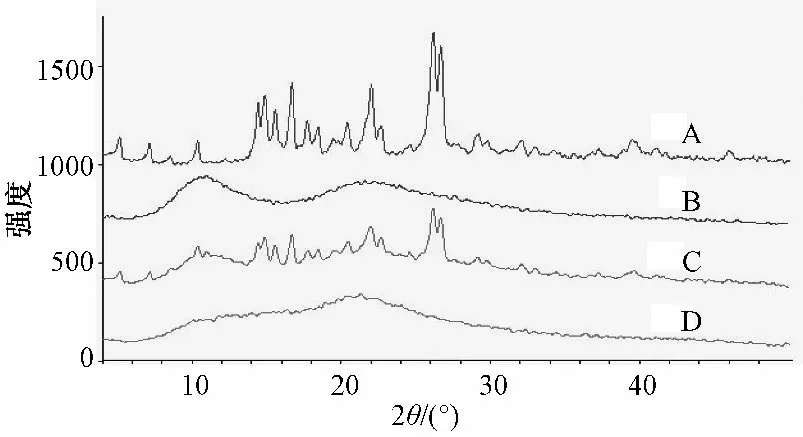
图3 广金钱草总黄酮(A)、PVP-K30 (B)、广金钱草总黄酮∶PVP-K30 =1 ∶2 物理混合物、(C)广金钱草总黄酮∶PVP-K30 =1 ∶2 固体分散体(D)X-射线衍射图Fig.3 XRD patterns:A (TFDS);B (PVP-K30 );C(physical mixture of TFDS and PVP-K30 (1 ∶2));and D (the solid dispersion of TFDS and PVP-K300 (1 ∶2))
3.3.3 红外光谱分析 广金钱草总黄酮含有-OH及C=O,-OH 在3 427 cm-1有一强吸收峰,C=O在1 601 cm-1有一强吸收峰,PVP-K30 分子含有C=O,在1 662 cm-1有一强吸收峰。原料药、物理混合物与固体分散体红外图谱比较分析:①原料药及物理混合物在3 427 cm-1和2 939 cm-1均有强吸收峰,固体分散体中红外吸收波数由原有的3 427 cm-1减小到3 398 cm-1,且尖锐吸收峰变宽钝,2 939 cm-1处吸收峰增加到2 951 cm-1,且峰强度增强;②PVP-K30 含有C =O,在1 662 cm-1有一强吸收峰,原料药和物理混合物在1 656 cm-1和1 601 cm-1均有尖锐吸收峰,而固体分散体中只在1 659 cm-1有一强吸收峰。一般情况下氢键的形成能够使吸收频率向低波数方向移动,吸收强度亦有所增加,且基团间产生的缔合易使尖锐的吸收峰变宽钝,由此推断药物与PVP-K30 之间可能有氢键形成[11-12],结果见图4。

图4 广金钱草总黄酮(A)、PVP-K30 (B)、广金钱草总黄酮∶PVP-K30 =1 ∶2 物理混合物、(C)广金钱草总黄酮∶ PVP-K30 =1 ∶2 固体分散体(D)红外光谱图Fig.4 IR spectrograms:A (TFDS );B (PVP-K30 );C (physical mixture of TFDS and PVPK30 (1 ∶2));and D (the solid dispersion of TFDS and PVP-K300 (1 ∶2))
4 讨论
实验中发现:药物-PVP-K30 比例为1 ∶1 制备固体分散体时,溶液混合后减压旋蒸过程中出现絮状沉淀、结团及严重黏壁现象,其他3 种比例组的固体分散体制备过程中不存在此种现象;1 ∶3 及1 ∶4等高比例组固体分散体与1 ∶2 固体分散体之间溶出差异不具有统计学意义 (P >0.05),而1 ∶1 固体分散体与1 ∶2 固体分散体之间溶出差异具有统计学意义(P <0.05),即当载体比例达一定程度后,固体分散体溶解速率及程度并没有随载体比例的增加而有明显增加。综上分析造成此种现象的原因可能是:药物-PVP-K30 比例为1 ∶1 时,载体比例过少,不足以高度分散并抑制原料药结晶而出现絮状沉淀及结团现象;载体比例增加时,药物溶出速率及程度未见明显增加,可能是由于载体出现相对饱和状态,药物与载体之间的相互作用(如氢键、络合、黏度等)不再增加,从而导致其增溶作用不再增加[13-15]。
固体分散体能显著改善难溶药物的溶出,关于其增溶机制有多种解释。本实验制备的固体分散体可显著提高广金钱草总黄酮的溶出度,原因可能在于:①PVP-K30 为水溶性载体,可提高药物的可润湿性,从而提高药物的溶出速率;②适量的PVPK30 可保证药物的高度分散性,当药物分散在载体中,高度分散的药物被大量载体分子包围,使药物不易聚集成团,故保证了药物的高度分散性,加快了药物的溶出;③PVP-K30 对广金钱草总黄酮具有抑晶作用,由于氢键作用,阻碍了药物分子聚集成晶。
[1] 李晓亮,汪 豪,刘 戈,等. 广金钱草的化学成分研究[J]. 中药材,2007,30(7):802-805.
[2] 王 萍,沈玉华,谢安建,等. 金钱草提取液对尿液中草酸钙晶体生长的影响[J]. 安徽大学学报:自然科学版,2006,30(1):80-84.
[3] 邹志辉. 广金钱草黄酮类化合物对草酸钙结石防治机制探讨[J]. 国际泌尿系统杂志,2008,28(4):502-504.
[4] 孔 艳,尹蓉莉,李 开,等. 满山红总黄酮-PEG6000 固体分散体的制备及体外溶出度考察[J]. 中国实验方剂学杂志,2013,19(4):62-64.
[5] 张 蕾,韩 坚,冯志强,等. 大孔吸附树脂富集纯化广金钱草总黄酮的工艺研究[J]. 中草药,2011,42(12):2442-2446.
[6] 国家药典委员会. 中华人民共和国药典:2010 年版一部[S]. 北京:中国医药科技出版社,2010:339.
[7] 胡绍英,张振海,贾晓斌. 以羟基磷灰石为载体的穿心莲内酯固体分散体研究[J]. 中国中药杂志,2013,38(3):341-345.
[8] 王 昕,唐素芳,高立勤. 溶出曲线相似性的两种评价方法[J]. 天津药学,2011,23(1):53 -56.
[9] 胡祥珍,董 荩. Excel 在测定药物制剂溶出度参数数据处理中的应用[J]. 解放军药学学报,2003,19(1):74-76.
[10] 何朝星,张贵琴,向 柏,等. 固体分散体鉴别方法研究进展[J]. 河 北 医 科 大 学 学 报,2009,30 (12):1354-1357.
[11] 戴春兰,王光发,廖正根,等. 柚皮素-PVPK-30 固体分散体的制备及体外特性研究[J]. 中成药,2011,33(1):45-49.
[12] 白炳莲,韦 珏,王海涛,等. 用红外光谱技术研究氢键的键合方式[J]. 化学通报,2013,14(2):167-170.
[13] Konno H,Taylor L S. Influence of different polymers on the crystallization tendency of molecularly dispersed amorphous felodipine[J]. Pharm Sci,2006,95(12):2692.
[14] 王秋红,匡海学,吴 伦,等. 二氢槲皮素固体分散体片的制备及体外溶出度的研究[J]. 中成药,2011,33(10):1692-1695.
[15] 蒋 苹,刘 芳,戴 青,等. 靛玉红固体分散体的制备及其体外溶出研究[J]. 第三军医大学学报,2012,34(6):538-541.
