立方晶系Li0.29Ni0.71O的电化学性质
2013-12-03王庆伟别晓非王春忠寇春雷
陈 红, 王庆伟, 别晓非, 杜 菲, 王春忠, 寇春雷
(1. 北华大学 物理学院, 吉林 吉林 132013; 2. 吉林师范大学 环境友好材料制备与应用省部共建教育部重点实验室, 吉林 四平 136000; 3. 吉林大学 物理学院, 长春 130012)
锂离子二次电池在笔记本电脑、 移动电话、 相机、 混合动力汽车(HEV)、 无间断电源(UPS)、 太空及军事等领域应用广泛. 在具有商用前景的正极/负极材料中, NiO和LiNiO2分别作为负极材料[1-4]和正极材料[5-9]已引起人们广泛关注. 但整数比例的LiNiO2不易制备, 所合成获得的材料通常为非整数比LixNi1-xO(或LixNi2-xO2)化合物[10-11]. 由于NiO中Li+部分取代Ni2+将改变材料的微结构, 因此制备的LixNi1-xO材料与纯NiO材料具有不同的电化学性能[12-14].
本文通过熔盐法制备Li+取代材料Li0.29Ni0.71O. 利用X射线衍射、 循环伏安法、 充放电循环测试及电化学阻抗谱研究材料的结构及电化学性能.
1 实 验
Li0.29Ni0.71O由熔盐法制备. 按V(硝酸锂)∶V(硝酸镍)=2的比例研磨, 混合4 h后压片置于坩埚中. 混合物先在氮气气氛下预烧至400 ℃并保温2 h, 再加热至650 ℃保温48 h. 加热及冷却速率为1 ℃/min. 样品冷却至室温后, 用去离子水清洗. 在200 ℃下烘干制得最终产物.
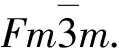
在电化学实验中, 电池负极为金属锂箔, 电极材料为质量分数为80%的活性物质+质量分数为10%的乙炔黑+质量分数为10%的粘结剂(PVDF)在N甲基吡咯烷酮中搅拌混合所得. 混合后浆液均匀涂抹在铜箔上并用真空烘箱烘干. 电解液为1 mol/L LiPF6EC/DMC溶液. 在Land电池测试系统进行恒流充放电实验. 在VSP多通道电化学工作站(Bio-Logic SAS, 法国)上进行循环伏安及电化学阻抗测试.
2 结果与分析
Li0.29Ni0.71O材料的循环伏安曲线如图1所示, 其中扫描速率为0.1 mV/s. 由图1可见, 在0.8 V处出现还原峰, 对应电极材料表面膜的形成以及Li+和Li0.29Ni0.71O的反应[6]. 反应化学方程式为

(1)
与典型的过渡金属氧化物类似[7], Li0.29Ni0.71O晶体在化学反应过程中粉化为纳米级颗粒. 反应式(1)表明, Li0.29Ni0.71O材料理论容量(1.71 mol Li+插入)小于NiO(2.0 mol Li+插入). 在氧化过程中, 位于2.2 V处的氧化峰对应部分表面膜分解及单质Ni氧化为Ni2+过程, 其反应式为

(2)
由式(1)和式(2)可见, 在首次放电充电循环后, 约有0.29 mol Li+在电极内形成Li2O.

图1 Li0.29Ni0.71O材料的循环伏安曲线Fig.1 Cyclic voltammogram of Li0.29Ni0.71O
Li0.29Ni0.71O材料以100 mA/g电流密度充放电曲线如图2所示. 由图2可见, 放电曲线先迅速降至约为1.0 V, 随后逐渐降至0.1 V. 在该过程中, 约有1.7 mol Li+插入材料, 与Li0.29Ni0.71O理论容量相符. 由于形成SEI膜, 因此所有活性物质并未全部参与电化学反应. 在首次充放电循环中, 存在较大的不可逆容量损失, 对应的库仑效率为63.4%. 不可逆容量损失也是由电解液沉降反应在电极表面形成SEI表面膜所致.
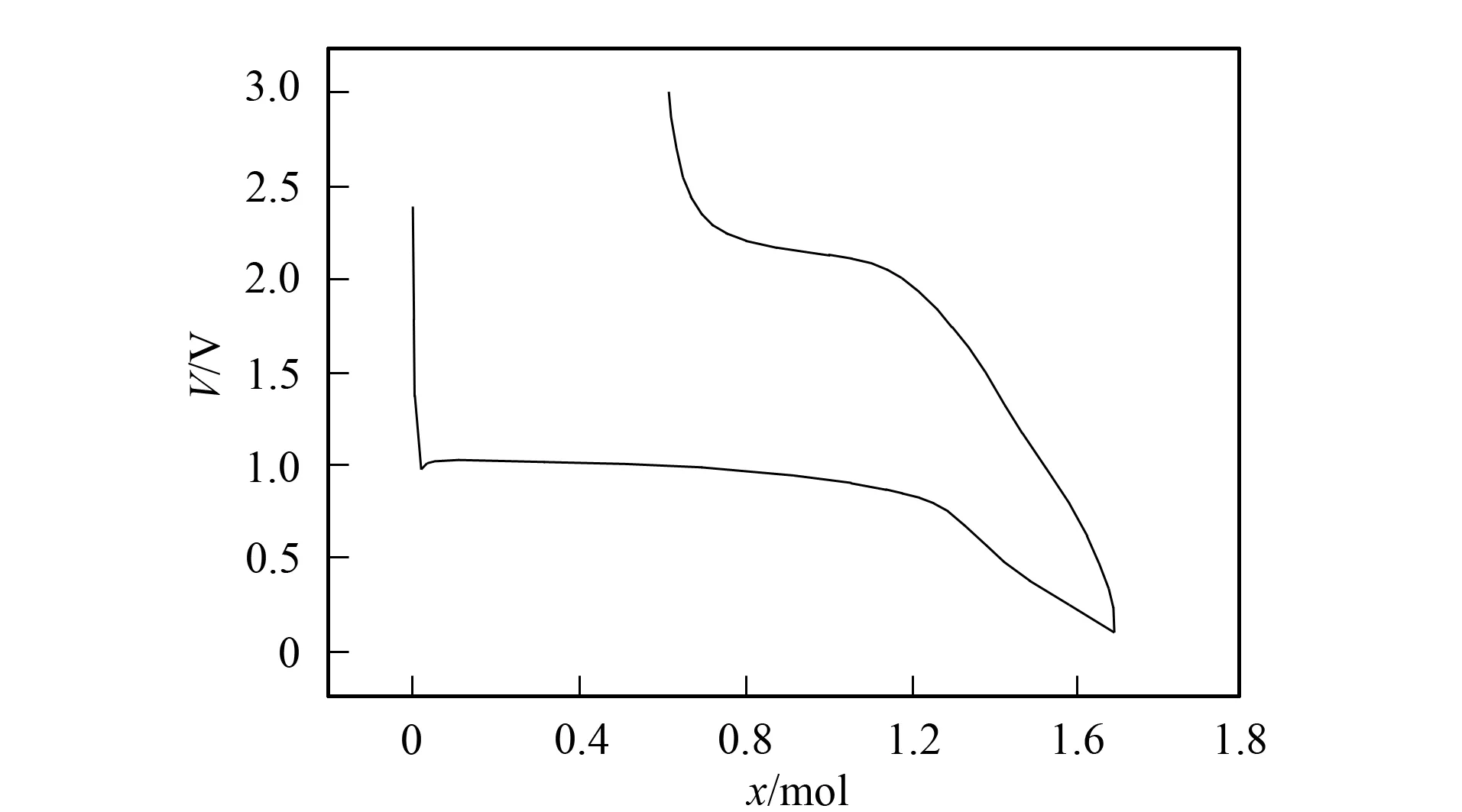
图2 Li0.29Ni0.71O材料充放电曲线Fig.2 Charge-discharge curve of Li0.29Ni0.71O
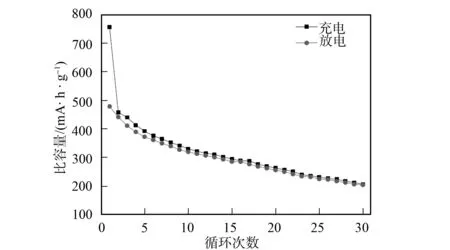
图3 Li0.29Ni0.71O材料的电化学循环性能曲线Fig.3 Curve of electrochemical cycling performance of Li0.29Ni0.71O
Li0.29Ni0.71O材料的电化学循环性能曲线如图3所示. 由图3可见, 材料的首次放电比容量为756 mA·h/g, 通常纯NiO的首次放电比容量大于1 000 mA·h/g[7-9]. 材料的循环容量衰减迅速, 30次循环后的放电比容量为208 mA·h/g. 由于Li2O不具有电化学活性, 因此, 随着循环进行, 较大的容量损失是由于未反应的Li2O在电极中累积所致.
图4(A)为Li0.29Ni0.71O电极经过首次、 第三次和第五次循环后的Nyquist曲线. 由图4(A)可见, 所有曲线在高中频区间均呈半圆形, 在低频区间为倾斜线. 其中高频区间的半圆与SEI膜的形成有关, 中频区间的半圆与电荷转移有关[7,15], 低频区间(Warburg区间)的倾斜线与电极中Li+扩散有关. Nyquist曲线可用图4(B)的等效电路分析, 其中Rs为电极的欧姆电阻,Rf和Rct为SEI膜和电荷的转移电阻,Q1和Q2为常相角元件. Li0.29Ni0.71O材料在不同循环次数后电化学阻抗谱(EIS)的等效电路拟合数据列于表1.
表1 Li0.29Ni0.71O材料在不同循环次数后的EIS等效电路拟合数据
由表1可见, Li0.29Ni0.71O材料从首次到30次循环后,Rf降低, 这是由于Li0.29Ni0.71O晶体颗粒在电化学过程中受到粉化作用, 使得电极比表面积逐渐增大所致. 结构变化完成后, 比表面积稳定, SEI膜的厚度随电解液沉积而增加. 由于Rf与SEI膜厚度成正比, 因此Rf从第三次到第五次循环中开始增大. 此外,Rct随充放电循环次数的增加而增大, 表明在SEI膜的形成及结构转变中不易发生电荷转移.

图4 Li0.29Ni0.71O材料的Nyquist曲线(A) 和拟合等效电路(B)Fig.4 Nyquist plots for Li0.29Ni0.71O (A) and equivalent circuit for fitting of the Nyquist plots (B)
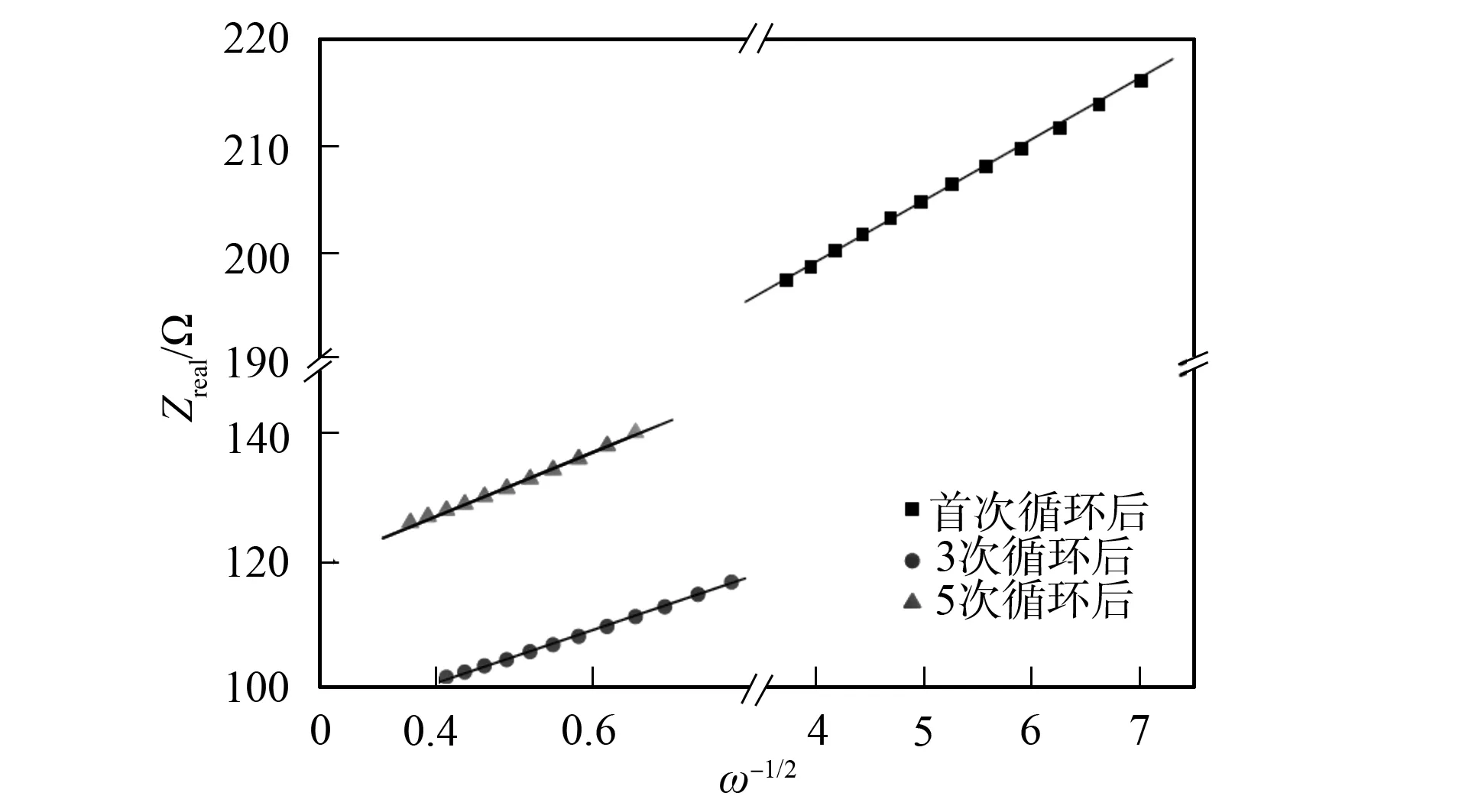
图5 Li0.29Ni0.71O材料在首次、 第三次和第五次 循环后的Zreal与ω-1/2线性拟合曲线Fig.5 Linear fitting curves of Zreal vs ω-1/2 of Li0.29Ni0.71O after 1,3 and 5 cycles
材料的化学扩散率DLi可在Warburg区间用下式计算[16]:
(3)
其中:R为气体常数;T为绝对温度;S为电极活性物质表面积;C为Li+在电极材料中的浓度;n为反应电子转移数;F为Faraday常数;σ为Warburg系数, 可由下式计算求得:
Zreal=Rs+Rct+σω-1/2.
(4)
Li0.29Ni0.71O材料在首次、 第三次和第五次循环后的Zreal与ω-1/2线性拟合曲线如图5所示, 斜率σ由Zreal与ω-1/2线性拟合得到. 由σ及式(3)可得Li0.29Ni0.71O在首次、 第三次和第五次循环后的化学扩散率分别为3.83×10-12,7.31×10-14,5.16×10-14cm2·s-1. 由于化学扩散率主要由结构及温度决定. 因此在环境温度不变的条件下,DLi从首次到3次循环后降低是由于活性物质从晶态到非晶态的结构转变所致. Li+在分解后的非晶相中比Li0.29Ni0.71O晶体中更难扩散. 由图5可见,DLi从第三次到第五次循环后的变化较小, 从而可知结构变化在前三次循环内完成.
综上, 本文研究了Li+取代对NiO材料结构及电化学性能的影响. 结果表明: 材料在Li+取代后仍为立方结构, 但由于Li+取代Ni2+时生成了离子半径更小的Ni3+, 从而压缩了立方NiO结构而使材料晶胞参数变小; 材料在Li+取代后的电化学容量比NiO略低; 首次循环时, 材料中形成的Li2O加速了材料电化学循环容量损失.
[1] Kanno R, Kubo H, Kawamoto Y, et al. Phase Relationship and Lithium Deintercalation in Lithium Nickel Oxides [J]. J Solid State Chem, 1994, 110(2): 216-225.
[2] Nagasaka Y, Ohta H, Kawakami K, et al. Millimeter Wave Spectroscopy of Secondary Battery Substance Li1-xNi1+xO2[J]. J Phys Chem Solid, 2003, 64(9/10): 1949-1951.
[3] Morales J, Pérez-Vicente C, Tirado J L. Cation Distribution and Chemical Deintercalation of Li1-xNi1+xO2[J]. Mater Res Bull, 1990, 25(5): 623-630.
[4] LI Wu, Reimers J N, Dahn J R. Crystal Structure of LixNi2-xO2and a Lattice-Gas Model for the Order-Disorder Transition [J]. Phys Rev B, 1992, 46(6): 3236-3246.
[5] WANG Chi-wei, MA Xiao-ling, LI Zi-cheng, et al. Simple, Rapid and Accurate Determination of Lattice Composition and Evaluation of Electrochemical Properties of LixNi2-xO2Electrode Material for Lithium Ion Battery by a Novel Method [J]. Electrochemistry Communications, 2006, 8(2): 289-292.
[6] Huang X H, Tu J P, Zhang B, et al. Electrochemical Properties of NiO-Ni Nanocomposite as Anode Material for Lithium Ion Batteries [J]. J Power Sources, 2006, 161(1): 541-544.
[7] Huang X H, Tu J P, Zhang C Q, et al. Net-Structured NiO-C Nanocomposite as Li-Intercalation Electrode Material [J]. Electrochem Commun, 2007, 9(5): 1180-1184.
[8] Oh Sung Woo, Bang Hyun Joo, Bae Young Chan, et al. Effect of Calcination Temperature on Morphology, Crystallinity and Electrochemical Properties of Nano-Crystalline Metal Oxides (Co3O4,CuO and NiO) Prepared via Ultrasonic Spray Pyrolysis [J]. J Power Sources, 2007, 173(1): 502-509.
[9] Rahman M M, CHOU Shu-lei, ZHONG Chao, et al. Spray Pyrolyzed NiO-C Nanocomposite as an Anode Material for the Lithium-Ion Battery with Enhanced Capacity Retention [J]. Solid State Ionics, 2010, 180(40): 1646-1651.
[10] Belhomme C, Cassir M, Devynck J, et al. Synthesis by a Soft Chemistry Route and Characterization of LixNi1-xO (0 [11] Bajpai A, Banerjee A. Characterization of the Metastable Magnetic Phase of LixNi1-xO Using Non-linear Susceptibility [J]. J Phys Condens Matter, 2001, 13(4): 637-647. [12] Manna S, De S K. Magnetic Properties of Li and Fe Co-doped NiO [J]. Solid State Communications, 2009, 149(7/8): 297-300. [13] Elp J, Van, Eskes H, Kuiper P, et al. Electronic Structure of Li-Doped NiO [J]. Phys Rev B, 1992, 45(4): 1612-1622. [14] WU Jun-bo, NAN Ce-wen, LIN Yuan-hua, et al. Giant Dielectric Permittivity Observed in Li and Ti Doped NiO [J]. Phys Rev Lett, 2002, 89(21): 217601. [15] YANG Shu-bin, SONG Huai-he, CHEN Xiao-hong. Electrochemical Performance of Expanded Mesocarbon Microbeads as Anode Material for Lithium-Ion Batteries [J]. Electrochem Commun, 2006, 8(1): 137-142. [16] Bard A J, Faulkner L R. Electrochemical Methods: Fundamentals and Applications [M]. 2nd ed. New York: Wiley, 1980: 328.
