磷酸化油菜秸秆纤维素吸附剂的制备和对牛血清白蛋白的吸附
2013-11-26李步海石荧原
李步海,石荧原
(中南民族大学化学与材料科学学院,分析化学国家民委重点实验室,武汉430074)
秸秆是地球上储量巨大的可再生资源,但秸秆中天然纤维素成分的结晶度高、分子间和分子内存在大量的氢键,难溶于大多数溶剂,是秸秆在应用开发中的最大障碍[1,2].卢炜[3]以油菜秸秆为原料提取天然的纤维素,在离子液体中用马来酸酐等改性秸秆纤维素,并用于 Cu(II)、Cd(II)、Pb(II)和 Hg(II)的吸附,改性后的吸附剂对重金属离子的最大吸附量比未改性前提高了约2~3倍.但合成离子液体价格昂贵,改性操作繁杂费时.Mucalo M.R.等[4]用磷酸化纤维素制成一种新型生物吸附剂,用于吸附细胞色素C,较未磷酸化纤维素获得较好的吸附效果.
近年来,用吸附的方法分离和纯化蛋白质的研究主要通过静电作用、离子交换、氢键、亲和吸附选择性吸附或特异性结合目标蛋白[5].Tanyolac D.等[6]利用多孔聚乙烯丁醛表面的-OH吸附牛血清白蛋白(BSA).胡杰等[7]利用磺化的聚甲基丙烯酸甲酯微球吸附BSA.张静等[8]利用辛巴蓝 F-3GA修饰的壳聚糖微球吸附BSA.吴晖等[9]研究了胶原固载Zr(Ⅳ)亲和吸附材料对牛血清蛋白的吸附特性.
本文选用新的基质-油菜秸秆纤维素,以二甲基甲酰胺为交联剂,用磷酸修饰制备一种新型生物吸附剂,并考察了吸附剂对BSA的吸附性能的影响因素.
1 实验部分
1.1 仪器、试剂与材料
荧光/磷光/发光光度计(LS-55型,美国 PE公司),傅里叶红外光谱仪(NEXUS 470智能型,美国珀金一埃尔默公司),X射线光电子能谱仪(VG Multilab 2000),手提式中药粉碎机(青州天地中药设备厂),精密酸度计(pHS-3C型,上海虹益仪表有限公司),透射电子显微镜(Tecanai G220 S-TWIN,200 kv,FEI公司).
牛血清白蛋白BSA(Sigma公司),二甲基甲酰胺(SY国药集团化学试剂有限公司),磷酸(武汉化学试剂厂),尿素(重庆化学试剂厂).
油菜秸秆取于武汉市周边田间,油菜秸秆用粉碎机打碎过筛,选取100~200目颗粒.
1.2 吸附剂的制备
1.2.1 油菜秸秆纤维素的预处理
干燥的油菜秸秆粉末先用甲苯-无水乙醇混合液脱尽蜡质.用去离子水80℃浸2 h过滤.未滤过的物质用次氯酸钠处理.以10% 醋酸调pH为0.4~3.8,75℃加热2 h.过滤后20℃以10%NaOH提取10 h再过滤.用去离子水洗至pH中性,再用95%乙醇洗,50℃真空干燥16 h备用.
1.2.2 磷酸化油菜秸秆纤维素吸附剂的制备
取5.028 g预处理后油菜秸秆纤维素粉于500 mL圆底烧瓶中,加入200 mL二甲基甲酰胺,40.2 g尿素,33.9 g磷酸溶液,于205℃下反应2 h.水洗至中性,40℃下真空干燥20 h得磷酸化油菜秸秆纤维素吸附剂.
1.3 油菜秸秆纤维素吸附剂的表征
1.3.1 红外光谱
用KBr压片,FTIR检测400~4000 cm-1处的光谱吸收,观察修饰前后油菜秸秆纤维素粉表面官能团的变化.
1.3.2 TEM 表征
样品与无水乙醇混合后超声分散,用毛细管吸取样品溶液滴于表面附有碳膜的铜网上,待样品晾干后,进行TEM测试,观察微球的粒径大小和分布情况.
1.3.3 XPS 能谱
用XPS分析修饰前后吸附剂表面的各元素组成的变化(主要为O,P和C),干燥的样品表面在10~8 托真空度条件下,用 3.6 keV Mg X-ray分析,谱图用284.6 eV 的C1s基碳峰校正,Avantage 4.54软件拟合.
1.4 吸附试验
分别称取20.0 mg磷酸化改性和原始油菜秸秆粉微球,置于25 mL锥形瓶中,加10.0 mL不同pH值缓冲溶液,0.4 mg/mL的 BSA,放入摇床(转速120 r/min)吸附20 h后离心.用荧光分光光度法测定上清液中剩余牛血清白蛋白的浓度.按式(1)计算吸附剂吸附率E.

式中C0为吸附溶液中加入的BSA初始浓度(mg/mL),Ce为吸附后上清液中BSA的浓度(mg/mL).
1.5 洗脱实验
吸附完毕后离心,弃上清液,加入10.0 mL洗脱剂溶液,将锥形瓶放入摇床(转速120 r/min)振荡洗脱,20 h后离心.取上清液测定洗脱下来的目标组分的含量,按式(2)计算洗脱率W.

式中C1为洗脱液中BSA浓度(mg/mL).
2 结果与讨论
2.1 吸附剂的表征
2.1.1 红外光谱分析

图1 未修饰和修饰后秸秆粉的红外光谱Fig.1 FTIR spectra of cole straw before and after modification
未修饰和修饰后的秸秆粉红外光谱如图1所示.由图1可见,3421 cm-1为O-H的伸缩振动吸收峰,修饰后明显减弱,表明-OH参与修饰反应,修饰后的秸秆纤维素红外光谱在1052 cm-1有P-O伸缩振动,并且峰较修饰前明显,说明秸秆纤维素已成功磷酸化.
2.1.2 透射电子显微镜表征(TEM)
未修饰和修饰后的秸秆TEM图如图2所示.由图2可见,未修饰前秸秆粉表面光滑规整,修饰后秸秆粉层次较薄,表面不规整,有毛绒化,碎片化等明显特征.这是因为秸秆粉在修饰反应后,表面结构分解碎裂造成表面损伤.说明吸附剂修饰后,表面增加了一定数量的活性基团,表面积增大了.

图2 秸秆粉的透射电子显微镜图谱Fig.2 TEM of cole straw before and after modification
2.1.3 XPS 能谱分析
修饰前后秸秆粉吸附剂表面C、O、P三种元素的面积之比见表1.如表1所示,修饰后吸附剂表面各元素的比例发生了较大变化,氧元素的比例提高很大,由原来的16.56%提高到33.81%,磷元素由0.28%提高到0.58%.原因是经修饰后,纤维素吸附剂表面增加了大量的磷酸基等活性基团,氧、磷元素的比例也相应增加;并有明显的P2p峰,表明元素P成功地修饰到了秸秆粉吸附剂的表面,与红外解析一致,见图3.
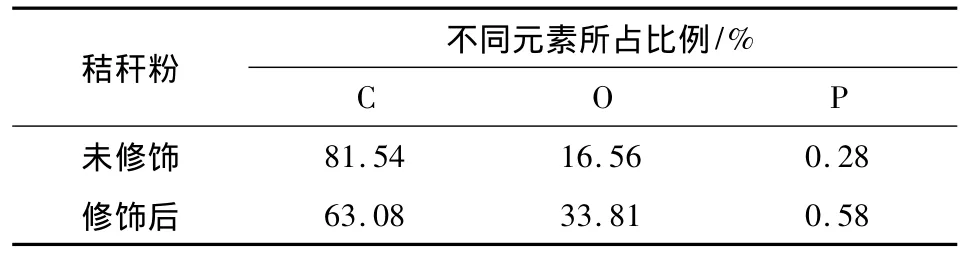
表1 未修饰和修饰后秸秆粉吸附剂各元素比例比较Tab.1 Comparison of element proportions of the biomass before and after modification
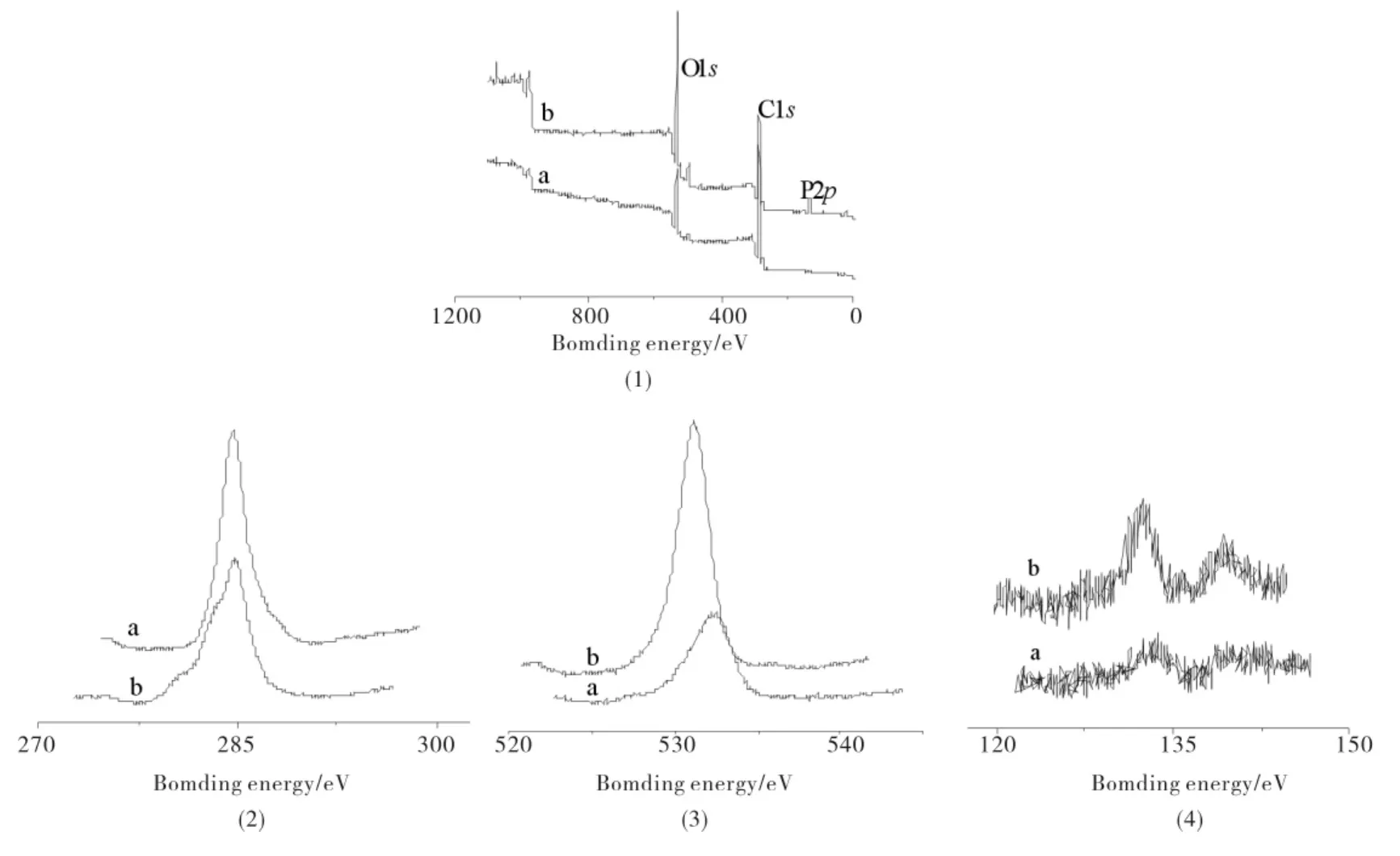
图3 未修饰和修饰后秸秆粉吸附剂的能谱图Fig.3 XPS scan of the unmodified and modified biomass
2.2 不同条件对磷酸化油菜秸秆纤维素粉微球吸附BSA的影响
2.2.1 溶液pH 的影响
溶液pH对BSA吸附率的影响见图4.由图4可见,随着溶液pH值的增大,纤维素对BSA的吸附率先增大后减小.修饰后纤维素粉在溶液pH值为6时达到最大吸附率.BSA的等电点约为pH值4.8,当溶液pH值低于4.8时,BSA带正电荷,吸附剂表面由于羧基的离群,表面带负电荷,此时吸附剂与蛋白质之间的作用以静电引力为主;在等电点附近时,BSA呈电中性,此时,疏水作用成为吸附的主要驱动力,因此吸附率继续增大;在pH值为6时达到最大.当溶液pH值继续增大时,蛋白质表面所带负电荷增多,吸附剂与蛋白质之间的静电斥力使其吸附率降低.原始油菜秸秆纤维素粉表面的活性基团较少,在低pH时(<蛋白质的PI),静电引力较小,故吸附率较低.

图4 溶液pH与BSA吸附率的关系Fig.4 Effect of pH on BSA adsorption efficiency
2.2.2 吸附时间的影响
不同的吸附时间对磷酸化油菜秸秆纤维素粉的吸附性能的影响见图5.如图5所示.修饰纤维素粉在吸附进行15 h后达到吸附平衡,原始纤维素粉在吸附20 h后达到平衡.根据不同吸附剂的性质,确定后续实验吸附时间为20 h.因为修饰后吸附剂相比修饰前,表面有更多的活性基团,能更快达到吸附平衡.

图5 反应时间与BSA吸附率的关系Fig.5 Effect of contact time on BSA adsorption efficiency
2.2.3 BSA 初始浓度的影响
牛血清白蛋白的初始浓度与未修饰、磷酸修饰纤维素粉吸附量的关系见图6.由图6可见,随着牛血清白蛋白初始浓度的增加,两种吸附剂的吸附量逐渐增加.趋于吸附饱和后,吸附量基本不变.未修饰纤维素粉在牛血清白蛋白初始浓度为0.7 mg/mL时,达到最大吸附容量值68.98 mg/g;磷酸修饰纤维素粉在0.9 mg/mL,吸附容量达最大值127.39 mg/g,是未修饰的1.85倍.

图6 BSA初始浓度与吸附量的关系Fig.6 Effect of BSA initial concentration on adsorption capacity
用 Langmuir[10]和 Freundlich[11]方程模拟 2 种吸附剂的吸附过程,所得相关系数列于表2.从模拟结果可见,Langmuir模型所得直线的相关系数优于Freundlich模型,用Langmuir模型方程式算出的未修饰和修饰后的吸附剂最大吸附容量的理论值(73.96、133.51mg/g)和 实 验 值 (68.98、127.39 mg/g)能较好的吻合,故油菜秸秆纤维素吸附剂和磷酸修饰纤维素吸附剂对BSA的吸附过程可能只存在一种类型的吸附机制,两种吸附剂对BSA的吸附为单分子层吸附(图7).
Langmuir等温吸附方程为:

线型方程为:

qe平衡吸附量mg/g;Ce平衡浓度mg/L;qm是理论最大吸附量mg/g.
Freundlich等温式是一个经验公式,没有假设条件,方程式如下:

线性方程为:

其中,K(L/mg)和n是经验常数,qe(mg/g)是平衡时的吸附容量,Ce(mg/L)是吸附平衡时溶液中吸附质的浓度.

表2 纤维素对BSA吸附的Langmuir和Freundlich吸附等温线模拟参数Tab.2 Langmuir and Freundlich parameters for the absorption of BSA

图7 Langmuir和Freundlich吸附等温线模拟图Fig.7 Langmuir and Freundlich isotherms for BSA adsorption
2.2.4 吸附温度
25~45℃时,温度对牛血清白蛋白吸附率的影响不大,但温度的升高使部分蛋白质变性,为保持较高的活性和方便操作,吸附温度选定25℃.
2.2.5 离子强度的影响
NaCl浓度对BSA吸附率的影响见图8.由图8可见,随着溶液中NaCl浓度的增大,2种吸附剂对BSA的吸附率均明显下降.因为离子强度增加,双电层增厚,蛋白质与吸附剂结合的空间阻碍和静电排斥力加大;此外,溶液中离子浓度高时或极性增加时,蛋白质得到更大的稳定性,平衡往脱附方向移动,造成吸附率降低.

图8 NaCl浓度对BSA吸附率的影响Fig.8 Effect of NaCl concentration on adsorption ratio
2.2.6 BSA 的洗脱
NaCl和NaSCN溶液在不同浓度下作为洗脱剂对BSA的洗脱效果见图9.由图9可见,随洗脱剂浓度的增加,洗脱率增大,当 c(NaCl)>1.0 mol/L,c(NaSCN)>0.8 mol/L后洗脱率下降,NaCl和NaSCN的最大洗脱率分别为54.68%,42.26%.NaCl对BSA的脱附效果更好.这是因为盐浓度升高,离子强度增大,双电层增厚,BSA与吸附剂配体间的静电结合力和疏水作用减弱.其次,Cl-1相比SCN-1更活跃与自由,故能更好地稳定蛋白质.
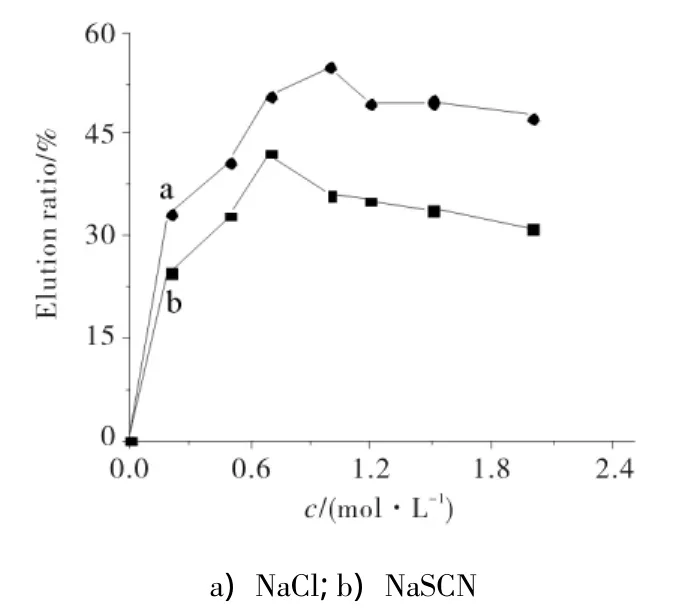
图9 不同洗脱剂对BSA洗脱率的影响Fig.9 Effect of varying eluants on BSA elution ratio
3 结语
用磷酸化油菜秸秆纤维素粉微球,制备的生物吸附剂可选择吸附BSA.因其表面有更多的活性基团,其具有吸附平衡快,吸附容量大等优点.实验结果表明磷酸化油菜秸秆纤维素粉微球对BSA的最大吸附容量为127.39 mg/g,而未修饰油菜秸秆纤维素粉微球对BSA的最大吸附容量只有68.98 mg/g,表明改性能获得较好的吸附性能.吸附剂的吸附等温线符合Langmuir方程,属单分子层吸附.
[1]刘瑞伟.我国农作物秸秆利用现状及对策[J].农业与技术,2009,29(1):7-9.
[2]吴少杰.秸秆焚燃污染与生物质能的开发利用[J].工业安全与环保,2008,34(5):54-56.
[3]卢 炜.秸秆纤维素在离子液体中的溶解、功能化及其应用[D].武汉:华中农业大学,2009:11-17.
[4]Mucalo M R,Kato K,Yokogawa Y.Phosphorylated,cellulose-based substrates as potential adsorbents for bone morphogenetic proteins in biomedical applications:a protein adsorption screening study using cytochrome C as a bone morphogenetic protein mimic[J].Colloids Surf B Biointerfaces,2009,71(1):52-58.
[5]Kawai T,Saito K,Lee W.Protein binding to polymer brush,based on ion-exchange,hydrophobic and affinity interactions[J].J Chromatogr B Analyt Technol Biomed Life Sci,2003,790(1/2):131-42.
[6]Tanyolac D,Sönmezisik H,Özdural A R,et al.A low cost porous polyvinylbutyral membrane for BSA adsorption[J].Biochem Eng J,2005,22(3):221-228.
[7]Hu J,Li S,Liu B.Adsorption of BSA onto sulfonated microspheres[J].Biochem Eng J,2005,23(3):259-263.
[8]Zhang J,Zhang Z,Song Y,et al.Bovine serum albumin(BSA)adsorption with Cibacron Blue F-3GA attached chitosan microspheres[J].React Funct Polym,2006,66(9):916-923.
[9]吴 晖,张米娜,姜苏杰,等.胶原固载 Zr(Ⅳ)亲和吸附材料的制备及其对牛血清蛋白的吸附特性[J].生物质化学工程,2008,42(1):17-21.
[10]Blackburn R S,,Harvey A,Kettle L L,et al.Sorption of chlorhexidine on cellulose:mechanism of binding and molecular recognition[J].J Phys Chem B,2006,111(30):8775-8784.
[11]Hameed B H,Din A T,M,Ahmad A L.Adsorption of methylene blue onto bamboo-based activated carbon:kinetics and equilibrium studies[J].J Hazard Mate,2007,141(3):819-825.
